Une forte probabilité de cause à effet mais de nombreux facteurs confondants…
Développées à partir des années 1960, les benzodiazépines (BZD) ont des effets psychotropes par modulation allostérique du complexe transmembranaire GABA-canal chlore. En France, les autorisations de mise sur le marché leur confèrent les indications suivantes : troubles sévères du sommeil, manifestations anxieuses sévères et/ou invalidantes, prévention et traitement du delirium tremens.
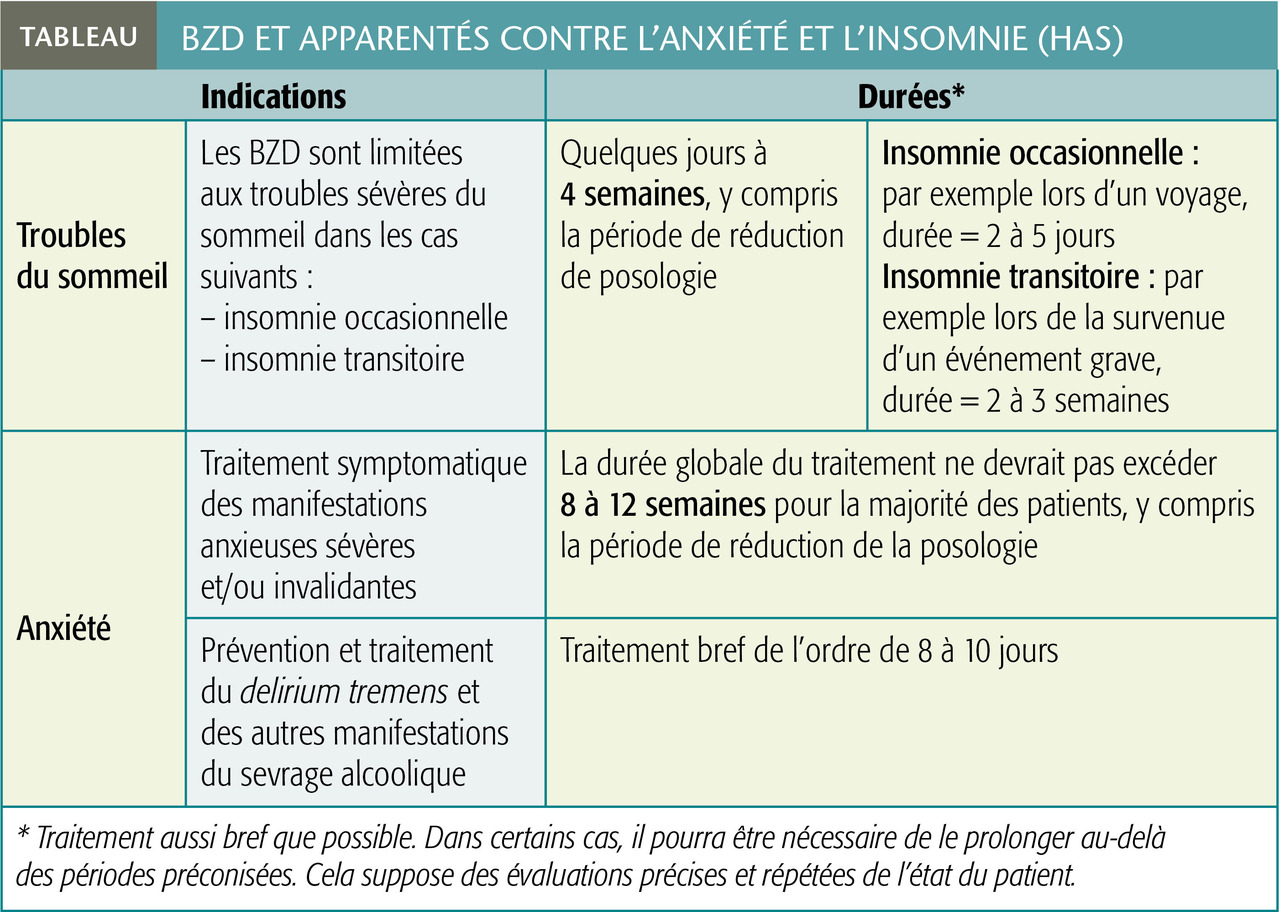
Dans ce cadre réglementaire, les recommandations limitent leur prescription dans le temps. La durée maximale est de 12 semaines pour les anxiolytiques et de 4 semaines pour les hypnotiques : ces durées incluent la période de sevrage (tableau ).
Dans ce cadre réglementaire, les recommandations limitent leur prescription dans le temps. La durée maximale est de 12 semaines pour les anxiolytiques et de 4 semaines pour les hypnotiques : ces durées incluent la période de sevrage (
Épidémiologie
La prescription de BZD augmente avec l’âge du patient, davantage chez les femmes.
Au sein de la cohorte Paquid (2 792 personnes âgées de 65 ans et plus vivant à domicile – hors institution – choisies de manière aléatoire sur les listes électorales), la consommation d’au moins une molécule était retrou- vée chez 31 % des sujets dans les 2 dernières semaines. Il s’agissait d’une seule molécule pour 86 % des interrogés, de deux différentes pour 13 %, voire de trois pour 1 % de la cohorte.
Publié en 2006, le rapport de l’Office parlementaire d’évaluation des politiques de santé sur le bon usage des médicaments psychotropes, établi à partir de données des caisses d’Assurance maladie, indique une prévalence instantanée de benzodiazépines anxiolytiques à 33,7 % dans la tranche des 51-70 ans, et 48,5 % chez les plus de 70 ans.
Dans la cohorte rétrospective ThalEs incluant 1 300 456 patients de plus de 65 ans suivis par un médecin généraliste entre 2001 et 2006 et ne recevant ni benzodiazépine ni apparentés en 2000 avant leur participation, l’incidence cumulée dans les ordonnances se monte à 32,8 % en 6 ans : soit 5,5 % annuellement. Au total, 50 % de ces primo-prescriptions avaient une durée supérieure ou égale à 45 jours.1
Au sein de la cohorte Paquid (2 792 personnes âgées de 65 ans et plus vivant à domicile – hors institution – choisies de manière aléatoire sur les listes électorales), la consommation d’au moins une molécule était retrou- vée chez 31 % des sujets dans les 2 dernières semaines. Il s’agissait d’une seule molécule pour 86 % des interrogés, de deux différentes pour 13 %, voire de trois pour 1 % de la cohorte.
Publié en 2006, le rapport de l’Office parlementaire d’évaluation des politiques de santé sur le bon usage des médicaments psychotropes, établi à partir de données des caisses d’Assurance maladie, indique une prévalence instantanée de benzodiazépines anxiolytiques à 33,7 % dans la tranche des 51-70 ans, et 48,5 % chez les plus de 70 ans.
Dans la cohorte rétrospective ThalEs incluant 1 300 456 patients de plus de 65 ans suivis par un médecin généraliste entre 2001 et 2006 et ne recevant ni benzodiazépine ni apparentés en 2000 avant leur participation, l’incidence cumulée dans les ordonnances se monte à 32,8 % en 6 ans : soit 5,5 % annuellement. Au total, 50 % de ces primo-prescriptions avaient une durée supérieure ou égale à 45 jours.1
Surdosage et effets indésirables
Particulièrement fréquente chez la personne âgée, l’administration de ces médicaments dans cette classe d’âge n’est pourtant estimée appropriée que dans un tiers des cas.2 En outre, les modifications physiologiques liées au vieillissement favorisent l’accumulation de métabolites actifs, exposant le sujet sénescent à des risques majorés de surdosage et d’effets indésirables. Parmi ceux-ci, la confusion et la chute sont particulièrement délétères.
Sont également à craindre les troubles cognitifs. Les principaux identifiés concernent les processus sensoriel et psychomoteur, la mémoire non verbale, les activités visuo-spatiales et la résolution de problème. Ces molécules induisent en particulier une amnésie antérograde et un déficit de la mémoire épisodique/biographique, ainsi que des difficultés d’acquisition de nouvelles informations.3
Facteur de démence ?
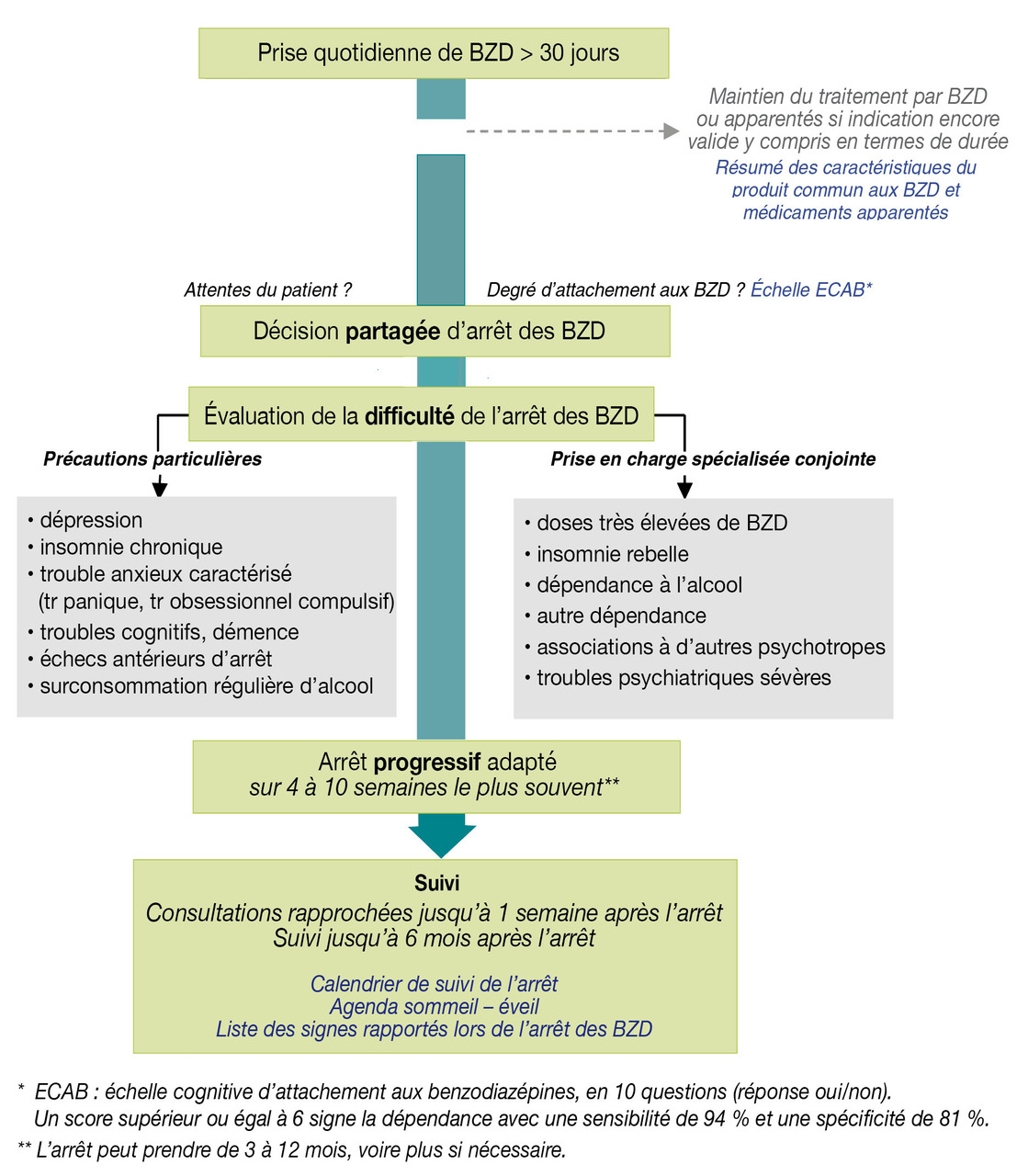
Depuis une dizaine d’années, le lien entre BZD et détérioration cognitive fait l’objet de débats. Une méta-analyse de 8 études observationnelles (incluant au total 66 177 sujets âgés) indique un lien significatif, pendant le suivi, entre une prescription supérieure à 30 jours et la survenue d’une démence. Le risque (OR) est multiplié par 1,78 sous ce traitement comparativement aux sujets non consommateurs (IC 95 % = 1,33-2,38). L’impact est plus modéré si l’on s’en tient aux seules études européennes (OR = 1,43 ; IC 95 % = 1,16-1,75). Cette association significative n’est cependant pas un lien de causalité.4
Entre le 1er janvier 1990 et le 1er mars 2016 ont été publiés 10 articles de pharmaco-épidémiologie évaluant la relation entre exposition aux BZD et risque démentiel chez des personnes d’au moins 60 ans. Quatre études de cohorte et 6 en cas-témoins portaient au total sur 191 078 sujets. Dans 7 d’entre elles avec des durées de suivi entre 6 et 22 ans, les BZD sont un facteur de risque de troubles cognitifs survenant pendant la période d’évaluation. Mais la synthèse reste délicate au vu de l’hétérogénéité des méthodologies et des critères diagnostiques utilisés, en particulier la définition de l’exposition aux benzodiazépines et celle de la démence incidente.
On retrouve cependant une cohérence et une stabilité des résultats dans plusieurs essais bien menés qui montrent un lien entre prise de BZD et démences. La causalité est soutenue par la force statistique de l’association (risque relatif ou odds ratio significatifs), la cohérence des données (répétition des observations dans différentes populations), les relations dose-effet d’une part et temporelle d’autre part.
La principale limite méthodologique (en particulier des études cas-témoins) est le « biais protopathique », facteur de confusion retrouvé lorsque l’effet précède la cause. En l’occurrence, on ne sait pas si les benzodiazépines sont prescrites pour une symptomatologie s’intégrant aux prodromes démentiels, ou si ces molécules provoquent l’entrée dans la maladie d’Alzheimer.
Sont également à craindre les troubles cognitifs. Les principaux identifiés concernent les processus sensoriel et psychomoteur, la mémoire non verbale, les activités visuo-spatiales et la résolution de problème. Ces molécules induisent en particulier une amnésie antérograde et un déficit de la mémoire épisodique/biographique, ainsi que des difficultés d’acquisition de nouvelles informations.3
Facteur de démence ?
Depuis une dizaine d’années, le lien entre BZD et détérioration cognitive fait l’objet de débats. Une méta-analyse de 8 études observationnelles (incluant au total 66 177 sujets âgés) indique un lien significatif, pendant le suivi, entre une prescription supérieure à 30 jours et la survenue d’une démence. Le risque (OR) est multiplié par 1,78 sous ce traitement comparativement aux sujets non consommateurs (IC 95 % = 1,33-2,38). L’impact est plus modéré si l’on s’en tient aux seules études européennes (OR = 1,43 ; IC 95 % = 1,16-1,75). Cette association significative n’est cependant pas un lien de causalité.4
Entre le 1er janvier 1990 et le 1er mars 2016 ont été publiés 10 articles de pharmaco-épidémiologie évaluant la relation entre exposition aux BZD et risque démentiel chez des personnes d’au moins 60 ans. Quatre études de cohorte et 6 en cas-témoins portaient au total sur 191 078 sujets. Dans 7 d’entre elles avec des durées de suivi entre 6 et 22 ans, les BZD sont un facteur de risque de troubles cognitifs survenant pendant la période d’évaluation. Mais la synthèse reste délicate au vu de l’hétérogénéité des méthodologies et des critères diagnostiques utilisés, en particulier la définition de l’exposition aux benzodiazépines et celle de la démence incidente.
On retrouve cependant une cohérence et une stabilité des résultats dans plusieurs essais bien menés qui montrent un lien entre prise de BZD et démences. La causalité est soutenue par la force statistique de l’association (risque relatif ou odds ratio significatifs), la cohérence des données (répétition des observations dans différentes populations), les relations dose-effet d’une part et temporelle d’autre part.
La principale limite méthodologique (en particulier des études cas-témoins) est le « biais protopathique », facteur de confusion retrouvé lorsque l’effet précède la cause. En l’occurrence, on ne sait pas si les benzodiazépines sont prescrites pour une symptomatologie s’intégrant aux prodromes démentiels, ou si ces molécules provoquent l’entrée dans la maladie d’Alzheimer.
RÉFÉRENCES
1. HAS. Recommandations professionnelles. Modalités d’arrêt des benzodiazépines et médicaments apparentés chez le patient âgé. Argumentaire. Octobre 2007.
2. Airagnes G, Pelissolo A, Lavallée M, Flament M, Limosin F. Benzodiazepine Misuse in the Elderly: Risk Factors, Consequences, and Management. Curr Psychiatry Rep 2016;18:89.
3. Barker MJ, Greenwood KM, Jackson M, Crowe SF. Cognitive effects of long-term benzodiazepine use: a metaanalysis. CNS drugs 2004;18:37-48.
4. Islam MM, Iqbal U, Walther B, et al. Benzodiazepine Use and Risk of Dementia in the Elderly Population: A Systematic Review and Meta-Analysis. Neuroepidemiology 2016;47: 181-91.
5. HAS. Arrêt des benzodiazépines et médicaments apparentés : démarche du médecin traitant en ambulatoire. Juin 2015.
2. Airagnes G, Pelissolo A, Lavallée M, Flament M, Limosin F. Benzodiazepine Misuse in the Elderly: Risk Factors, Consequences, and Management. Curr Psychiatry Rep 2016;18:89.
3. Barker MJ, Greenwood KM, Jackson M, Crowe SF. Cognitive effects of long-term benzodiazepine use: a metaanalysis. CNS drugs 2004;18:37-48.
4. Islam MM, Iqbal U, Walther B, et al. Benzodiazepine Use and Risk of Dementia in the Elderly Population: A Systematic Review and Meta-Analysis. Neuroepidemiology 2016;47: 181-91.
5. HAS. Arrêt des benzodiazépines et médicaments apparentés : démarche du médecin traitant en ambulatoire. Juin 2015.