Diagnostiquer les principales dyslipidémies primitives et secondaires.
Connaître les recommandations pour la prise en charge des dyslipidémies
Importance de l’évaluation du risque cardiovasculaire global (rang A)
Les dyslipidémies représentent un des facteurs de risque cardiovasculaire majeurs (
Dyslipidémies
Rappel du métabolisme des lipides (rang B)
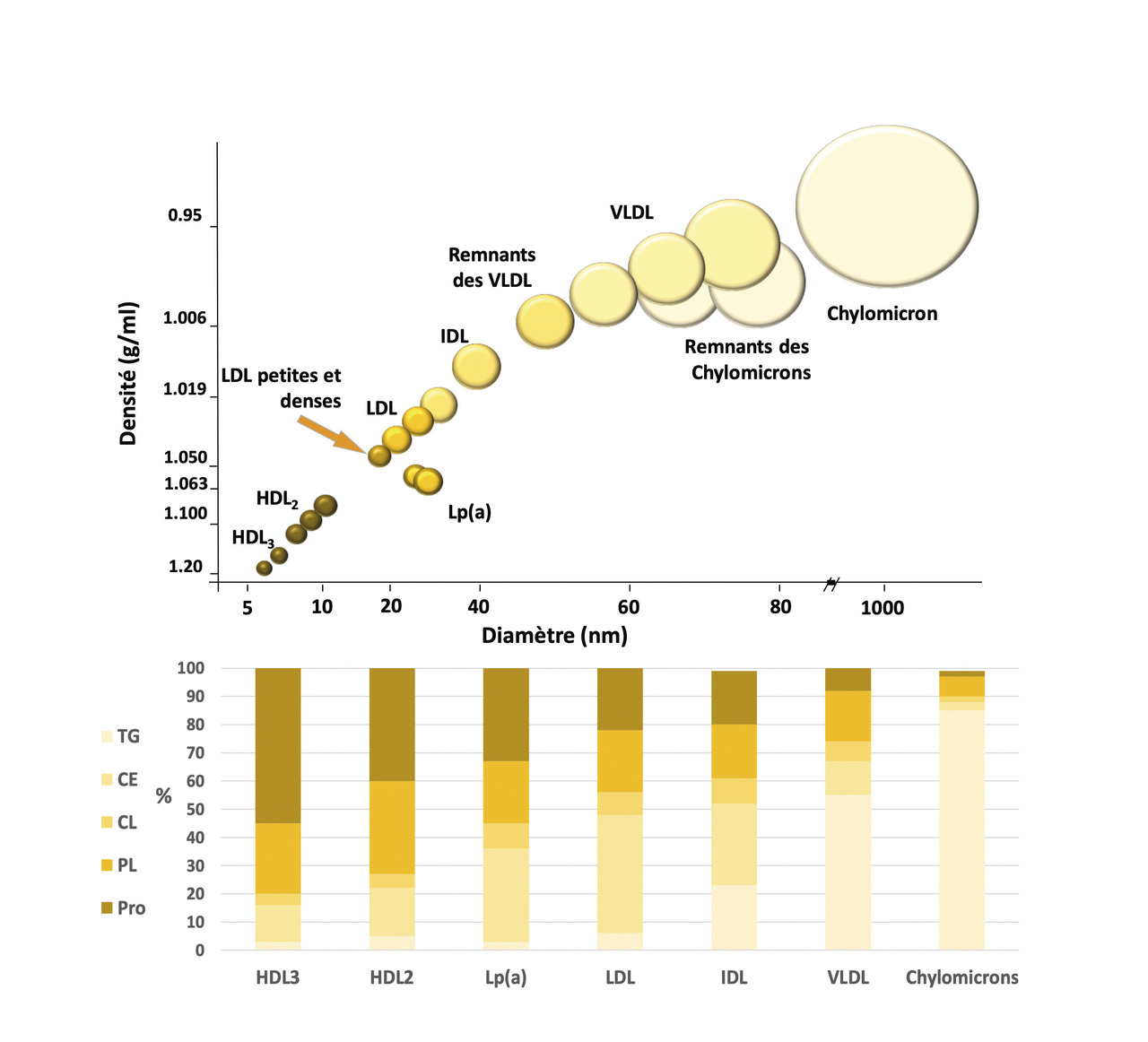
Les lipides sanguins sont transportés par des lipoprotéines, qui sont composées de lipides neutres, lipides polaires et protéines spécialisées, appelées apolipoprotéines (Apo). La plupart des lipides neutres sont représentés par les esters du cholestérol (CE) et les triglycérides (TG) ; les lipides polaires sont représentés par la phosphatidylcholine, la sphingomyéline et le cholestérol libre (CL) avec de petites quantités de phosphatidyléthanolamine et des traces d’autres phospholipides (PL).
La composition et la densité des lipoprotéines détermineront leur volume (
Chylomicrons : dérivés de l’absorption intestinale du cholestérol, ils sont composés plutôt de lipides alimentaires et de petites quantités de protéines, et représentent le résultat de la voie exogène du métabolisme des lipoprotéines. Leur formation suit l’hydrolyse de la graisse consommée lors d’un repas par les enzymes pancréatiques au niveau intestinal (lipase pancréatique). Des micelles de monoglycérides, acides gras libres (AGL), phospholipides et sels biliaires traversent la barrière intestinale, où les acides gras libres sont assemblés au glycérol pour former les triglycérides, tandis que le cholestérol est transformé via l’acyl-CoA-cholestérol acyltransférase (ACAT) pour former les esters de cholestérol. L’absorption du cholestérol se fait par le transporteur Niemann-Pick C1-like 1 (NPC1L1). Une fois la formation des chylomicrons réalisée dans les cellules intestinales, ils sont transportés dans la circulation portale ou lymphatique via le conduit thoracique. Dans la circulation sanguine, ils sont transformés en remnants de chylomicrons et VLDL (very-low density lipoproteins) par la lipoprotéine lipase (LPL). Les remnants des chylomicrons pourront entrer dans le foie par l’intermédiaire de l’Apo E, qui se lie au récepteur des LDL.
Lipoprotéines à très basse densité (VLDL) : elles sont synthétisées au niveau du foie à partir des remnants de chylomicrons, ce qui correspond à la première étape de la voie endogène du métabolisme des lipoprotéines. Cette transformation se fait par l’intermédiaire de la microsomal TG transfer protein (MTTP), qui est responsable de l’assemblage de l’Apo B avec triglycérides, esters de cholestérol et phospholipides pour la formation de pré-VLDL qui seront ensuite transformées en VLDL. Les VLDL sont le transporteur principal des triglycérides, et leur demi-vie est de 30-60 minutes. En conditions normales, leur métabolisme s’associe au stockage des acides gras libres dans le tissu adipeux et dans les muscles. La présence de conditions telles que l’insulinorésistance ou le syndrome métabolique s’associe à une dysfonction de ce procès de stockage, ce qui détermine une augmentation des taux des triglycérides à jeun.
Lipoprotéines à densité intermédiaire (intermediate density lipoproteins, IDL) : issues du métabolisme des VLDL par la lipoprotéine lipase, ces lipoprotéines ne font pas l’objet de l’action de la lipoprotéine lipase, du fait que l’Apo C-II, facilitateur de l’activité de la lipoprotéine lipase, n’est pas liée aux IDL. Le métabolisme des IDL est assuré au niveau hépatique par la lipase hépatique (HL), qui les transforme en LDL.
Lipoprotéines à basse densité (low-density lipoproteins, LDL) : les LDL sont transportées par l’Apo B-100, qui est le responsable principal de l’interaction avec le récepteur LDL. Cela permet aux LDL d’entrer dans la cellule hépatique pour être à nouveau métabolisées et transformées en acides biliaires, puis sécrétées par les voies biliaires dans la lumière intestinale. La demi-vie des LDL est de 2-3 jours. Presque le tiers des LDL sera absorbé en périphérie, par les tissus non hépatiques.
Lipoprotéines à haute densité (high-density lipoproteins, HDL) : constituées à partir de l’Apo A-1, elles sont les acteurs principaux du transport inverse du cholestérol. Grâce à l’interaction avec les transporteurs de la famille ATP-binding cassette (ABCA1, ABCG1/G4), l’Apo A-1, pauvre en lipides, augmente son contenu en esters de cholestérol donnant lieu aux HDL2 qui seront ensuite transformés en HDL3, plus grandes et riches en esters de cholestérol. Ces dernières seront absorbées au niveau hépatique pour être métabolisées. En condition d’augmentation des concentrations de triglycérides, des HDL riches en triglycérides se formeront, issues de l’action de la cholesteryl-ester transfer protein (CETP) responsable de l’échange de triglycérides et d’esters de cholestérol entre VLDL et HDL.
Lipoprotéine (a), Lp(a) : il s’agit d’une lipoprotéine qui présente les mêmes caractéristiques de densité et de taille que les LDL, mais elle a la particularité d’être liée à l’apo(a) en plus de l’Apo B. La présence de cette apo(a) la différencie complètement des autres lipoprotéines : c’est une protéine qui présente une similitude de structure avec le plasminogène et qui est impliquée dans des mécanismes liés à la coagulation. La Lp(a) n’est donc pas un produit du métabolisme de lipoprotéine lipases, et ses taux ne diminuent pas après un régime alimentaire pauvre en graisse ; aussi, elle ne répond pas aux statines. Le nombre de Kringles qui caractérise l’apo(a) est inversement lié aux taux sanguins de Lp(a), ce qui fait de l’apo(a) le modulateur principal de la production de cette lipoprotéine. Néanmoins, des études ont montré que l’Apo B est aussi un régulateur des taux de Lp(a).
Définition et classification des dyslipidémies (rang A)
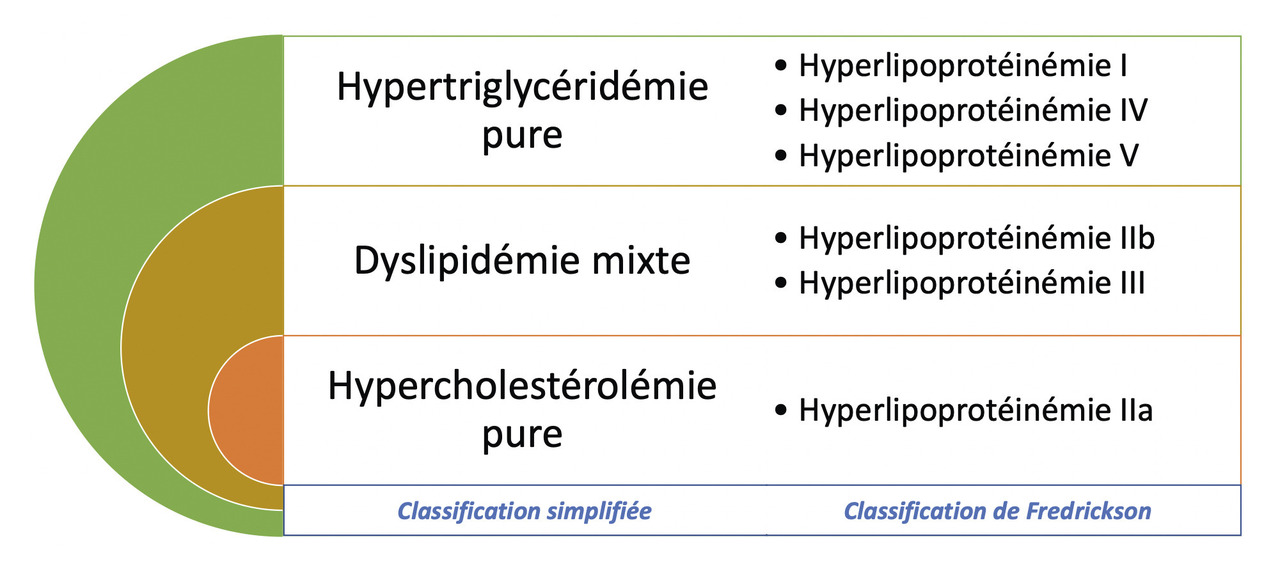
On peut individualiser en pratique clinique courante trois grands types de dyslipidémies selon le phénotype : l’hypercholestérolémie pure, l’hypertriglycéridémie pure et l’hyperlipidémie mixte avec augmentation conjointe de la cholestérolémie et de la triglycéridémie. Il est toutefois indispensable de savoir repérer des formes rares mais graves de dyslipidémies, par exemple les hyperchylomicronémies familiales (
Ces phénotypes regroupent des génotypes multiples, et un malade porteur d’une anomalie génétique unique peut exprimer au fil du temps des phénotypes lipidiques multiples. Il n’y a donc pas de relation d’équivalence stricte génotype-phénotype dans le domaine des dyslipidémies.
Il existe, par ailleurs, une classification historique, la classification de Fredrickson, fondée sur le phénotype lipidique. La correspondance entre les deux classifications est montrée dans la
Hypercholestérolémie pure
Elle se caractérise par une augmentation isolée des taux de cholestérol total et LDL-c. Bien que le risque cardiovasculaire associé au LDL-c soit graduel, une valeur seuil pour le diagnostic d’hypercholestérolémie a été fixée à > 1,60 g/L.
Formes monogéniques
L’hypercholestérolémie familiale hétérozygote, fréquente (environ 1/500, voire 1/250 dans les cohortes avec dépistage génétique) à transmission autosomique dominante, est causée par une mutation des récepteurs aux LDL-c (50 % des récepteurs sont fonctionnels) ou de l’Apo B ou de la proproteine convertase subtilisine/kexine de type 9 (PCSK9). Dans la forme homozygote, exceptionnelle (1/300 000), il existe un déficit complet en récepteurs. Un LDL-c > 1,9 g/L doit faire suspecter une hypercholestérolémie familiale hétérozygote, tandis qu’un LDL-c > 5 g/L suggère un diagnostic d’hypercholestérolémie familiale homozygote.
Hypercholestérolémie familiale homozygote
- LDL-c > 5 g/L (6-10 g/L) ;
- dépôts lipidiques dès l’enfance : xanthomatose cutanéotendineuse (xanthomes plans, tubéreux et tendineux majeurs) ;
- complications cardiovasculaires ischémiques dès la première décennie ; en l’absence de traitement : décès vers l’âge de 20 ans ;
- fréquence (+++) des rétrécissements aortiques athéromateux supravalvulaires.
Hypercholestérolémie familiale hétérozygote
Caractéristiques liées à la forme hétérozygote du gène du récepteur des LDL :
- LDL-c compris entre 1,9 et 4,0 g/L ;
- xanthomes tendineux présents dans 30 % des cas seulement ;
- complications cardiovasculaires ischémiques précoces en l’absence d’hypocholestérolémiant efficace :
- chez l’homme : vers 40-50 ans ;
- chez la femme : vers 50-60 ans.
En cas d’hypercholestérolémie familiale, il sera important de faire un dépistage d’une hypercholestérolémie chez les apparentés au premier degré.
Formes polygéniques
Les plus fréquentes, ces formes sont la conséquence de l’interaction entre des facteurs génétiques affectant l’absorption intestinale du cholestérol, la synthèse des acides biliaires ou du cholestérol, la synthèse ou le catabolisme des LDL et des facteurs environnementaux (alimentation riche en acides gras saturés et en cholestérol). Elles répondent souvent bien aux mesures diététiques.
Les critères suivants permettent de les distinguer des formes monogéniques :
- absence de caractère familial d’allure autosomique dominante (moins de 10 % des apparentés ont une hypercholestérolémie pure contre plus de 50 % dans les formes monogéniques) ;
- caractère souvent plus modéré ;
- survenue plus tardive dans la vie et sensibilité au régime.
Hypertriglycéridémie
Il s’agit d’une dyslipidémie associée à un taux de triglycérides > 1,5 g/L. Quand le taux de triglycérides est > 10 g/L on parle d’hypertriglycéridémie majeure, ou hyperchylomicronémie, ce qui suggère la présence de chylomicrons dans la circulation sanguine.
Formes monogéniques
Il s’agit du syndrome d’hyperchylomicronémie familiale, très rare (1/1 000 000) et à transmission autosomique récessive.
Sur un plan biologique, l’activité lipoprotéine lipase est diminuée dans le plasma (dosage complexe), et sur un plan génétique, il existe des mutations qui affectent le métabolisme de cette enzyme (mutation de la lipoprotéine lipase elle-même, ou de ses coactivateurs et précurseurs).
Les formes familiales monogéniques sont les plus rares et sont souvent découvertes dans l’enfance ou chez l’adulte jeune. Elles ont une sensibilité aux graisses alimentaires. Le poids est normal, voire bas. Dans ces formes, il y a absence de cause secondaire, en dehors de la grossesse qui est une situation très à risque pour ces dyslipidémies.
Formes polygéniques
Elles sont caractérisées par des élévations transitoires des triglycérides liées à un excès d’apport en sucre ou en alcool. Dans le cas de la dyslipidémie diabétique (ou athérogène), on retrouve en effet une augmentation des taux de triglycérides associée à une baisse des taux de HDL, avec des valeurs quasi normales de LDL-c. Dans cette dyslipidémie, les valeurs de LDL-c sont faussement basses car il y a plus de particules LDL petites et denses, non détectées car plus petites, mais également athérogènes car transportées par l’Apo B100. Il entre dans cette catégorie une bonne partie des dyslipidémies secondaires, notamment iatrogènes (détaillé par la suite).
Dyslipidémie mixte
Il s’agit d’une dyslipidémie combinant une hypercholestérolémie (LDL-c > 1,60 g/L) et une hypertriglycéridémie (TG > 1,5 g/L). Son association avec un risque cardiovasculaire élevé est variable, dépendant de l’intensité et de la durée de l’exposition mais aussi de l’association d’autres facteurs de risque (obésité, hypertension, diabète…).
Formes oligogéniques
La dysbêtalipoprotéinémie (anciennement connue comme hyperlipoprotéinémie de type III) est caractérisée par les aspects suivants :
- transmission récessive pour la forme classique : phénotype E2/E2 de l’apolipoprotéine E (Apo E) ;
- accumulation d’IDL (intermediate-density lipoproteins) [remnants de VLDL et de chylomicrons] de type III ;
- fréquence rare (1 pour 10 000) ;
- hyperlipidémie mixte sévère, étroitement dépendante des mesures diététiques ;
- élévation harmonieuse de la cholestérolémie et de la triglycéridémie, avec une cholestérolémie totale comprise entre 3 et 5 g/L, une triglycéridémie comprise entre 4 et 8 g/L et des valeurs d’Apo B normales/basses ;
Formes polygéniques
Elles représentent le type de dyslipidémie le plus fréquent, étant caractérisées par une hypercholestérolémie et une hypertriglycéridémie modérées (LDL-c < 2 g/L et TG < 5 g/L), souvent associées à un syndrome métabolique et/ou à un diabète de type 2.
Une forme polygénique mais avec une transmission héréditaire non mendélienne oligogénique est représentée par l’hypercholestérolémie familiale combinée, concernant 1 à 2 % de la population générale. Le phénotype est typiquement retrouvé dans la même famille, mais il est très variable chez un même individu et au moins un apparenté de premier degré au fil du temps, en alliant une dyslipidémie mixte à une hypercholestérolémie ou hypertriglycéridémie pure. Contrairement à la dysbêtalipoprotéinémie, le dosage de l’Apo B mettra en évidence des taux normaux/élevés de cette apolipoprotéine. Un syndrome métabolique et/ou un diabète de type 2 peuvent également être associés à cette dyslipidémie.
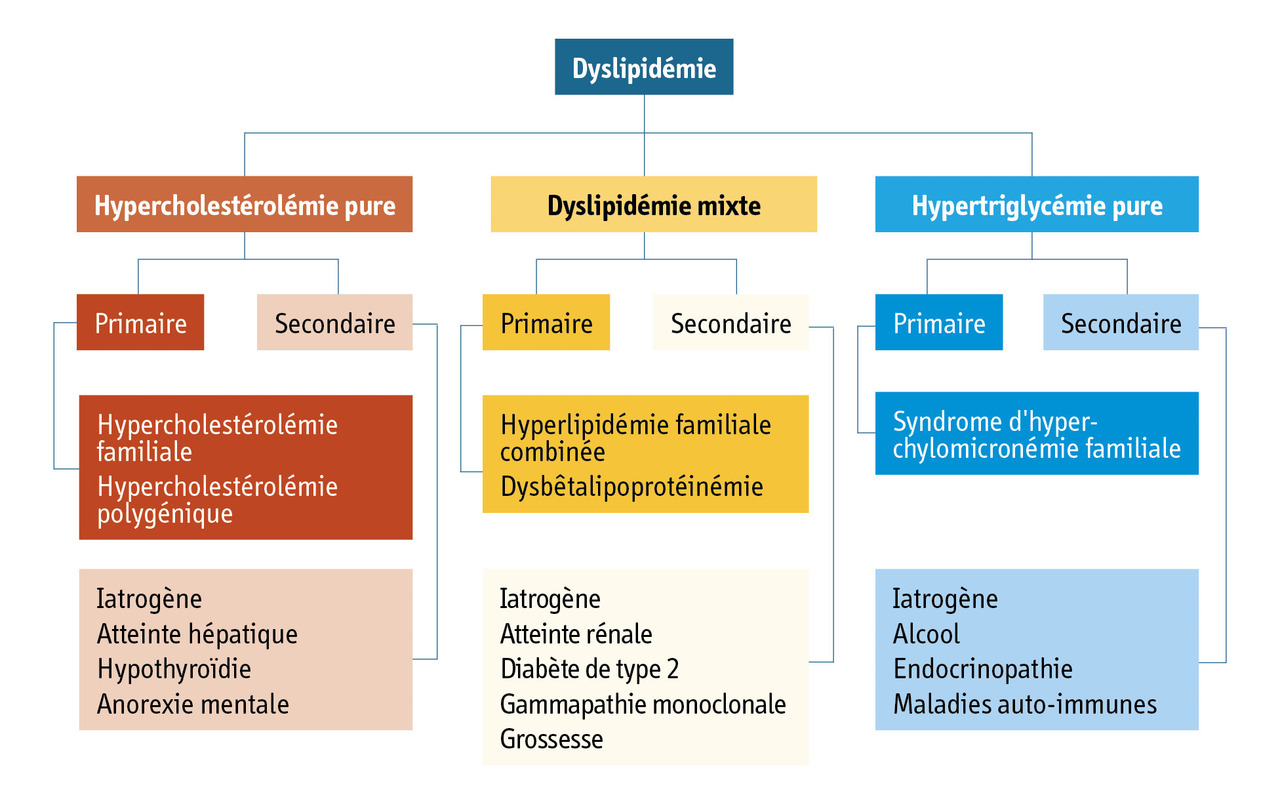
Dyslipidémies secondaires (rang A)
Dans le diagnostic d’une dyslipidémie, avant d’introduire un traitement hypolipémiant, il est important d’exclure une cause secondaire. Les hyperlipidémies secondaires s’améliorent avec un traitement à visée étiologique, sans employer d’hypolipémiants, ici inutiles, voire dangereux dans certaines situations.
Une hyperlipidémie peut se rencontrer dans les situations suivantes.
Les dyslipidémies iatrogènes sont fréquentes et comportent des élévations mineures des lipides sanguins (diurétiques et bêtabloquants par exemple) dont les conséquences cliniques sont faibles, des élévations potentiellement importantes (contraception estroprogestative, corticothérapie, antirétroviraux, traitement de certains cancers) et des élévations secondaires à la prise de poids surtout à prédominance abdominale (certains neuroleptiques).
Les autres causes d’hyperlipidémies secondaires sont :
- endocrinopathie : hypothyroïdie, acromégalie, syndrome de Cushing ;
- atteinte hépatique : cholestase ;
- atteinte rénale : le syndrome néphrotique et l’insuffisance rénale ;
- l’obésité, en particulier abdominale, modifie les paramètres lipidiques ;
- la consommation excessive d’alcool est chez certains patients un facteur majeur d’hypertriglycéridémie ;
- le diabète de type 2 est non seulement une cause de dyslipidémie mais aussi un facteur de majoration du risque cardiovasculaire. La mesure de la glycémie à jeun doit être réalisée de façon systématique en cas de dyslipidémie. En cas de décompensation (carence en insuline), une hypertriglycéridémie très sévère avec hyperchylomicronémie peut être observée ;
- la grossesse est associée à une augmentation physiologique du cholestérol.
(Rang B)
Les examens complémentaires sont orientés en fonction du contexte clinique : dosage de TSH, créatininémie, protéinurie et gamma GT, phosphatases alcalines.
Les causes de dyslipidémie secondaire et les dyslipidémies associées sont listées dans le
Complications des dyslipidémies (rang B)
Une augmentation du LDL-c, une augmentation modérée des triglycérides et une baisse de l’HDL-c sont associées à une augmentation du risque de maladie cardiovasculaire.
L’ampleur et la durée de l’exposition à une augmentation de taux de LDL-c circulants sont liées proportionnellement au risque cardiovasculaire. Le risque est surtout coronarien. L’excès de cholestérol sanguin sollicite l’interaction avec la paroi artérielle. Cela entraîne un dysfonctionnement endothélial qui impliquera l’internalisation des LDL dans l’intima, où elles seront oxydées, et le recrutement de macrophages au niveau de la média, qui seront transformés en cellules spumeuses, donnant lieu à une plaque d’athérome. Les conséquences ultimes de ce processus seront la sténose artérielle ischémique chronique (angor d’effort, claudication intermittente…) et les pathologies vasculaires aiguës par rupture de la plaque d’athérome (syndrome coronaire aigu, accident vasculaire cérébral ischémique, ischémie aiguë d’un membre inférieur…).
L’hypercholestérolémie familiale homozygote constitue un modèle exemplaire d’athérosclérose accélérée. Il existe une fréquente infiltration athéromateuse de la partie initiale de l’aorte. Les complications coronariennes peuvent survenir avant la fin de la première décennie, et la majorité des patients décédaient avant l’âge de 20 ans en l’absence de traitement. Le pronostic, directement lié à la concentration du cholestérol, est sévère. Dans l’hypercholestérolémie familiale hétérozygote, les complications ischémiques surviennent chez les fumeurs dans les formes sévères dès l’âge de 30 ans. La moitié des hommes étaient victimes d’un infarctus à l’âge de 50 ans avant la disponibilité des statines.
L’hypertriglycéridémie constitue un facteur de risque cardiovasculaire moins puissant que l’augmentation du LDL-c. Dans le cas de la dyslipidémie diabétique (ou athérogène), on observe une augmentation du risque cardiovasculaire malgré des taux de LDL-c circulant faussement normaux (excès de LDL petites et denses). Dans le cas de la dysbêtalipoprotéinémie, l’augmentation du risque cardiovasculaire est inconstante.
Le risque majeur, très rare, associé aux hyperchylomicronémies est la pancréatite aiguë. Ce risque est d’autant plus marqué qu’il y a déjà eu un antécédent similaire, et augmente avec le taux de triglycérides, avec un seuil classique de 10 g/L. Le lien entre hyperchylomicronémie et maladie cardiovasculaire n’est pas établi.
Diagnostic positif d’une dyslipidémie (rang A)
Quand dépister ?
Le premier dépistage d’une dyslipidémie doit être fait dans les conditions suivantes :
- enquête familiale devant une dyslipidémie chez un apparenté ;
- pathologie associée ou prescription induisant une dyslipidémie secondaire ;
- un ou plusieurs facteurs de risque coexistant (estimation du risque cardiovasculaire absolu) ;
- hommes à partir de l’âge de 50 ans, femmes en post- ménopause.
Interrogatoire
L’interrogatoire consiste à :
- rechercher des antécédents personnels ischémiques ou des signes fonctionnels évocateurs tels qu’angor, artériopathie oblitérante des membres inférieurs (AOMI), accident ischémique transitoire (AIT) ;
- recueillir des antécédents familiaux cardiovasculaires (apparentés de premier degré++) ;
- rechercher la présence d’autres facteurs de risque cardiovasculaire.
Examen clinique
L’examen somatique a pour objectif de rechercher :
- des signes cliniques de dyslipidémie ;
- un athérome asymptomatique (pouls périphérique, souffles vasculaires) ;
- un athérome infraclinique.
Signes cliniques d’hypercholestérolémie
Les dépôts extravasculaires sont inconstants et comprennent un arc cornéen (valeur sémiologique avant 45 ans) ou un xanthélasma (valeur sémiologique avant 60 ans).
Plus rarement, des xanthomes sont observés :
- xanthomes tendineux :
- extenseurs des doigts ;
- tendons d’Achille ;
- xanthomes plans cutanés, xanthomes tubéreux (uniquement les formes homozygotes).
Signes cliniques d’hypertriglycéridémie
Les hypertriglycéridémies légères ou modérées ne sont pas associées à des signes cliniques spécifiques. Lors d’une hypertriglycéridémie majeure transitoire, de façon très inconstante il peut être observé une xanthomatose éruptive faite de vésicules de petite taille, jaune vif, non inflammatoires, non douloureuses, non prurigineuses, localisées sur le thorax, les flancs, la face antérieure des genoux, la face postérieure des coudes et des fesses.
Il peut exister des douleurs post-prandiales, une hépatosplénomégalie et une lipémie rétinienne.
Signes cliniques de dyslipidémie mixte
Il n’y a pas de signe clinique associé à cette condition. La seule exception est représentée par des xanthomes des plis palmaires et des xanthomes tubéreux, peu fréquents mais pathognomoniques de la dysbêtalipoprotéinémie.
Procédures diagnostiques
Bilan lipidique
Ses modalités de réalisation sont les suivantes :
- il doit être effectué après 12 heures de jeûne pour le dépistage des hypertriglycéridémies majeures ; sinon un bilan lipidique non à jeun est parfaitement possible (i.e. dépistage le jour de l’hospitalisation pour syndrome coronaire aigu) ;
- étant prescrit devant un facteur de risque cardiovasculaire ou une complication, il se doit d’être complet pour mieux stratifier le risque et il doit être répété en cas d’anomalies pour confirmation ;
- si les anomalies lipidiques ne sont pas suffisamment importantes pour justifier un traitement, le bilan lipidique doit alors être contrôlé tous les 3 ans, sauf pour les diabétiques de type 2 chez qui il doit être vérifié annuellement.
Le dépistage d’une dyslipidémie repose sur l’exploration d’une anomalie lipidique (EAL). L’aspect du sérum peut apporter des informations importantes sur le contenu excessif en cholestérol (sérum limpide) ou en triglycérides (sérum trouble, lactescent dans ce cas). Cela correspond à une situation instantanée, qui pourrait ne pas être confirmée lors d’un deuxième prélèvement.
Le LDL-c est le plus souvent calculé par la formule de Friedwald, valable à condition que les triglycérides soient inférieurs à 3,4 g/L : LDL-c = CT - HDL-c - TG/5 (en g/L).
En cas de triglycérides > 3,4 g/L (3,9 mmol/L), la formule de Friedwald n’est plus valide pour calculer le LDL-c : il faut alors réaliser un dosage direct du LDL-c.
Les facteurs de conversion de mmol/L en g/L sont : cholestérol × 0,387 ; triglycérides × 0,875.
Les valeurs normales sont en général définies dans les résultats biologiques comme étant les valeurs usuelles de la population. Ces valeurs sont à interpréter en fonction du risque vasculaire. En cas de valeurs anormales, une confirmation est le plus souvent nécessaire.
Dépistage de l’atteinte vasculaire infraclinique
En l’état actuel des connaissances, des explorations telles que l’électrocardiogramme d’effort, l’imagerie carotidienne et l’évaluation de l’athérome coronarien par le score calcique d’Agatston ne sont pas recommandées pour un premier dépistage systématique chez les patients dyslipidémiques asymptomatiques.
Elles peuvent toutefois aider à la reclassification des patients à risque intermédiaire et être un outil de motivation pour des patients réticents à l’idée d’un traitement.
Les recommandations sur la prise en charge des dyslipidémies (rang A)
Principe de stratification du risque
La présence d’un ou plusieurs facteurs de risque permet d’identifier un risque cardiovasculaire global pour un certain sujet.
La stratégie thérapeutique repose sur l’évaluation du risque cardiovasculaire à dix ans.
Trois étapes principales sont à prendre en compte pour la prise en charge d’une dyslipidémie :
Stratifier le risque cardiovasculaire
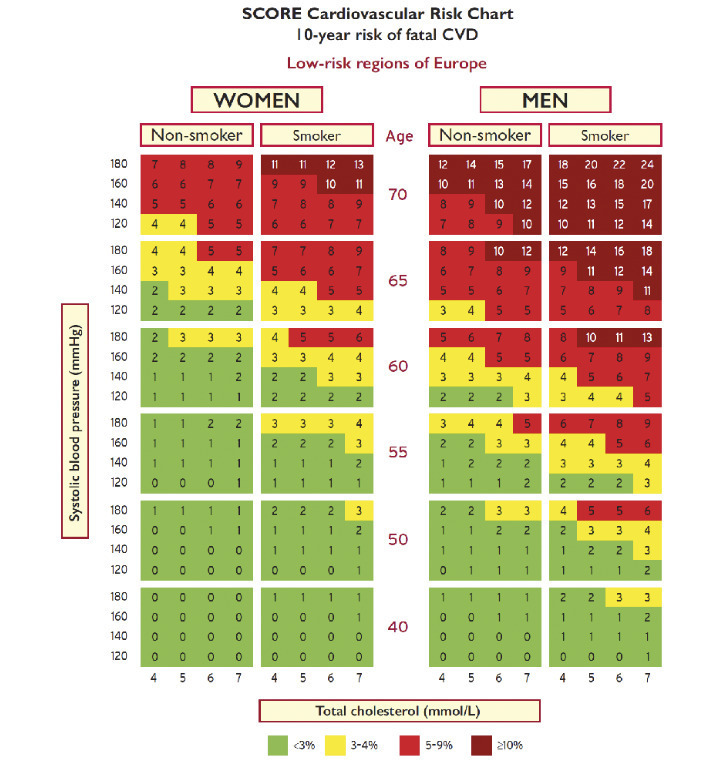
L’ensemble des facteurs de risque sont évalués dans des cartes de risque issues du projet européen SCORE, qui estime le risque de mortalité de cause cardiovasculaire (
Règles d’utilisation
SCORE n’est pas valable dans les situations cliniques du très haut et haut risque (notamment chez les patients en prévention secondaire et chez les diabétiques).
SCORE donne un risque de mortalité : le très haut risque est une mortalité > 10 %, le haut risque entre 5 et 10 %. Le risque intermédiaire est un risque de 1 à 5 %. Le bas risque est inférieur à 1 %.
SCORE n’est pas valable chez le patient traité par hypolipémiant ou hypotenseur.
Pour l’évaluation, prendre la valeur de l’âge ou du facteur de risque la plus proche.
SCORE existe en deux versions pour les pays à bas et haut risque. Maladie cardiovasculaire, diabète compliqué ou non, insuffisance rénale et hypercholestérolémie génétique sont associés en eux-mêmes à un certain degré de risque.
En l’absence de ces conditions, le risque des patients est stratifié par l’échelle SCORE.
Retenons que la simple présence d’athérosclérose documentée avec un événement pathologique classe en très haut risque cardiovasculaire. De plus, un diabète avec atteinte d’organe cible, une insuffisance rénale sévère et une hypercholestérolémie familiale avec atteintes d’organes sont aussi à très haut risque.
Très haut risque cardiovasculaire
- Maladie artérielle symptomatique ou significative*.
- Diabète de type 2 avec atteinte d’organe cible ou plus de 3 facteurs de risque ou type 1 de plus de vingt ans.
- Insuffisance rénale sévère (clairance inférieure à 30 mL/min/1,73 m2).
- Hypercholestérolémie familiale avec un facteur de risque majeur.
- Score supérieur à 10 %.
Haut risque cardiovasculaire
- Facteur de risque majeur.
- PA > 180/110 mmHg.
- Hypercholestérolémie familiale ou LDL-c > 1,9 g/L.
- Diabète sans atteinte d’organe cible** de dix ans ou associé à un facteur de risque.
- Insuffisance rénale modérée (clairance entre 30 et 60 mL/min/1,73 m2).
- Score de 5 à 10 %.
Risque intermédiaire
- Diabète du sujet jeune (type 1 < 35 ans et type 2 < 50 ans).
- Score de 1 à 5 %.
Risque bas
- Score de moins de 1 %.
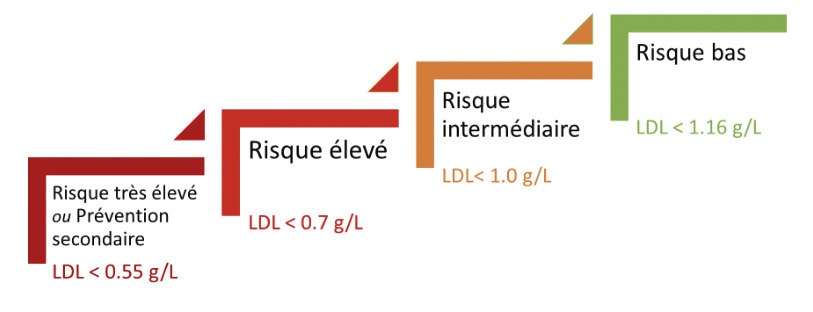
Établir les objectifs de LDL-c
Les objectifs cibles sont fonction du risque cardiovasculaire du patient. Il faut distinguer l’objectif idéal et le seuil justifiant un traitement médicamenteux.
La
Choisir la stratégie d’intervention
Sur la base de l’objectif et du risque estimé, le bilan lipidique permettra de choisir l’intervention la plus adaptée à introduire en première intention. On peut avoir deux scénarios :
- scénario 1 : intervention non pharmacologique (règles hygiénodiététiques) en première intention. C’est le cas des patients ayant un LDL-c modérément élevé en rapport à l’objectif idéal de LDL-c estimé en fonction du risque cardiovasculaire. Par exemple :
risque bas (objectif LDL-c < 1,16 g/L) et EAL montrant un LDL-c égal à 1,68 g/L (seuil d’intervention).
Dans ce cas, des règles hygiénodiététiques seront à introduire, suivies par un nouveau bilan lipidique (à 6-8 semaines idéalement) : si LDL-c non à l’objectif, l’introduction d’un traitement hypolipémiant pourra être envisagée ;
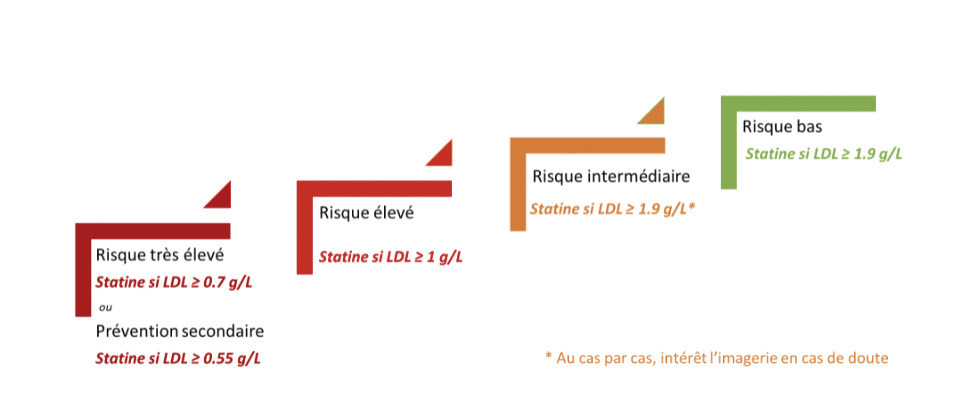
- scénario 2 : intervention pharmacologique et non pharmacologique en première intention (fig. 6). Dans ce cas, un LDL-c significativement élevé en rapport à la cible de LDL-c en fonction du risque cardiovasculaire devra faire l’objet de l’introduction au même temps de règles hygiénodiététiques et d’un traitement hypolipémiant de première intention.
Traitement
En dehors des formes familiales de dyslipidémies, pour les patients à faible risque cardiovasculaire associé, les modifications nutritionnelles peuvent souvent permettre, à elles seules, d’atteindre les objectifs thérapeutiques. Quand une thérapeutique médicamenteuse est indiquée, il s’agit le plus souvent d’une statine, sauf dans les trois circonstances suivantes : intolérance aux statines, contre-indications aux statines (grossesse et intolérance à l’un des composés du traitement) et hypertriglycéridémie isolée (TG > 4 g/L). Les fibrates ne doivent pas être utilisés en première intention dans les hypercholestérolémies pures ou mixtes.
La diététique entre dans un contexte plus ample représenté par le mode de vie. C’est pour cela que les recommandations sur la diététique sont toujours incomplètes si elles ne sont pas associées à d’autres conseils concernant d’autres comportements à risque.
Les recommandations diététiques doivent prendre en compte les habitudes locales. Elles reposent sur une alimentation variée, avec un apport en calories adapté pour éviter la prise de poids. Il est toujours recommandé de consommer des fruits, légumes, légumineuses, noix (au sens large), produits céréaliers complets et poissons. Les acides gras saturés doivent être diminués (drastiquement), avec un apport correspondant à moins de 7 % des calories au profit des acides gras insaturés. Le cholestérol alimentaire doit être réduit à moins de 300 mg/j. Les graisses trans (acides gras insaturés) doivent aussi être réduites.
La consommation de sel doit être réduite à moins de 5 g/j, avec une réduction du sel de table et des aliments riches en sel (en France, pain, fromages, charcuterie et conserves).
Pour ceux qui consomment de l’alcool, il ne faut pas dépasser 10-20 g chez les femmes et 20-30 g chez les hommes. En cas d’hypertriglycéridémie, il est souhaitable de s’abstenir.
Les boissons sucrées et les produits avec sucres ajoutés doivent être limités.
L’activité physique doit être encouragée (sur la base de 30 min/j).
Le tabac doit être proscrit.
Un sommaire de ces recommandations est présenté dans les tableaux ci-dessous (tableaux 3 et 4).
Les principales classes de médicaments utilisées dans la prise en charge des différentes dyslipidémies sont (
- les statines (simvastatine, atorvastatine, pravastatine, fluvastatine et rosuvastatine), inhibition de la synthèse intrahépatique du cholestérol ;
- les résines (cholestyramine), inhibition de l’absorption du cholestérol alimentaire ;
- l’ézétimibe, inhibition de l’absorption intestinale du cholestérol ;
- les anticorps anti-PCSK9 (alirocumab, évolocumab), inhibiteurs de la dégradation du LDL-R ;
- les fibrates (fénofibrate, bézafibrate, ciprofibrate, gemfibrozil), activateurs de PPAR-α ;
- d’autres médicaments sont disponibles dans certaines maladies rares des lipides (sébélipase alfa, lomitapide, acide bempédoïque, volanesorsen, évinacumab).
En prévention primaire
Les conseils nutritionnels seront proposés en première intention. Ils seront poursuivis même si l’objectif thérapeutique est atteint.
Si l’objectif thérapeutique n’est pas atteint, une thérapeutique médicamenteuse visant à obtenir une diminution supplémentaire du LDL-c doit être instituée, en complément de ces modifications.
En prévention secondaire
Le traitement médicamenteux doit être institué d’emblée, associé aux modifications nutritionnelles et à la prise en charge des autres facteurs de risque (tabagisme, surpoids, sédentarité…).
Tous les médicaments, à l’exception des résines chélatrices des acides biliaires, sont contre-indiqués en cas de grossesse.
Une bithérapie peut être nécessaire en deuxième intention chez certains patients à haut risque. En fonction de l’anomalie lipidique résiduelle sous monothérapie sont possibles :
- pour diminuer le LDL-c : statine + ézétimibe ;
- pour diminuer les TG : statine + fibrate à l’exclusion du gemfibrozil.
L’association de plusieurs hypolipémiants appartenant à la même classe pharmacologique est illogique et potentiellement dangereuse.
L’association statine + fénofibrate, déconseillée en routine, peut se discuter après avis spécialisé. Elle nécessite une surveillance clinique et biologique régulière et rigoureuse.
La combinaison gemfibrozil + statine est formellement contre-indiquée.
POINTS FORTS À RETENIR
Il faut distinguer les hyperlipémies primaires et secondaires.
Le LDL-c est la principale lipoprotéine athérogène et est la cible thérapeutique.
La stratégie thérapeutique repose sur l’évaluation du risque cardiovasculaire à dix ans.
Les règles hygiénodiététiques sont la base du traitement et souvent permettent de rétablir un bilan lipidique normal.
Les statines sont les traitements de première intention. Elles sont contre-indiquées en cas de grossesse.
Le taux de triglycérides supérieurs à 10 g/L expose au risque de pancréatite aiguë.
Mach F, Baigent C, Catapano AL, et al.; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J 2020 Jan 1;41(1):111-88. doi: 10.1093/eurheartj/ehz455. Erratum in: Eur Heart J 2020 Nov 21;41(44):4255. PMID: 31504418.
Dans cet article
- Importance de l’évaluation du risque cardiovasculaire global (rang A)
- Dyslipidémies
- Définition et classification des dyslipidémies (rang A)
- Dyslipidémies secondaires (rang A)
- Complications des dyslipidémies (rang B)
- Diagnostic positif d’une dyslipidémie (rang A)
- Les recommandations sur la prise en charge des dyslipidémies (rang A)
- Traitement

 Encadrés
Encadrés