L’incontinence anale se définit communément comme la perte incontrôlée de selles et/ou de gaz. Récemment, des conférences d’experts ont proposé d’élargir la définition également aux urgences, c’est-à-dire à l’incapacité de se retenir de façon suffisante pour différer l’évacuation. En effet, cette situation qui impose au patient de se précipiter à la selle et de renoncer à une vie sociale normale a le même retentissement sur la qualité de vie que la présence de fuites authentiques.1
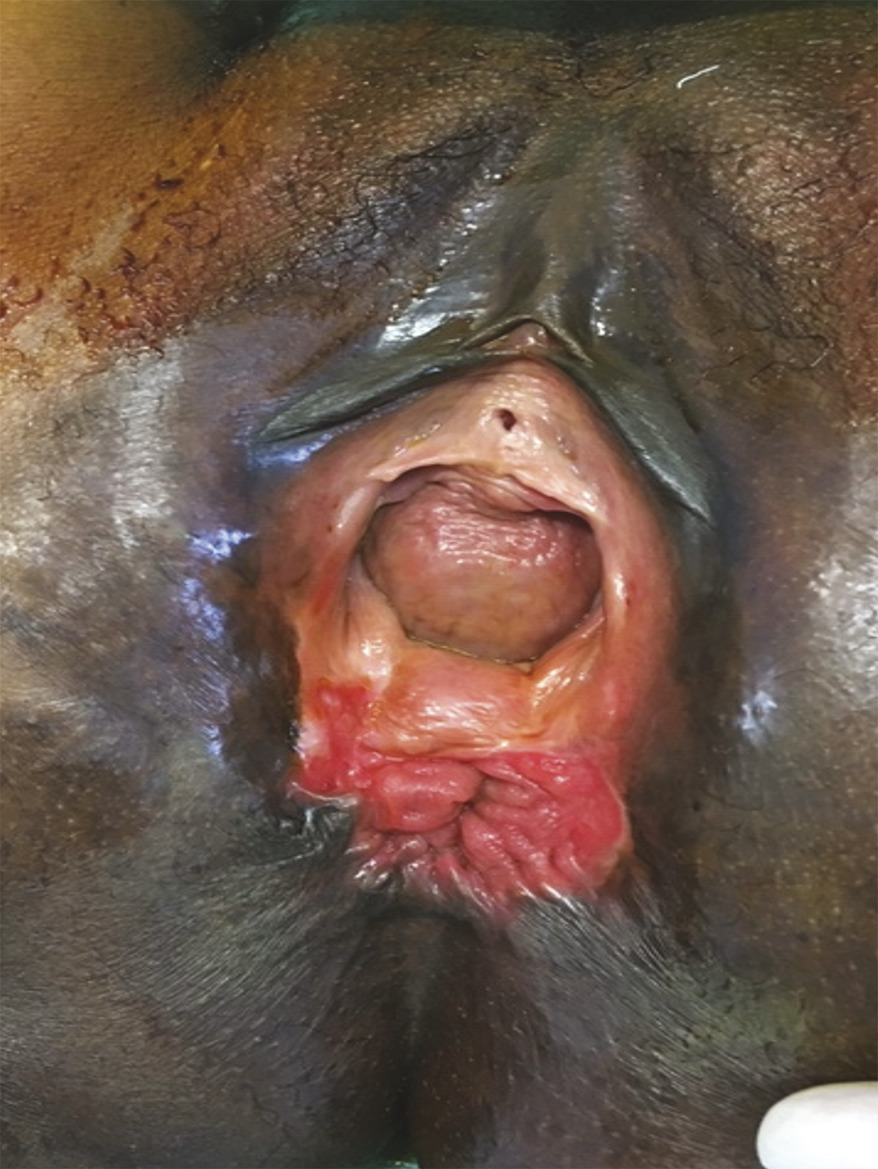
Les causes d’incontinence sont variées, impliquant les défaillances du muscle sphinctérien (fig. 1 ) et de la musculature périnéale, les anomalies fonctionnelles du rectum et les causes neurologiques. Ces atteintes sont souvent combinées, et il est rare qu’une cause unique soit identifiée. C’est le caractère multifactoriel de la majorité des cas d’incontinence anale qui rend difficiles un diagnostic et un traitement uniforme.
La prise en charge thérapeutique a pourtant bénéficié de nombreux progrès ces dernières années. Il est aujourd’hui possible d’améliorer le niveau de continence de quasiment chaque patient, mais dans une proportion qui n’est pas toujours conforme aux espoirs. C’est pourquoi il est indispensable d’évaluer avec lui le niveau d’amélioration qui sera satisfaisant. De cet entretien dépendent l’investissement des équipes et le recours aux approches plus invasives.
Les causes d’incontinence sont variées, impliquant les défaillances du muscle sphinctérien (
La prise en charge thérapeutique a pourtant bénéficié de nombreux progrès ces dernières années. Il est aujourd’hui possible d’améliorer le niveau de continence de quasiment chaque patient, mais dans une proportion qui n’est pas toujours conforme aux espoirs. C’est pourquoi il est indispensable d’évaluer avec lui le niveau d’amélioration qui sera satisfaisant. De cet entretien dépendent l’investissement des équipes et le recours aux approches plus invasives.
La fréquence augmente avec l’âge
Il n’est pas facile de donner des chiffres précis de prévalence de l’incontinence anale. C’est d’ailleurs un des objectifs prioritaires de nombreux programmes de recherche. Plusieurs travaux récents ont ainsi permis de préciser ces chiffres. On estime que, dans la population générale, la prévalence de l’incontinence anale est de 7 à 15 %, chez les femmes comme chez les hommes.2,3 Cette fréquence augmente de façon significative lorsqu’on cible des populations plus âgées, en institution. Les pathologies proctologiques sont donc fréquentes, d’autant que le tabou tombe progressivement et que les patients consultent de plus en plus facilement.
Retentissement socio-économique
Plusieurs études ont évalué le coût que représente l’incontinence anale pour les patients : elle coûte au patient 4 000 dollars par an (environ 3 763 euros) pour une population américaine, et 3 500 dollars (environ 3 279 euros) par an pour une population néerlandaise.4,5
Lorsqu’on inclut le coût des traitements chirurgicaux innovants, l’évaluation médico-économique est plus complexe car il est difficile de prendre en compte tous les paramètres, y compris les économies engendrées par l’amélioration des patients. Une étude a évalué le surcoût lié au recours aux thérapies innovantes, comme la neuromodulation sacrée. Le surcoût a été évalué à 35 000 dollars (environ 32 798 euros).6 Ces données récentes sont à mettre en perspective afin de prévoir les investissements nécessaires pour garantir aux patients l’accès aux soins innovants pour les années à venir.
Lorsqu’on inclut le coût des traitements chirurgicaux innovants, l’évaluation médico-économique est plus complexe car il est difficile de prendre en compte tous les paramètres, y compris les économies engendrées par l’amélioration des patients. Une étude a évalué le surcoût lié au recours aux thérapies innovantes, comme la neuromodulation sacrée. Le surcoût a été évalué à 35 000 dollars (environ 32 798 euros).6 Ces données récentes sont à mettre en perspective afin de prévoir les investissements nécessaires pour garantir aux patients l’accès aux soins innovants pour les années à venir.
Approches conservatrices en premier lieu
Le traitement de l’incontinence anale repose d’abord sur des approches conservatrices, qui constituent toujours la première étape du traitement, quelle que soit l’origine de l’incontinence.
Régime alimentaire personnalisé
Dans ce cadre, le régime alimentaire est essentiel, puisqu’il influence la consistance des selles. Il est cependant difficile aujourd’hui de recommander tel ou tel régime standardisé (riche en fibres, FODMAP [fermentable oligosaccharides, disaccharides, monosaccharides and polyols]…) qui serait adapté à chacun. Il est probable que la variation de la consistance des selles dans la population générale soit telle qu’il faille adapter à chaque patient le régime alimentaire. Une récente étude a évalué l’impact du régime alimentaire selon le niveau social des patients. Elle a montré qu’une alimentation estimée de plus bas niveau socio-économique (plus riche en sucres et aliments transformés) était associée à davantage d’incontinence anale.7
Neurostimulation tibiale : effet retardé
Parmi les traitements récents et non invasifs, la neurostimulation tibiale a fait l’objet de très nombreuses études, dont certaines randomisées. Le principe de ce traitement est d’administrer au niveau de la cheville un courant électrique à proximité du nerf tibial postérieur. Le mode d’action est encore hypothétique, mais il repose sur la stimulation nerveuse des nerfs pelviens (via le nerf tibial), permettant ainsi d’améliorer la continence par voie neurologique. Les résultats sont débattus dans la littérature, notamment en raison de l’importance de l’effet placebo dans les groupes contrôles. À lui seul, l’effet placebo compte en effet pour environ 30 % de l’effet thérapeutique dans l’incontinence anale.
Une récente méta-analyse des essais randomisés a toutefois permis d’affiner les différences en poolant les effectifs des études publiées.8 Il ressort que cette approche a très probablement un effet qui surpasse l’effet placebo. Ce traitement, remboursé par la Sécurité sociale, se prescrit pour une durée de trois mois initialement, renouvelable ensuite. Les effets sont souvent retardés de plusieurs semaines, et il est important d’informer les patients de ces délais. Dans la plupart des études, les séances sont quotidiennes (de 15 à 20 minutes par jour). Elles peuvent être effectuées à la maison en cas de stimulation percutanée.
Il existe une alternative transcutanée au cours de laquelle une aiguille est implantée au niveau du nerf tibial postérieur. Dans ce cas, le patient ne peut pas réaliser les séances seul. Et la mise en place de l’électrode est effectuée par un soignant. Ce dispositif est plus évalué dans la littérature, mais non disponible actuellement en France.
Une récente méta-analyse des essais randomisés a toutefois permis d’affiner les différences en poolant les effectifs des études publiées.8 Il ressort que cette approche a très probablement un effet qui surpasse l’effet placebo. Ce traitement, remboursé par la Sécurité sociale, se prescrit pour une durée de trois mois initialement, renouvelable ensuite. Les effets sont souvent retardés de plusieurs semaines, et il est important d’informer les patients de ces délais. Dans la plupart des études, les séances sont quotidiennes (de 15 à 20 minutes par jour). Elles peuvent être effectuées à la maison en cas de stimulation percutanée.
Il existe une alternative transcutanée au cours de laquelle une aiguille est implantée au niveau du nerf tibial postérieur. Dans ce cas, le patient ne peut pas réaliser les séances seul. Et la mise en place de l’électrode est effectuée par un soignant. Ce dispositif est plus évalué dans la littérature, mais non disponible actuellement en France.
Irrigations coliques : amélioration de la qualité de vie
Les irrigations coliques sont aussi un traitement non invasif de l’incontinence anale,9 popularisé au cours des dix dernières années. Avec le développement de dispositifs dédiés incluant une canule avec ballonnet et un dispositif d’auto-administration de lavement, ce traitement est tout à fait adapté aux patients souffrant d’incontinence anale. Plusieurs publications ont ainsi rapporté une amélioration très significative de la qualité de vie des patients qui suivent ce traitement. Le principal inconvénient est la contrainte imposée par la réalisation, quotidienne le plus souvent, des irrigations. C’est la raison pour laquelle certains patients renoncent (environ 20 %). Néanmoins, et en particulier lorsque les patients ont un transit plutôt solide, voire constipé, et des difficultés de vidange du rectum, cette option peut représenter une solution durable.
Approches thérapeutiques interventionnelles
Essor de la neuromodulation sacrée
La neuromodulation sacrée est aujourd’hui au centre de la prise en charge de l’incontinence anale. Apparue depuis la fin des années 1990, elle a progressivement démontré son innocuité et son efficacité pour améliorer la continence anale, quelle qu’en soit la cause. Ainsi, même en cas de lésion sphinctérienne authentique, la neuromodulation peut améliorer les patients aussi bien que la chirurgie de réparation sphinctérienne.10 En France, ce traitement est pris en charge par la Sécurité sociale et comprend deux phases.
La première étape consiste en la réalisation d’un test temporaire d’une durée de deux à trois semaines. En hospitalisation de jour, une électrode est implantée au niveau du sacrum sous anesthésie, puis reliée à un boîtier de stimulation temporaire. Le patient regagne son domicile avec ce stimulateur temporaire.
Si la fréquence des fuites diminue d’au moins 50 %, lors d’une seconde étape, un boîtier permanent est implanté sous anesthésie locale au niveau de la fosse lombaire.
Un registre français créé depuis plus de quinze ans (groupe NEMO : neuromodulation sacrée) a récemment rapporté les résultats à long terme de ce traitement chez des patients implantés depuis plus de dix ans.11 Cette publication confirme le caractère durable et efficace de la neuromodulation. Il est toutefois nécessaire de suivre les patients (plusieurs révisions sont nécessaires pour changer les pacemakers, dont la durée de vie est d’environ cinq ans). Une autre publication sur un registre français prospectif constitué à la demande des tutelles pour une durée de trois ans a également démontré la faible morbidité et l’efficacité du traitement sur les urgences et les fuites des patients.12
La première étape consiste en la réalisation d’un test temporaire d’une durée de deux à trois semaines. En hospitalisation de jour, une électrode est implantée au niveau du sacrum sous anesthésie, puis reliée à un boîtier de stimulation temporaire. Le patient regagne son domicile avec ce stimulateur temporaire.
Si la fréquence des fuites diminue d’au moins 50 %, lors d’une seconde étape, un boîtier permanent est implanté sous anesthésie locale au niveau de la fosse lombaire.
Un registre français créé depuis plus de quinze ans (groupe NEMO : neuromodulation sacrée) a récemment rapporté les résultats à long terme de ce traitement chez des patients implantés depuis plus de dix ans.11 Cette publication confirme le caractère durable et efficace de la neuromodulation. Il est toutefois nécessaire de suivre les patients (plusieurs révisions sont nécessaires pour changer les pacemakers, dont la durée de vie est d’environ cinq ans). Une autre publication sur un registre français prospectif constitué à la demande des tutelles pour une durée de trois ans a également démontré la faible morbidité et l’efficacité du traitement sur les urgences et les fuites des patients.12
Chirurgie de réparation sphinctérienne indiquée dans les ruptures post-obstétricales
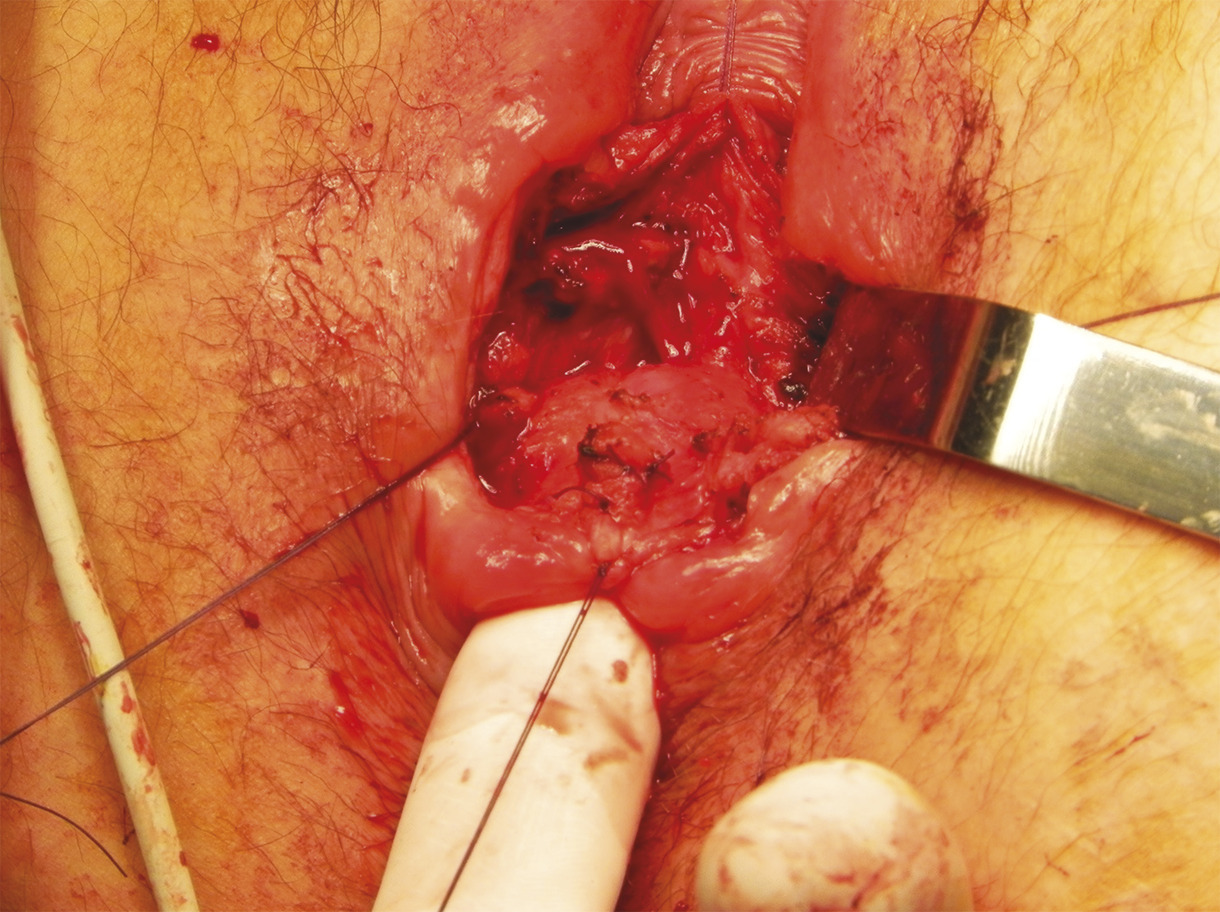
La chirurgie de réparation reste toujours d’actualité pour les cas précis (qui ne sont pas les plus fréquents) de rupture sphinctérienne post-obstétricale.13 Dans ces situations, la réparation sphinctérienne peut transformer le quotidien des patientes, qui sont souvent jeunes et traumatisées par cette complication de l’accouchement (fig. 2 ). Avec le temps toutefois, le résultat tend à s’amenuiser, et après cinq ans, la moitié des patientes ressentent de nouveau des troubles de la continence. Il est alors possible de réopérer ou de mettre en place des traitements différents, comme la neuromodulation sacrée.
Récemment, il a été mis en évidence d’autres lésions possibles au niveau du muscle puborectal, qu’une évaluation échographique peut mettre en évidence et qui est aussi accessible à une réparation. Les résultats sont encore préliminaires, et les séries ont des effectifs assez limités, mais cette approche opératoire de reconstruction du muscle puborectal (uni- ou bilatérale) peut être complémentaire et potentialiser les effets d’une réparation sphinctérienne.14
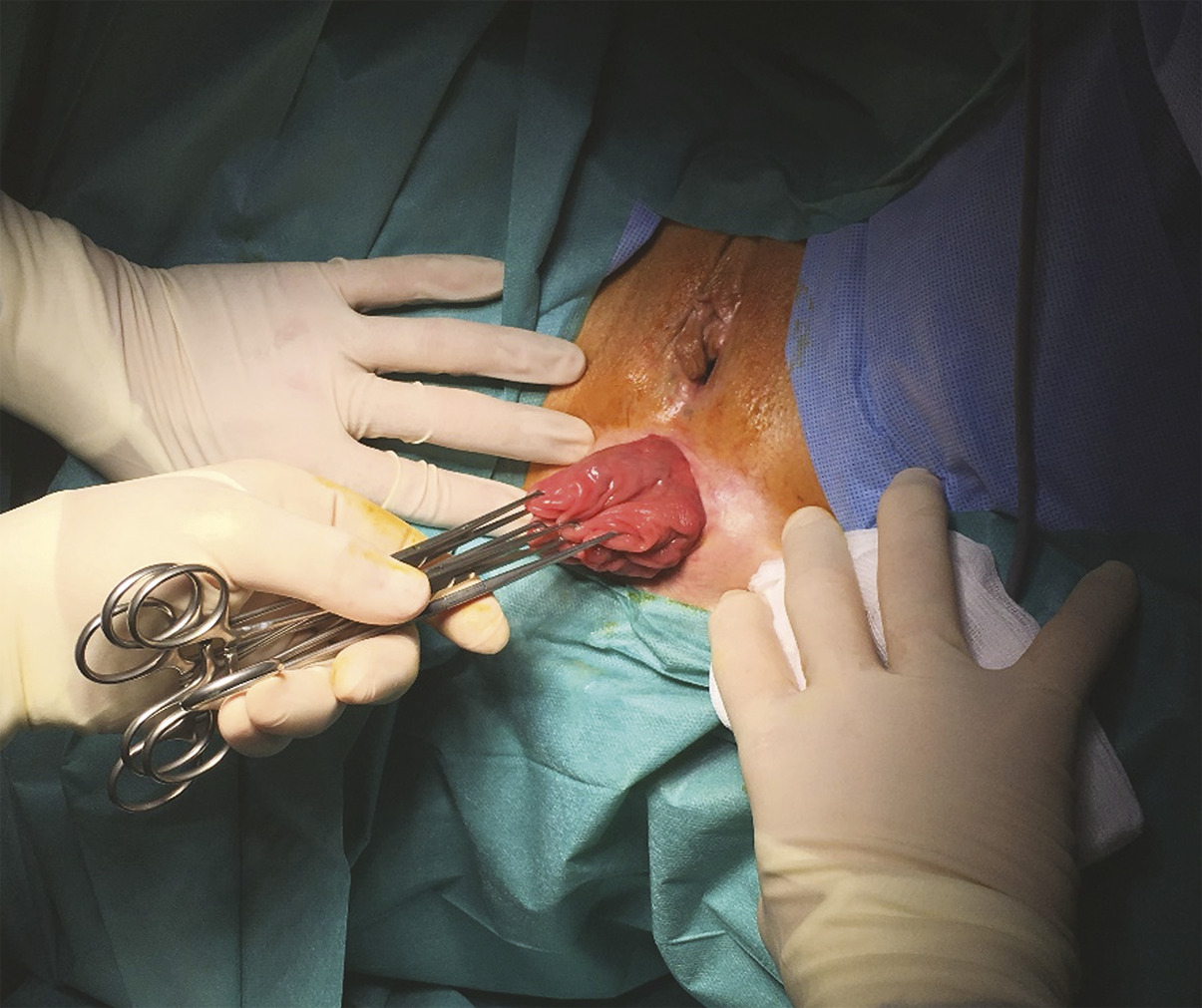
On sait enfin que la chirurgie des troubles de la statique pelvienne et en particulier le prolapsus du compartiment postérieur a un effet positif sur la continence (fig. 3 ). C’est surtout la rectopexie par voie abdominale laparoscopique qui a été évaluée15, avec un recul suffisant pour valider la recherche systématique d’un trouble de la statique pelvienne chez les patientes souffrant d’incontinence anale.
Récemment, il a été mis en évidence d’autres lésions possibles au niveau du muscle puborectal, qu’une évaluation échographique peut mettre en évidence et qui est aussi accessible à une réparation. Les résultats sont encore préliminaires, et les séries ont des effectifs assez limités, mais cette approche opératoire de reconstruction du muscle puborectal (uni- ou bilatérale) peut être complémentaire et potentialiser les effets d’une réparation sphinctérienne.14
On sait enfin que la chirurgie des troubles de la statique pelvienne et en particulier le prolapsus du compartiment postérieur a un effet positif sur la continence (
Plusieurs techniques opératoires débattues
Sphincter artificiel
Le sphincter artificiel est une approche opératoire peu invasive, développée au cours des années 1990, avec des espoirs importants pour les patients avec une incontinence anale liée à une défaillance sphinctérienne. Deux dispositifs ont été implantés en France : la manchette de silicone reliée à une pompe et un ballonnet dérivé du sphincter urinaire artificiel ; puis l’anneau magnétique.16,17 Ces deux dispositifs ne sont plus disponibles aujourd’hui. Les résultats étaient pourtant prometteurs et satisfaisants pour certains patients, mais le nombre limité de patients implantés et la nécessité de révisions chirurgicales au cours du suivi ont finalement conduit les fabricants à interrompre la commercialisation des dispositifs.Lambeaux musculaires
La chirurgie de reconstruction plus invasive avec les lambeaux musculaires (graciloplastie dynamisée) est aujourd’hui une chirurgie d’exception.18 Elle expose le patient à une morbidité plus significative. Les résultats dans une population hypersélectionnée sont plutôt bons, mais cette approche doit être réservée aux patients informés des risques et pour qui toute alternative (et en particulier la stomie) semble inenvisageable.Recherches sur les cellules souches
Depuis plusieurs années, il existe de nombreux projets d’injections de cellules souches pour coloniser le sphincter et reconstituer la continence anale.19 Dans une revue récente, une synthèse de ces avancées, encore du domaine de la recherche, démontre à quel point cette approche suscite des espoirs. Dans ce domaine, et parmi l’ensemble des injections intrasphinctériennes qui ont pu être testées, les cellules souches incarnent l’avenir des traitements innovants du sphincter défaillant.
Stomie en dernier recours
Pour les patients qui, malgré les efforts, restent gênés, la stomie représente toujours une option. Les progrès réalisés dans les appareillages permettent aujourd’hui aux patients d’envisager une vie proche de la normale.20
Recommandations des sociétés savantes
Il existe actuellement de nombreuses recommandations établies par les sociétés savantes : celles de la Société nationale française de colo-proctologie ont été éditées en 2014 ; plus récemment, en 2021, la Société européenne de coloproctologie a publié de nouvelles recommandations qui reprennent le bilan et la prise en charge thérapeutique.22
La première étape est toujours conservatrice et le bilan souvent limité à un examen endoscopique. La mise en place d’une gestion diététique et d’un traitement médical freinateur associés à la rééducation est alors recommandée. Cette rééducation, qui n’a pas été abordée dans cet article sur les avancées récentes dans le traitement de l’incontinence, garde toutefois toute sa place, et la preuve de son efficacité est connue de longue date. Cette dernière est multimodale, et inclut souvent du biofeedback. Les kinésithérapeutes/rééducateurs connaissent aujourd’hui bien ces méthodes.23
C’est en cas d’échec que deux approches peuvent être discutées avec le patient : une approche non invasive avec les irrigations coliques et la stimulation tibiale ; et une approche plus invasive avec la neuromodulation sacrée et les gestes chirurgicaux. Ces recommandations insistent surtout sur la nécessité de diagnostiquer l’incontinence anale, car, aujourd’hui, c’est le principal obstacle à l’accès aux soins.
La première étape est toujours conservatrice et le bilan souvent limité à un examen endoscopique. La mise en place d’une gestion diététique et d’un traitement médical freinateur associés à la rééducation est alors recommandée. Cette rééducation, qui n’a pas été abordée dans cet article sur les avancées récentes dans le traitement de l’incontinence, garde toutefois toute sa place, et la preuve de son efficacité est connue de longue date. Cette dernière est multimodale, et inclut souvent du biofeedback. Les kinésithérapeutes/rééducateurs connaissent aujourd’hui bien ces méthodes.23
C’est en cas d’échec que deux approches peuvent être discutées avec le patient : une approche non invasive avec les irrigations coliques et la stimulation tibiale ; et une approche plus invasive avec la neuromodulation sacrée et les gestes chirurgicaux. Ces recommandations insistent surtout sur la nécessité de diagnostiquer l’incontinence anale, car, aujourd’hui, c’est le principal obstacle à l’accès aux soins.
Références
1. Bharucha AE, Dunivan G, Goode PS, Lukacz ES, Markland AD, Matthews CA, et al. Epidemiology, pathophysiology, and classification of fecal incontinence: State of the science summary for the National Institute of Diabetes and Digestive and Kidney Diseases (NIDDK) workshop. Am J Gastroenterol 2015;110(1):127-36.
2. Perry S, Shaw C, McGrother C, Matthews RJ, Assassa RP, Dallosso H, et al. Prevalence of faecal incontinence in adults aged 40 years or more living in the community. Gut 2002;50(4):480-4.
3. Whitehead WE, Borrud L, Goode PS, Meikle S, Mueller ER, Tuteja A, et al. Fecal incontinence in US adults: Epidemiology and risk factors. Gastroenterology 2009;137(2):512-7.
4. Deutekom M, Dobben AC, Dijkgraaf MGW, Terra MP, Stoker J, Bossuyt PMM. Costs of outpatients with fecal incontinence. Scand J Gastroenterol 2005;40(5):552-8.
5. Xu X, Menees SB, Zochowski MK, Fenner DE. Economic cost of fecal incontinence. Dis Colon Rectum 2012;55(5):586-98.
6. Hetzer FH, Bieler A, Hahnloser D, Löhlein F, Clavien PA, Demartines N. Outcome and cost analysis of sacral nerve stimulation for faecal incontinence. Br J Surg 2006;93(11):1411-7.
7. Okada C, Kim JI, Melamed ML, Abraham N, Halani PK. The relationship between fecal incontinence and food insecurity in US women: An analysis of 2005-2010 National Health and Nutrition Examination Survey (NHANES). Am J Obstet Gynecol 2022:S0002-9378(22)02267-0.
8. Qi Jin, Ying Zhu, Ping Yin, Xiaojia Li. Tibial nerve electrical stimulation for fecal incontinence: A systematic review and meta‑analysis Updates Surg 2022. Online.
9. Vollebregt PF, Elfrink AKE, Meijerink WJHJ, Felt-Bersma RJF. Results of long-term retrograde rectal cleansing in patients with constipation or fecal incontinence. Tech Coloproctol 2016;20(9):633-9.
10. Ong K, Bordeianou L, Brunner M, Buntzen S, Collie MHS, Hanly Al. Changing paradigm of sacral neuromodulation and external anal sphincter repair for faecal incontinence in specialist centres. Colorectal Dis 2021;23(3):710-5.
11. Desprez C, Damon H, Meurette G, Mege D, Faucheron JL, Brochard C. Ten-year evaluation of a large retrospective cohort treated by sacral nerve modulation for fecal incontinence: Results of a french multicenter study. Ann Surg 2022;275(4):735-42.
12. Meurette G, Siproudhis L, Leroi AM, Damon H, Keller DUJ, Faucheron JL, et al. Sacral neuromodulation with the InterStim™ system for faecal incontinence: Results from a prospective French multicentre observational study. French Faecal Registry Study Group. Colorectal Dis 2021;23(6):1463-73.
13. Venara A, Brochard C, Fritel X, Bridoux V, Abramowitz L, Legendre G, et al. Management of obstetrical injuries to the anal sphincter: A survey of French current practice and perceptions according to the specialties. J Visc Surg 2021;158(5):378-84.
14. Alketbi MSG, Meyer J, Robert-Yap J, Scarpa R, Gialamas E, Abbassi Z, et al. Levator ani and puborectalis muscle rupture: Diagnosis and repair for perineal instability. Tech Coloproctol 2021;25(8):923-33.
15. Rogier-Mouzelas F, Drissi F, Podevin J, Duchalais E, Meurette G. Anatomic and functional results of ventral biological mesh rectopexy for posterior pelvic floor disorders. J Visc Surg 2022:S1878-7886(22)00149-7.
16. Wong MT, Meurette G, Wyart V, Glemain P, Lehur PA. The artificial bowel sphincter: A single institution experience over a decade. Ann Surg 2011;254(6):951-6.
17. Wong MTC, Meurette G, Stangherlin P, Lehur PA. The magnetic anal sphincter versus the artificial bowel sphincter: A comparison of 2 treatments for fecal incontinence. Dis Colon Rectum 2011;54(7):773-9.
18. Garoufalia Z, Gefen R, Emile SH, Silva-Alvarenga E, Freund MR, Horesh N, et al. Outcomes of graciloplasty in the treatment of fecal incontinence: A systematic review and meta-analysis of the literature. Tech Coloproctol 2022. Online.
19. Balaphas A, Meyer J, Meier RPH, Liot E, Buchs NC, Roche B, et al. Cell therapy for anal sphincter incontinence: Where do we stand? Cells 2021;10(8):2086.
20. Skibsted CV, Jensen BT, Juul T, Kristensen HO. Patient reported outcome measures assessing quality of life in patients with an intestinal stoma: A systematic review. Kristensen HØ. Colorectal Dis 2022;24(10):1128-39.
21. Vitton V, Soudan D, Siproudhis L, Abramowitz L, Bouvier M, Faucheron JL, et al; French National Society of Coloproctology. Treatments of faecal incontinence: Recommendations from the French national society of coloproctology. Colorectal Dis 2014;16(3):159-66.
22. Assmann SL, Keszthelyi D, Kleijnen J, Anatasiou F, Bradshaw E, Brannigan AE, et al. Guideline for the diagnosis and treatment of Faecal Incontinence-A UEG/ESCP/ESNM/ESPCG collaboration. United European Gastroenterol J 2022;10(3):251-86.
23. Bialy A, Kolomanska D, Oplawski M, Tim S. Physiotherapy for prevention and treatment of fecal incontinence in women, systematic review of methods. J Clin Med 2020;9(10):3255.
2. Perry S, Shaw C, McGrother C, Matthews RJ, Assassa RP, Dallosso H, et al. Prevalence of faecal incontinence in adults aged 40 years or more living in the community. Gut 2002;50(4):480-4.
3. Whitehead WE, Borrud L, Goode PS, Meikle S, Mueller ER, Tuteja A, et al. Fecal incontinence in US adults: Epidemiology and risk factors. Gastroenterology 2009;137(2):512-7.
4. Deutekom M, Dobben AC, Dijkgraaf MGW, Terra MP, Stoker J, Bossuyt PMM. Costs of outpatients with fecal incontinence. Scand J Gastroenterol 2005;40(5):552-8.
5. Xu X, Menees SB, Zochowski MK, Fenner DE. Economic cost of fecal incontinence. Dis Colon Rectum 2012;55(5):586-98.
6. Hetzer FH, Bieler A, Hahnloser D, Löhlein F, Clavien PA, Demartines N. Outcome and cost analysis of sacral nerve stimulation for faecal incontinence. Br J Surg 2006;93(11):1411-7.
7. Okada C, Kim JI, Melamed ML, Abraham N, Halani PK. The relationship between fecal incontinence and food insecurity in US women: An analysis of 2005-2010 National Health and Nutrition Examination Survey (NHANES). Am J Obstet Gynecol 2022:S0002-9378(22)02267-0.
8. Qi Jin, Ying Zhu, Ping Yin, Xiaojia Li. Tibial nerve electrical stimulation for fecal incontinence: A systematic review and meta‑analysis Updates Surg 2022. Online.
9. Vollebregt PF, Elfrink AKE, Meijerink WJHJ, Felt-Bersma RJF. Results of long-term retrograde rectal cleansing in patients with constipation or fecal incontinence. Tech Coloproctol 2016;20(9):633-9.
10. Ong K, Bordeianou L, Brunner M, Buntzen S, Collie MHS, Hanly Al. Changing paradigm of sacral neuromodulation and external anal sphincter repair for faecal incontinence in specialist centres. Colorectal Dis 2021;23(3):710-5.
11. Desprez C, Damon H, Meurette G, Mege D, Faucheron JL, Brochard C. Ten-year evaluation of a large retrospective cohort treated by sacral nerve modulation for fecal incontinence: Results of a french multicenter study. Ann Surg 2022;275(4):735-42.
12. Meurette G, Siproudhis L, Leroi AM, Damon H, Keller DUJ, Faucheron JL, et al. Sacral neuromodulation with the InterStim™ system for faecal incontinence: Results from a prospective French multicentre observational study. French Faecal Registry Study Group. Colorectal Dis 2021;23(6):1463-73.
13. Venara A, Brochard C, Fritel X, Bridoux V, Abramowitz L, Legendre G, et al. Management of obstetrical injuries to the anal sphincter: A survey of French current practice and perceptions according to the specialties. J Visc Surg 2021;158(5):378-84.
14. Alketbi MSG, Meyer J, Robert-Yap J, Scarpa R, Gialamas E, Abbassi Z, et al. Levator ani and puborectalis muscle rupture: Diagnosis and repair for perineal instability. Tech Coloproctol 2021;25(8):923-33.
15. Rogier-Mouzelas F, Drissi F, Podevin J, Duchalais E, Meurette G. Anatomic and functional results of ventral biological mesh rectopexy for posterior pelvic floor disorders. J Visc Surg 2022:S1878-7886(22)00149-7.
16. Wong MT, Meurette G, Wyart V, Glemain P, Lehur PA. The artificial bowel sphincter: A single institution experience over a decade. Ann Surg 2011;254(6):951-6.
17. Wong MTC, Meurette G, Stangherlin P, Lehur PA. The magnetic anal sphincter versus the artificial bowel sphincter: A comparison of 2 treatments for fecal incontinence. Dis Colon Rectum 2011;54(7):773-9.
18. Garoufalia Z, Gefen R, Emile SH, Silva-Alvarenga E, Freund MR, Horesh N, et al. Outcomes of graciloplasty in the treatment of fecal incontinence: A systematic review and meta-analysis of the literature. Tech Coloproctol 2022. Online.
19. Balaphas A, Meyer J, Meier RPH, Liot E, Buchs NC, Roche B, et al. Cell therapy for anal sphincter incontinence: Where do we stand? Cells 2021;10(8):2086.
20. Skibsted CV, Jensen BT, Juul T, Kristensen HO. Patient reported outcome measures assessing quality of life in patients with an intestinal stoma: A systematic review. Kristensen HØ. Colorectal Dis 2022;24(10):1128-39.
21. Vitton V, Soudan D, Siproudhis L, Abramowitz L, Bouvier M, Faucheron JL, et al; French National Society of Coloproctology. Treatments of faecal incontinence: Recommendations from the French national society of coloproctology. Colorectal Dis 2014;16(3):159-66.
22. Assmann SL, Keszthelyi D, Kleijnen J, Anatasiou F, Bradshaw E, Brannigan AE, et al. Guideline for the diagnosis and treatment of Faecal Incontinence-A UEG/ESCP/ESNM/ESPCG collaboration. United European Gastroenterol J 2022;10(3):251-86.
23. Bialy A, Kolomanska D, Oplawski M, Tim S. Physiotherapy for prevention and treatment of fecal incontinence in women, systematic review of methods. J Clin Med 2020;9(10):3255.