Diagnostiquer une insuffisance cardiaque chez l’adulte. Identifier les situations d’urgence et planifier leur prise en charge. Argumenter l’attitude thérapeutique et planifier le suivi du patient.
Introduction
L’insuffisance cardiaque est une cause de morbi-mortalité majeure dans les pays développés, touchant 1 à 3 % de la population adulte et plus de 10 % des plus de 70 ans, soit plus de 1 million de personnes en France. Chaque année, en France, plus de 70 000 patients décèdent d’insuffisance cardiaque.
L’insuffisance cardiaque peut être secondaire à une pathologie directe du myocarde, mais une atteinte coronarienne, valvulaire, hypertensive, péricardique, congénitale ou rythmique (cardiomyopathie liée à une fibrillation atriale rapide par exemple) peut également en être la cause. Son pronostic est directement corrélé à la symptomatologie.
Physiopathologie
Débit cardiaque
Le VES correspond à la différence entre les volumes télédiastolique et télésystolique du ventricule gauche. Il dépend :
- de la précharge : remplissage du ventricule gauche, fonction de la volémie, de la fonction ventriculaire droite et de la capacité de relaxation du ventricule gauche (fonction diastolique) ;
- de la post-charge : forces s’opposant à l’éjection du ventricule gauche (comme par exemple l’hypertension artérielle ou un rétrécissement aortique) ;
- de l’inotropisme ventriculaire, c’est-à-dire la contractilité ventriculaire (fonction systolique).
La fraction d’éjection du ventricule gauche (FEVG) correspond au rapport du volume d’éjection systolique sur le volume télédiastolique du ventricule gauche. Il reflète donc la proportion du volume télédiastolique éjecté dans l’aorte en systole. La fraction d’éjection est le paramètre le plus utilisé pour caractériser la fonction systolique.
En cas d’insuffisance cardiaque, il existe des mécanismes de compensation physiologiques cardiaques (= remodelage cardiaque) et extracardiaques (hormonaux).
Remodelage cardiaque
- une dilatation ventriculaire, afin d’augmenter le volume télédiastolique et donc maintenir un VES stable. Cette dilatation du ventricule gauche (l’étirement des fibres musculaires) entraîne une augmentation de l’inotropisme (loi de Frank-Starling), du moins jusqu’à un certain degré de dilatation ;
- une hypertrophie ventriculaire (loi de Laplace) : la tension sur les parois (pression intracavitaire contre laquelle les myocytes doivent lutter pour se contracter) augmente avec la dilatation du cœur. Une augmentation de la tension pariétale entraîne donc une hypertrophie concentrique compensatoire.
- une dilatation trop importante du ventricule gauche diminue alors son inotropisme et le débit cardiaque ;
- une hypertrophie ventriculaire trop importante entraînera une augmentation de la rigidité des parois et donc une altération de la fonction de relaxation et de remplissage (dysfonction diastolique).
Mécanismes d’adaptation extracardiaques
Augmentation de la sécrétion de rénine : secondaire à la diminution du débit sanguin artériel rénal par la diminution du débit cardiaque. Elle va stimuler, d’une part, la production d’angiotensine II (puissant vasoconstricteur périphérique, majorant la post-charge) et, d’autre part, la sécrétion d’aldostérone (augmentant la réabsorption sodée rénale, donc la rétention hydrosodée et la précharge).
Activation du système sympathique : sécrétion d’adrénaline, inotrope et chronotrope positif. L’accélération de la fréquence cardiaque permet de compenser la diminution du volume d’éjection systolique, afin de maintenir le débit cardiaque.
Cette adaptation est vitale dans l’insuffisance cardiaque aiguë, mais peut à terme avoir des conséquences délétères : augmentation de la consommation énergétique du myocarde (épuisement), et diminution du temps de diastole ventriculaire par la tachycardie. L’effet des catécholamines est également épuisable du fait d’une diminution progressive du nombre de récepteurs adrénergiques.
Sécrétion de peptide B natriurétique (BNP) : par les myocytes atriaux, secondaire à une surcharge en pression ou volume des cavités cardiaques. Le BNP favorise l’excrétion sodée rénale.
Comprendre la physiologie de l’insuffisance cardiaque est indispensable pour comprendre sa prise en charge médicamenteuse :
- insuffisance cardiaque aiguë : les vasodilatateurs de type dérivés nitrés vont diminuer la précharge (par baisse de la pression veineuse centrale) et la post-charge (par baisse de la pression artérielle) ; les diurétiques de l’anse vont diminuer la précharge par baisse de la volémie (surcharge hydrosodée) ;
- insuffisance cardiaque chronique : les bêtabloquants vont lutter contre l’effet sympathique et adrénergique ; les inhibiteurs de l’enzyme de conversion de l’angiotensine (IEC) contre la production d’angiotensine II ; les diurétiques antialdostérone contre l’aldostérone ; et enfin le sacubitril qui est un inhibiteur de la néprilysine qui dégrade le BNP. Ce sont les médicaments de choix de l’insuffisance cardiaque chronique à FEVG altérée.
Insuffisance cardiaque et FEVG
Les recommandations européennes définissent la FEVG préservée > 50 % (IC-FEP) et la FEVG réduite < 40 % (IC-FER). Entre 40 et 50 %, la FEVG est dite modérément altérée.
Insuffisance cardiaque à FEVG diminuée
Il existe une altération de la fonction systolique ventriculaire gauche, avec pour conséquences une diminution du volume d’éjection systolique et une élévation des pressions de remplissage.Insuffisance cardiaque à FEVG préservée
Il existe une altération de la fonction diastolique (de remplissage) du ventricule gauche. Le volume télédiastolique s’en retrouve diminué, entraînant alors une diminution du volume d’éjection systolique et une élévation des pressions de remplissage.Cette altération de la relaxation est habituellement causée par une augmentation de la rigidité des parois du myocarde, elle-même secondaire à une hypertrophie ventriculaire gauche (hypertension artérielle, rétrécissement aortique) ou à une cardiomyopathie hypertrophique ou restrictive.
À ce jour, les thérapies médicamenteuses dans l’insuffisance cardiaque chronique n’ont montré un bénéfice de réduction de mortalité que pour la FEVG < 40 %.
Diagnostic
Signes généraux
Signes fonctionnels
- dyspnée d’effort ou de repos, orthopnée, toux à l’effort ou au décubitus, dyspnée paroxystique nocturne (par augmentation de la pression capillaire pulmonaire) ;
- asthénie ; fatigabilité musculaire ; douleur épigastrique postprandiale, difficulté à digérer et perte de poids (par diminution du débit sanguin musculaire et digestif) ;
- prise de poids (par surcharge hydrosodée).
Les signes fonctionnels pulmonaires (dyspnée) de l’insuffisance cardiaque gauche résultent d’une inondation de l’interstitium pulmonaire et des alvéoles par du transsudat. En effet, l’augmentation des pressions dans l’oreillette gauche se répercute en amont par une élévation des pressions dans les veines et capillaires pulmonaires, causant cette inondation transcapillaire. Elle est majorée en position allongée.
Pour quantifier la dyspnée, on utilise l’échelle de la New York Heart Association (NYHA) [
Signes physiques
Insuffisance cardiaque gauche
Œdème aigu pulmonaire (OAP)
Bruit de galop diastolique
Le B3 est un bruit sourd protodiastolique, correspondant à la phase initiale rapide de remplissage ventriculaire. Généralement gauche, il est recherché à la pointe du cœur, le malade en décubitus latéral gauche, mais est habituellement inaudible. Lorsqu’il est perçu, il traduit soit une augmentation de la pression auriculaire gauche, soit une dysfonction systolique du ventricule gauche. Sa valeur sémiologique est donc considérable. Il peut disparaître lors du traitement de l’insuffisance ventriculaire.
Le B4 est également sourd, télédiastolique, correspondant à la phase de remplissage actif du ventricule par la contraction de l’oreillette. Il disparaît en cas de fibrillation atriale. À la différence du B3, il est toujours pathologique et traduit avant tout une perte de compliance ventriculaire (ventricule peu distensible).
Autres signes physiques
Lorsque ces signes s’accompagnent d’une hypotension artérielle, tachycardie, oligurie et des anomalies du bilan rénal et/ou hépatique, c’est l’état de choc cardiogénique.
Insuffisance cardiaque droite
Les signes d'insuffisance cardiaque droite sont :- turgescence jugulaire et reflux hépatojugulaire, par élévation de la pression veineuse jugulaire, signes d'insuffisance cardiaque droite plutôt aigus ;
- œdèmes des membres inférieurs bilatéraux, symétriques, blancs, indolores ;
- ascite, hépatalgie et hépatomégalie, par congestion veineuse hépatique.
Chronologie de l’insuffisance cardiaque
Une insuffisance cardiaque aiguë se manifeste par un œdème aigu pulmonaire, un état de choc cardiogénique ou un tableau d’insuffisance cardiaque droite aiguë.
Il faut rechercher un facteur déclenchant : infarctus du myocarde, fibrillation atriale rapide, pic hypertensif, écart de régime (sel), sepsis, majoration récente des bêtabloquants, embolie pulmonaire.
Le pronostic de l’insuffisance cardiaque chronique est fonction des symptômes au domicile (échelle de la NYHA) et du nombre de décompensations durant les 12 derniers mois.
Bilan initial
Dosage du peptide B natriurétique
Le dosage sanguin du BNP, ou de sa forme inactive le NT-proBNP, est un marqueur très sensible d’insuffisance cardiaque, avec une valeur prédictive négative de 95 %. Ainsi un BNP normal rend le diagnostic d’insuffisance cardiaque peu probable. La limite supérieure du BNP est de 35 pg/mL pour l’insuffisance cardiaque chronique, et de 100 pg/mL pour l’insuffisance cardiaque aiguë (respectivement 125 et 300 pg/mL pour le NT-proBNP).Le dosage du BNP est également un marqueur de suivi prédictif de décompensation cardiaque imminente et de morbi-mortalité.
Électrocardiogramme (ECG)
Il peut retrouver des arguments pour une cardiopathie ischémique, une hypertrophie ventriculaire gauche, une fibrillation atriale, un bloc de branche témoignant d’un asynchronisme intra- ou interventriculaire, un microvoltage (cardiopathies infiltratives).Échographie cardiaque
Indispensable pour établir le diagnostic et rechercher une cardiopathie sous-jacente, afin de guider la thérapeutique et les modalités du suivi.Le diagnostic d’insuffisance cardiaque repose sur l’association de symptômes avec une élévation du BNP ou NT-proBNP et une anomalie cardiaque structurelle ou fonctionnelle à l’échographie.
Étiologie
Insuffisance cardiaque gauche
Cardiopathie ischémique
Elle représente la première cause d’insuffisance cardiaque à FEVG diminuée.L’antécédent d’infarctus du myocarde entraîne une perte de myocytes remplacés par une cicatrice fibreuse. L’ischémie myocardique chronique entraîne une perte de fonctionnalité des myocytes, qui peut être réversible ou non après revascularisation (viabilité).
Cardiopathie congénitale
Les patients avec une cardiopathie congénitale atteignent désormais habituellement l’âge adulte grâce aux réparations chirurgicales. Ils peuvent développer à un moment une insuffisance cardiaque systolique ou diastolique.Cardiopathie hypertensive
L’augmentation de la pression artérielle aortique entraîne une augmentation de la post-charge, avec pour conséquence une hypertrophie du ventricule gauche (loi de Laplace). Cette hypertrophie augmente la rigidité des parois ventriculaires, à l’origine d’une dysfonction diastolique.Cardiopathies valvulaires
Parmi les plus fréquentes :- rétrécissement aortique : l’augmentation de la post-charge par la réduction du diamètre d’ouverture de valve entraîne une hypertrophie ventriculaire gauche à l’origine d’une dysfonction diastolique ;
- insuffisance mitrale et insuffisance aortique : surcharge volumique par le sang stagnant dans les cavités cardiaques, qui va provoquer une dilatation ventriculaire, puis une diminution de la FEVG. Lorsque ces valvulopathies deviennent symptomatiques, elles sont habituellement sévères et imposent alors une correction chirurgicale ou interventionnelle ;
- rhumatisme articulaire aigu : valvulopathies liées à une maladie inflammatoire systémique secondaire à une angine à streptocoque insuffisamment traitée dans l’enfance. Devenu rare en Occident, il est à évoquer en cas de population immigrée et/ou dont l’accès aux soins fut limité.
Pathologie du péricarde
Il s’agit de :- l’épanchement péricardique : il empêche la relaxation et la dilatation des cavités cardiaques, jusqu’à la compression des cavités droites en cas de tamponnade ;
- la péricardite constrictive : généralement secondaire à des péricardites à répétition, une péricardite tuberculeuse ou une radiothérapie. Le péricarde se rigidifie en formant une coque fibrocalcaire, causant alors une dysfonction diastolique associée à des signes d’insuffisance cardiaque droite.
Cardiopathies rythmiques
Atriales ou ventriculaires : la tachycardie entraîne un raccourcissement du temps de diastole, diminuant le volume télédiastolique et donc le volume d’éjection systolique. Ces troubles du rythme peuvent évoluer vers une véritable cardiomyopathie rythmique, avec apparition d’une dysfonction ventriculaire sévère.Cardiomyopathies
Il s’agit d’une maladie du muscle cardiaque en soi (après exclusion donc de toute cardiopathie ischémique [coronaires normales], valvulaire, hypertensive, congénitale, péricardique ou rythmique…). Il existe différents type de cardiomyopathies.Cardiomyopathies dilatées (CMD)
Toxiques. Il s’agit de :
- l’alcool : l’éthylisme chronique est une cause de CMD qui peut être sévère, mais d’évolution favorable ou « réversible » après sevrage ;
- les amphétamines, cocaïne (qui peut également être à l'origine d'infarctus du myocarde) ;
- la chimiothérapies : au premier rang desquelles les anthracyclines. Certaines immunothérapies peuvent avoir une toxicité cardiaque (exemple de l'herceptine). Les thérapies ciblées peuvent entraîner des myocardites auto-immunes ;
- la radiothérapie thoracique (CMD, restriction, constriction, valvulopathies ou coronaropathie). Le ventricule gauche est souvent peu dilaté.
Métaboliques. Sont en cause :
- la grossesse, le péri-partum ;
- les carences : thiamine, calcium, fer, zinc, sélénium ;
- les causes endocriniennes (dysthyroïdie, phéochromocytome, acromégalie, hyper/hypocorticisme, diabète, acromégalie, obésité) ;
- la cardiomyopathie de stress ou le syndrome de tako-tsubo : sidération myocardique secondaire à un stress émotionnel ou organique, touchant préférentiellement l’apex du ventricule gauche en forme de tako-tsubo, piège à pieuvre japonais, souvent de bon pronostic en dehors du risque rythmique.
CMD génétiques. Tout jeune patient < 65 ans présentant une cardiomyopathie dilatée avec altération de la FEVG dite idiopathique doit faire suspecter une cause génétique : mitochondriopathies, laminopathies, dystrophies musculaires, non-compaction. Il convient de rechercher systématiquement des antécédents familiaux de CMD ou de mort subite.
Une dysfonction ventriculaire droite avec troubles du rythme ventriculaire devra faire rechercher une dysplasie arythmogène du ventricule droit (DVDA).
Cardiomyopathie hypertrophique
Cardiomyopathie restrictive
L’amylose, cause la plus fréquente, peut toucher le cœur de façon isolée ou non. L’infiltration du myocarde par des dépôts amyloïdes entraîne une rigidité des parois, un trouble de la relaxation ainsi que des troubles du rythme ou de la conduction.
Cas particulier de l’insuffisance cardiaque à débit augmenté (FEVG préservée)
Les causes d’hyperdébit sanguin pouvant engendrer une insuffisance cardiaque par épuisement myocardique sont : anémie sévère, thyrotoxicose, fistule artérioveineuse, grossesse, carence en vitamine B1.Insuffisance cardiaque droite
Examens complémentaires
La cardiopathie ischémique étant la première cause d’insuffisance cardiaque à FEVG diminuée, il convient de réaliser une évaluation coronarienne (coroscanner si jeune et à bas risque cardiovasculaire, autrement coronarographie) devant la découverte d’une FEVG altérée.
L’IRM cardiaque peut aider au diagnostic étiologique, et permettre une quantification de la fibrose (qui elle-même est corrélée au risque de mort subite).
L’échographie d’effort ou la scintigraphie myocardique : en cas de suspicion d’ischémie et de recherche de viabilité myocardique.
Le holter ECG des 24 heures : à la recherche de troubles du rythme.
Le test d’effort avec mesure de la consommation en oxygène (VO2) est réalisé pour apprécier l’amélioration des performances lors de la réadaptation cardiaque, ou à visée pronostique dans le cadre du bilan prégreffe : un pic de VO2 inférieur à 10-12 mL/kg/min sous bêtabloquant est en faveur de l’indication de transplantation.
Le cathétérisme droit est réalisé pour mesurer l’index cardiaque (bas si < 2,2 L/min/m2), les pressions pulmonaires et l’origine d’une hypertension pulmonaire (pré- ou post-capillaire) dans le cadre notamment du bilan prégreffe.
Enfin, la biologie suivante doit être réalisée lors du bilan minimal de toute insuffisance cardiaque : numération formule sanguine, ionogramme sanguin, bilan hépatocellulaire, hémoglobine glyquée, bilan lipidique, TSH, bilan martial, peptide B natriurétique. Un dosage de troponine pourra être ajouté en cas d’insuffisance cardiaque aiguë. Le bilan étiologique des cardiomyopathies dilatées sera prélevé en 2e intention.
Traitement
Insuffisance cardiaque aiguë – Œdème aigu pulmonaire
- symptomatique : oxygénothérapie ; et en cas de désaturation ou polypnée persistante : ventilation non invasive. Un traitement déplétif par diurétiques de l’anse doit être administré en intraveineux, ainsi qu’un traitement vasodilatateur par dérivés nitrés en l’absence d’hypotension ou de pathologie obstructive (rétrécissement aortique, cardiomyopathie hypertrophique obstructive…) ;
- étiologique : revascularisation coronarienne, contrôle tensionnel, contrôle du rythme, chirurgie valvulaire en cas de fuite sévère aiguë.
Insuffisance cardiaque chronique
La cardiopathie causale doit être traitée (remplacement valvulaire, revascularisation myocardique, sevrage éthylique, etc.). L’éducation thérapeutique est indispensable.
Mesures générales
Elles reposent sur :- un régime hyposodé à visée symptomatique (< 6 g de sel par jour) ;
- la vaccination antigrippale annuelle et antipneumococcique tous les 5 ans ;
- l'arrêt du tabac et de l’alcool ;
- une activité physique régulière pour lutter contre le déconditionnement neuromusculaire ;
- un accompagnement psychologique et addictologique si besoin.
- le suivi en télésurveillance en cas d’hospitalisations itératives ;
- la réadaptation cardiaque : à proposer après une décompensation cardiaque ou pour les patients demeurant symptomatiques sous traitement médical. Elle améliore les capacités à l’effort, la qualité de vie et diminue le nombre d’hospitalisations pour décompensation.
Traitement pharmacologique
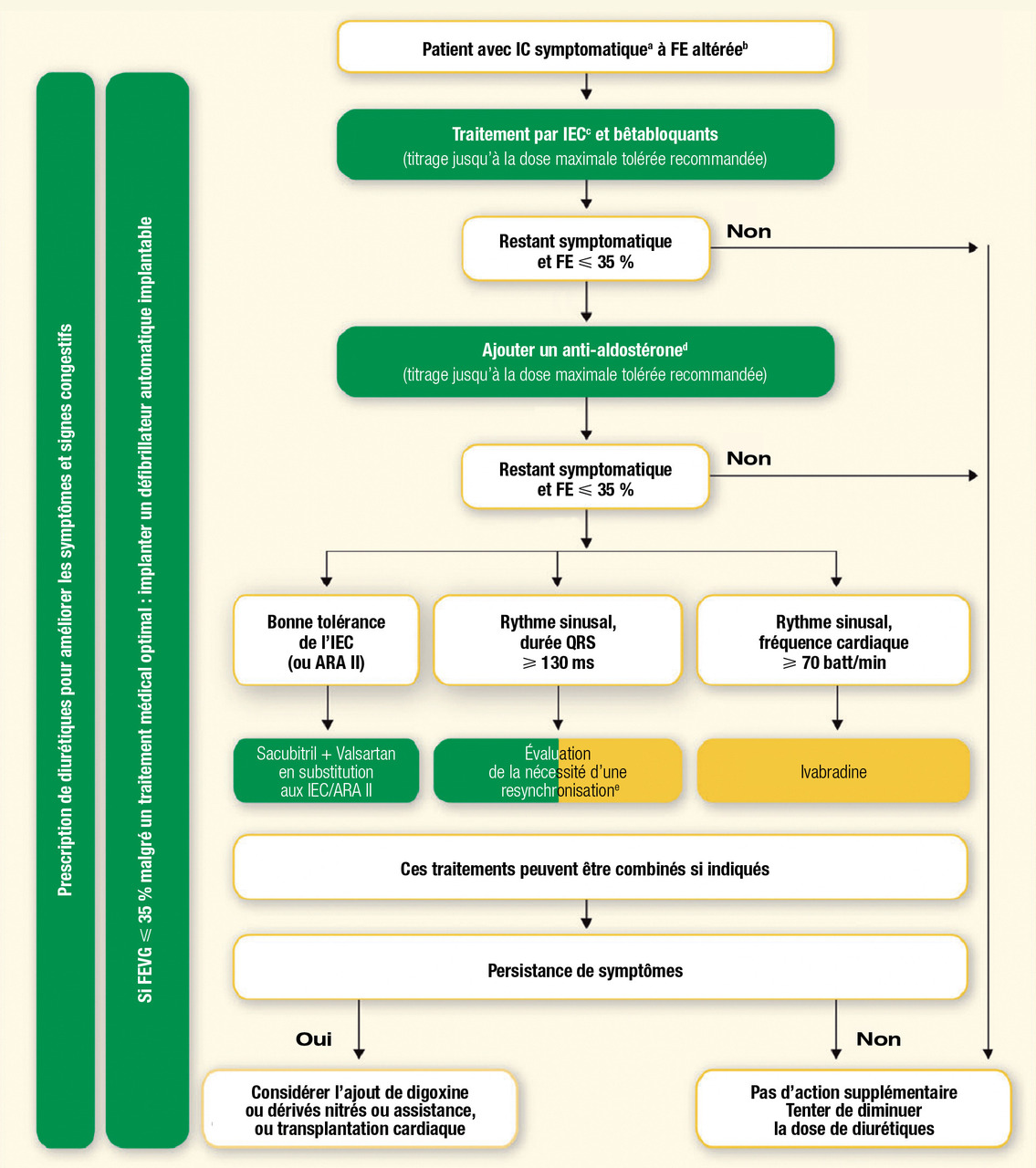
Insuffisance cardiaque à FEVG altérée < 40 % (figure)
Il faut débuter par une dose minimale à augmenter par paliers toutes les 2 semaines, jusqu’à l’obtention de la dose maximale tolérée par le patient (pas d’hypotension symptomatique, pas de vertiges, pas de bradycardie, pas d’asthénie). Il conviendra de contrôler la fonction rénale et la kaliémie.
Un antialdostérone sera ajouté si le patient reste symptomatique (NYHA ≥ II) avec une FEVG ≤ 35 % malgré la bithérapie, avec également titration jusqu’à la dose maximale tolérée. La triple association IEC-ARA 2-spironolactone est contre-indiquée en raison du risque d’hyperkaliémie.
Un traitement combinant sacubitril (inhibiteur de la néprilysine) et valsartan (ARA II) sera introduit en substitution aux IEC si la FEVG reste ≤ 35 %, symptomatique (NHYA ≥ II), malgré la trithérapie bêtabloquants-IEC-antialdostérone.
Ces médicaments permettent une amélioration de la survie et une diminution du nombre d’hospitalisations pour insuffisance cardiaque.
L’ivabradine (inhibiteur du courant If du nœud sinusal) est proposée chez les patients symptomatiques, en rythme sinusal, ayant une fréquence cardiaque de repos > 70 batt/min malgré les bêtabloquants ou en cas de contre-indication aux bêtabloquants.
Les diurétiques de l'anse ne sont recommandés qu’en cas de signes congestifs, à visée symptomatique. Les diurétiques thiazidiques (par exemple l’hydrochlorothiazide) sont réservés aux formes graves d’insuffisance cardiaque, en cas de résistance aux diurétiques (persistance de signes de rétention hydrosodée malgré de fortes doses de furosémide). Dans ce cas, on les donne en association au furosémide.
La digoxine, qui est la plus ancienne molécule utilisée dans le traitement de l’insuffisance cardiaque, peut améliorer les symptômes des patients qui gardent des symptômes malgré un traitement optimal, en particulier chez les patients les plus symptomatiques (NYHA III et IV) en fibrillation atriale difficile à ralentir. Sa prescription justifie un dosage régulier de sa concentration plasmatique au 6e jour de l'introduction, surtout pour les cas des patients âgés ou ayant une insuffisance rénale.
Les dérivés nitrés sont des vasodilatateurs principalement veineux considérés comme un traitement d’appoint chez les patients symptomatiques (NYHA III-IV) qui gardent des pressions de remplissage élevées.
Les inhibiteurs calciques ne sont pas des traitements de l’insuffisance cardiaque. Le diltiazem et le vérapamil sont contre-indiqués dans l’IC systolique.
L’amiodarone est le seul (hormis les bêtabloquants) antiarythmique qui peut être prescrit en cas d’insuffisance cardiaque systolique.
Insuffisance cardiaque à FEVG ≥ 40 %
Défibrillateur automatique implantable (DAI)
Il s’implante en prévention de la mort subite par trouble du rythme ventriculaire seulement chez les patients ayant une espérance de vie supérieure à 1 an.En prévention primaire, l’implantation du DAI est recommandée chez les patients avec une FEVG ≤ 35 % symptomatique persistante malgré au moins 3 mois de traitement médical optimal (ou au moins 40 jours après un infarctus du myocarde).
Si les QRS sont fins et en l’absence de trouble de conduction, le DAI sera sous-cutané ou simple chambre dans le ventricule droit. Il aura pour seule fonction théorique la prévention primaire de la mort subite.
Si les QRS sont ≥ 130 ms (en particulier en cas de bloc de branche gauche), le DAI sera triple chambre afin d’assurer également une resynchronisation cardiaque (en stimulant simultanément le ventricule droit et le ventricule gauche via le sinus coronaire).
Le gilet défibrillant (dit LifeVest du laboratoire Zoll) est maintenant disponible et remboursé, à proposer pendant un temps limité aux patients exposés à un risque transitoire de mort subite (post-infarctus du myocarde avec FEVG ≤ 35 %, attente de transplantation cardiaque…).
Traitement chirurgical
En cas d’insuffisance cardiaque sévère NYHA III ou IV réfractaire au traitement optimal, la transplantation cardiaque est envisagée.Elle n’est réalisable qu’en l’absence de contre-indication (âge élevé > 65-70 ans bien qu’il n’existe pas de contre-indication absolue, mauvaise observance attendue, maladie psychiatrique décompensée, néoplasie évolutive, hypertension artérielle pulmonaire [HTAP] fixée, multiples défaillances d’organes, arthériopathie oblitérante des membres inférieurs [AOMI] sévère, addictions (alcool, tabac...).
La transplantation nécessite la prise d’un traitement immunosuppresseur (corticoïdes, anticalcineurines, antimétabolites) afin de diminuer les risques de rejet.
Les complications à long terme sont la défaillance du greffon chronique, liée au rejet et à la coronaropathie du greffon, les événements cardiovasculaires (hypertension artérielle, diabète cortico-induit, dyslipidémie), les néoplasies, les infections, l’insuffisance rénale.
En cas d’état de choc cardiogénique, une assistance circulatoire de courte durée (ECMO) peut être mise en place en réanimation, par voie fémorale, dans l’attente d’un autre projet à long terme (greffe, assistance cardiaque de longue durée ou récupération). L’assistance monoventriculaire gauche ou biventriculaire est une assistance mécanique de longue durée, implantée chirurgicalement en attente de la greffe cardiaque, de la récupération (myocardites) ou en thérapie définitive (contre-indication à une transplantation).
Suivi
POINTS FORTS À RETENIR
L’insuffisance cardiaque aiguë comme chronique est une cause de morbi-mortalité majeure, qu’il faut savoir prendre en charge précocement. Un patient symptomatique NYHA IV, malgré le traitement optimal, a un risque de mortalité > 50 % à 1 an.
L’électrocardiogramme, l’échographie cardiaque transthoracique et le dosage du peptide B natriurétique doivent être réalisés devant toute suspicion d’insuffisance cardiaque.
Les principales causes sont les cardiopathies ischémique, hypertensive, valvulaire, rythmique, congénitale, en rapport avec une pathologie péricardique, ainsi que les cardiomyopathies (dilatées, hypertrophiques, restrictives).
La prise en charge de l’insuffisance cardiaque aiguë (œdème aigu pulmonaire) repose sur la triade oxygénothérapie, déplétion par diurétiques de l’anse, et dérivés nitrés, en plus du traitement étiologique (ralentir une fibrillation atriale rapide, revasculariser un infarctus aigu du myocarde, etc.).
Il existe un traitement pharmacologique de l’insuffisance cardiaque chronique à FEVG diminuée (< 40 %) ayant montré son efficacité en termes de réduction de morbi-mortalité : bêtabloquants, inhibiteurs de l’enzyme de conversion ou ARA2, antialdostérone, et plus récemment un inhibiteur de la néprilysine en association avec un ARA2. Les autres traitements (diurétiques, digoxine, nitrés, ivabradine) ne sont prescrits qu'à visée symptomatique.
Toute FEVG ≤ 35 % malgré au moins trois mois de traitement médical optimal doit bénéficier de la pose d’un défibrillateur automatique implantable (si le patient présente une espérance de vie d'au moins 1 an), en prévention de la mort subite. Si les QRS sont ≥ 130 ms, le défibrillateur doit être triple chambre (dit biventriculaire) afin d’assurer également une resynchronisation ventriculaire.
Insuffisance cardiaque de l’adulte
L'insuffisance cardiaque n'est pas une simple manifestation mécanique, mais une véritable pathologie neurohormonale. Identifier la cause sous-jacente est crucial. Associé aux mesures hygiéno-diététiques, le traitement pharmacologique permet d'en améliorer le pronostic (diminution de la morbimortalité) et de diminuer la symptomatologie. La mise en place d'un défibrillateur automatique implantable en présence d'une dysfonction ventriculaire gauche sévère, associé à un système de resynchronisation (si QRS large), complètera l'arsenal thérapeutique. L'assistance et la greffe cardiaque seront proposés en cas d'insuffisance cardiaque réfractaire au traitement optimal.

 Encadrés
Encadrés