Selon l’Agence de sécurité du médicament et des produits de santé, 1,49 million de patients étaient sous anticoagulants oraux en France en 2013.
Les antagonistes de la vitamine K ou AVK (warfarine, Coumadine ; acénocoumarol, Sintrom ; fluindione, Préviscan) sont la première cause d’hospitalisation d’origine iatrogène en France ; on dénombre 5 000 à 6 000 accidents hémorragiques mortels par an. Nécessité d’une surveillance biologique, nombreuses interactions médicamenteuses et alimentaires, ajustements en cas de modification des coprescriptions, indice thérapeutique étroit, leur utilisation n’est pas simple. Leur effet procoagulant se manifeste dans les premières heures et ils ne sont antithrombotiques qu’après 3 à 6 jours. En revanche, on dispose d’un antidote (la vitamine K). Mais son efficacité est discutable en cas d’urgence vitale compte tenu de l’effet retardé (6 à 12 heures) et de l’action prolongée pouvant gêner la reprise des AVK.
Depuis 2018, l’Ansm préconise de privilégier la warfarine par rapport au fluindione (Préviscan) en raison d’effets secondaires notamment immuno-allergiques, et d’abandonner l’acénocoumarol (Sintrom), compte tenu de sa demi-vie plus courte, y compris chez les patients stables.
Les héparines non fractionnées (HNF) et les héparines de bas poids moléculaire (HBPM) sont les anticoagulants indirects les plus anciens. Les HNF ont une activité anti-Xa et anti-IIa équivalente, tandis que les HBPM ont un effet anti-Xa prédominant. Disponibles uniquement sous forme injectable, ces médicaments requièrent une adaptation posologique individuelle. Par ailleurs, ils sont d’origine animale et font courir un risque de thrombopénie induite et d’ostéoporose.
Le fondaparinux (Arixtra), inhibiteur sélectif synthétique de l’activité anti-Xa, a été développé plus récemment. Ses avantages : dose fixe et pas de thrombopénie induite.
Les anticoagulants oraux d’action directe (AOD), disponibles depuis 2008 en France, sont une alternative à la fois aux anticoagulants rapides injectables et aux AVK.
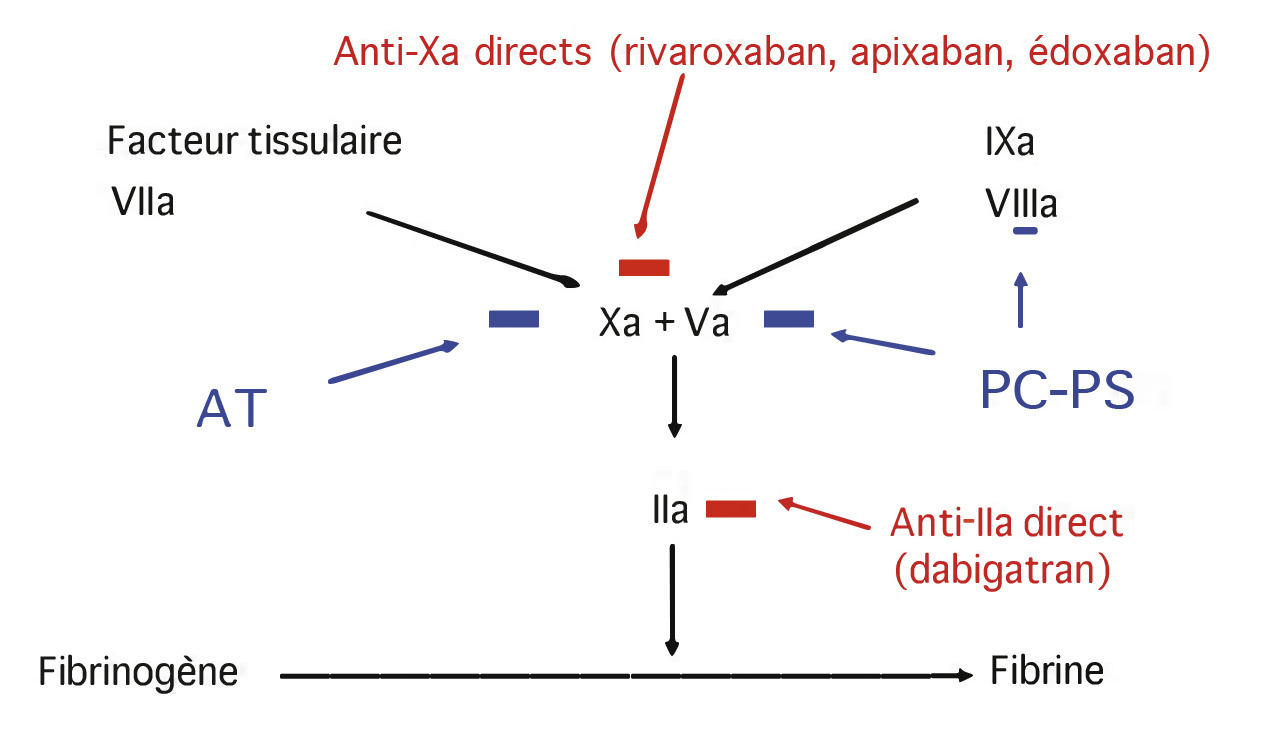
Mécanisme d’action, contre-indications
Le pic d’action survient entre 1 et 3 heures après ingestion, offrant une efficacité rapide, la demi-vie est courte, comprise entre 9 et 17 heures suivant les molécules. L’élimination est rénale (80 % pour le dabigatran et 25 % pour l’apixaban) et hépatique. L’insuffisance rénale expose à un risque de surdosage, et les AOD sont contre-indiqués si la clairance de la créatinine calculée selon la formule de Cockcroft est inférieure à 30 mL/min. Ils le sont également en cas de cirrhose Child B ou C (cirrhose décompensée).
En raison de leur faible poids moléculaire, ils traversent la barrière placentaire. Aucun effet fœtotoxique n’a été notifié, mais on a peu d’informations sur leur tératogénicité éventuelle. Ils ne doivent donc pas être prescrits chez la femme enceinte ou allaitante. Si une grossesse est débutée sous AOD, un relais par HBPM est instauré.
Les interactions médicamenteuses sont en rapport avec leur métabolisme (
Prévention primaire en chirurgie
La durée de l’anticoagulation est respectivement (
– après prothèse du genou : de 14 jours pour le rivaroxaban, de 10 à 14 jours pour l’apixaban et de 10 jours pour le dabigatran ;
– après prothèse de la hanche : de 32 à 38 jours pour l’apixaban et de 35 jours pour le dabigatran et le rivaroxaban. Posologies : 220 mg 1 x/j (2 gélules) pour le dabigatran, 10 mg 1 x/j pour le rivaroxaban, et 2,5 mg 2 x/j pour l’apixaban.
Pour le dabigatran, une dose réduite à 150 mg/j en 1 prise est nécessaire si : insuffisance rénale (IR)modérée, âge > 75 ans, association avec l’amiodarone, la quinidine ou le vérapamil. En cas d’IR modérée et prise conjointe de vérapamil : réduction de la posologie à 75 mg 1 x/j.
En l’absence de données cliniques, les AOD ne sont pas recommandés après chirurgie pour fracture de la hanche.
Maladie veineuse thrombo-embolique
Les AOD sont recommandés en première intention (SPLF 2019),2 que ce soit dans le traitement immédiat (grade 1+), au cours des 3 premiers mois (grade 2+), et au long cours (grade 2+), chez les patients avec une thrombose veineuse profonde ou une embolie pulmonaire (EP) sans pathologie cancéreuse sous-jacente. Ils sont, en revanche, positionnés en 2e intention, en cas d’intolérance aux HPBM chez les sujets atteints d’un cancer, devant les AVK et en l’absence de tumeur urologique ou digestive (grade 2+).
En cas de MVTE récidivante sous AVK ou AOD, un relais par HBPM est proposé (grade 2 +).
Une stratification des EP selon le niveau de risque évalué par le Pulmonary Embolism Severity Index simplifié (score sPESI ;
Dans ce cas, après évaluation du risque hémorragique (fonction rénale, contexte médical et social, souhaits et possibilités de suivi), il est suggéré de programmer une consultation spécialisée précoce (filière spécifique) dans les 72 heures suivant la sortie, afin de valider le diagnostic, le traitement initial et d’organiser le suivi ultérieur en lien avec le médecin référent.
Les embolies à « risque intermédiaire » sont traitées à l’hôpital par AOD ou anticoagulation classique, tandis que celles à haut risque, c’est-à-dire associées à un état de choc ou à une instabilité hémodynamique, relèvent de l’héparine IV à la seringue électrique et pas d’un traitement par AOD, du moins à la phase aiguë.
En traitement prolongé (
Le rivaroxaban 20 mg/j induit une réduction significative (vs placebo) du risque embolique mais une augmentation des hémorragies non majeures dans EINSTEIN-EXTENSION, tandis que, dans EINSTEIN CHOICE, le taux de récidive thrombo-embolique (fatale ou non) est près de 3 fois inférieur avec le rivaroxaban à dose pleine (20 mg) ou réduite (10 mg) par rapport à l’aspirine, avec un risque hémorragique identique entre les 3 groupes.
Toutefois, ces études n’ont pas une puissance suffisante pour affirmer la supériorité des AOD à dose réduite par rapport à la posologie pleine sur le risque hémorragique et une efficacité non inférieure chez les patients à haut risque de récidive.
L’essai randomisé contrôlé RENOVE, évaluant l’apixaban ou le rivaroxaban à dose pleine versus dose réduite, en cours d’inclusion, tente de répondre à cette question au terme de 2 ans de suivi moyen.
Fibrillation atriale non valvulaire
Selon les guidelines européennes réactualisées en 2017,3 une anticoagulation, de préférence par AOD (grade IA), est à envisager si le score = 1 chez un homme ou 2 chez une femme < 65 ans. Elle est formellement indiquée s’il est > 2 chez l’homme ou à 3 chez une femme de moins de 65 ans (grade 2A).
Non-indication des AOD
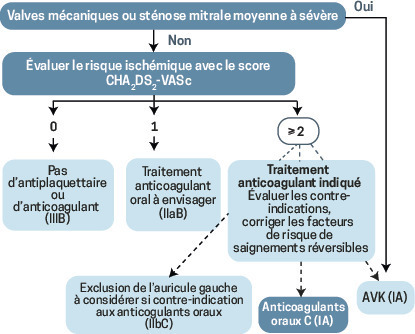
Le terme de FA valvulaire a récemment été abrogé par la Société européenne de cardiologie car il regroupait des populations hétérogènes de patients à niveau de risque embolique variable. On parle aujourd’hui de pathologie valvulaire sous-jacente ; elle guide la stratification du risque.
Les FA survenant dans un contexte de sténose mitrale modérée à sévère et en présence d’une valve prothétique mécanique ont été systématiquement exclues des essais cliniques évaluant les AOD dans la FA : ils n’ont pas d’indication dans ce contexte, car il y a un sur-risque de thrombose de la valve.
Une méta-analyse des essais de phase III montrait une efficacité et une sécurité similaire des AOD qu’il y ait ou non une pathologie valvulaire.6
L’étude RE-ALIGN – comparant le dabigatran (à une posologie supérieure à celle utilisée dans la FA) à la warfarine dans la survenue d’événements thrombo-emboliques et hémorragiques après remplacement valvulaire mitral ou aortique7 – a été interrompue prématurément.
En cause : une augmentation du taux d’événements thrombo-emboliques et hémorragiques avec le dabigatran par rapport à la warfarine. Cet échec pourrait être secondaireà la combinaison d’une exposition du sous-endothélium lors de la mise en place d’une prothèse valvulaire, à l’exposition du matériel prothétique à la circulation et à une libération de facteur tissulaire dans la circulation. Une concentration plasmatique en anticoagulant plus faible dans les premiers jours de mise en place pourrait aussi être en cause.
Indications potentielles
L’Agence européenne des médicaments a autorisé la molécule en prévention des événements athérothrombotiques après un SCA et pour les patients atteints d’une maladie coronaire ou artérielle périphérique stable et considérés à haut risque d’événement ischémique.
Les AOD ont été évalués dans la FA chez le coronarien bénéficiant d’une angioplastie. Avec l’association dabigatran-inhibiteur de P2Y12 (clopidogrel ou ticagrélor) : réduction des saignements et non-infériorité sur le plan thrombo-embolique par rapport à inhibiteur de P2Y12-aspirine-warfarine. L’apixaban est également en cours d’évaluation dans cette indication (études ENTRUST-AF, PCI).
Selon la Société européenne de cardiologie,8 la poursuite d’un AOD est possible à la phase aiguë d’un syndrome coronaire chez les patients traités au préalable par AOD et nécessitant une double antiagrégation plaquettaire, soit l’association aspirine-clopidogrel, pour 1 mois au minimum. Le rivaroxaban dans cette indication est prescrit à la posologie de 15 mg/j.
Dans les maladies thrombo-emboliques associées au cancer, il n’y a pas de preuve formelle de la supériorité des AOD sur les HBPM. Ces dernières sont privilégiées en première intention par les recommandations actuelles, en attendant les résultats des études en cours.
Les essais Hokusai-VTE-Cancer, SELECT-D et ADAM-VTE ont suggéré une non-infériorité de l’edoxaban, du rivaroxaban et de l’apixaban par rapport à la daltéraparine en cas de cancer, avec cependant dans les 2 premiers essais un risque hémorragique digestif et urinaire accru sous AOD. Ces résultats doivent être confirmés. Sont en cours : CARAVAGGIO comparant la daltéparine à l’apixaban à dose pleine à la phase aiguë de la MVTE et API-CAT évaluant l’apixaban à pleine versus demi-dose au-delà des 6 premiers mois.
AOD dans la « vraie vie »
D’après l’analyse d’une base de données incluant 64 661 patients atteints de FA non valvulaire entre 2010 et 2014, 47,5 % des patients sous AOD contre 40,2 % de ceux sous AVK prenaient leur traitement pendant au moins 80 % de la période d’étude.10 L’observance semble varier selon le type d’AOD (meilleure pour l’apixaban par rapport au rivaroxaban et au dabigatran) et le niveau de risque (augmentation avec l’élévation du score CHA2DS2-VASc).
Le risque d’AVC ischémique et d’embolie systémique au-delà du CHA2DS2-VASc 1 augmente chez les patients non observants pendant plusieurs mois par rapport aux malades observants.
Hémostase, risque hémorragique, antidotes
Les AOD perturbent significativement l’héparinémie et rendent son dosage difficilement interprétable dans les jours suivant un relais par héparine. Le monitoring des tests d’hémostase n’a donc pas d’intérêt.
Le seul dosage à effectuer en routine est la clairance de la créatinine, 1 fois par an, avec la formule de Cockcroft (seule utilisée dans les essais cliniques). Il est possible de mesurer la concentration des AOD, mais l’interprétation des résultats est étroitement corrélée à l’heure de la dernière prise, et la variabilité inter-individuelle importante.
Le seuil de risque hémorragique est de 30 à 50 ng/mL ; un surdosage en dabigatran est à craindre au- dessus de 200 ng/mL et probablement pour tous les AOD au-delà de 500 ng/mL.
Le dosage a un intérêt en cas d’hémorragie grave : si la concentration de l’AOD est en dessous de 30 ng/mL : pas d’antagonisation spécifique.
En cas de saignement sous AOD, il est crucial de connaître l’heure et la posologie de la dernière prise : la demi-vie de ces traitements étant courte, la restauration de l’hémostase intervient dans les 12 à 24 heures. Le risque de surdosage et le temps d’élimination dépendant de la fonction rénale, une estimation du DFG est primordiale. On peut donner du charbon activé dans les 6 heures après la prise. En cas d’hémorragie menaçant le pronostic vital, des concentrés de complexes prothrombiniques (50 UI/kg) sont administrés. Le dabigatran se lie peu aux protéines plasmatiques, permettant la dialyse en cas d’hémorragie massive, ce qui n’est pas le cas des anti-Xa actuellement sur le marché.
La place des antidotes est difficile à apprécier, la méthodologie des études les évaluant étant discutable. Le seul actuellement disponible est l’idarucizumab (Praxbind), anticorps monoclonal humanisé ayant une forte affinité pour le dabigatran : il neutralise son effet anticoagulant sans interférer avec la cascade de la coagulation physiologique. Il est réservé à l’usage hospitalier : 2 perfusions ou bolus de 2,5 g pour une dose totale de 5 g, pouvant être renouvelée une fois. Il induit la réversibilité des tests d’activité biologique spécifiques, mais la restauration de l’hémostase est longue, en moyenne à 11,4 heures.
L’andexanet alfa est une protéine humaine recombinée, capable d’antagoniser les xabans ; dans une étude de cohorte multicentrique sans groupe comparateur, chez les patients ayant une hémorragie majeure, elle a induit une réduction rapide et substantielle de l’activité anti-Xa et une réponse hémostatique à 12 heures. L’administration sous forme de bolus est suivie d’une perfusion continue de 120 minutes avec une posologie adaptée à l’heure de la dernière prise d’anti-Xa. Ce traitement n’est pas disponible en France.
1. Indice de sévérite de l’EP simplifié (sPESI)
Âge > 80 ans 1 point
SpO2 < 90 % 1 point
PAS < 100 mmHg 1 point
Fc > 110 batt/min 1 point
Maladie cardiorespiratoire 1 point
1 point
2. Anticoagulants oraux directs et sujet âgé
Alors que l’incidence de la fibrillation atriale (FA) et de la maladie veineuse thrombo-embolique (MVTE) augmente avec l’âge, les patients de plus 75 ans sont sous-représentés dans les essais cliniques évaluant les AOD.
Une méta-analyse portant sur l’efficacité et le risque de saignement chez des personnes âgées traitées pour une MVTE aiguë ou en prévention des AVC dans la FA suggère leur non-infériorité par rapport aux AVK.2 Concernant le risque de saignement, par rapport aux AVK, il serait légèrement augmenté avec le dabigatran (à la dose de 150 mg/j), moindre avec l’apixaban, et équivalent avec le rivaroxaban.
Selon toutes les études dans la MVTE ou la FA non valvulaire, le risque d’hémorragie cérébrale est diminué de 50 % dans le bras AOD par rapport aux AVK.
En revanche, les saignements gastro-intestinaux sont plus importants chez les patients sous dabigatran.
On ne dispose pas de données sur la polypathologie et la fragilité des patients inclus dans ces études. Dans cette population, il faut toujours prendre en compte la fonction rénale et les interactions médicamenteuses (polymédication fréquente).
2. Sanchez O, Benhamou Y, Bertoletti L, et al. Recommandations de bonne pratique pour la prise en charge de la maladie veineuse thromboembolique chez l’adulte. Version courte. Médecine Nucléaire 2019;43:323-50.
3. Kirchhof P, Benussi S, Kotecha D, et al. 2016 ESC guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur Heart J 2016;37:2893-962.
4. Sharma M, Cornelius VR, Patel JP, Davies JG, Molokhia M. Efficacy and harms of direct oral anticoagulants in the elderly for stroke prevention in atrial fibrillation and secondary prevention of venous thromboembolism: systematic review and meta-analysis. Circulation 2015;132:194-204.
5. Cohen AT, Harrington RA, Goldhaber SZ, et al. Extended Thromboprophylaxis with Betrixaban in Acutely Ill Medical Patients. N Engl J Med 2016;375:534-44.
6. Renda G, Ricci F, Giugliano RP, De Caterina R. Non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation and valvular heart disease. J Am Coll Cardiol 2017;69:1363-71.
7. Eikelboom JW, Connolly SJ, Brueckmann M, et al. Dabigatran versus warfarin in patients with mechanical heart valves. N Engl J Med 2013;369: 1206-14.
8. Ibanez B, James S, Agewall S, et al. 2017 ESC Guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevation. The Task Force for the management of acute myocardial infarction in patients presenting with ST-segment elevation of the European Society of Cardiology (ESC). Eur Heart J 2018;39:119-77.
9. Ruff CT, Giugliano RP, Braunwald E, et al. Comparison of the efficacy and safety of new oral anticoagulants with warfarin in patients with atrial fibrillation: a meta-analysis of randomised trials. Lancet 2014;383:955-62.
10. Yao X, Abraham NS, Sangaralingham LR, et al. Effectiveness and safety of dabigatran, rivaroxaban, and apixaban versus warfarin in non valvular atrial fibrillation. J Am Heart Assoc 2016;5:e003725.

 Encadrés
Encadrés