Depuis la pandémie de Covid, les demandes de consultation pour les adolescents en souffrance psychique ont fortement augmenté. Le médecin généraliste est souvent en première ligne pour répondre à la demande du jeune et de sa famille. En effet, il est malheureusement difficile, dans de nombreux départements, de consulter un pédopsychiatre dans les délais souhaités. La question se pose donc : devant un épisode dépressif caractérisé (EDC) véritable chez l’adolescent (et après exclusion d'un éventuel trouble bipolaire), que faire ?
L’orientation vers une prise en charge psychothérapeutique est la règle. Les psychotropes sont prescrits de manière plus restreinte chez les ados, à la fois par crainte des effets secondaires, mais aussi devant des preuves d’efficacité plus minces, en particulier pour les antidépresseurs. S’ils peuvent parfois être utilisés en première intention devant un EDC sévère, ils ont généralement une place en deuxième intention, en cas d’échec d’une psychothérapie bien menée.
Il convient de prendre toujours un temps avec le jeune seul et lui poser la question du harcèlement scolaire, du cyberharcèlement et de l’ambiance familiale. Résoudre ces situations dans lesquelles le jeune se sent « piégé sans possibilité de fuir » est indispensable, plutôt que d’opter pour une prescription précoce.
En pratique, quels antidépresseurs prescrire ?
Selon les méta-analyses, seule la fluoxétine est supérieure au placebo, bien que les études et les participants inclus soient bien moins importants que chez l’adulte. La taille d’effet de ce traitement est également plus faible. La fluoxétine est le seul traitement ayant l’AMM en France chez le mineur (à partir de 8 ans).
Sur le terrain, la sertraline est utilisée comme alternative à la fluoxétine. En effet, malgré l’absence de preuves formelles, elle est généralement bien tolérée. Il peut être judicieux de la prescrire chez les ados ayant une comorbidité anxieuse (dont les TOC). La sertraline peut être privilégiée aussi chez les ados maigres, la fluoxétine pouvant entraîner une perte de poids par diminution de l’appétit (selon son RCP).
En troisième intention, l’escitalopram a l’AMM dans l’EDC à partir de 12 ans aux États-Unis. Son utilisation est déconseillée mais possible selon son RCP français (à bien argumenter dans le dossier). En pratique, il est rarement utilisé en raison de la fréquence de co-prescription d’hydroxyzine, notamment pour les troubles du sommeil invalidants (contre-indication absolue du fait de l’augmentation du QTc).
Quel dosage ?
En pratique, on commence souvent par une demi-dose pendant 1 semaine pour une meilleure tolérance.
Les posologies habituelles sont : 20 mg/j pour la fluoxétine, 50 mg/j pour la sertraline et 10 mg/j pour l’escitalopram. De rares patients peuvent nécessiter de plus hautes doses, mais ce n’est pas la règle et il n’y a pas de preuve de meilleure efficacité. Il est recommandé d’attendre 4 semaines de traitement bien observé pour juger de l’efficacité ou non de la molécule et d’un éventuel changement.
Après rémission, le traitement doit être maintenu de 6 à 12 mois et arrêté pendant une période peu stressante pour le jeune (grandes vacances, par exemple…).
Quels antidépresseurs ne pas prescrire ?
Pour la paroxétine et la venlafaxine, il n’y a pas de preuve d’efficacité, l’arrêt est difficile et, surtout, il y a une augmentation du risque suicidaire avant 25 ans : les guidelines NICE 2019 précisent qu’elles ne doivent pas être utilisées.
Pour la duloxétine, tricycliques, IMAO : pas de preuve d’efficacité, nombreux effets secondaires.
Mirtazapine, miansérine, vortioxétine, agomélatine : pas de preuve d’efficacité, pas utilisé en pratique.
Comment switcher les 3 ISRS ?
D’après le Vidal, qui cite lui-même un travail du journal Australian Prescriber :
- fluoxétine 20 mg vers sertraline ou escitalopram : arrêter la fluoxétine, attendre 7 j de wash-out puis débuter l’autre antidépresseur à basse dose ;
- sertraline 50 mg vers fluoxétine :
- diminuer à 25 mg pendant 2 (à 4) semaines puis arrêter et commencer la fluoxétine à 10 mg,
- possibilité d’arrêter directement et commencer le lendemain la fluoxétine 20 mg, mais le switch peut être moins bien toléré ;
- sertraline 50 mg vers escitalopram :
- diminuer à 25 mg pendant 2 (à 4) semaines puis arrêter et commencer l’escitalopram 10 mg,
- possibilité d’arrêter directement et commencer le lendemain l’escitalopram 10 mg mais le switch peut être moins bien toléré.
Quels bilans ?
Il n’y pas de bilan somatique systématique, mais il faut avoir en tête 2 réflexes somatiques :
- hypothyroïdie ;
- anémie ferriprive : selon le JAMA, jusqu'à 40 % des jeunes adolescentes (premières règles) seraient carencées en fer. Il s’agit d’un facteur de risque ou d’aggravation facilement corrigeable de nombreuses manifestations psychologiques.
Quid des co-prescriptions ?
Benzodiazépines : à bannir en raison de leurs nombreux effets secondaires cognitifs et du risque d’addiction ; elles pourraient augmenter le risque suicidaire lors d’EDC chez adolescent.
Hydroxyzine : parfois utile, devant des troubles du sommeil invalidants le temps qu’un antidépresseur agisse. Attention au risque d’augmentation du QTc avec l’escitalopram.
Un guide pratique
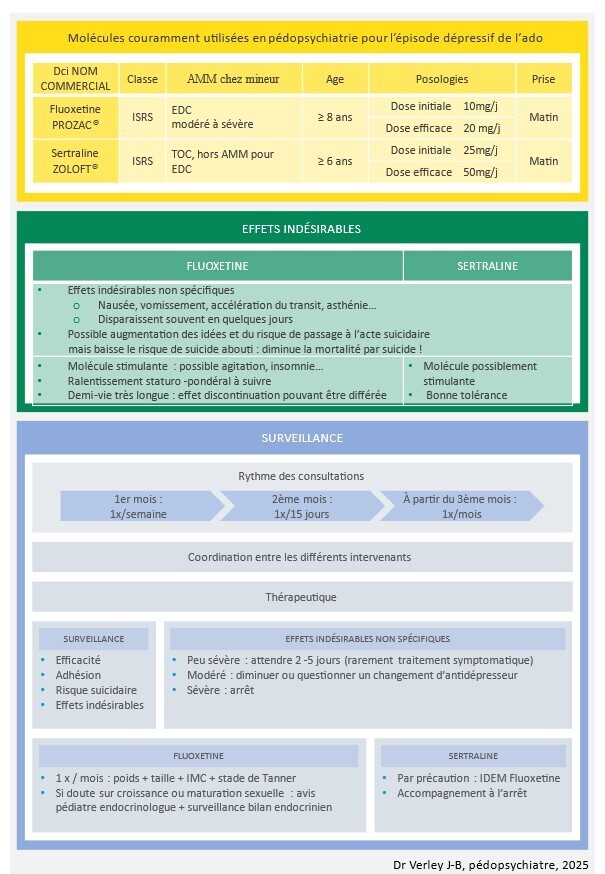
La fiche ci-contre précise le maniement, les effets indésirables à connaître et le suivi concernant les deux principaux antidépresseurs utilisés dans l’EDC à l’adolescence.
Pendant le premier mois, un suivi hebdomadaire permet de traquer les effets secondaires, évaluer la tolérance et une éventuelle augmentation du risque suicidaire. Bien utilisés dans cette indication, ces deux antidépresseurs diminuent le risque de décès par suicide de l’adolescent qui fait face à un EDC, suicidogène par nature.
Site web de la SFPEADA.
Korsia-Meffre S. Changement de traitement antidépresseur : le point sur les stratégies de substitution. 14 novembre 2019.
National Institute for Health and Care Excellence. Depression in children and young people: identification and management. 25 juin 2019.
HAS. Manifestations dépressives à l’adolescence repérage, diagnostic et prise en charge
en soins de premier recours. Novembre 2014.
Dodds TJ. Prescribed Benzodiazepines and Suicide Risk: A Review of the Literature. Prim Care Companion CNS Disord 2017;19(2):16r02037.
Lagerberg T, Fazel S, Sjölander A, et al. Selective serotonin reuptake inhibitors and suicidal behaviour: a population-based cohort study. Neuropsychopharmacology. Neuropsychopharmacology 2022;47(4):817‑23.
ANSM. Thesaurus des interactions médicamenteuses. 7 juin 2024.
Weyand AC, Chaitoff A, Freed GL, et al. Prevalence of Iron Deficiency and Iron-Deficiency Anemia in US Females Aged 12-21 Years, 2003-2020. JAMA 2023;329(24):2191-3.
Kassir A. Carence en fer : une perspective diagnostique et thérapeutique en psychiatrie. L’Encéphale 2017;43(1):85‑9.
Walter HJ, Abrught AR, Bukstein OG, et al. Clinical Practice Guideline for the Assessment and Treatment of Children and Adolescents With Major and Persistent Depressive Disorders. J Can Acad Child Adolesc Psychiatr 2023;62(5):479-502.