Chaque année, 10 à 15 % des patients sous anticoagulants requièrent une chirurgie ou un acte invasif ; 4 à 15 % des sujets stentés, traités par agents antiplaquettaires (AAP), ont une intervention chirurgicale non cardiaque dans l’année suivant la pose du stent.
Chez les patients à haut risque d’événement ischémique ou ayant fait un infarctus récent : différer toute chirurgie non urgente au-delà de 6 mois.1, 2
Chez les patients à haut risque d’événement ischémique ou ayant fait un infarctus récent : différer toute chirurgie non urgente au-delà de 6 mois.1, 2
Arrêter le traitement antithrombotique ?
Cette décision revient à l’équipe médicochirurgicale qui a prévu l’intervention, elle fait partie de la consultation d’anesthésie. Elle dépend du type de traitement pris, du risque thrombotique du patient et du risque hémorragique lié à la chirurgie. Plusieurs référentiels l’ont harmonisée.1, 3
AAP : indiqués pour prévenir et traiter les accidents athérothrombotiques, principalement artériels. L’aspirine (quelle que soit la dose) fait peu saigner.
Les inhibiteurs du récepteur plaquettaire P2Y12 – clopidogrel (Plavix), prasugrel (Efient), ticagrelor (Brilique) – associés à l’aspirine ont un risque hémorragique plus élevé.
Bithérapie antiplaquettaire, indiquée lorsque le risque thrombotique est maximal : dans les premières semaines suivant la pose d’un stent coronaire, quel que soit son type.2
Anticoagulants au long cours : prescrits dans la fibrillation atriale (FA), la maladie thrombo-embolique veineuse, les infarctus du myocarde compliqués, et en cas de valve cardiaque mécanique.
Recommandations d’arrêt et de reprise distinctes selon qu’il s’agit d’un antivitamine-K (AVK)3 – warfarine, fluindione, acénocoumarol – ou d’un anticoagulant oral direct (AOD) – dabigatran (Pradaxa), rivaroxaban (Xarelto), apixaban (Eliquis).1
Objectif : réduire au minimum la fenêtre d’arrêt pour limiter le risque thrombotique.
AAP : indiqués pour prévenir et traiter les accidents athérothrombotiques, principalement artériels. L’aspirine (quelle que soit la dose) fait peu saigner.
Les inhibiteurs du récepteur plaquettaire P2Y12 – clopidogrel (Plavix), prasugrel (Efient), ticagrelor (Brilique) – associés à l’aspirine ont un risque hémorragique plus élevé.
Bithérapie antiplaquettaire, indiquée lorsque le risque thrombotique est maximal : dans les premières semaines suivant la pose d’un stent coronaire, quel que soit son type.2
Anticoagulants au long cours : prescrits dans la fibrillation atriale (FA), la maladie thrombo-embolique veineuse, les infarctus du myocarde compliqués, et en cas de valve cardiaque mécanique.
Recommandations d’arrêt et de reprise distinctes selon qu’il s’agit d’un antivitamine-K (AVK)3 – warfarine, fluindione, acénocoumarol – ou d’un anticoagulant oral direct (AOD) – dabigatran (Pradaxa), rivaroxaban (Xarelto), apixaban (Eliquis).1
Objectif : réduire au minimum la fenêtre d’arrêt pour limiter le risque thrombotique.
Relayer par héparine ?
Pas d’héparine ni d’AINS en relais des AAP.
En revanche, chez les patients sous anti-P2Y12 en monothérapie, relayer par aspirine à 75 mg/j plus de 7 jours avant la chirurgie.
Quel que soit le risque hémorragique, on arrête l’aspirine lorsqu’elle est prescrite en prévention primaire.
Lorsque la suspension de l’AVK est décidée : relais héparinique uniquement si le risque thrombo-embolique est élevé : valve cardiaque mécanique, fibrillation atriale emboligène, maladie thrombo-embolique veineuse récente (< 3 mois) ou récidivante.
Dans ce cas : 1re injection d’héparine 24 heures (acénocoumarol) ou 48 heures (fluindione, warfarine) après la dernière prise d’AVK.
Si AOD stoppé : pas de relais par héparine, sauf cas exceptionnels (risque thrombo-embolique très élevé) où l’avis d’une équipe multidisciplinaire référente est nécessaire.
En revanche, chez les patients sous anti-P2Y12 en monothérapie, relayer par aspirine à 75 mg/j plus de 7 jours avant la chirurgie.
Quel que soit le risque hémorragique, on arrête l’aspirine lorsqu’elle est prescrite en prévention primaire.
Lorsque la suspension de l’AVK est décidée : relais héparinique uniquement si le risque thrombo-embolique est élevé : valve cardiaque mécanique, fibrillation atriale emboligène, maladie thrombo-embolique veineuse récente (< 3 mois) ou récidivante.
Dans ce cas : 1re injection d’héparine 24 heures (acénocoumarol) ou 48 heures (fluindione, warfarine) après la dernière prise d’AVK.
Si AOD stoppé : pas de relais par héparine, sauf cas exceptionnels (risque thrombo-embolique très élevé) où l’avis d’une équipe multidisciplinaire référente est nécessaire.
Risque hémorragique élevé
Pose de prothèse de hanche, colectomie, hystérectomie.
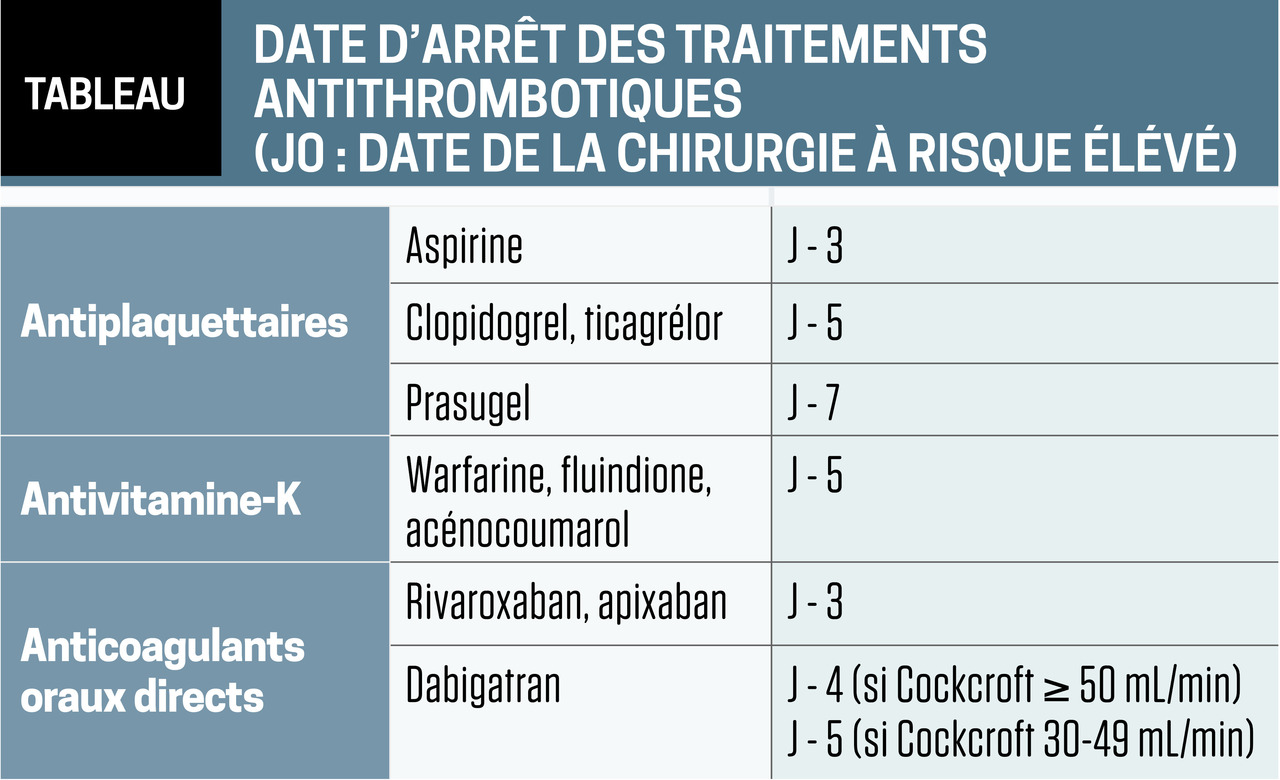
Généralement, ces interventions imposent l’arrêt du traitement anticoagulant et des anti-P2Y12 (tableau ), mais peuvent se faire sous aspirine en monothérapie (jusqu’à 300 mg/j).
Dernière prise à J - 3 pour rivaroxaban, apixaban. À J - 4 pour dabigatran si clairance de la créatinine ≥ 50 mL/min et J - 5 si clairance entre 30 et 50 (tableau ).
Arrêt des AVK à J - 5.
Seuls quelques actes ciblés comme la neurochirurgie intracrânienne imposent l’arrêt de tout antithrombotique et le retour d’une hémostase strictement normale : soit des délais d’interruption plus élevés : J - 5 pour les AOD, les AVK et l’aspirine ; J - 7 pour le clopidrogrel et le ticagrelor, J - 9 pour le prasugrel.
Généralement, ces interventions imposent l’arrêt du traitement anticoagulant et des anti-P2Y12 (
Dernière prise à J - 3 pour rivaroxaban, apixaban. À J - 4 pour dabigatran si clairance de la créatinine ≥ 50 mL/min et J - 5 si clairance entre 30 et 50 (
Arrêt des AVK à J - 5.
Seuls quelques actes ciblés comme la neurochirurgie intracrânienne imposent l’arrêt de tout antithrombotique et le retour d’une hémostase strictement normale : soit des délais d’interruption plus élevés : J - 5 pour les AOD, les AVK et l’aspirine ; J - 7 pour le clopidrogrel et le ticagrelor, J - 9 pour le prasugrel.
Risque hémorragique faible
Chirurgie de la cataracte, cutanée, certains actes buccodentaires, quelques pratiques en rhumatologie, endoscopies digestives ou bronchiques diagnostiques…
Ces gestes responsables de saignements peu fréquents (ou aisément contrôlables) peuvent être pratiqués sous bithérapie antiplaquettaire et sous anticoagulant.
Pour les AVK, vérifier l’absence de surdosage objectivé par un INR récent, généralement entre 2 et 3 (7 à 10 jours avant l’intervention).
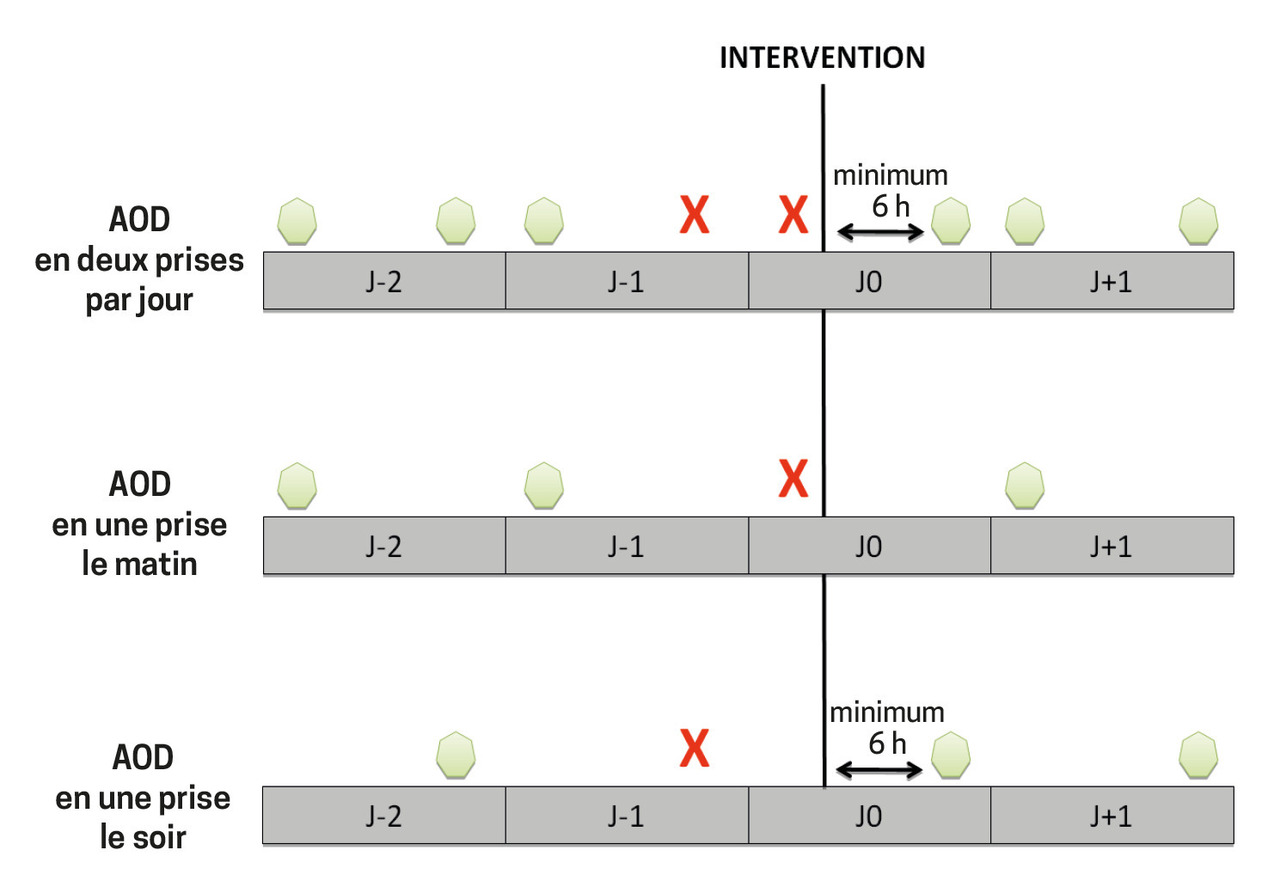
Pour les AOD, supprimer la prise de la veille au soir et celle du matin de l’intervention (si 2 prises/j ;figure ).
Concernant les endoscopies digestives, la gestion des antithrombotiques peut être définie par chaque centre. Si les explorations diagnostiques peuvent être réalisées sous bithérapie antiplaquettaire et anticoagulant à dose curative, la nécessité d’une biopsie ou de résection d’une lésion fait parfois stopper l’antithrombotique, pourvu que le risque thrombotique du patient ne soit pas très élevé.
En l’absence d’événement hémorragique : reprise du traitement 6 heures au moins après la fin de la chirurgie.
Ces gestes responsables de saignements peu fréquents (ou aisément contrôlables) peuvent être pratiqués sous bithérapie antiplaquettaire et sous anticoagulant.
Pour les AVK, vérifier l’absence de surdosage objectivé par un INR récent, généralement entre 2 et 3 (7 à 10 jours avant l’intervention).
Pour les AOD, supprimer la prise de la veille au soir et celle du matin de l’intervention (si 2 prises/j ;
Concernant les endoscopies digestives, la gestion des antithrombotiques peut être définie par chaque centre. Si les explorations diagnostiques peuvent être réalisées sous bithérapie antiplaquettaire et anticoagulant à dose curative, la nécessité d’une biopsie ou de résection d’une lésion fait parfois stopper l’antithrombotique, pourvu que le risque thrombotique du patient ne soit pas très élevé.
En l’absence d’événement hémorragique : reprise du traitement 6 heures au moins après la fin de la chirurgie.
Encadre
Qu’est-ce qu’une intervention à risque ?
Le risque hémorragique lié à la chirurgie correspond au volume de saignement attendu ou à la localisation particulièrement menaçante d’un saignement du site opératoire. Ainsi la cure d’un anévrisme de l’aorte abdominale par laparotomie et la neurochirurgie intracrânienne sont toutes deux des chirurgies à haut risque hémorragique. De même, la technique d’anesthésie retenue peut influer sur la gestion du traitement antithrombotique : l’anesthésie locorégionale périmédullaire (rachianesthésie et anesthésie péridurale) ne peut se faire qu’en l’absence de traitement antithrombotique, ou sous aspirine seule.
Références
1. Godier A, Fontana P, Motte S, et al. Management of antiplatelet therapy in patients undergoing elective invasive procedures. Proposals from the French Working Group on perioperative haemostasis (GIHP) and the French Study Group on thrombosis and haemostasis (GFHT). In collaboration with the French Society for Anaesthesia and Intensive Care Medicine (SFAR). Anaesth Crit Care Pain Med 2018;37:379-89.
2. Valgimigli M, Bueno H, Byrne RA, et al. 2017 ESC focused update on dual anti- platelet therapy in coronary artery disease developed in collaboration with EACTS: The Task Force for dual antiplatelet therapy in coronary artery disease of the European Society of Cardiology (ESC) and of the European Association for Cardio- Thoracic Surgery (EACTS). Eur Heart J 2018;39:213-60.
3. Albaladejo P, Bonhomme F, Blais N, et al. Management of direct oral anticoagulants in patients undergoing elective surgeries and invasive procedures: Updated guidelines from the French Working Group on Perioperative Hemostasis (GIHP). Anaesth Crit Care Pain Med 2017;36:73-6.
4. Pernod G, Godiér A, Gozalo C, Tremey B, Sié P. French clinical practice guidelines on the management of patients on vitamin K antagonists in at-risk situations (overdose, risk of bleeding, and active bleeding). Thromb Res 2010;126:e167-74.
5. Steffel J, Verhamme P, Potpara TS, et al. The 2018 European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J 2018;39:1330-93.
2. Valgimigli M, Bueno H, Byrne RA, et al. 2017 ESC focused update on dual anti- platelet therapy in coronary artery disease developed in collaboration with EACTS: The Task Force for dual antiplatelet therapy in coronary artery disease of the European Society of Cardiology (ESC) and of the European Association for Cardio- Thoracic Surgery (EACTS). Eur Heart J 2018;39:213-60.
3. Albaladejo P, Bonhomme F, Blais N, et al. Management of direct oral anticoagulants in patients undergoing elective surgeries and invasive procedures: Updated guidelines from the French Working Group on Perioperative Hemostasis (GIHP). Anaesth Crit Care Pain Med 2017;36:73-6.
4. Pernod G, Godiér A, Gozalo C, Tremey B, Sié P. French clinical practice guidelines on the management of patients on vitamin K antagonists in at-risk situations (overdose, risk of bleeding, and active bleeding). Thromb Res 2010;126:e167-74.
5. Steffel J, Verhamme P, Potpara TS, et al. The 2018 European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J 2018;39:1330-93.

 Encadrés
Encadrés