La maladie variqueuse est souvent considérée, à tort, comme une pathologie bénigne.
Ses complications, même si elles restent rares, peuvent être graves. Elles vont des atteintes cutanées à l’hémorragie aiguë par rupture de varices et la maladie thromboembolique veineuse (MTEV).
Ses complications, même si elles restent rares, peuvent être graves. Elles vont des atteintes cutanées à l’hémorragie aiguë par rupture de varices et la maladie thromboembolique veineuse (MTEV).
Atteintes cutanées chez un patient sur dix
Les complications cutanées touchent près de 10 % des patients atteints d’insuffisance veineuse chronique.
Conséquences d’une hyperpression veineuse, entre autres
Les atteintes cutanées et l’ulcère veineux sont principalement la conséquence d’une hyperpression veineuse ambulatoire liée à une insuffisance veineuse superficielle et/ou profonde. Cependant, il existe d’autres éléments qui participent à la survenue des troubles trophiques tels que le dysfonctionnement microvasculaire, la défaillance de la pompe musculaire du mollet, l’inflammation du derme, le dysfonctionnement des fibroblastes, la malnutrition, l’obésité et la colonisation bactérienne. L’hypertension veineuse provoque l’activation des neutrophiles et des monocytes qui, à leur tour, déclenchent des lésions de l’endothélium. Celles-ci entraînent une inflammation chronique de la peau connue cliniquement sous le nom de lipodermatosclérose. Ce phénomène est médié par les cellules inflammatoires périvasculaires, principalement les macrophages, dans la microcirculation cutanée. Ces cellules stimulent les fibroblastes de la peau, ce qui provoque un remodelage et la formation de tissus fibreux. Dans cet état, la peau est susceptible de s’ulcérer en réponse à une blessure mineure.1 Des études ont également démontré le rôle des métalloprotéinases matricielles (MMP) dans le remodelage de la peau via la dégradation des protéines de la matrice extracellulaire qui génère une altération de la cicatrisation.
Stades C4 à C6 de la classification CEAP
La classification clinique, étiologique, anatomique et physiopathologique (Clinical-Etiology-Anatomy-Pathophysiology classification ; CEAP) est utilisée pour décrire l’insuffisance veineuse chronique des membres inférieurs.2 Sa partie C se réfère à l’état clinique de la jambe et l’atteinte cutanée correspond au stade C4, C5 et C6 (voir le tableau dans l’article « Diagnostic de la maladie variqueuse », page 738 ).
Le stade C4 correspond au stade débutant des remaniements cutanés et se décline en trois entités.3
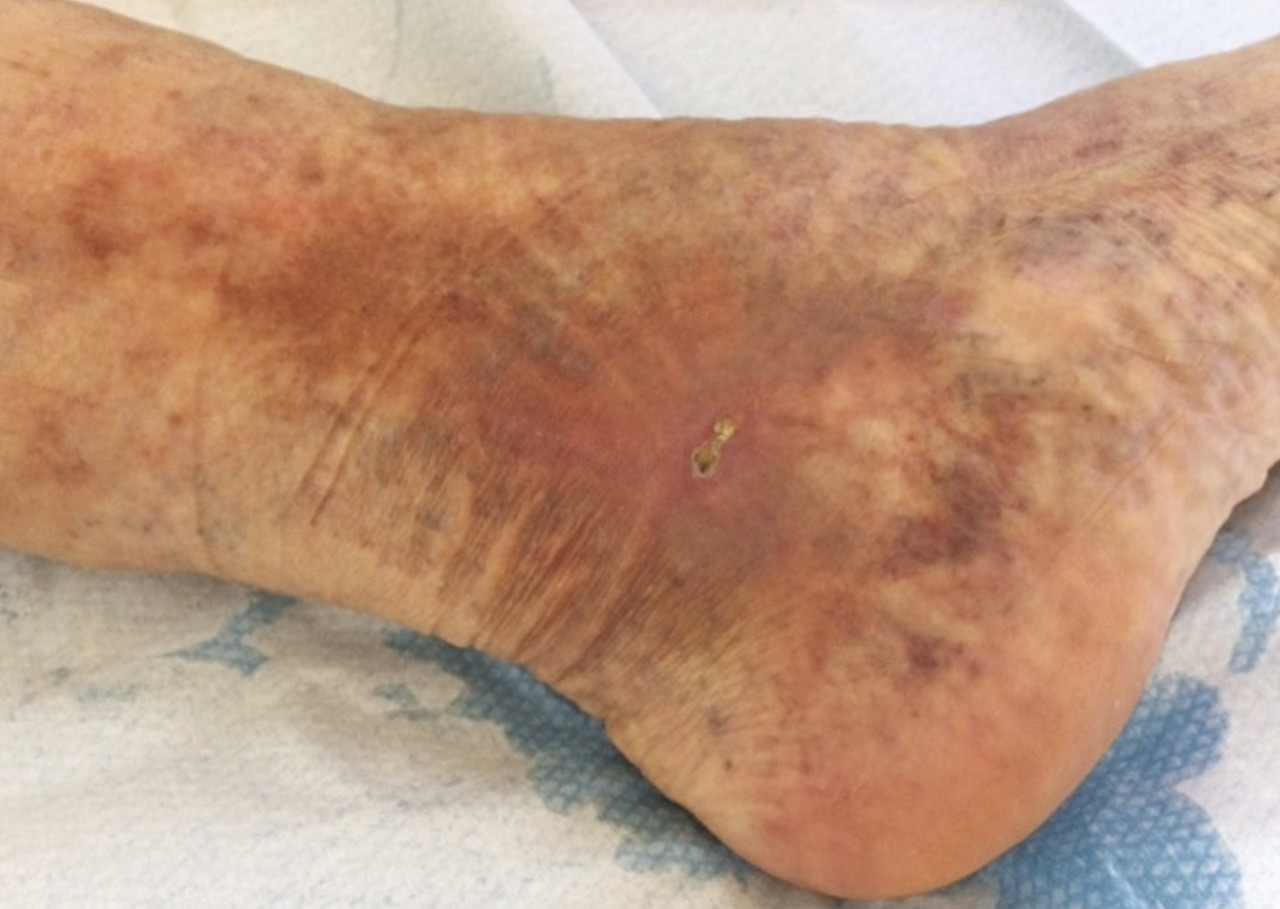
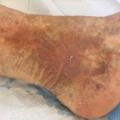
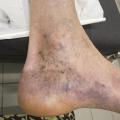
Elle se manifeste par des taches brunâtres plus ou moins étendues entre le genou et le pied (fig. 1 ).
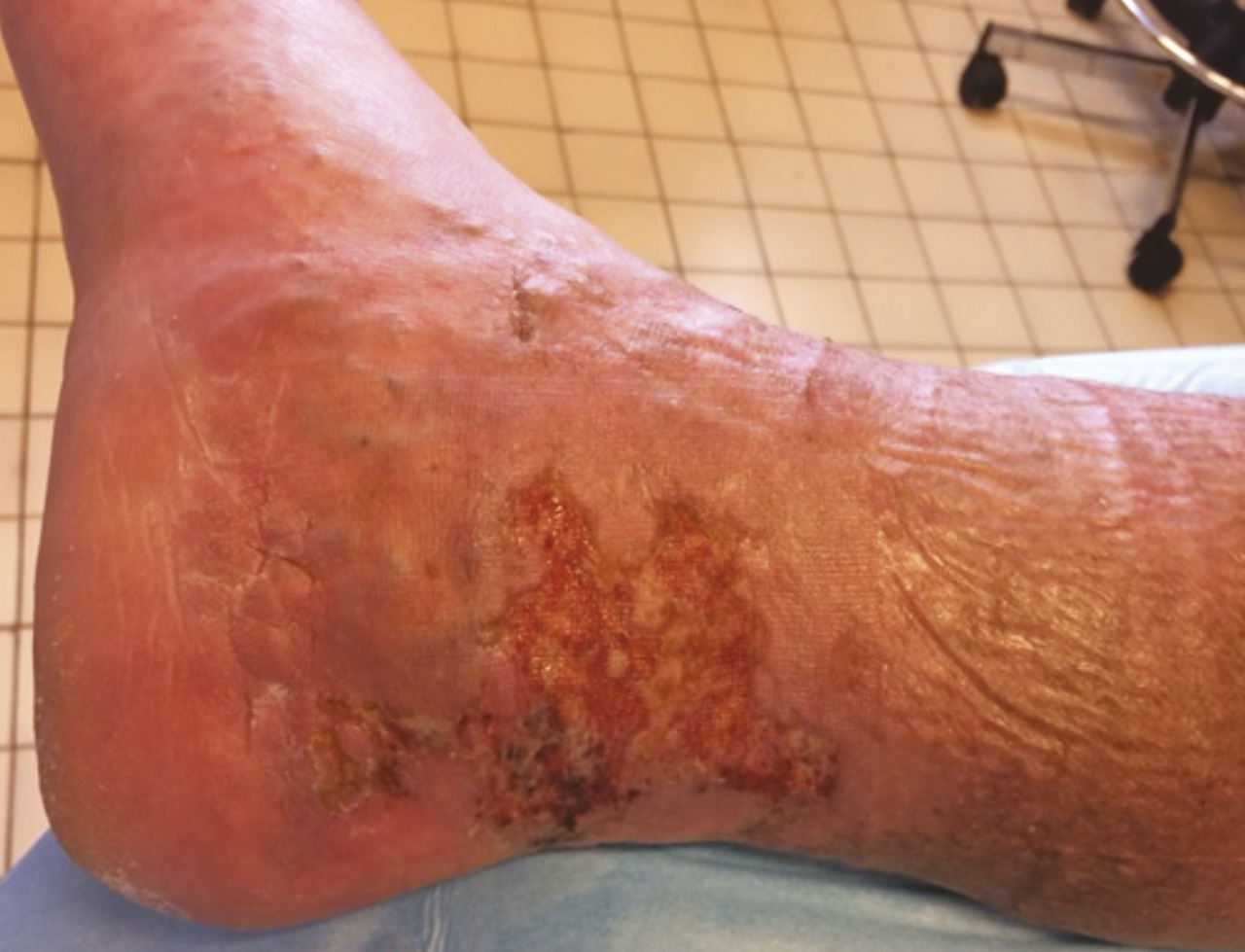
L’eczéma se traduit par des plaques érythémateuses mal délimitées, une desquamation, un érythème et une xérose des membres inférieurs. Les symptômes caractéristiques sont le prurit, la douleur, l’inflammation, un suintement, une desquamation, des changements de couleur et un épaississement de la peau.
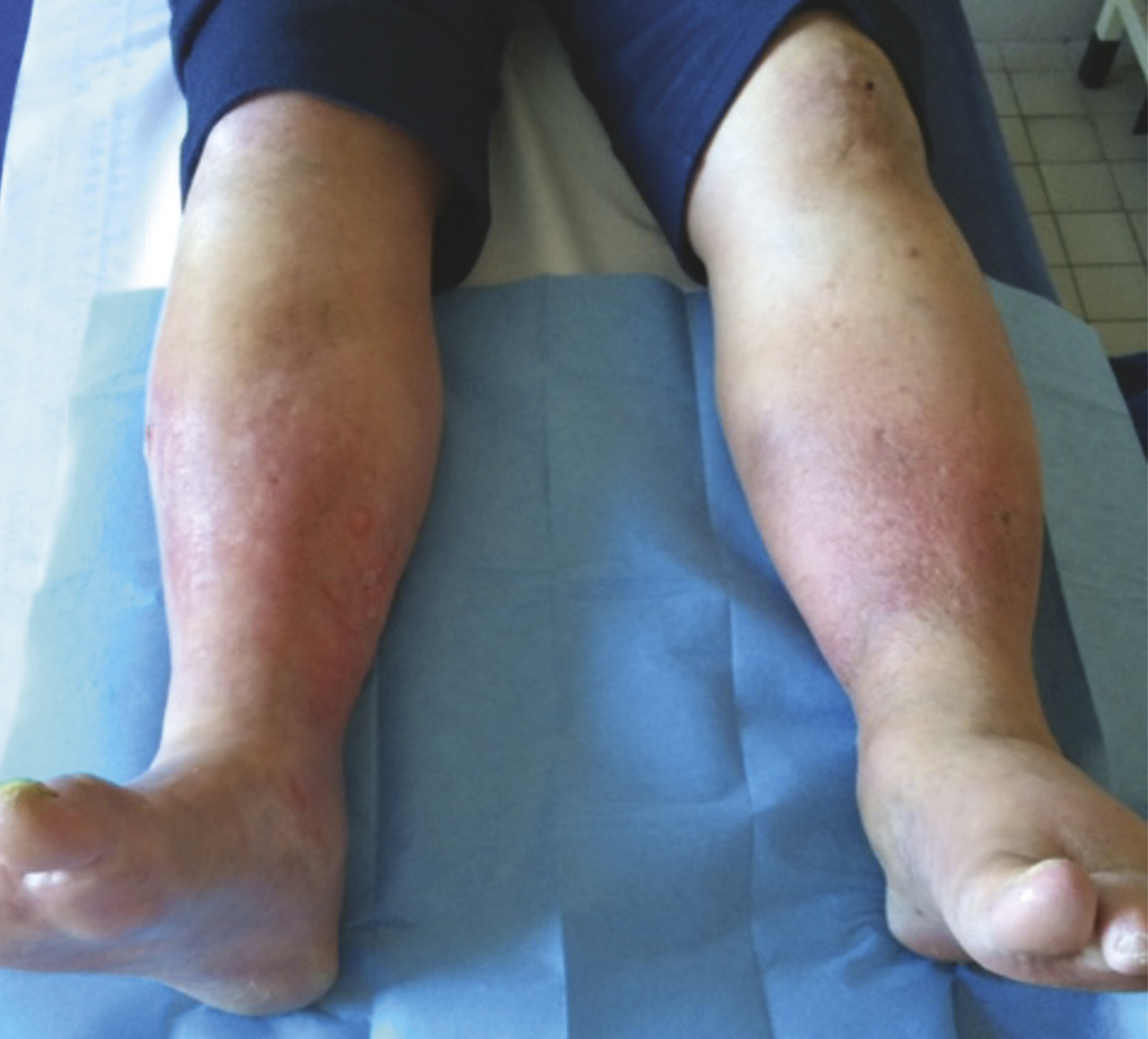
fig. 2 ).
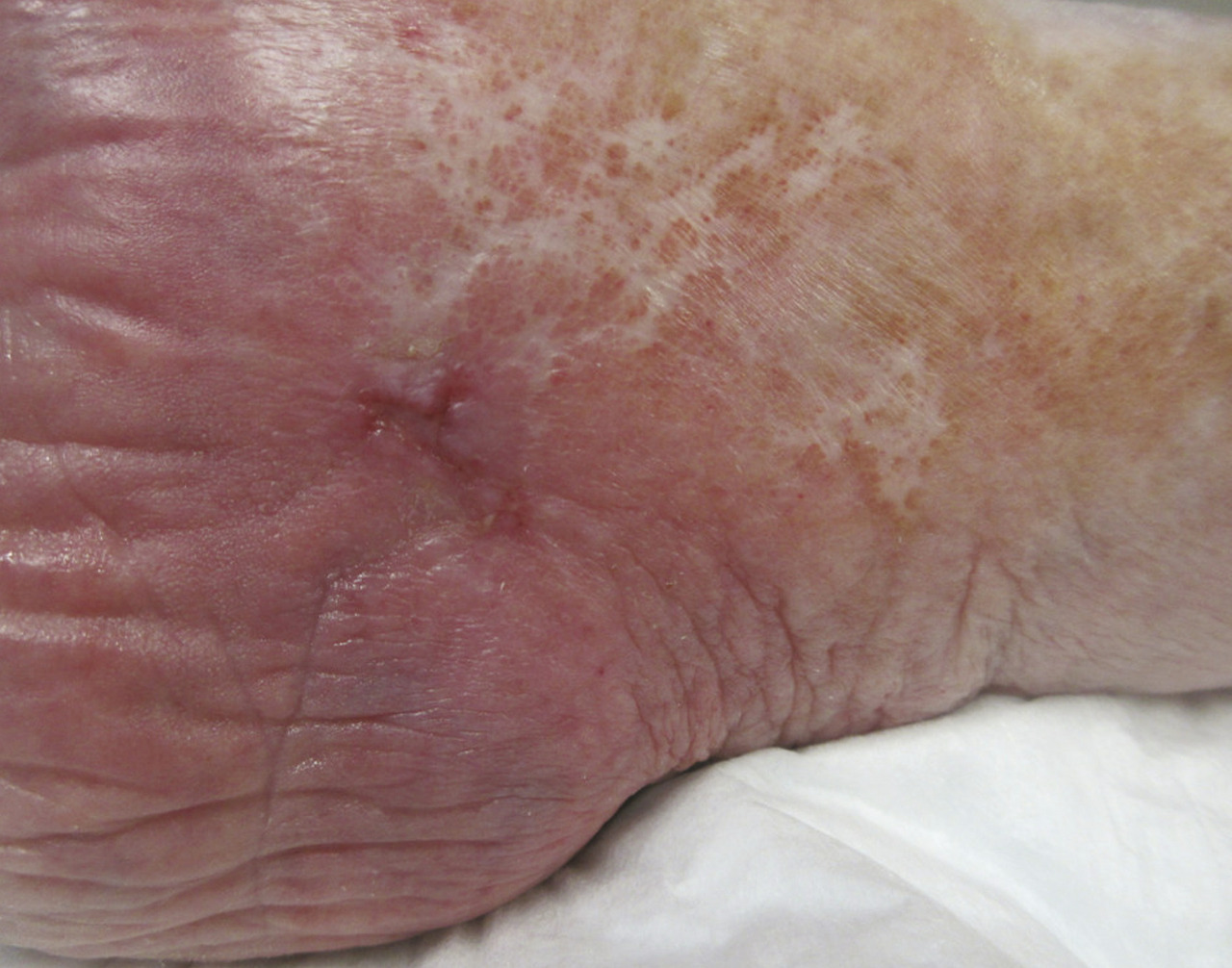
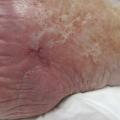
L’atrophie blanche est une zone dépigmentée et dépourvue de capillaires se présentant sous la forme d’une plaque lisse de couleur blanc ivoire (fig. 3 ). Elle est généralement localisée aux membres inférieurs. L’étiopathologie est multiple, mais l’insuffisance veineuse est une cause possible. Il s’agit de ne pas la confondre avec des zones cicatricielles.
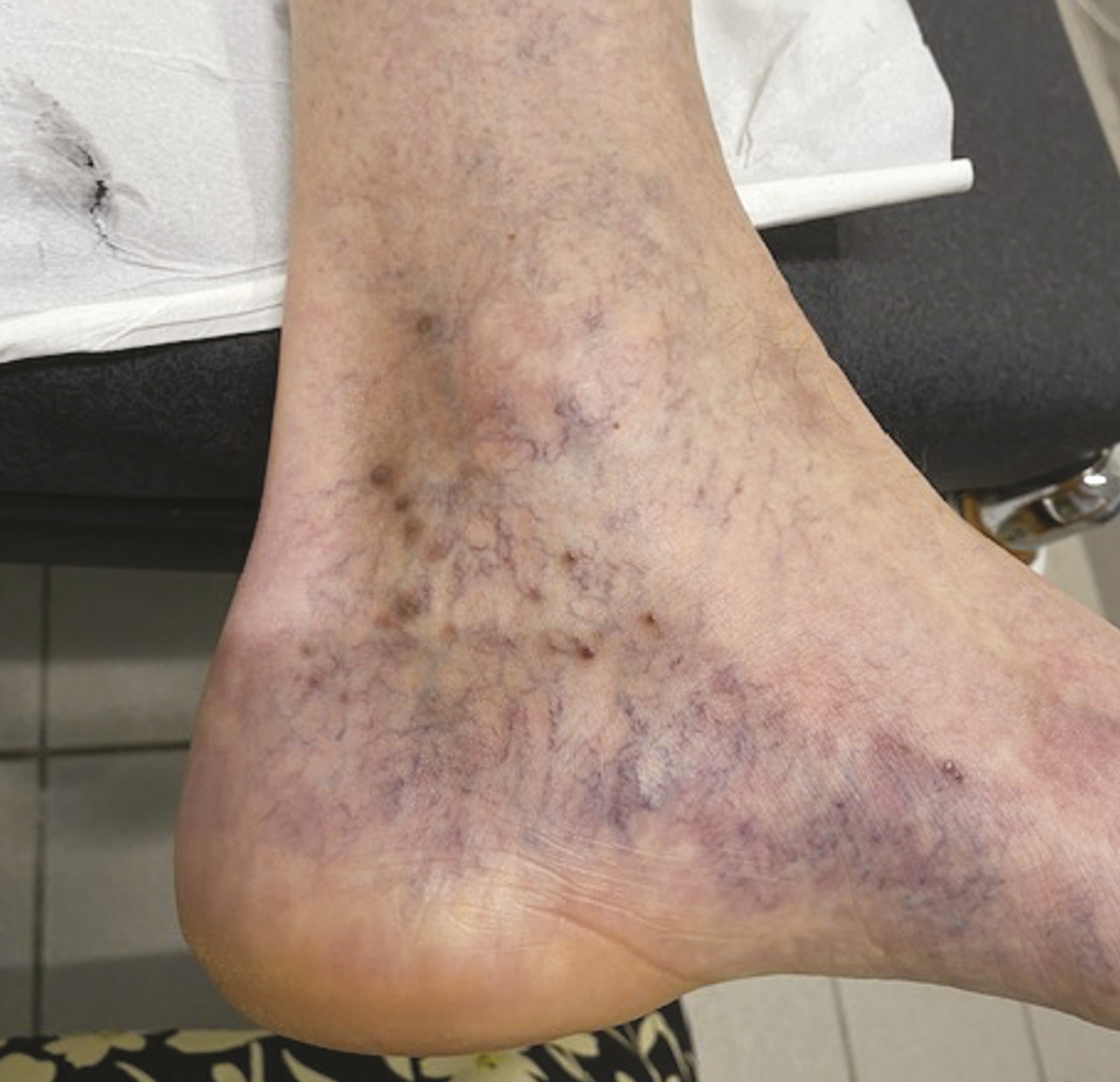
fig. 4 ). De nombreuses publications suggèrent que la présence d’une corona phlebectatica correspond à un stade avancé d’insuffisance veineuse chronique, et les patients atteints sont 5,3 fois plus susceptibles de développer un ulcère.4
Le stade C4 correspond au stade débutant des remaniements cutanés et se décline en trois entités.3
C4a : dermite ocre (pigmentation) ou eczéma
La dermite ocre (ou pigmentation) est la conséquence d’un dépôt d’hémosidérine (produit dérivé de l’hémoglobine des érythrocytes extravasés sous la peau) et de la stase veineuse.Elle se manifeste par des taches brunâtres plus ou moins étendues entre le genou et le pied (
L’eczéma se traduit par des plaques érythémateuses mal délimitées, une desquamation, un érythème et une xérose des membres inférieurs. Les symptômes caractéristiques sont le prurit, la douleur, l’inflammation, un suintement, une desquamation, des changements de couleur et un épaississement de la peau.
C4b : lipodermatosclérose ou atrophie blanche
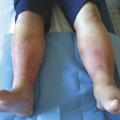
La lipodermatosclérose est une panniculite du tissu sous-cutané et de la peau qui induit progressivement une fibrose cutanée. Cliniquement, la peau perd sa souplesse, et l’induration sous-cutanée provoque une rétraction des tissus donnant un aspect dit en « mollet de coq ». En cas de poussée inflammatoire, la lipodermatosclérose peut se manifester sous la forme de plaques érythémateuses douloureuses (L’atrophie blanche est une zone dépigmentée et dépourvue de capillaires se présentant sous la forme d’une plaque lisse de couleur blanc ivoire (
C4c : corona phlebectatica
La corona phlebectatica correspond à la présence de petits vaisseaux intradermiques localisés au niveau des régions malléolaires, disposés en forme d’éventail (Ulcère de jambe veineux, plaie chronique
L’ulcère de jambe est une plaie chronique des membres inférieurs (c’est-à-dire n’ayant pas la capacité de cicatriser spontanément après quatre à six semaines d’évolution). Un pour cent de la population française a un ulcère de jambe.
Dans 80 % des cas, une cause vasculaire est retrouvée, avec près de 65 % d’ulcère veineux et 15 % d’ulcère artériel dont 15 % d’ulcère mixte.
L’ulcère de jambe est le stade ultime de l’évolution de la maladie vasculaire et témoigne de sa gravité. Il est donc indispensable de réaliser une évaluation vasculaire par un écho-Doppler artériel et/ou veineux des membres inférieurs.5 En cas d’ulcère de jambe veineux (UJV), il existe une insuffisance veineuse superficielle dans 40 à 50 % des cas.
Le stade C5 de la classification CEAP correspond à un ulcère veineux cicatrisé, le stade C6 à un ulcère ouvert et le C6r correspond à un ulcère ouvert récidivant.
L’UJV évolue souvent depuis plusieurs années, et les patients décrivent des périodes de cicatrisation qui alternent avec des phases de récidive. Il est généralement localisé au tiers inférieur de la jambe dans la région périmalléolaire et ne touche pas le pied. La présentation clinique habituelle est celle d’une ulcération cutanée superficielle dont les berges sont irrégulières et « émiettées » (« en carte de géographie »), souvent étendue, parfois circonférentielle, exsudative, pouvant être douloureuse et dont la peau périulcéreuse est souvent pathologique (érythème, macération, hyperkératose, eczéma, œdème, etc.) [fig. 5 ]. Des signes d’insuffisance veineuse chronique peuvent lui être associés, dont les atteintes cutanées précédemment détaillées. Dans sa forme pure, en l’absence de participation artérielle, les pouls périphériques sont présents et l’indice de pression systolique à la cheville (IPS) est compris entre 0,91 et 1,40.
La durée moyenne de cicatrisation d’un UJV est de 210 jours, et moins de 40 % guérissent en moins de trois mois. Véritable problème de santé publique, le coût de prise en charge par la Caisse nationale d’assurance maladie (Cnam) est estimé à plus de 272 millions d’euros par an.6 Cette pathologie chronique altère considérablement la qualité de vie des patients. Le taux de récidive est de 30 % et atteint 70 % en cas de syndrome post-thrombotique.
Le traitement des atteintes cutanées et de l’UJV repose sur la correction de l’hyperpression veineuse ambulatoire. Pour cela, une compression veineuse par bandages multicouches ou orthèses est indispensable. Les sociétés savantes recommandent un niveau de compression élevé (entre 30 et 40 mmHg : classes 3 ou 4) auquel doivent être associées une bonne hygiène de vie, une réduction de la surcharge pondérale et une activité physique adaptée.7,8 En parallèle, une prise en charge dédiée de la maladie veineuse doit être appliquée (traitements des varices et du syndrome post-thrombotique) pour accélérer la cicatrisation et prévenir les récidives.9
Dans 80 % des cas, une cause vasculaire est retrouvée, avec près de 65 % d’ulcère veineux et 15 % d’ulcère artériel dont 15 % d’ulcère mixte.
L’ulcère de jambe est le stade ultime de l’évolution de la maladie vasculaire et témoigne de sa gravité. Il est donc indispensable de réaliser une évaluation vasculaire par un écho-Doppler artériel et/ou veineux des membres inférieurs.5 En cas d’ulcère de jambe veineux (UJV), il existe une insuffisance veineuse superficielle dans 40 à 50 % des cas.
Le stade C5 de la classification CEAP correspond à un ulcère veineux cicatrisé, le stade C6 à un ulcère ouvert et le C6r correspond à un ulcère ouvert récidivant.
L’UJV évolue souvent depuis plusieurs années, et les patients décrivent des périodes de cicatrisation qui alternent avec des phases de récidive. Il est généralement localisé au tiers inférieur de la jambe dans la région périmalléolaire et ne touche pas le pied. La présentation clinique habituelle est celle d’une ulcération cutanée superficielle dont les berges sont irrégulières et « émiettées » (« en carte de géographie »), souvent étendue, parfois circonférentielle, exsudative, pouvant être douloureuse et dont la peau périulcéreuse est souvent pathologique (érythème, macération, hyperkératose, eczéma, œdème, etc.) [
La durée moyenne de cicatrisation d’un UJV est de 210 jours, et moins de 40 % guérissent en moins de trois mois. Véritable problème de santé publique, le coût de prise en charge par la Caisse nationale d’assurance maladie (Cnam) est estimé à plus de 272 millions d’euros par an.6 Cette pathologie chronique altère considérablement la qualité de vie des patients. Le taux de récidive est de 30 % et atteint 70 % en cas de syndrome post-thrombotique.
Le traitement des atteintes cutanées et de l’UJV repose sur la correction de l’hyperpression veineuse ambulatoire. Pour cela, une compression veineuse par bandages multicouches ou orthèses est indispensable. Les sociétés savantes recommandent un niveau de compression élevé (entre 30 et 40 mmHg : classes 3 ou 4) auquel doivent être associées une bonne hygiène de vie, une réduction de la surcharge pondérale et une activité physique adaptée.7,8 En parallèle, une prise en charge dédiée de la maladie veineuse doit être appliquée (traitements des varices et du syndrome post-thrombotique) pour accélérer la cicatrisation et prévenir les récidives.9
Rupture des varices, risque d’hémorragie grave
La rupture spontanée ou liée à un traumatisme de la varice est une complication pouvant conduire à une mort naturelle inattendue, due à une hémorragie grave et est documentée dans 0,15 à 2 % de la population. L’hémorragie veineuse se distingue de l’hémorragie artérielle par un débit plus faible. Cependant, dans certains cas, le saignement peut être important lorsque la pression du sang dans les veines distendues est élevée. Les premiers rapports de décès par hémorragie aiguë par rupture de varices datent des années 1970. Deux grands types de plaies hémorragiques ont été décrits. Le premier est une ulcération aiguë avec de petites lésions superficielles et une pigmentation adjacente sur la peau saine environnante pouvant survenir spontanément ou après un traumatisme mineur. L’autre type est l’ulcère chronique, plus étendu et plus profond.
De nombreux patients ayant des varicosités de degré non sévère sous-estiment le risque d’une rupture de varice alors qu’il existe une menace potentielle d’hémorragie massive et mortelle, notamment si le patient est sous traitement antithrombotique.
Le risque de rupture de varices est accru chez les sujets socialement vulnérables et chez les personnes âgées en raison de la fragilité de leurs peau et tissus mous. En cas de rupture de varices, la surélévation du membre et l’application d’un pansement compressif permet de traiter le saignement dans la majorité de cas.10
De nombreux patients ayant des varicosités de degré non sévère sous-estiment le risque d’une rupture de varice alors qu’il existe une menace potentielle d’hémorragie massive et mortelle, notamment si le patient est sous traitement antithrombotique.
Le risque de rupture de varices est accru chez les sujets socialement vulnérables et chez les personnes âgées en raison de la fragilité de leurs peau et tissus mous. En cas de rupture de varices, la surélévation du membre et l’application d’un pansement compressif permet de traiter le saignement dans la majorité de cas.10
Thrombose veineuse profonde et embolie pulmonaire, rares mais graves
La thrombose veineuse profonde (TVP) et l’embolie pulmonaire (EP) sont des complications rares mais potentiellement graves des veines variqueuses. Outre la détérioration de la circulation sanguine causée par les varices, l’inflammation est très probablement un dénominateur commun entre les varices et la thrombose car elle favorise un état procoagulant et la formation de thrombus, y compris dans les veines profondes. Les patients atteints de varices ont des niveaux accrus d’interleukines, marqueurs inflammatoires les plus spécifiques de l’inflammation de la paroi vasculaire, qui favorisent la coagulation. Les études ont montré que les varices peuvent augmenter le risque de TVP, mais peu de données existent sur l’incidence de la TVP chez les patients atteints de varices et sans facteurs de risque supplémentaires. Un risque accru est associé aux antécédents de maladie thromboembolique veineuse (MTEV), aux tumeurs malignes, à l’utilisation d’œstrogènes, à la grossesse et au post-partum, à l’hospitalisation au cours des six derniers mois, à l’âge et à l’obésité. Les varices constituent également un risque accru de MTEV lors d’une immobilisation de longue durée et de longs voyages en avion ou en voiture.
En outre, la thrombose veineuse superficielle est liée à un risque accru de TVP, en particulier si le thrombus de la veine superficielle s’étend près de la jonction saphéno-fémorale ou fémoro-poplitée. Le risque de TVP est augmenté pendant et après le traitement invasif des varices ; la thromboprophylaxie est alors recommandée chez les sujets de plus de 60 ans et chez ceux ayant un autre état thrombophilique.11
En outre, la thrombose veineuse superficielle est liée à un risque accru de TVP, en particulier si le thrombus de la veine superficielle s’étend près de la jonction saphéno-fémorale ou fémoro-poplitée. Le risque de TVP est augmenté pendant et après le traitement invasif des varices ; la thromboprophylaxie est alors recommandée chez les sujets de plus de 60 ans et chez ceux ayant un autre état thrombophilique.11
Références
1. Coleridge Smith P. The causes of skin damage and leg ulceration in chronic venous disease. Int J Low Extrem Wounds 2006;5(3):160-8.
2. Lurie F, Passman M, Meisner M, Dalsing M, Masuda E, Welch H, et al. The 2020 update of the CEAP classification system and reporting standards. J Vascul Surg Ven Lymph Disord 2020;8(3):342-52.
3. Yosipovitch G, Nedorost S, Silverberg J. Stasis dermatitis: An overview of its clinical presentation, pathogenesis, and management. American Journal of Clinical Dermatology 2023;24:275-86.
4. Uhl JF, Cornu-Thenard A, Satger B, Carpentier PH. Clinical analysis of the corona phlebectatica. J Vasc Surg 2012;55:150-3.
5. Haute Autorité de santé. Recommandations pour la pratique clinique. Prise en charge de l’ulcère de jambe à prédominance veineuse hors pansement. 2006.
6. Rames O, Sebo S, Pecault R, Agamaliyev E, Tuppin P, Rodde Dunet M, et al. Chronic wounds in France: Prevalence, characteristics and evolution. Improved implementation of management on discharge on hospital. Journal des Plaies et Cicatrisation 2014;92(14):12-8.
7. Shi C, Dumville JC, Cullum N, Connaughton E, Norman G. Compression bandages or stockings versus no compression for treating venous leg ulcers. Cochrane Database of Systematic Reviews 2021;7(7):CD013397.
8. De Maeseneer MG, Kakkos SK, Aherne T, Baekgaard N, Black S, Blomgren L, et al. European Society for Vascular Surgery (ESVS) 2022 Clinical practice guidelines on the management of chronic venous disease of the lower limbs. Eur J Vasc Endovasc Surg 2022;63(2):184-267.
9. Gohel MS, Heatley F, Liu X, Bradbury A, Bulbulia R, Cullum N, et al. Early versus deferred endovenous ablation of superficial venous reflux in patients with venous ulceration: The EVRA RCT. Health Technol Assess 2019;23(24):1-96.
10. Gentile G, Tambuzzi S, Boracchi M, Gobbo A, Bailo P, Zoia R. Fatal hemorrhage from peripheral varicose vein rupture. Autops Case Rep 2021;11:e2021330.
11. Poredos P, Kozak M, Antignani P, Jezovnik M. From varicose veins to venous thromboembolic events. Int Angiol 2023;42(3):254-9.
2. Lurie F, Passman M, Meisner M, Dalsing M, Masuda E, Welch H, et al. The 2020 update of the CEAP classification system and reporting standards. J Vascul Surg Ven Lymph Disord 2020;8(3):342-52.
3. Yosipovitch G, Nedorost S, Silverberg J. Stasis dermatitis: An overview of its clinical presentation, pathogenesis, and management. American Journal of Clinical Dermatology 2023;24:275-86.
4. Uhl JF, Cornu-Thenard A, Satger B, Carpentier PH. Clinical analysis of the corona phlebectatica. J Vasc Surg 2012;55:150-3.
5. Haute Autorité de santé. Recommandations pour la pratique clinique. Prise en charge de l’ulcère de jambe à prédominance veineuse hors pansement. 2006.
6. Rames O, Sebo S, Pecault R, Agamaliyev E, Tuppin P, Rodde Dunet M, et al. Chronic wounds in France: Prevalence, characteristics and evolution. Improved implementation of management on discharge on hospital. Journal des Plaies et Cicatrisation 2014;92(14):12-8.
7. Shi C, Dumville JC, Cullum N, Connaughton E, Norman G. Compression bandages or stockings versus no compression for treating venous leg ulcers. Cochrane Database of Systematic Reviews 2021;7(7):CD013397.
8. De Maeseneer MG, Kakkos SK, Aherne T, Baekgaard N, Black S, Blomgren L, et al. European Society for Vascular Surgery (ESVS) 2022 Clinical practice guidelines on the management of chronic venous disease of the lower limbs. Eur J Vasc Endovasc Surg 2022;63(2):184-267.
9. Gohel MS, Heatley F, Liu X, Bradbury A, Bulbulia R, Cullum N, et al. Early versus deferred endovenous ablation of superficial venous reflux in patients with venous ulceration: The EVRA RCT. Health Technol Assess 2019;23(24):1-96.
10. Gentile G, Tambuzzi S, Boracchi M, Gobbo A, Bailo P, Zoia R. Fatal hemorrhage from peripheral varicose vein rupture. Autops Case Rep 2021;11:e2021330.
11. Poredos P, Kozak M, Antignani P, Jezovnik M. From varicose veins to venous thromboembolic events. Int Angiol 2023;42(3):254-9.