L’accompagnement des parents est primordial.
Les surdités moyennes à profondes concernent 1 enfant sur 1 000 à la naissance et 1 sur 750 secondairement.1 Le dépistage néonatal universel est en vigueur en France depuis 2012,2 abaissant l’âge moyen au diagnostic.3 Une prise en charge précoce améliore l’acquisition d’une communication verbale et non verbale, avec un impact en termes de comportement, sociabilité, scolarité.1, 4 Des atteintes syndromiques peuvent être associées dans 10 % des cas, et un traitement étiopathogénique est parfois proposé (fœtopathie à CMV).5 Pour rappel, si l’on ne dépiste que les enfants à risque, on ne repère que la moitié des surdités à la naissance.4
Ce sont les agences régionales de santé (ARS) qui organisent le dépistage. Elles s’appuient, en fonction des régions, soit sur les réseaux de périnatalité, soit sur les ARDPHE (Associations régionales de dépistage, dépendantes de l’AFDPHE, Association française pour le dépistage et la prévention des handicaps de l’enfant) soit sur les deux.
Ce sont les agences régionales de santé (ARS) qui organisent le dépistage. Elles s’appuient, en fonction des régions, soit sur les réseaux de périnatalité, soit sur les ARDPHE (Associations régionales de dépistage, dépendantes de l’AFDPHE, Association française pour le dépistage et la prévention des handicaps de l’enfant) soit sur les deux.
Quels tests ?
Les oto-émissions acoustiques provoquées (OEAP) sont des émissions sonores produites par la contraction des cellules ciliées externes de la cochlée (donc par l’oreille interne) en réponse à une stimulation à 35 dB (clics émis par une sonde placée dans le conduit auditif externe). Elles sont absentes dès 30 dB de perte. Le résultat est binaire, de type « bien/à recontrôler ». Le taux de faux positifs (absence d’OEAP alors que l’audition est normale) est de 3-8 % au premier test et de 0,7-6 % au second à 48 heures (persistance de liquide dans l’oreille externe ou moyenne, milieu ambiant trop bruyant). Les faux négatifs (OEAP présentes alors que l’enfant est sourd) varient de 0,009 à 0,2 % (neuropathies auditives : atteinte élective des cellules ciliées internes, ou rétro-cochléaire ; synaptopathie liée à la mutation du gène de l’otoferline).
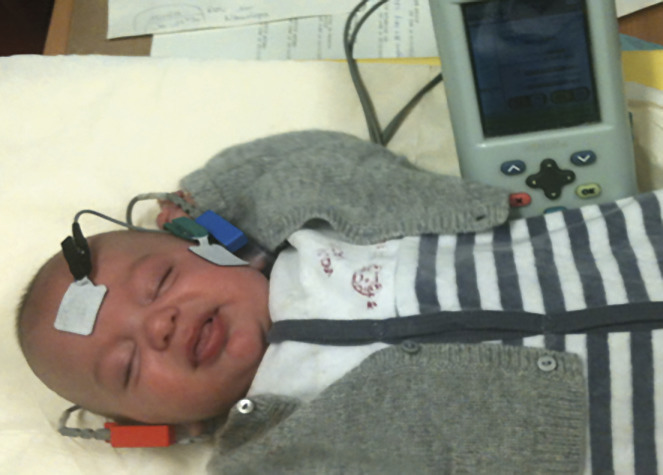
Les potentiels évoqués auditifs automatisés (PEAA) témoignent de l’activité électrique des voies auditives jusqu’aux premiers relais du tronc cérébral en réponse à une stimulation sonore à 35 dB sur les fréquences 2 000-4 000 Hz. La réponse est binaire : « bien /à recontrôler ». Le taux de faux positifs est de 0,2 à 0,8 % au second test.6 Pas de faux négatif. C’est l’outil à choisir pour les enfants à risque, dans les maternités de niveau 3, les services de néonatalogie et de réanimation (fig. 1).
Les potentiels évoqués auditifs automatisés (PEAA) témoignent de l’activité électrique des voies auditives jusqu’aux premiers relais du tronc cérébral en réponse à une stimulation sonore à 35 dB sur les fréquences 2 000-4 000 Hz. La réponse est binaire : « bien /à recontrôler ». Le taux de faux positifs est de 0,2 à 0,8 % au second test.6 Pas de faux négatif. C’est l’outil à choisir pour les enfants à risque, dans les maternités de niveau 3, les services de néonatalogie et de réanimation (fig. 1).
Trois étapes
Les hôpitaux reçoivent un financement de 18,70 euros par nouveau-né dépisté. Les tests sont réalisés par le personnel paramédical formé par les ORL.
Il faut être très vigilant sur la qualité de l’information qui est donnée aux familles. L’accord des parents pour le dépistage doit être recueilli au préalable. En aucun cas, on ne pose un diagnostic de surdité en maternité, il s’agit d’une vérification de l’audition. Attention aux annonces non justifiées et à leur retentissement psychologique. Pour cela, le personnel réalisant le test doit être formé, afin d’avoir un discours bien codifié (encadré). Sur 1 000 naissances, 10 enfants seront à recontrôler, et parmi eux un seul aura une perte auditive.
Première étape, on réalise un test OEAP ou PEAA :
– s’il est satisfaisant sur les 2 oreilles, les parents sont rassurés sur l’audition de leur enfant ;
– s’il est anormal des 2 côtés, un nouveau test est pratiqué dans les 48 heures avant la sortie de maternité ; si le 2e test reste anormal des 2 côtés, le nouveau-né doit être revu pour contrôle en étape 2 (c’est à la maternité de prendre le rendez-vous pour les parents auprès d’un professionnel, dans les 28 jours) ;
– si le test est normal d’un seul côté, et que l’enfant a un facteur de risque : rendez-vous de contrôle (étape 2). En l’absence de facteur de risque, l’attitude diffère selon les régions. En Île-de-France, on rassure les parents sur l’audition globale de leur enfant ; on conseille de faire une évaluation à 1 an et de rester vigilants sur le développement du langage.
Dans tous les cas, les résultats sont expliqués à la famille et notés dans le carnet de santé. Parallèlement, ils sont consignés sur le carton de Guthrie et transmis à l’ARDPHE et/ou aux réseaux de périnatalité, en fonction de l’organisation propre à chaque région.
Si l’enfant sort avant le test, la maternité doit organiser le suivi. S’il est transféré vers une autre structure de soins (réanimation, néonatalogie), l’ARDPHE et les réseaux doivent être prévenus. C’est à la structure qui accueille l’enfant qu’incombe l’organisation du dépistage. Il faut être particulièrement attentif à ces enfants, car ils sont le plus à risque de surdité (7,12/1 000 vs 0,81/1 000 chez les non-transférés) mais les moins dépistés (75,4 % vs 97,5 %).6
Deuxième étape. Le contrôle peut être effectué par un ORL de ville, dans un CAMSP (centre d’action médico-sociale précoce) ou un centre hospitalier de proximité. Il est réalisé préférentiellement par PEAA. Si une déficience auditive est suspectée ou confirmée, l’enfant est alors adressé au CDOS référent (centre de diag-nostic et d’orientation de la surdité) pour l’étape suivante. Les coordonnées du centre sont données aux familles par les acteurs de l’étape 2. Dans certaines régions, ces derniers peuvent aussi prendre en charge les surdités légères à moyennes. Les résultats sont envoyés à l’ARDPHE par la poste, via un formulaire prévu à cet effet.
Troisième étape. Dans le CDOS référent, le bilan comporte :
– recherche des antécédents familiaux et personnels, et des facteurs de risque (encadré) ;
– détection de signes de surdité syndromique (syndrome branchio-oto-rénal, de Waardenburg...), analyse des tympans sous microscope ;
– PEA standard, ASSR (Auditory Steady-State Responses), OEAP, impédancemétrie ;
– audiométrie comportementale.
Ces examens permettent de poser le diag-nostic de surdité en précisant le type d’atteinte auditive (transmission, perception, mixte) et le degré (de léger à profond). Il s’agit d’une consultation longue et difficile qui nécessite une grande disponibilité de l’équipe médicale et paramédicale, afin d’accompagner les familles lors de l’annonce d’un handicap chez leur enfant.
Un suivi psychologique et orthophonique est organisé en attendant que la prise en charge multidisciplinaire adaptée se mette en place.
Il faut être très vigilant sur la qualité de l’information qui est donnée aux familles. L’accord des parents pour le dépistage doit être recueilli au préalable. En aucun cas, on ne pose un diagnostic de surdité en maternité, il s’agit d’une vérification de l’audition. Attention aux annonces non justifiées et à leur retentissement psychologique. Pour cela, le personnel réalisant le test doit être formé, afin d’avoir un discours bien codifié (encadré). Sur 1 000 naissances, 10 enfants seront à recontrôler, et parmi eux un seul aura une perte auditive.
Première étape, on réalise un test OEAP ou PEAA :
– s’il est satisfaisant sur les 2 oreilles, les parents sont rassurés sur l’audition de leur enfant ;
– s’il est anormal des 2 côtés, un nouveau test est pratiqué dans les 48 heures avant la sortie de maternité ; si le 2e test reste anormal des 2 côtés, le nouveau-né doit être revu pour contrôle en étape 2 (c’est à la maternité de prendre le rendez-vous pour les parents auprès d’un professionnel, dans les 28 jours) ;
– si le test est normal d’un seul côté, et que l’enfant a un facteur de risque : rendez-vous de contrôle (étape 2). En l’absence de facteur de risque, l’attitude diffère selon les régions. En Île-de-France, on rassure les parents sur l’audition globale de leur enfant ; on conseille de faire une évaluation à 1 an et de rester vigilants sur le développement du langage.
Dans tous les cas, les résultats sont expliqués à la famille et notés dans le carnet de santé. Parallèlement, ils sont consignés sur le carton de Guthrie et transmis à l’ARDPHE et/ou aux réseaux de périnatalité, en fonction de l’organisation propre à chaque région.
Si l’enfant sort avant le test, la maternité doit organiser le suivi. S’il est transféré vers une autre structure de soins (réanimation, néonatalogie), l’ARDPHE et les réseaux doivent être prévenus. C’est à la structure qui accueille l’enfant qu’incombe l’organisation du dépistage. Il faut être particulièrement attentif à ces enfants, car ils sont le plus à risque de surdité (7,12/1 000 vs 0,81/1 000 chez les non-transférés) mais les moins dépistés (75,4 % vs 97,5 %).6
Deuxième étape. Le contrôle peut être effectué par un ORL de ville, dans un CAMSP (centre d’action médico-sociale précoce) ou un centre hospitalier de proximité. Il est réalisé préférentiellement par PEAA. Si une déficience auditive est suspectée ou confirmée, l’enfant est alors adressé au CDOS référent (centre de diag-nostic et d’orientation de la surdité) pour l’étape suivante. Les coordonnées du centre sont données aux familles par les acteurs de l’étape 2. Dans certaines régions, ces derniers peuvent aussi prendre en charge les surdités légères à moyennes. Les résultats sont envoyés à l’ARDPHE par la poste, via un formulaire prévu à cet effet.
Troisième étape. Dans le CDOS référent, le bilan comporte :
– recherche des antécédents familiaux et personnels, et des facteurs de risque (encadré) ;
– détection de signes de surdité syndromique (syndrome branchio-oto-rénal, de Waardenburg...), analyse des tympans sous microscope ;
– PEA standard, ASSR (Auditory Steady-State Responses), OEAP, impédancemétrie ;
– audiométrie comportementale.
Ces examens permettent de poser le diag-nostic de surdité en précisant le type d’atteinte auditive (transmission, perception, mixte) et le degré (de léger à profond). Il s’agit d’une consultation longue et difficile qui nécessite une grande disponibilité de l’équipe médicale et paramédicale, afin d’accompagner les familles lors de l’annonce d’un handicap chez leur enfant.
Un suivi psychologique et orthophonique est organisé en attendant que la prise en charge multidisciplinaire adaptée se mette en place.
Bilan de la surdité
Devant toute surdité, il faut pratiquer :5
– audiométrie des parents et de la fratrie ;
– examen ophtalmologique avec FO ;
– si surdité de perception : IRM (cérébrale, conduits auditifs internes, rochers, bulbes olfactifs) ;
– si surdité de transmission : scanner des rochers ;
– recherche d’infection congénitale par le CMV : PCR CMV (sur salive avant 1 an, urine ou sur carton de Guthrie avant 2 ans) ; sérologies CMV mère et enfant après 2 ans ;
– si marche acquise après 18 mois : bilan vestibulaire ;
– si surdité profonde sans malformation d’oreille interne : ECG (allongement de l’espace QT), pour rechercher un syndrome de Jervell-Lange-Nielsen ;
– si surdité évolutive : bandelette urinaire pour identifier une hématurie, une protéinurie (syndrome d’Alport).
Une consultation de génétique permet de : déterminer la cause dans environ deux tiers des cas ; rechercher une atteinte syndromique ; dépister les cas familiaux ; donner un pronostic évolutif selon l’étiologie ; déterminer le mode de transmission et donc le risque de récurrence en cas de nouvelle grossesse.
– audiométrie des parents et de la fratrie ;
– examen ophtalmologique avec FO ;
– si surdité de perception : IRM (cérébrale, conduits auditifs internes, rochers, bulbes olfactifs) ;
– si surdité de transmission : scanner des rochers ;
– recherche d’infection congénitale par le CMV : PCR CMV (sur salive avant 1 an, urine ou sur carton de Guthrie avant 2 ans) ; sérologies CMV mère et enfant après 2 ans ;
– si marche acquise après 18 mois : bilan vestibulaire ;
– si surdité profonde sans malformation d’oreille interne : ECG (allongement de l’espace QT), pour rechercher un syndrome de Jervell-Lange-Nielsen ;
– si surdité évolutive : bandelette urinaire pour identifier une hématurie, une protéinurie (syndrome d’Alport).
Une consultation de génétique permet de : déterminer la cause dans environ deux tiers des cas ; rechercher une atteinte syndromique ; dépister les cas familiaux ; donner un pronostic évolutif selon l’étiologie ; déterminer le mode de transmission et donc le risque de récurrence en cas de nouvelle grossesse.
Encadre
Facteurs de risque
Prématurité, PN < 1 500 g, anoxie néonatale (Apgar < 4 à 1 min, < 7 à 5 min), ventilation assistée pendant plus de 5 jours.
Hyperbilirubinémie > 300-350 µmol/L
Embryofœtopathie, CMV, rubéole toxoplasmose, , herpès, syphilis
Traitements ototoxiques de plus de 5 jours (fin de grossesse ou néonatal)
Méningite bactérienne ou encéphalite, atteinte neurologique centrale
Antécédents familiaux (appareillage auditif avant 50 ans)
Signes de syndrome associé avec surdité, malformations cranio-faciales
références
1. HAS. Évaluation du dépistage néonatal systématique de la surdité permanente bilatérale. Janvier 2007. www.has-sante.fr
2. Arrêté relatif à l’organisation du dépistage de la surdité permanente néonatale. Avril 2012. http://www.legifrance.gouv.fr
3. Antoni M, Rouillon I, Denoyelle F, et al. Newborn hearing screening : Prevalence and medical and paramedical treatment of bilateral hearing loss in a neonatal series in the Île-de-France region of France. Eur Ann Otorhinolaryngol Head Neck Dis 2016;133:95-9.
4. JCIH. Year 2007 position statement: Principles and guidelines for early hearing detection and intervention programs. Pediatrics 2007;120:898-921.
5. Blanchard M, Thierry B, Marlin S, Denoyelle F. Genetic aspects of congenital sensorineural hear-ing loss. Arch Pediatr. 2012;19:886-9.
6. Dauman R, Roussey M, Belot V, et al. Screening to detect permanent childhood hearing impairment in neonates transferred from the newborn nursery. Int J Pediatr Otorhinolaryngol. 2009;73: 457-65
2. Arrêté relatif à l’organisation du dépistage de la surdité permanente néonatale. Avril 2012. http://www.legifrance.gouv.fr
3. Antoni M, Rouillon I, Denoyelle F, et al. Newborn hearing screening : Prevalence and medical and paramedical treatment of bilateral hearing loss in a neonatal series in the Île-de-France region of France. Eur Ann Otorhinolaryngol Head Neck Dis 2016;133:95-9.
4. JCIH. Year 2007 position statement: Principles and guidelines for early hearing detection and intervention programs. Pediatrics 2007;120:898-921.
5. Blanchard M, Thierry B, Marlin S, Denoyelle F. Genetic aspects of congenital sensorineural hear-ing loss. Arch Pediatr. 2012;19:886-9.
6. Dauman R, Roussey M, Belot V, et al. Screening to detect permanent childhood hearing impairment in neonates transferred from the newborn nursery. Int J Pediatr Otorhinolaryngol. 2009;73: 457-65

 Encadrés
Encadrés