Les dermatophytoses sont des infections fongiques cutanées dont la prévalence est élevée et qui sont provoquées par des champignons filamenteux kératinophiles, appelés dermatophytes. Depuis peu, émergent en France des souches de dermatophytes résistantes à la terbinafine, appelant à un dépistage précoce, à une prévention efficace et à des choix thérapeutiques ciblés.
Évolution épidémiologique majeure des mycoses superficielles à dermatophytes
Au cours des cinq dernières années, un véritable tournant s’est opéré dans l’épidémiologie des dermatophytoses. Des changements notables ont été observés dans les présentations cliniques de ces infections superficielles. Jusqu’alors considérées comme banales et peu graves – souvent liées à la pratique de certains sports ou au contact avec des animaux – et jusqu’alors généralement bien contrôlées par des antifongiques, les dermatophytoses peuvent maintenant prendre la forme d’une nouvelle entité clinique : les dermatophytoses étendues résistantes à la terbinafine (DERT).1
Présentations cliniques
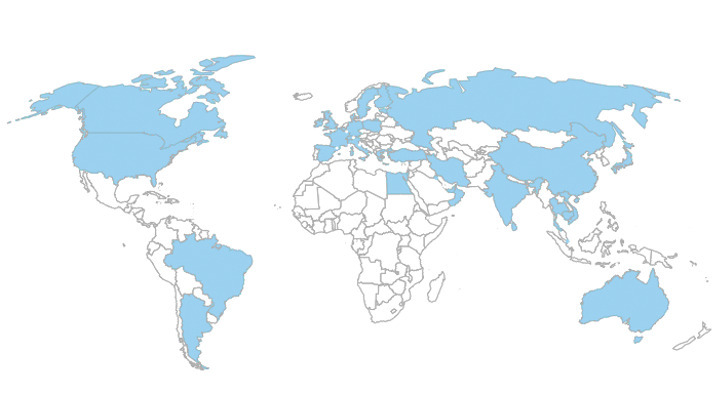
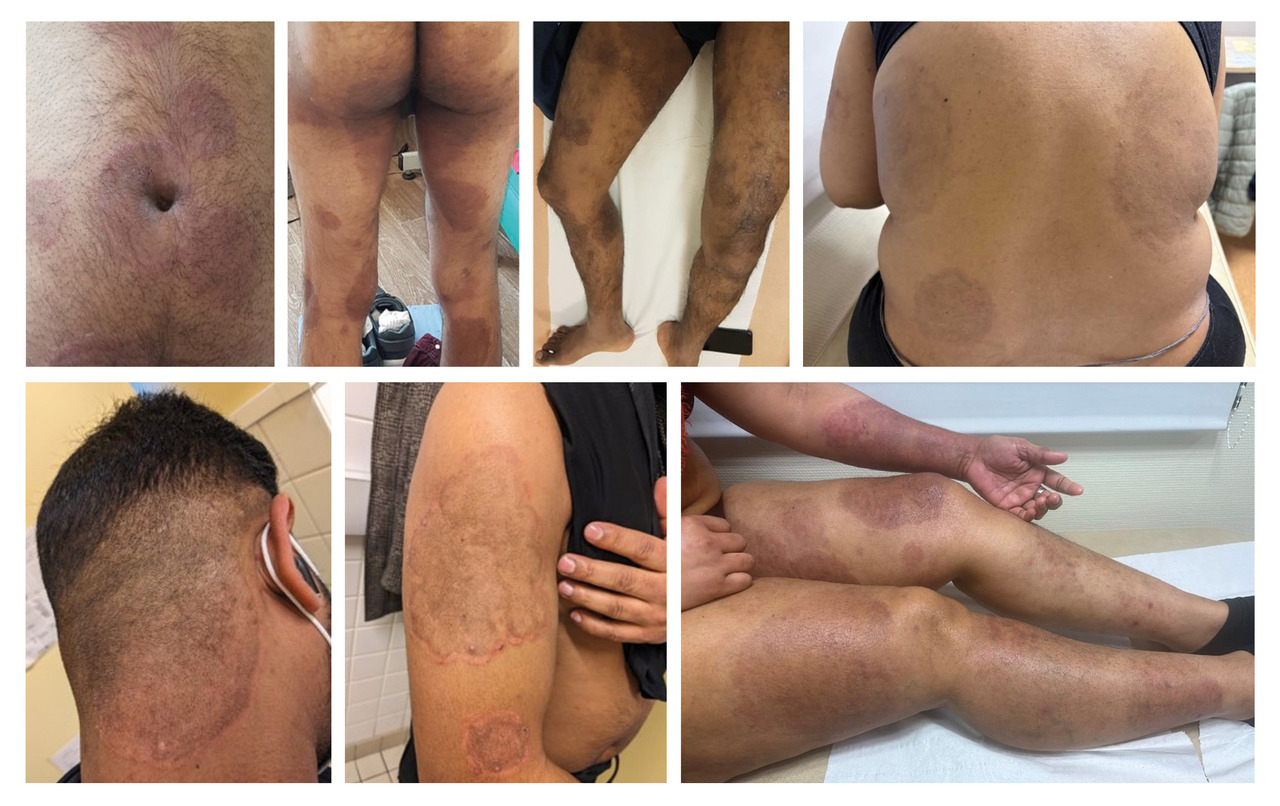
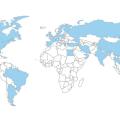
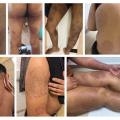
Auparavant rares, les DERT sont désormais plus fréquentes, notamment chez les patients rapportant un voyage récent en Inde, en Iran ou au Bangladesh (fig. 1). La forme clinique habituelle peut concerner l’ensemble du corps (Tinea corporis) ou l’aine (Tinea cruris) et se caractérise par l’absence de clairance centrale, l’apparition de plaques parfois étendues à l’aspect eczémateux plus ou moins inflammatoires.2 Une atteinte du visage est parfois observée, avec des formes atypiques se manifestant par une desquamation discrète, une bordure squameuse ou une extension vers l’oreille externe, la racine des cheveux, voire le cuir chevelu.2 Une pigmentation marquée est également possible, en particulier chez les patients à peau foncée (fig. 2). L’association à une atteinte palmaire et/ou plantaire (Tinea manuum/pedis), voire à une onychomycose, a aussi été rapportée.2 Enfin, un prurit persistant peut subsister, même après guérison clinique et mycologique.
Les enfants, même très jeunes, peuvent être infectés, souvent dans un contexte où un adulte est atteint au sein du foyer familial. En effet, la transmission intrafamiliale est fréquente et responsable d’infections simultanées ou successives de plusieurs membres du même foyer ; néanmoins, le rôle des vêtements ou objets de la vie quotidienne dans la propagation de la maladie reste à confirmer. La symptomatologie chez l’enfant ne diffère pas de celle de l’adulte.3
Un responsable identifié : Trichophyton indotineae
Ce changement de présentation clinique coïncide en grande partie avec l’émergence et l’expansion mondiale de Trichophyton indotineae, nouvelle espèce de dermatophyte récemment décrite. Sa fréquente résistance à la terbinafine – l’antifongique de première ligne pour les mycoses superficielles – explique notamment l’émergence de ces dermatophytoses étendues.
Initialement décrit en Asie du Sud et en Océanie, T. indotineae a été à l’origine d’importantes épidémies en Inde, où – malgré les recommandations du corps médical indien – l’utilisation excessive de crèmes en vente libre contenant de la terbinafine, combinée à des antibiotiques et des corticostéroïdes, a favorisé l’émergence de souches résistantes.2,4 Les mouvements de population ont ensuite provoqué sa propagation. Ainsi, au cours des cinq dernières années, des cas ont été rapportés dans 34 pays (fig. 1), dont la France.5
Actions proposées pour lutter contre la progression de T. indotineae
Une collaboration étroite entre mycologues, médecins généralistes, dermatologues et infectiologues est essentielle pour une prise en charge efficace de ces infections. Pour freiner la progression de T. indotineae et limiter son implantation en France, des défis restent à relever.
Optimiser les stratégies thérapeutiques au quotidien
En cas de suspicion de dermatophytose à T. indotineae, et en raison du risque élevé de transmission interhumaine, il est recommandé :
- de réaliser un examen mycologique ainsi qu’une détermination de la sensibilité in vitro aux antifongiques (a minima terbinafine et itraconazole) ;
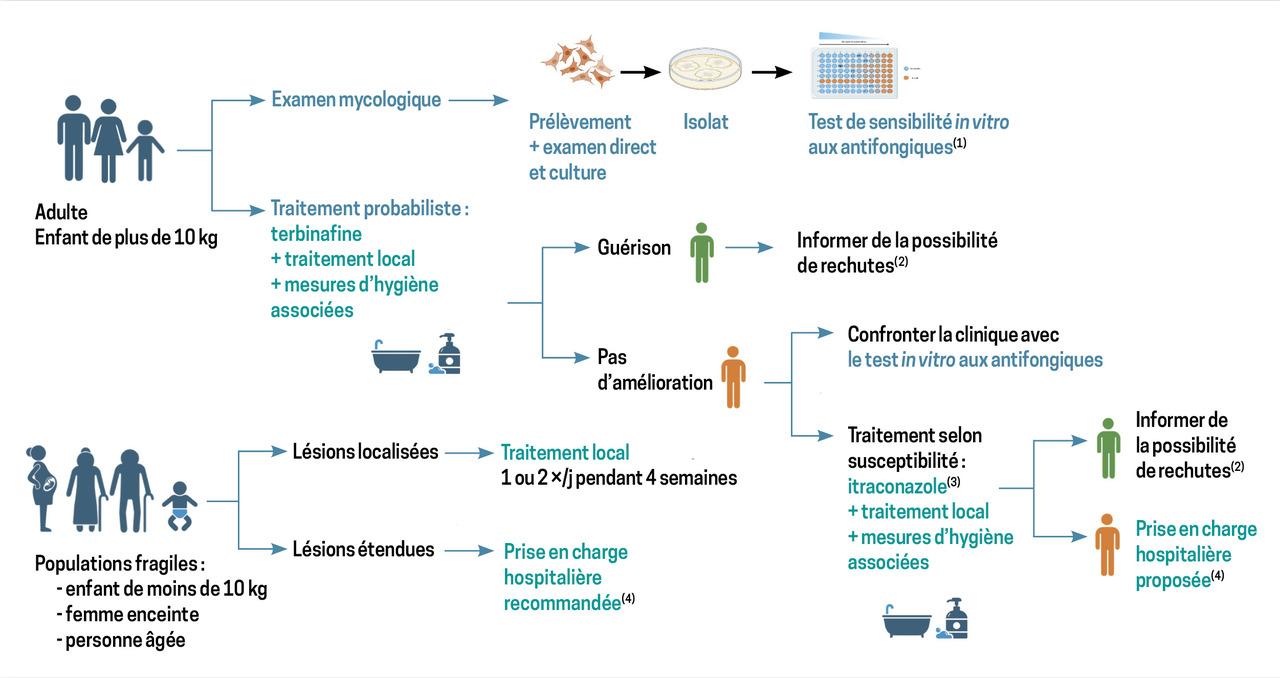
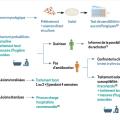
- de prescrire un traitement probabiliste dès la première consultation (fig. 3).
Les infections à T. indotineae pouvant infecter différentes populations, le traitement doit tenir compte de l’âge du patient, de l’étendue des lésions et des éventuelles comorbidités – tout en sachant que peu d’antifongiques ont une autorisation de mise sur le marché. Un traitement systémique doit être privilégié pour la prise en charge des DERT.4
Bien que les mycologues soient activement impliqués dans les études épidémiologiques pour guider les cliniciens dans le choix optimal de ces traitements, des recommandations nationales issues de groupes d’experts font encore défaut. Les recommandations actuelles, mises en place en Inde à la suite de l’épidémie qui sévit depuis 2016, restent valables.4 Elles comportent cependant des zones d’ombre, constituant ainsi des défis pour les praticiens, qui soulignent la nécessité d’établir des recommandations nationales (fig. 3).
Posologie, en pratique
La terbinafine orale, à la dose de 250 mg/j, après bilan hépatique, est recommandée pour un mois en traitement probabiliste de première intention si le patient n’a jamais reçu cet antifongique. Cette prescription est éventuellement renouvelable pour un à deux mois supplémentaires (avec bilan hépatique mensuel) en cas d’absence de guérison mais avec une évolution favorable. Les lésions disparaissent généralement en moins de trois mois.
En cas de résistance
Si le traitement de première ligne échoue, après confirmation par la persistance du champignon à l’analyse mycologique, la détermination de la sensibilité in vitro aux antifongiques permet de mettre en évidence une résistance et d’adapter le traitement.
Un traitement prolongé ou une augmentation de la posologie de la terbinafine à 500 mg/j (avec hémogramme et bilan hépatique mensuels en raison des effets indésirables) peut s’avérer efficace, bien que la durée optimale ainsi que la tolérance restent mal connues.
En cas de résistance avérée in vitro à la terbinafine, l’itraconazole doit être privilégié.2 Les posologies varient entre 100 et 400 mg/j, l’efficacité étant meilleure à la dose de 400 mg/j, avec un temps de guérison raccourci (10 à 15 semaines).6 Néanmoins, les échecs thérapeutiques sont fréquents et liés notamment à des taux sériques insuffisants d’itraconazole en raison de la variabilité interindividuelle d’absorption de cet antifongique.6
Un nouvel examen mycologique est recommandé à chaque rechute, afin de détecter une résistance acquise, sans négliger la recherche de sources potentielles de recontamination.2
Dans tous les cas, une surveillance hépatique rapprochée est indispensable en cas de traitements prolongés par terbinafine ou itraconazole. Il convient de souligner qu’actuellement la résistance à l’itraconazole est rare en France mais a été néanmoins documentée, incitant à la plus grande vigilance. Face à cette situation, de nouveaux schémas thérapeutiques sont en cours d’évaluation.
Le voriconazole (utilisé pour les infections invasives à champignons filamenteux) a montré une efficacité de 90 % après quinze jours de traitement, mais celle-ci diminue drastiquement à 75 % après six semaines, avec un taux de rechute de 5 %.7
Une étude récente suggère que le posaconazole pourrait aussi constituer une alternative.8
Pour la prise en charge des populations fragiles telles que les nouveau-nés, nourrissons, femmes enceintes, personnes âgées ou avec comorbidités, il faut se référer aux recommandation indiennes4 ou préconiser une prise en charge hospitalière.
Mesures non médicamenteuses
Enfin, l’hygiène personnelle est essentielle pour prévenir l’infection, limiter sa propagation et sa persistance. Le lavage des vêtements et du linge de lit à 60 °C est efficace. Le partage des savons, vêtements, serviettes et linge de lit est à proscrire.
Renforcer le diagnostic mycologique pour mieux identifier le risque
Une deuxième action consiste en l’identification précise de l’espèce responsable.
Le médecin, lors de la première consultation, doit prescrire un examen mycologique à réaliser avant la prise de tout traitement afin de permettre l’identification de l’espèce responsable et la réalisation d’un antifongigramme. L’identification peut nécessiter jusqu’à quatre semaines, en raison de la croissance lente de ces champignons, mais les premiers résultats peuvent parfois être disponibles après deux semaines.
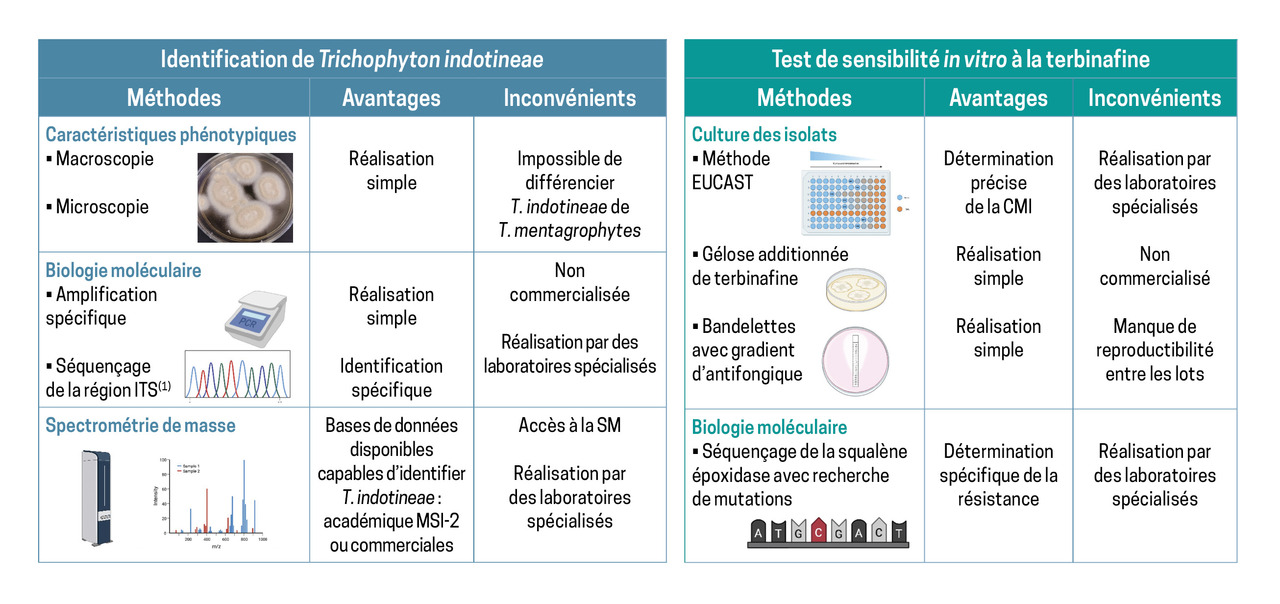
Dans le cas particulier de T. indotineae, le biologiste ou le mycologue se heurte fréquemment aux limites des techniques microscopiques classiquement utilisées en laboratoire de biologie médicale (fig. 4) : elles ne permettent pas de différencier T. indotineae des autres espèces du complexe T. mentagrophytes/interdigitale. De nouvelles technologies, telles que la spectrométrie de masse MALDI-TOF,9 le séquençage de l’ADN ou encore des PCR ciblées sur des prélèvements cutanés, ont donc été développées. Par ailleurs, des techniques pour évaluer la sensibilité aux antifongiques, combinées à la détection des mutations du gène codant pour la squalène époxidase (cible de la terbinafine), ont été mises au point pour dépister plus rapidement la résistance à la terbinafine.10
Ces approches, qui s’implantent progressivement dans les laboratoires spécialisés de mycologie des centres hospitalo-universitaires, restent encore peu disponibles dans les laboratoires de biologie médicale de ville. Ainsi, en cas de DERT, et notamment en présence de facteurs de risque comme un voyage en zone d’endémie ou la présence de cas similaires dans l’entourage, il est essentiel d’orienter le patient vers un laboratoire de mycologie hospitalo-universitaire pour un diagnostic formel. Le cas échéant, tout laboratoire peut transmettre ce prélèvement et sous-traiter cette analyse à ces laboratoires spécialisés.
Améliorer l’accès à l’information et à la formation des professionnels de santé
En France, les DERT dues à T. indotineae sont encore principalement des pathologies d’importation, le plus souvent acquises en Inde, en Iran ou au Bangladesh. Les premiers cas dans l’Hexagone ont concerné des migrants sans couverture sociale, souvent pris en charge dans des structures de permanence d’accès aux soins de santé (PASS). Bien que l’émergence de T. indotineae soit relayée par la presse scientifique, en France, elle est encore trop souvent méconnue des soignants des établissements de santé, des structures médico-sociales et de la médecine de ville. Une troisième action consiste donc à faciliter l’accès à l’information pour les médecins de première ligne et à mettre en place des formations, notamment sur l’importance du prélèvement mycologique pour identifier l’espèce et sa sensibilité aux antifongiques, garantissant une prise en charge thérapeutique optimale.
Mettre en place une action concertée et pluridisciplinaire pour freiner la propagation
Afin de freiner sa propagation sur notre territoire, la lutte contre T. indotineae ne peut être efficace sans une collaboration étroite entre médecins généralistes, dermatologues, infectiologues et mycologues et/ou microbiologistes. En l’absence de toute coordination, l’implantation durable de T. indotineae sur le territoire national est un réel risque. Les autorités de santé sont également concernées au premier plan. Bien que le coût de la prise en charge de ces patients ne soit pas encore évalué, l’expérience indienne souligne la nécessité de relever ces défis, de clarifier les incertitudes actuelles et de mettre en place des systèmes d’alerte afin de prévenir l’implantation de cette infection en France.
Que dire à vos patients ?
Les dermatophytoses étendues résistantes à la terbinafine se transmettent principalement par contact direct au sein de la famille et probablement par l’intermédiaire des vêtements ou objets contaminés par le champignon.
Le traitement antifongique et les mesures d’hygiène doivent être scrupuleusement respectés afin de limiter sa dispersion et protéger l’entourage.
En l’absence d’amélioration des lésions, en dépit d’un traitement adapté et bien suivi, il faut reconsulter.
2. Khurana A, Sharath S, Sardana K, et al. Clinico-mycological and therapeutic updates on cutaneous dermatophytic infections in the era of Trichophyton indotineae. J Am Acad Dermatol 2024;91(2):315-23.
3. Fattahi A, Shirvani F, Ayatollahi A, et al. Multidrug-resistant Trichophyton mentagrophytes genotype VIII in an Iranian family with generalized dermatophytosis: Report of four cases and review of literature. Int J Dermatol 2021;60(6):686-92.
4. Rengasamy M, Shenoy MM, Dogra S, et al. Indian association of dermatologists, venereologists and leprologists (IADVL) task force against recalcitrant tinea (ITART) consensus on the management of glabrous tinea (INTACT). Indian Dermatol Online J 2020;11(4):502-19.
5. Jabet A, Brun S, Normand AC, et al. Extensive Dermatophytosis Caused by Terbinafine-Resistant Trichophyton indotineae, France. Emerg Infect Dis 2022;28(1):229-33.
6. Khurana A, Agarwal A, Singh A, et al. Predicting a therapeutic cut-off serum level of itraconazole in recalcitrant tinea corporis and cruris – A prospective trial. Mycoses 2021;64(12):1480-8.
7. Chandrashekar BS, Poojitha DS. Evaluation of efficacy and safety of oral voriconazole in the management of recalcitrant and recurrent dermatophytosis. Clin Exp Dermatol 2022;47(1):30-6.
8. Fernandez-Gonzalez P, Garcia-Donoso C, Garcia-Mouronte E, et al. Trichophyton indotineae extensive tinea: Successful posaconazole treatment in four cases from Spain. Clin Exp Dermatol 2025;50(2):431-4.
9. Normand AC, Moreno-Sabater A, Jabet A, et al. MALDI-TOF mass spectrometry online identification of Trichophyton indotineae using the MSI-2 application. J Fungi (Basel) 2022;8(10):1103.
10. Bidaud AL, Moreno-Sabater A, Normand AC, et al. Evaluation of gradient concentration strips for detection of terbinafine resistance in Trichophyton spp. Antimicrob Agents Chemother 2023;67(6):e0171622.

 Encadrés
Encadrés