Les angiodysplasies digestives (AGD) sont des anomalies vasculaires superficielles acquises, souvent incriminées dans des hémorragies digestives.
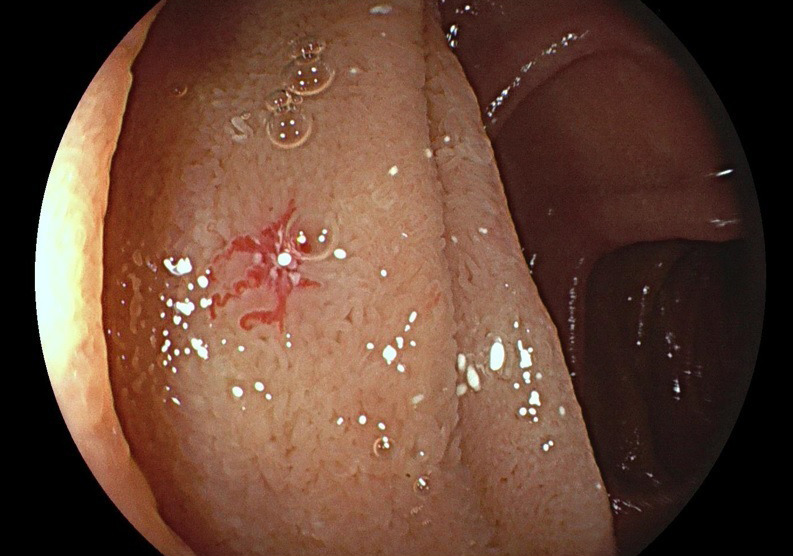
Les AGD se présentent généralement sous la forme de lésions rouge vif, rondes, petites (inférieures à 10 mm de diamètre), planes ou légèrement surélevées et aux contours irréguliers mais nets (fig. 1). Leur examen histologique (rarement nécessaire) montre une dilatation des veines sous-muqueuses pauvres en muscles lisses drainant des veinules et capillaires de siège muqueux anormal.1 Parmi les diagnostics différentiels figurent les hémangiomes, les angiosarcomes, la maladie de Rendu-Osler, les ectasies vasculaires antrales (EVA), les télangiectasies radiques et les ulcérations simplex de Dieulafoy.
Physiopathologie encore hypothétique
Les mécanismes conduisant à la constitution d’AGD ne sont pas encore complètement élucidés. Les hypothèses les plus étudiées sont celles de l’obstruction partielle de veines sous-muqueuses, de l’hypoxie muqueuse chronique avec un excès de facteurs pro-angiogéniques (VEGF notamment) et de l’inhibition de la sécrétion du facteur de von Willebrand (vW), aboutissant à une néo-angiogenèse.1
Lésions multiples dans la majorité des cas
Les AGD touchent indifféremment les deux sexes et surtout les patients âgés de plus de 60 ans (avec une prévalence de l’ordre de 1 %), volontiers sous antiagrégants plaquettaires (AAP) et/ou traitements anticoagulants (TAC). La maladie est souvent associée à une insuffisance cardiaque, rénale ou hépatique chronique, ou à une maladie de vW innée ou acquise.2 L’association d’AGD à une sténose aortique définit le syndrome de Heyde, à risque élevé d’hémorragie (en lien, d’une part, avec les TAC et, d’autre part, avec une dépolymérisation du facteur vW).2
Les AGD sont multiples dans 40 à 60 % des cas.1 Elles peuvent siéger partout dans le tube digestif, mais leurs sites électifs sont le duodénum, le jéjunum proximal, l’iléon terminal et le côlon droit.
On leur attribue 2 à 5 % des hémorragies digestives. L’hémorragie cesse spontanément dans 40 à 45 % des cas, mais le risque de récidive est élevé (de l’ordre de 15 et 65 % à un et trois ans respectivement), notamment chez les patients valvulaires. La mortalité de ces hémorragies est de l’ordre de 2 à 4 %.1
Approche diagnostique reposant sur l’endoscopie
Les AGD peuvent être asymptomatiques et découvertes de façon fortuite lors d’une endoscopie digestive. Le plus souvent néanmoins, elles sont diagnostiquées pendant ou au décours d’une hémorragie digestive. Dans ce contexte, la stratégie habituelle est de réaliser de façon successive (tant que le diagnostic n’est pas effectué), dans cet ordre, et dans un délai court (idéalement moins de quarante-huit heures lorsque l’hémorragie est extériorisée et moins de quinze jours lorsque l’hémorragie est occulte) : une endoscopie œsogastroduodénale (EOGD) puis (ou dans le même temps) une coloscopie, et enfin une vidéocapsule endoscopique (VCE) de l’intestin grêle.3,4
L’EOGD et la coloscopie peuvent être d’emblée thérapeutiques. La VCE permet uniquement d’estimer la localisation et la cause du saignement, avec un rendement diagnostique de l’ordre de 60 % dans cette séquence.
Les AGD représentent alors la cause la plus fréquente.
Lorsque le site et la cause de l’hémorragie ne sont ni l’un ni l’autre identifiés par cette approche (hémorragie alors dite « obscure »), une reprise de cette séquence diagnostique est discutée, en optimisant les examens dont la qualité aurait pu être sous-optimale (EOGD réalisée aux horaires de garde, préparation imparfaite de la coloscopie, VCE incomplète ne montrant pas toute la longueur de l’intestin grêle, par exemple).
Selon les ressources locales, et notamment lorsque l’accès à la coloscopie est limité et/ou que des signes de sévérité immédiate existent, un artérioscanner peut être réalisé (suivi éventuellement d’une embolisation, voire dans de rares cas d’une chirurgie).3
L’entéroscopie s’envisage essentiellement à visée thérapeutique, après que la VCE a identifié une (ou des) lésion(s) causale(s). Elle doit être idéalement « profonde », réalisée par voie haute, basse, ou les deux (selon la localisation estimée par la VCE) avec des artifices techniques de progression dans l’intestin grêle (au premier rang desquels la technique du « double ballon »).5 L’entéroscopie est cependant très souvent dite « poussée » (avec un coloscope pédiatrique par voie haute donnant accès au cadre duodénal et aux toutes premières anses jéjunales), notamment lorsque la VCE montre les AGD duodéno-jéjunales, tant les ressources en entéroscopie profonde sont insuffisantes.6 Le recours ultime, dans les situations de sauvetage ou réfractaires, est l’entéroscopie peropératoire, lors de laquelle un coloscope examine l’ensemble du grêle par une ou plusieurs entérotomies chirurgicales.
Prise en charge en plusieurs temps
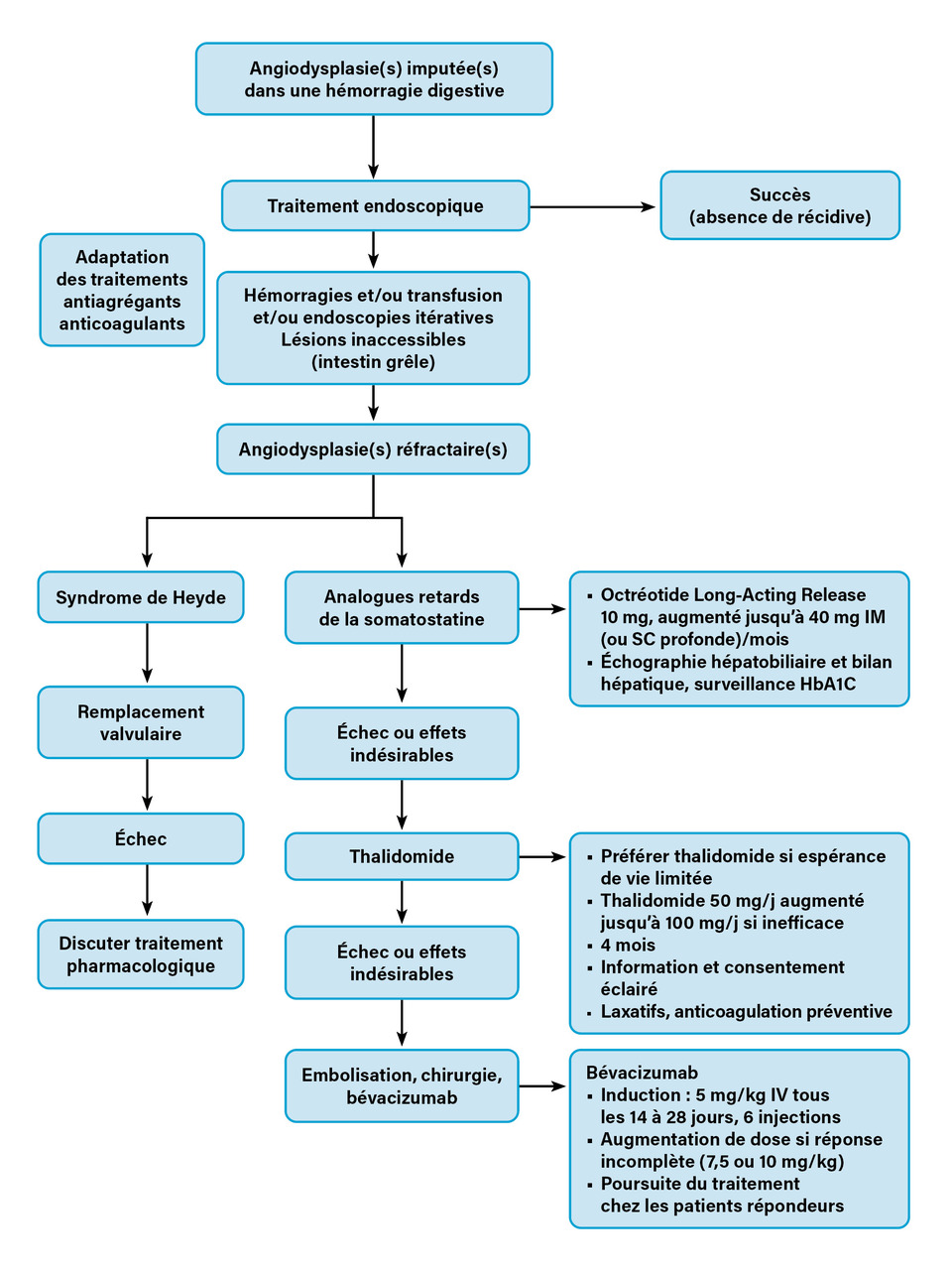
Un algorithme de prise en charge est proposé (fig. 2) pour les AGD hémorragiques.
Traitement non spécifique
Comme pour toute hémorragie digestive, qu’elle soit extériorisée ou occulte, plusieurs traitements non spécifiques doivent s’envisager. L’interruption et l’adaptation des AAP et TAC se discutent au cas par cas (souvent avec les cardiologues ou neurologues), de même que des interventions dans les situations complexes (ablation de fibrillation ou flutter atriaux, fermeture d’auricule, filtre cave, par exemple).
La correction de l’anémie est également un préalable important :
- par l’administration de fer par voie orale dans les situations non sévères ou chroniques ;
- par voie intraveineuse lorsque la prise orale est mal tolérée, impossible ou dans les situations où une augmentation rapide des réserves de fer est nécessaire ;
- par transfusion de culots globulaires rouges (CGR) dans les anémies les plus profondes et/ou les plus aiguës.
Ces traitements non spécifiques sont parfois suffisants chez les patients les plus fragiles, lorsque les besoins transfusionnels restent modestes (de l’ordre de quatre perfusions de fer ou de CGR par an).7
Traitement endoscopique
Les AGD asymptomatiques, diagnostiquées fortuitement, ne nécessitent pas de traitement (le risque de survenue d’un épisode hémorragique étant alors très faible).
Dans les autres cas, le traitement de première intention consiste en la destruction des AGD, afin d’arrêter le saignement mais aussi de prévenir d’autres épisodes.
Le type d’endoscopie dépend, bien sûr, de la localisation des lésions, et l’atteinte du grêle distal (au-delà de l’angle de Treitz) peut rapidement être limitante5 tant les ressources en entéroscopie profonde sont faibles en France.6
Les techniques endoscopiques font essentiellement appel à une électrocoagulation superficielle, avec un risque très faible de perforation. Ainsi, la coagulation au plasma d’argon (CPA), dont la profondeur de coagulation varie de 0,5 à 3 mm, est la plus répandue (vidéo). En plus d’être sûre, elle est simple et peu coûteuse.
La récidive hémorragique après traitement d’AGD par CPA varie entre 7 et 15 % pour le côlon et atteint 50 % pour l’intestin grêle.7
D’autres techniques de destruction existent (autres sondes et pinces d’électrocoagulation, cryothérapie, injection de produits sclérosants, résection par mucosectomie, oblitération par clips), sans que des études comparatives n’aient été réalisées.
Le traitement endoscopique peut néanmoins s’avérer insuffisant. Dans les situations où les besoins en fer et/ou en CGR restent importants après traitement endoscopique (mais sans qu’il n’y ait de seuil consensuel de recours aux perfusions ou aux endoscopies), d’autres approches peuvent se discuter.
Remplacement de la valve aortique dans le syndrome de Heyde
Le syndrome de Heyde correspond à l’association d’AGD hémorragiques à un rétrécissement aortique (RA).1 Le remplacement valvulaire aortique, soit chirurgical (RVAC), soit radiologique (transcatheter aortic valve implantation, TAVI) est un traitement souvent efficace sur les tableaux hémorragiques (tableau 1), en raison de la correction fréquente de l’activité vW qui en résulte.8 Une méta-analyse suggère que les techniques de réparation valvulaire permettent l’arrêt des saignements chez trois patients sur quatre.8 Les TAVI de nouvelle génération, qui diminuent les fuites paravalvulaires, ont une efficacité similaire à celle du RAVC tout en étant moins invasives. Des travaux récents suggèrent, par ailleurs, que le nombre et la taille des AGD diminue après TAVI.9,10 Par conséquent, lorsqu’il est applicable, le remplacement valvulaire devrait être privilégié par rapport aux traitements pharmacologiques détaillés ci-après. Chez les patients les plus âgés et fragiles, une dilatation valvulaire aortique par voie vasculaire peut s’envisager à moindre risque.
Traitements pharmacologiques
Trois types de molécules peuvent être envisagés : analogues de la somatostatine en première intention, puis la thalidomide, et enfin le bévacizumab en dernier recours.
Analogues de la somatostatine
Les analogues de la somatostatine (AS) ont fait l’objet d’évaluations favorables dans le traitement des AGD hémorragiques. Ils n’ont cependant pas encore d’autorisation de mise sur le marché dans cette indication. Leur efficacité serait liée à une diminution du flux sanguin splanchnique, à une augmentation de l’agrégation plaquettaire, à l’inhibition des facteurs angiogéniques (via le VEGF) et à une possible inhibition directe de l’angiogenèse. Plusieurs études combinant l’utilisation de préparations à courte et à longue durée d’action ont d’abord suggéré des résultats cliniques favorables (tableau 2). Plus récemment, une méta-analyse de données individuelles a montré une réduction d’au moins 50 % du nombre de transfusions de CGR chez 83 % des patients traités par AS.11 Enfin, un essai contrôlé randomisé (ECR), ouvert et multicentrique a comparé une dose élevée d’octréotide retard (40 mg par mois) pendant douze mois à un traitement standard, chez les patients gardant des besoins transfusionnels élevés malgré un traitement endoscopique.12 Les AS ont diminué significativement le recours aux traitements intraveineux (fer ou CGR) et aux endoscopies. Leurs principaux effets indésirables (avec une fréquence atteignant 20 %) sont la diarrhée, les crampes abdominales et ballonnements, les irritations aux points d’injection, le déséquilibre glycémique et la lithiase biliaire (dont les complications surviennent souvent à l’arrêt du traitement).
Thalidomide
La thalidomide a été introduite dans les années 1970 comme sédatif et est connue pour provoquer de graves malformations congénitales. Elle a été « redécouverte » dans les années 1990 comme modulateur immunitaire et inhibiteur de l’angiogenèse (VEGF). De courtes séries et un ECR de faible effectif ont suggéré, dans les années 2000, son intérêt dans le traitement des AGD hémorragiques (tableau 3).7
Plus récemment, un ECR multicentrique, en double aveugle, contrôlé par placebo, a été réalisé.13 Cent cinquante patients atteints de AGD du grêle ont été inclus, comparant la thalidomide 50 ou 100 mg par voie orale à un placebo pendant quatre mois. Le taux de réponse défini comme une réduction supérieure à 50 % du nombre d’épisodes hémorragiques survenus au cours de l’année suivant la fin du traitement, par rapport à l’année précédente, a été de 68,6 %, 51 % et 16 %, dans chaque groupe respectivement. Les besoins en transfusion et en hospitalisation ont également été significativement plus faibles dans les groupes avec thalidomide.13
Malgré ces résultats confirmant l’efficacité de la thalidomide, le profil de tolérance et de sécurité en limite l’usage.
Parmi les effets indésirables figurent la somnolence, la constipation, le risque thromboembolique et la neuropathie périphérique (dose-dépendante). La tératogénicité de la thalidomide implique que le traitement ne soit délivré qu’en milieu hospitalier. Enfin, l’observance est plus faible que pour les injections mensuelles d’AS. Pour ces raisons, la thalidomide est plutôt considérée comme un traitement de seconde ligne, en cas d’intolérance ou d’échec des AS.
Bévacizumab
Le bévacizumab intraveineux est un anticorps monoclonal anti-VEGF humanisé. Il est principalement utilisé dans le traitement du cancer pour inhiber la croissance tumorale et les métastases. L’expérience dans le traitement des AGD se limite à des rapports de cas ou à de petites séries de cas rétrospectives, avec des résultats favorables, mais avec un probable biais de publication. Il est généralement administré à une dose plus faible qu’à des fins oncologiques, par exemple 5 mg/kg toutes les deux semaines pour l’induction pendant deux à trois mois, suivi de 5 mg/kg par mois en entretien, avec des perfusions complémentaires mais facultatives toutes les deux semaines ou à des doses plus élevées chez les patients présentant une réponse partielle.7,14
Le faible niveau de preuve ainsi que son coût élevé font du bévacizumab une option de dernier recours pour les patients souffrant d’AGD réfractaires.
Traitements interventionnels de sauvetage
L’embolisation transcathéter super-sélective est actuellement la technique angiographique préférée en cas d’hémorragie non contrôlée du tube digestif, avec un taux de succès élevé (environ 80 à 90 %) et un taux de récidive hémorragique faible.
Des événements indésirables surviennent dans 5 à 9 % des cas, à type d’hématomes, de dissections artérielles, de thromboses, de pseudo-anévrismes et rarement de nécrose intestinale.
Le recours à la chirurgie n’est justifié qu’en cas d’hémorragie digestive aiguë et sévère, nécessitant une transfusion de culots globulaires, lorsqu’une source a été clairement identifiée, et après l’échec de plusieurs techniques interventionnelles (endoscopiques, radiologiques). L’entéroscopie peropératoire peut accompagner et guider le geste chirurgical.
Diagnostic et traitement reposent sur l’endoscopie
L’endoscopie constitue la pierre angulaire de la prise en charge diagnostique et thérapeutique des AGD. Cependant, le remplacement valvulaire (radiologique ou chirurgical) se discute rapidement dans le syndrome de Heyde, et des traitements pharmacologiques (AS et thalidomide principalement) s’envisagent lorsque les besoins transfusionnels sont trop élevés ou que les épisodes hémorragiques et les recours à l’endoscopie sont trop fréquents. Le bévacizumab, l’embolisation et la chirurgie se discutent dans les situations les plus réfractaires ou de sauvetage.
Dans un futur proche, des biomarqueurs pourraient permettre de mieux sélectionner patients et traitements.
De même, la surveillance du VEGF ainsi que celle d’autres facteurs de croissance de l’angiogenèse, comme l’angiopoïétine 2, pourraient faciliter l’évaluation de la réponse au traitement.7
Vidéo : Destruction endoscopique par coagulation au plasma d’argon d’une angiodysplasie colique incriminée dans une hémorragie digestive.
2. Veyradier A, Balian A, Wolf M, et al. Abnormal von Willebrand factor in bleeding angiodysplasias of the digestive tract. Gastroenterology 2001;120:346-53.
3. Triantafyllou K, Gkolfakis P, Gralnek IM, et al. Diagnosis and management of acute lower gastrointestinal bleeding: European Society of Gastrointestinal Endoscopy (ESGE) Guideline. Endoscopy 2021;53:850-68.
4. Pennazio M, Rondonotti E, Despott EJ, et al. Small-bowel capsule endoscopy and device-assisted enteroscopy for diagnosis and treatment of small-bowel disorders: European Society of Gastrointestinal Endoscopy (ESGE) Guideline - Update 2022. Endoscopy 2023;55(1):58-95.
5. Rahmi G, Samaha E, Vahedi K, et al. Long-term follow-up of patients undergoing capsule and double-balloon enteroscopy for identification and treatment of small-bowel vascular lesions: A prospective, multicenter study. Endoscopy 2014;46:591-7.
6. Dray X, Buzzi J-C, Quentin V, et al. Small bowel capsule endoscopy and deep enteroscopy procedure load in France: A nationwide population-based study over 7 years. Endosc Int Open 2023;11:E1013-9.
7. Becq A, Sidhu R, Goltstein LCMJ, et al. Recent advances in the treatment of refractory gastrointestinal angiodysplasia. United European Gastroenterol J 2024;12:1128-35.
8. Goltstein LCMJ, Rooijakkers MJP, Hoeks M, et al. Effectiveness of aortic valve replacement in Heyde syndrome: A meta-analysis. Eur Heart J 2023;44:3168-77.
9. Yashige M, Inoue K, Zen K, et al. Gastrointestinal angiodysplasia before and after treatment of severe aortic stenosis. N Engl J Med 2023;389:1530-2.
10. Goltstein LCMJ, Rooijakkers MJP, Thierens NDE, et al. Gastrointestinal angiodysplasia resolution after transcatheter aortic valve implantation. JAMA Netw Open 2024;7 (10):e2442324.
11. Goltstein LCMJ, Grooteman KV, Rocco A, et al. Effectiveness and predictors of response to somatostatin analogues in patients with gastrointestinal angiodysplasias: A systematic review and individual patient data meta-analysis. Lancet Gastroenterol Hepatol 2021;6:922-32.
12. Goltstein LCMJ, Grooteman KV, Bernts LHP, et al. Standard of care versus octreotide in angiodysplasia-related bleeding (the OCEAN Study): A multicenter randomized controlled trial. Gastroenterology 2024;166:690-703.
13. Chen H, Wu S, Tang M, et al. Thalidomide for recurrent bleeding due to small-intestinal angiodysplasia. N Engl J Med 2023;389:1649-59.
14. Albitar HAH, Almodallal Y, Papadakis KA, et al. Intravenous bevacizumab reduces transfusion requirements and endoscopic interventions in patients with gastric antral vascular ectasia and small bowel angioectasia. Gastroenterology 2020;158(4):1162-3.e4.