La diverticulose colique est caractérisée par la présence d’anomalies anatomiques acquises, les diverticules, le long du cadre colique. Il s’agit de la première pathologie, en fréquence, mise en évidence lors d’une colonoscopie de routine. On estime que plus de la moitié des adultes âgés de plus de 50 ans en sont porteurs. Elle est asymptomatique dans la majorité des cas.
La maladie diverticulaire inclut la diverticulose asymptomatique et toutes les complications qui en découlent, principalement la diverticulite aiguë et le saignement diverticulaire.
La maladie diverticulaire a un impact majeur sur la santé individuelle mais également sur le système de santé. Bien que sa fréquence augmente avec l’âge et qu’on associe essentiellement ses complications à une population âgée, la hausse significative de sa prévalence dans des catégories d’âge plus jeunes (avant 50 ans, voire avant 40 ans) est significative.1 L’allongement de l’espérance de vie et le vieillissement de la population entraînent une hausse des consultations et des hospitalisations pour ce motif.
Une pathogenèse partiellement comprise
Les diverticules coliques sont exclusivement des pseudo-diverticules (ou « faux » diverticules), qui se définissent par des ectasies sacculaires intéressant uniquement la muqueuse et la sous-muqueuse du côlon, sans implication de la musculeuse. Ils s’observent typiquement sur des zones de faiblesse, aux points d’entrée des vaisseaux de la paroi colique (vasa recta). Leur pathogenèse et les facteurs de risque qui en découlent sont multiples et partiellement décrits mais souvent résumés à trois critères : l’âge, l’environnement et la motilité colique.2
La prévalence est clairement âge-dépendante, passant de moins de 20 % chez les adultes de moins de 40 ans à plus de 50 % au-delà de 60 ans. Outre leur présence, c’est également leur densité qui augmente avec l’âge, laissant suspecter un processus dynamique.
L’obésité est un facteur de risque bien identifié, avec une augmentation linéaire du risque relatif de maladie diverticulaire mais aussi de ses complications, selon l’indice de masse corporelle. La sédentarité est, au même titre, bien reconnue. Les patients de sexe masculin sont aussi davantage concernés. L’activité physique semble, en revanche, être protectrice. Un régime pauvre en fibres, occasionnant un ralentissement du transit et une augmentation des pressions intracoliques, est associé à une augmentation du risque. Toutefois, l’effet protecteur d’un régime riche en fibres n’est pas démontré et reste encore débattu. En dépit de cette incertitude, les nombreux avantages d’une telle alimentation suffisent à continuer de le recommander.
En outre, la diverticulose colique montre d’importantes variations géographiques, tant en matière de prévalence que de localisation des lésions : dans les pays occidentaux, plus de 75 % des diverticules sont situés au niveau du sigmoïde ; la diverticulose du côlon droit est majoritairement observée dans les populations asiatiques et semble principalement associée à des anomalies génétiques et à des modifications de la motilité colique.
Diverticulite aiguë
La diverticulite aiguë est la complication la plus fréquente de la diverticulose colique. Son incidence est en constante augmentation dans les pays industrialisés, notamment chez les patients jeunes (moins de 50 ans), avec une augmentation de l’incidence de 130 % aux États-Unis depuis les années 1980. On estime qu’environ 25 % des patients avec des diverticules coliques développeront au moins un épisode de diverticulite au cours de leur vie, et 12 % une diverticulite compliquée – le plus souvent un phlegmon ou un abcès. Contrairement à l’idée reçue que la maladie serait progressive – avec un risque plus élevé de diverticulite compliquée à chaque récidive –, les complications, à l’exception des fistules, sont plus fréquentes lors du premier épisode.3
Historiquement, la prise en charge de la diverticulite aiguë reposait sur une antibiothérapie systématique en milieu hospitalier et sur la réalisation d’une colonoscopie six à huit semaines après la fin des symptômes, et ce quelle que soit la sévérité de l’épisode. Depuis plusieurs années, on assiste à un changement de stratégie de prise en charge, bien rapporté dans les recommandations les plus récentes. Les principales modifications concernent :
la place de l’antibiothérapie ;
les modalités de prise en charge (ambulatoire ou hospitalière) ;
l’indication à la colonoscopie.
Diagnostic et classification
Le diagnostic de diverticulite sigmoïdienne aiguë, y compris chez les patients ayant des antécédents de diverticulite connus, ne peut pas être affirmé sur les seules données cliniques.
Il est recommandé de réaliser systématiquement un bilan sanguin, avec un hémogramme, un dosage de la CRP et de la créatininémie.
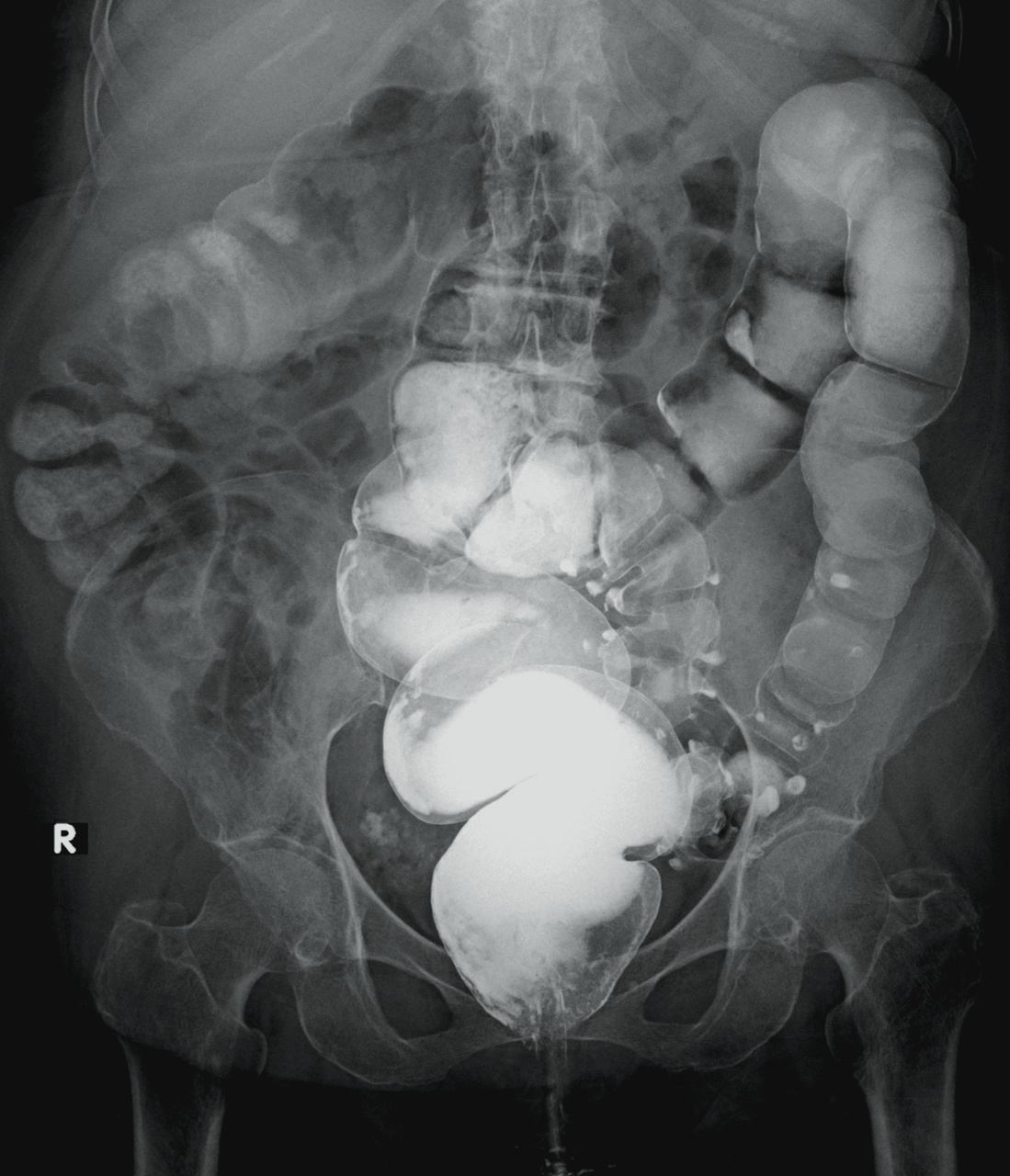
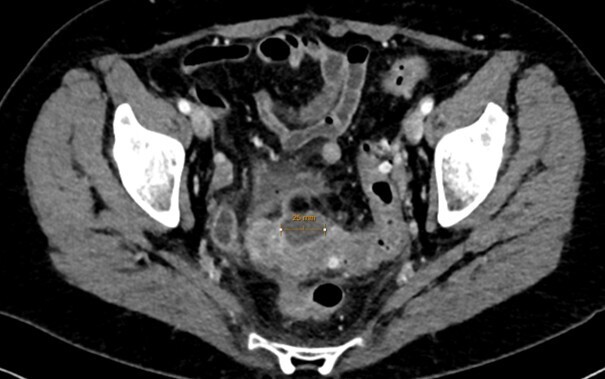
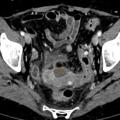
Le scanner abdomino-pelvien avec injection intra-veineuse de produit de contraste en l’absence de contre-indication (fig. 1) est recommandé en première intention pour le diagnostic et la recherche des complications ;1 l’IRM abdominale est une bonne alternative, notamment en cas d’allergie sévère au produit de contraste ou pour les femmes enceintes. L’opacification digestive basse n’est plus indiquée dans la prise en charge initiale. L’imagerie peut être discutée et parfois omise chez des patients aux multiples récidives et en l’absence de critères de gravité (péritonisme clinique, syndrome inflammatoire marqué…).
Il existe de multiples classifications de la diverticulite aiguë, la plus fréquemment utilisée est le score de Hinchey modifié, bien qu’historiquement fondé sur des constatations peropératoires, et donc peu informatif pour le traitement conservateur. La classification de Hansen et Stock, fondée sur des critères radiologiques, est une bonne alternative (tableau).
Traitement et place de l’antibiothérapie
Le traitement empirique d’une diverticulite aiguë impliquait, jusque dans les années 2000, une antibiothérapie systématique, pour une durée minimale de sept jours. Depuis, plusieurs études ont remis en question cette pratique et ont conclu qu’un traitement symptomatique, sans antibiothérapie, n’augmentait finalement pas le risque de développer une diverticulite compliquée, ni le risque de récidive ou le nombre d’interventions chirurgicales. Deux essais cliniques (AVOD en 2012, puis DIABOLO en 2020)4,5 ont ainsi démontré que l’omission du traitement antibiotique n’influençait pas l’incidence des complications, ni des sigmoïdectomies en urgence, ni du temps de récupération. Par ailleurs, le suivi à long terme de ces patients n’a pas montré de progression dans l’incidence des récidives.
Dès lors, le traitement symptomatique seul peut être recommandé en routine pour la diverticulite non compliquée.6
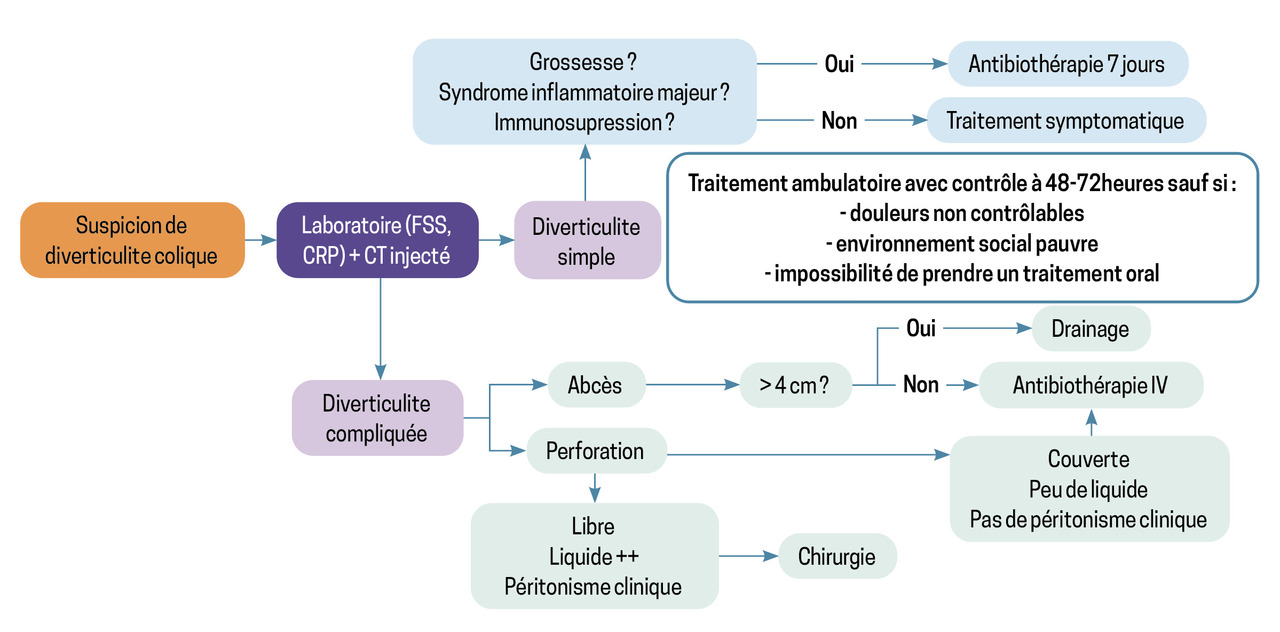
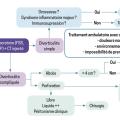
En revanche, l’antibiothérapie doit être considérée dans le traitement d’une diverticulite, même non compliquée, chez les patients immunodéprimés (immunodépression congénitale ou acquise, traitement immunosuppresseur ou immunomodulateur, corticothérapie systémique, cancer évolutif, insuffisance rénale terminale), lors de la grossesse, en présence de signes de gravité (signes de sepsis, syndrome inflammatoire majeur…) ou chez des patients très malades, que l’on classifie volontiers par le score de l’American Society of Anesthesiologists (ASA) selon la sévérité de leurs comorbidités (d’un patient sain [ASA I] à un état de mort cérébrale [ASA VI]).4,5 Dans ces cas, une antibiothérapie par voie orale est proposée, ne dépassant pas une durée de sept jours, associant amoxicilline et acide clavulanique ou, en cas d’allergie, une fluoroquinolone (lévofloxacine ou ciprofloxacine) et du métronidazole (fig. 2).
En l’absence de comorbidité significative et/ou de contexte social défavorable (logement non suffisamment salubre, absence de proche présent pour surveillance…), le traitement s’effectue en ambulatoire. Dans cette situation, une surveillance clinique et biologique est préconisée, idéalement quarante-huit à soixante-douze heures après le diagnostic.
En cas de diverticulite compliquée, abcédée notamment, de suivi ambulatoire impossible ou de traitement oral mal toléré, une antibiothérapie intraveineuse s’impose, suivant un schéma identique à celui du traitement per os.
Un régime alimentaire non restrictif est proposé au décours du traitement. En effet, aucune donnée ne montre qu’un régime alimentaire pauvre en fibres réduirait le risque de complications.1
Indications de la chirurgie
L’avènement du traitement conservateur a considérablement réduit l’indication chirurgicale lors d’événements aigus. Elle est désormais réservée aux patients ayant des signes de sepsis sévère, de choc septique ou en cas d’échec du traitement conservateur.
La technique chirurgicale de première intention est la résection colique, qui doit être réalisée par laparoscopie lorsque les conditions s’y prêtent.2 Une anastomose directe est possible et recommandée en l’absence de contre-indications (support aminergique important, cachexie, traitements par glucocorticoïdes ou contamination stercorale).
L’intervention de Hartmann (résection colique segmentaire et confection d’une colostomie) est une option chirurgicale dans les situations menaçant le pronostic vital du fait de la sévérité du sepsis.
Les diverticulites abcédées sont également traitées par antibiothérapie, couplée à un drainage radiologique pour les collections de grande taille (plus de 4 cm).
Une antibiothérapie seule, sans geste chirurgical ni drainage radiologique, est recommandée pour les diverticulites perforées avec présence de bulles de pneumo-péritoine péricolique ou même à distance et en l’absence de signes cliniques de péritonite ou de sepsis sévère.
Suivi et prévention des récidives
Le principal diagnostic différentiel de la diverticulite aiguë est le cancer colorectal : on estime que 1,3 % des patients avec une diverticulite simple et jusqu’à 7,9 % des patients avec une diverticulite compliquée ont en réalité un cancer colorectal. L’endoscopie doit donc être proposée systématiquement aux patients entrant dans les critères de dépistage du cancer colorectal ou ayant des symptômes compatibles (perturbation du transit, sang dans les selles, perte de poids…) ; sa réalisation reste controversée en dehors de ces critères après un épisode de diverticulite non compliquée.7
Les recommandations européennes et américaines en cas de diverticulite simple divergent légèrement. Selon les recommandations américaines, au décours d’un premier épisode de diverticulite simple, une colonoscopie ne serait pas nécessaire, le risque de carcinome colorectal étant identique au risque de la population générale. Les recommandations européennes proposent, quant à elles, la réalisation d’une colonoscopie de principe après un premier épisode de diverticulite, même simple, en l’absence d’examen endoscopique récent.2
Néanmoins, l’ensemble des recommandations est unanime concernant le recours à une colonoscopie après un épisode de diverticulite compliquée : sa réalisation est proposée six à huit semaines après l’épisode aigu, si la dernière endoscopie date de plus de trois ans.
Dans la littérature, le risque de récidive de diverticulite après une première poussée concerne environ un tiers des patients, avec un recul moyen de dix ans. Il n’existe malheureusement aujourd’hui aucun moyen efficace de limiter ce risque, notamment aucun régime ni restriction alimentaire. Même si le régime riche en fibres est recommandable pour ses multiples bénéfices sur la santé, il n’a pas montré d’effet protecteur en prophylaxie secondaire, après un épisode de diverticulite. Il n’y a pas non plus de risque à consommer des fruits à coque, du blé ou du maïs.
En l’absence d’argument scientifique probant, aucun traitement médical préventif n’est proposé (ni les probiotiques, ni la rifaximine, ni la mésalazine par exemple).
Autres complications
La diverticulose peut aussi être à l’origine d’hémorragie digestive basse ou de fistules.
Hémorragie digestive
L’hémorragie digestive basse diverticulaire est la deuxième complication la plus fréquente. Contrairement à la diverticulite, la majorité des saignements diverticulaires prennent leur origine dans le côlon droit. La pathogenèse est directement liée au fait que les diverticules émergent typiquement sur les points d’entrée des vaisseaux coliques, qui, du fait de l’herniation, s’étirent et s’amincissent autour du diverticule. Ils sont alors particulièrement fragiles et exposés aux traumatismes causés par le contenu luminal. La prise d’anti-inflammatoires non stéroïdiens et les traitements antiagrégants plaquettaires augmentent considérablement le risque de saignement, et plus de la moitié des hémorragies diverticulaires se manifestent sous ce type de médication. L’hémorragie digestive qui en résulte est typiquement indolore, souvent de grand volume et se tarit généralement spontanément. Malgré cela, environ un tiers des patient nécessitent un geste hémostatique et 15 % ont des saignements récidivants.8
L’examen de choix est la colonoscopie, qui permet d’associer diagnostic et geste thérapeutique. Étant donné l’histoire naturelle de ces saignements, l’examen endoscopique ne permet malheureusement pas d’identifier le diverticule incriminé, et le diagnostic est souvent supposé. Le scanner abdominal injecté doit être réservé aux patients instables sur le plan hémodynamique.9
Le traitement chirurgical lors d’hémorragie digestive reste anecdotique et doit être limité aux patients pour qui le traitement conservateur est un échec, avec persistance d’un saignement important, en dépit de plusieurs endoscopies. Il est primordial de pouvoir localiser en pré-opératoire la source du saignement afin d’effectuer une résection colique la plus segmentaire possible, tout en garantissant d’emporter la zone incriminée. Les colectomies subtotales, laissant uniquement le rectum en place, sont grevées d’une morbi-mortalité majeure, et les colectomies segmentaires à l’aveugle sont associées à un risque de récidive de saignement de plus de 40 %.
Fistules
La maladie diverticulaire, et surtout les inflammations répétées qui en découlent, peuvent engendrer des complications plus insidieuses, souvent chroniques, se développant sur plusieurs mois ou années. La fistulisation correspond à la formation d’une communication anormale entre deux organes, conséquence d’un processus inflammatoire persistant ou itératif. Les types les plus courants sont les fistules sigmoïdovésicales, jusqu’à 65 % des cas, et les fistules sigmoïdovaginales chez la femme. La maladie diverticulaire est responsable de plus de la moitié des fistules colovésicales observées.10
Les infections urinaires à répétition et une émission de selles ou de gaz par l’urètre ou le vagin respectivement sont les modes de révélation clinique typiques.
Le diagnostic nécessite généralement la réalisation d’un scanner, avec si possible injection de produit de contraste en intraluminal afin de déceler la fuite. Une colonoscopie doit impérativement faire partie du bilan, à but diagnostique mais surtout afin d’exclure une origine néoplasique de la fistule. En cas de communication avec la vessie, la cystoscopie peut être également utile. La prise en charge de ces complications est essentiellement chirurgicale.
Quand adresser le patient au chirurgien ?
On a longtemps considéré la répétition des épisodes comme une indication chirurgicale et donc proposé à tous les patients la sigmoïdectomie après deux crises de diverticulite aiguë. Cette affirmation a cependant progressivement été remise en cause, notamment par la constatation que le premier épisode est généralement le plus sévère et que le risque de complications aiguës n’est pas corrélé à la récidive des diverticulites.
L’objectif de la prise en charge chirurgicale doit être axé sur l’amélioration de la qualité de vie du patient. Le nombre de crises et/ou leur sévérité ne sont plus inclus dans l’arbre décisionnel mais sont à pondérer en fonction du retentissement sur la vie quotidienne. Il est donc essentiel de proposer une approche individualisée à chaque patient, selon son âge, son activité mais aussi selon sa perception de la maladie.
La persistance de symptômes digestifs, même en dehors d’un épisode aigu, doit motiver une consultation chirurgicale pour discuter d’une intervention élective. De même, l’apparition de complications chroniques, comme une fistulisation aux organes adjacents ou la présence d’une sténose nécessitent une évaluation spécialisée.
Il est important de noter qu’en dépit d’une prise en charge chirurgicale bien conduite, le risque de récidive après sigmoïdectomie n’est pas nul et est estimé entre 2 et 4 % à dix ans.11
Que dire à vos patients ?
La maladie diverticulaire est très fréquente. Souvent bénigne et asymptomatique, elle ne requiert alors aucun traitement spécifique. La principale complication est la survenue de poussées de diverticulite aiguë.
Les diverticulites simples sont traitées en ambulatoire, avec ou sans antibiotiques, mais imposent un suivi rapproché au cabinet, l’évolution vers une diverticulite compliquée étant possible, même sous traitement.
La chirurgie peut se discuter à tout moment, indépendamment du nombre de poussées aiguës, mais en fonction des symptômes et de leur retentissement sur la vie quotidienne.
Il n’est généralement pas possible de retirer tous les diverticules, ceux-ci pouvant s’étendre à tout le cadre colique. Ainsi, même après une chirurgie, les récidives sont possibles.
Le dépistage du cancer colorectal reste indiqué en routine dès l’âge de 50 ans, indépendamment de la présence ou non de diverticules, et doit être poursuivi même après une chirurgie colique.
2. Schultz JK, Azhar N, Binda GA, et al. European society of coloproctology: Guidelines for the management of diverticular disease of the colon. Colorectal Dis 2020;22(Suppl 2):5-28.
3. Strate LL, Morris AM. Epidemiology, pathophysiology, and treatment of diverticulitis. Gastroenterology 2019;156(5):1282-98.e1.
4. Chabok A, Påhlman L, Hjern F, et al. Randomized clinical trial of antibiotics in acute uncomplicated diverticulitis. Br J Surg 2012;99(4):532-9.
5. Daniels L, Ünlü Ç, de Korte N, et al. Randomized clinical trial of observational versus antibiotic treatment for a first episode of CT-proven uncomplicated acute diverticulitis. Br J Surg 2017;104(1):52-61.
6. Van Dijk ST, Chabok A, Dijkgraaf MG, et al. Observational versus antibiotic treatment for uncomplicated diverticulitis: An individual-patient data meta-analysis. Br J Surg 2020;107(8):1062-9.
7. Meyer J, Buchs NC, Schiltz B, et al. Comment on: Should a colonoscopy be offered routinely to patients with CT proven acute diverticulitis? A retrospective cohort study and meta-analysis of best available evidence. World J Gastrointest Endosc 2020;12(9):320-2.
8. Vajravelu RK, Mamtani R, Scott FI, et al. Incidence, risk factors, and clinical effects of recurrent diverticular hemorrhage: A large cohort study. Gastroenterology 2018;155(5):1416-27.
9. Sengupta N, Feuerstein JD, Jairath V, et al. Management of patients with acute lower gastrointestinal bleeding: An updated ACG guideline. Am J Gastroenterol 2023;118(2):208-31.
10. Melchior S, Cudovic D, Jones J, et al. Diagnosis and surgical management of colovesical fistulas due to sigmoid diverticulitis. J Urol 2009;182(3):978-82.
11. Choi KK, Martinolich J, Canete JJ, et al. Elective laparoscopic sigmoid colectomy for diverticulitis – An updated look at recurrence after surgery. J Gastrointest Surg 2020;24(2):388-95.

 Encadrés
Encadrés