Une cinquantaine, voire plus, telle est la quantité de causes de douleurs abdominales chroniques que l’on peut trouver dans les articles de revue. Évoquer toutes ces pathologies à titre systématique n’a pas d’intérêt et détourne la réflexion du maître symptôme ou du maître syndrome, s’il existe. Par exemple, évoquer une -tuberculose péritonéale sans autre argument que la douleur abdominale n’a pas de sens ; en revanche, y penser devant une ascite exsudative lymphocytaire devient facile. Si le raisonnement heuristique est efficace dans la plupart des situations aiguës, il ne peut pas être appliqué aux questions diagnostiques plus complexes, chroniques. Dans ces cas, mobiliser toutes ses ressources de raisonnement est indispensable pour ne pas s’égarer, ce qui demande du temps.
Le but ici n’est pas de donner clés en main les examens qui règleront la question étiologique de la douleur. Il est proposé de reprendre quelques points de physiologie et de l’examen clinique, et de détailler le groupe des douleurs abdominales d’origine pariétale, méconnues, y compris des spécialistes. Certaines causes trompeuses ou « à ne pas oublier » seront développées. Les troubles fonctionnels seront abordés sous l’angle du diagnostic positif, et non « d’élimination » ; il est fréquemment signalé l’absence d’utilité des examens d’imagerie et endoscopiques dans ces situations sans « drapeaux rouges ».
Limiter l’impact économique de nos prescriptions est un objectif de santé publique régulièrement rappelé.1 Pour le patient, prime de limiter l’iatrogénie et l’errance médicale induites par des prescriptions inutiles.
Systématisation neurologique et voies douloureuses
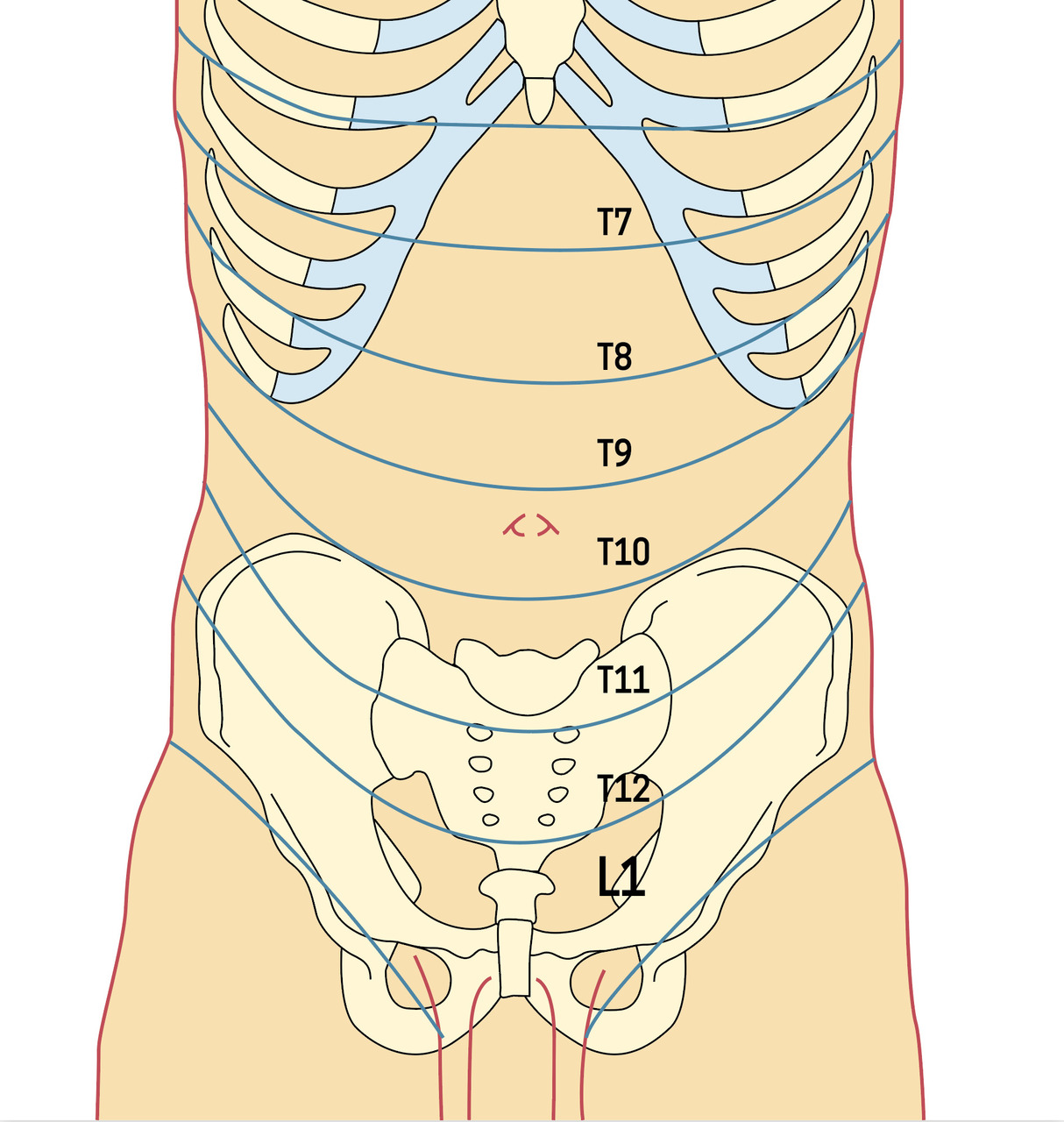
La paroi musculaire abdominale est constituée des muscles grands droits, obliques externes, obliques internes et transverses. Le gril costal prend fin à hauteur de la vertèbre L1. La crête iliaque correspond à la vertèbre L4 et à l’ombilic. Ces rapports anatomiques vertébraux ne se superposent pas aux territoires d’innervation de la paroi abdominale des dermatomes et des nerfs périphériques issus des branches antérieures des nerfs spinaux de T6 à L1. Les territoires de ces nerfs périphériques sont identiques aux dermatomes abdominaux, car il n’y a pas de plexus nerveux à ce niveau. Les repères d’intérêt sont le processus xiphoïde (T6), l’ombilic (T10) et le pli inguinal (L1) [figure]. Les branches des nerfs intercostaux (T6 à T11), sous-costaux (T12), ilio-hypogastriques et ilio-inguinaux (T12 -L1) traversent des structures, essentiellement des fascias, où des phénomènes compressifs peuvent survenir.1,2
Les voies sensitives sont très différentes selon qu’elles concernent la sensibilité viscérale ou la sensibilité somatique.
La douleur viscérale abdominale est mal systématisée, médiane, périombilicale ou épigastrique, plus rarement hypogastrique, sourde ou faite de crampes. Ceci est dû aux projections bilatérales et sur plusieurs métamères de ces neurones sensitifs, ainsi qu’à une moindre densité sensitive (10 % des afférences totales).
La douleur somatique abdominale d’origine pariétale, elle, est précise, désignée du bout du doigt, « en coup de couteau » ou à type de brûlure. Ceci est dû à l’innervation précise et localisatrice du système sensoriel somatique. Ce n’est pas strictement synonyme d’une douleur d’origine musculosquelettique ; le péritoine pariétal est concerné par cette sensibilité somatique, ce qui explique les constatations cliniques d’une péritonite.
Il existe des neurones à convergence dans la corne postérieure par lesquels communiquent les systèmes viscéral et somatique, expliquant les douleurs dites référées.1,2
Examiner la paroi en cas de « problème diagnostique »
Il s’agit ici de douleur abdominale chronique isolée. En effet, si la douleur s’accompagne d’un symptôme plus discriminant, comme une diarrhée chronique ou des vomissements répétés, c’est sur ce symptôme que s’articule plus volontiers la réflexion diagnostique.
L’examen de la paroi même de l’abdomen est souvent omis, par méconnaissance. Force est de constater qu’une douleur abdominale durable sans autre symptôme d’orientation est souvent d’origine pariétale.
Ainsi, l’examen musculocutané et rachidien mérite d’être pratiqué avant même d’envisager tout bilan complémentaire (échographie, scanner, IRM, endoscopie). Cela permet d’identifier les syndromes canalaires, myofasciaux, rachidiens et radiculaires. L’origine pariétale d’une douleur abdominale chronique peut concerner jusqu’à 30 % des patients étudiés.1,3
La désignation de la douleur du bout du doigt est un élément discriminant. Des scores sont proposés pour déterminer, par l’interrogatoire, l’origine pariétale d’une douleur abdominale chronique.2
En pratique, on palpe la paroi à la recherche d’un point douloureux précis déclenché du bout du doigt, on pratique le palper-rouler à la recherche d’une cellulalgie évocatrice d’une souffrance neuropathique, on cherche à déterminer si la contraction de la paroi exacerbe la douleur (test de Carnett [encadré] très en faveur de la mise en jeu de la sensibilité somatique), on examine les muscles latéraux et le rachis, à la recherche d’une douleur irradiée depuis celui-ci.
Causes pariétales de douleur abdominale chronique
Sept syndromes sont ici décrits comme étant responsables de douleur abdominale chronique d’origine pariétale.2
Syndrome du nerf cutané antérieur de l’abdomen
Le syndrome du nerf cutané antérieur de l’abdomen (anterior cutaneous nerve entrapment syndrome [ACNES]) est la cause pariétale de douleur la plus fréquente. Il s’agit d’un syndrome canalaire exercé sur un nerf cutané antérieur de l’abdomen (issu de la branche antérieure du nerf intercostal correspondant) par les structures musculo-aponévrotiques du muscle grand droit qu’il traverse. Cette traversée induit des conformations (angles droits) le rendant susceptible aux forces de traction ou de pression. Les phénomènes ischémiques qui en découlent sont responsables de la douleur. D’autres facteurs peuvent favoriser ces contraintes, comme l’obésité, la grossesse, le port d’une ceinture serrée, la toux, la défécation, etc.
La douleur est précise, montrée du bout du doigt, située sur la ligne semi-lunaire (bord latéral du muscle grand droit de l’abdomen). Une cellulalgie s’y associe et le test de Carnett (encadré) est positif.
Le traitement, pratiqué en centre d’évaluation et de traitement de la douleur, consiste en une injection locale d’anesthésiant (lidocaïne et cortisone) sous guidage échographique. L’échographie est utile au diagnostic différentiel (hernie, par exemple) et au repérage. L’effet est habituellement rapide, mais plusieurs injections peuvent être nécessaires. Un effet plus durable que ne le présageraient les propriétés pharmacologiques des produits injectés a été observé. Les hypothèses pour l’expliquer sont l’effet placebo, le diagnostic étiologique de la douleur permettant au patient de la comprendre et la levée de points gâchettes (trigger points) par le passage de l’aiguille. Les antalgiques classiques sont peu utiles. La chirurgie est une option pour les cas réfractaires3 (vignette clinique 1).
Syndromes des nerfs ilio-hypogastrique et ilio-inguinal
Les syndromes des nerfs ilio-hypogastrique et ilio-inguinal sont induits par une chirurgie hypogastrique la plupart du temps (chirurgie de hernie inguinale, appendicectomie, etc.). La douleur est basse : hypogastrique pour le premier, inguinale pour le second, jusqu’aux organes génitaux. Un déficit sensitif du territoire concerné est possible. Une zone gâchette peut se trouver en dessous et en dedans de l’épine iliaque antéro-supérieure.
Syndromes herniaires
Les hernies se trouvent surtout sur la ligne médiane, en région épigastrique ou ombilicale, ou au bord externe des muscles grands droits de l’abdomen (ligne semi-lunaire). Elles peuvent être responsables de douleur sans provoquer d’authentique syndrome occlusif (le contenu est parfois juste graisseux) ni même de franche masse.
Une hernie de la ligne semi-lunaire pourrait être difficile à distinguer d’un ACNES, car de localisation similaire. En cas de confusion avec un ACNES, l’injection d’anesthésiant étant échoguidée, le diagnostic est redressé par cet examen (vignette clinique 2).
Syndromes myofasciaux divers
Il s’agit de douleurs d’origine musculaire. Il existe typiquement des contractures musculaires douloureuses dont la pression déclenche la douleur (points gâchettes) et de la cellulalgie dans le territoire concerné. Les irradiations douloureuses, situées parfois bien loin du muscle en rapport, peuvent égarer, surtout en ce qui concerne les membres. Au niveau abdominal, les muscles grands droits de l’abdomen et psoas-iliaques en sont principalement à l’origine. Le diagnostic précis et la prise en soins sont plutôt l’affaire de la médecine manuelle encadrée.
Syndromes radiculaires
Toute pathologie radiculaire concernant les étages de T6 à L1 peut être concernée. Il s’agit plus fréquemment de douleurs post-zostériennes ou de neuropathies diabétiques. L’orientation étiologique est celle du syndrome neurologique radiculaire.
Syndrome rachidien irradié
Comme pour les radiculopathies de T6 à L1, un syndrome rachidien peut être responsable d’une irritation des branches des nerfs spinaux correspondants. Lorsque la branche postérieure est concernée, cela pose peu de difficultés, la douleur étant déjà proche du rachis. S’associent une rachialgie, une contracture des muscles paravertébraux et une douleur dans le territoire cutané correspondant, soit spontanée soit provoquée par le palper-rouler.
Lorsque la branche antérieure est concernée, la douleur est abdominale et le diagnostic moins aisé, la rachialgie étant peu rapportée spontanément. Le déclenchement de la douleur abdominale par les inflexions de colonne vertébrale et l’examen rachidien sont des signes précieux.
Les dérangements intervertébraux mineurs sont fréquents à la charnière dorsolombaire (T12 -L1) en raison des contraintes mécaniques locales (point de pivot). L’irritation de la branche postérieure du nerf spinal concerne la fosse lombaire et la partie postéro-médiale de la crête iliaque. L’irritation de la branche antérieure concerne la fosse iliaque et le pli inguinal.4 L’IRM rachidienne, avancée comme outil diagnostique par certains,5 est à interpréter avec précaution car il peut exister un syndrome rachidien sans hernie discale (ou autre anomalie visible), comme au cours d’un dérangement intervertébral mineur, et des anomalies à l’IRM sont possibles sans qu’elles ne soient responsables des symptômes (vignette clinique 3).
Et la paroi thoracique !
Le syndrome de Cyriax et la xiphodynie sont responsables de douleur des quadrants supéro-externes et épigastrique, respectivement.
Causes viscérales trompeuses
Il est utile de rappeler certaines causes à évoquer facilement. Il ne s’agit pas de les éliminer par la réalisation systématique d’examens complémentaires mais de les considérer, de peser les arguments pour et contre et de choisir, après délibération, si des examens complémentaires sont nécessaires.
Un bilan biologique de première ligne peut être proposé : hémogramme, protéine C réactive, créatininémie, natrémie, kaliémie, calcémie, glycémie à jeun, transaminases, phosphatases alcalines, bilirubinémie, lipasémie, ferritinémie, anticorps antitransglutaminase. Le dosage de la TSH est proposé par certains, mais l’hypothyroïdie est responsable de douleur abdominale dans le cadre d’un iléus : la recherche étiologique est alors davantage celle d’un iléus paralytique que celle d’une douleur abdominale.
En cas de suspicion de maladie inflammatoire de l’intestin, parce qu’une carence martiale est détectée par exemple, mais que la probabilité reste faible, le dosage de la calprotectine fécale peut être utile pour décider de la réalisation de l’endoscopie.
L’important est de rechercher des « drapeaux rouges », qui doivent faire remettre en question un diagnostic bénin. La plupart de ceux qui sont cités font partie du « bon sens » : début « tardif » des symptômes (après l’âge de 45 ans), douleur accompagnée d’une perte de poids ou d’une anorexie, de vomissements, d’un saignement digestif, d’une biologie anormale (anémie ferriprive ou seulement microcytose et hypochromie au stade précoce de la carence martiale, syndrome de malabsorption, syndrome inflammatoire, etc.), terrain vasculaire, antécédent de radiothérapie abdomino-pelvienne, antécédents familiaux (cancer digestif, maladie inflammatoire chronique de l’intestin).
Ischémie mésentérique chronique
L’ischémie mésentérique chronique est facile à évoquer si la description douloureuse est celle d’une claudication post-prandiale. La description des symptômes n’étant pas toujours claire, ce diagnostic doit être évoqué facilement chez des patients au terrain vasculaire ou ayant reçu une radiothérapie abdomino-pelvienne. Dans ces cas, il s’agit d’un mécanisme occlusif, par opposition aux mécanismes non occlusifs rencontrés dans le bas débit de l’insuffisant cardiaque chronique sévère ou dans l’hypoxie induite par l’anémie profonde. La perte de poids, fréquente, est à rechercher. La douleur peut devenir continue lorsque l’ischémie est critique (syndrome de menace mésentérique), annonçant une ischémie aiguë. Aucun marqueur biologique ne permet de confirmer ou d’infirmer le diagnostic ; l’acide lactique ne s’élève que tardivement et ne fait que signer la gravité de l’ischémie.6
Troubles métaboliques
Trois diagnostics sont à évoquer.
Insuffisance surrénale chronique
Les symptômes dominants en fréquence sont la fatigue, l’anorexie et la perte de poids. La douleur abdominale est plus souvent constatée lorsque l’insuffisance surrénale est périphérique (un tiers des cas).
Hypercalcémie
La douleur abdominale peut être spécifique ou liée à une complication (pancréatite, constipation, ulcère gastroduodénal).
Intoxication chronique au plomb
La douleur abdominale apparaît à des niveaux d’exposition importants. Pour des niveaux inférieurs, les symptômes peuvent être une hypertension artérielle, une néphropathie, des troubles neuro-cognitifs, un tremblement, des troubles de la fertilité.
Maladie de Crohn
Ce diagnostic est facile à évoquer en cas de diarrhée chronique avec un syndrome de malabsorption. Certains patients n’ont pas de diarrhée et ne se plaignent que d’une douleur. L’existence d’un syndrome inflammatoire, d’une carence martiale, d’une élévation de la calprotectine fécale sont des arguments devant amener à réaliser une endoscopie.
Endométriose
L’endométriose est responsable de dysménorrhée, de dyschésie, de dysurie, de dyspareunie et d’infertilité. Lorsque la localisation est extragénitale, le délai diagnostique est allongé. L’atteinte gastro-intestinale (et surtout recto-sigmoïde) est la plus fréquente des localisations extragénitales. Elle peut en imposer pour des troubles intestinaux fonctionnels : douleur abdominale cyclique ou chronique, diarrhée (cataméniale), constipation, flatulences. Le diagnostic est l’affaire du gynécologue, sur l’appui d’un examen clinique, d’une échographie endovaginale et d’une IRM abdomino-pelvienne. La coloscopie est souvent normale, même en cas d’hématochézie.7
Narcotic bowel syndrome
Chez un consommateur d’opioïdes, le narcotic bowel syndrome est une douleur abdominale chronique paradoxalement aggravée par l’escalade posologique. Le principal mécanisme physiopathologique invoqué est une hyperalgésie centrale médiée par les opioïdes. Le traitement est difficile, multimodal, associant une réduction des opioïdes, leur rotation et leur substitution (antidépresseurs), des adaptations de l’hygiène de vie (alimentation, exercice), une régularisation du transit et un suivi psychologique. L’adhésion du patient est évidemment indispensable.
Douleurs abdominales cycliques
Il ne s’agit pas d’une douleur chronique à proprement parler, mais la condition responsable de crises douloureuses l’est. On ne fera que citer : l’endométriose déjà abordée, l’angiœdème à bradykinine, la porphyrie aiguë intermittente, la fièvre méditerranéenne familiale, la drépanocytose.
Et les brides ?
Il n’est pas clair qu’une bride puisse générer une douleur abdominale chronique sans syndrome occlusif. Elles en auraient été rendues responsables en l’absence d’autre cause identifiée en laparoscopie dans les années 1980. Depuis, cette hypothèse a été largement remise en question par des méta-analyses.8
Troubles fonctionnels : un diagnostic positif
C’est une réflexion qui dépasse la sphère abdominale mais qui lui est applicable.
Il y a les troubles fonctionnels intestinaux avec modification du transit, certes, mais ils ne sont pas indispensables pour poser ce diagnostic. La variété des processus physiopathologiques attribués aux troubles fonctionnels intestinaux montre bien les limites pour les expliquer.9
Les troubles fonctionnels sont relégués au dernier rang du diagnostic : « Lorsqu’on ne trouve rien, c’est que c’est fonctionnel. » Ce mode de pensée diagnostique conduit à une prescription outrancière d’examens, répétés plusieurs fois pour la plupart, et place les patients dans l’attente d’être libérés de leurs tourments par un diagnostic médical considéré plus gratifiant. Lorsqu’on prononce « fonctionnel », ce qui est entendu est « C’est dans votre tête », autrement dit « Vous n’êtes pas malade ». Et pourtant ! C’est là que les soins sont les plus difficiles, parce qu’ils impliquent une équipe pluridisciplinaire, une prise en charge de longue durée et, surtout, la pleine participation des patients.
Il y a une incohérence à en faire, d’un côté, un diagnostic d’élimination et, de l’autre, de rapporter l’absence d’utilité de l’imagerie et des endoscopies lorsqu’il n’y a pas de « drapeau rouge ».9 L’important est donc de les rechercher par l’examen clinique et une biologie « minimale » (évoquée ci-avant).
Faire des troubles fonctionnels des diagnostics positifs (ie non « d’élimination ») est certainement un début. Est-il bien raisonnable de chercher à éliminer par tous les moyens l’entièreté des causes de douleur abdominale chronique si rien ne nous y incite, vu leur quantité ? Expliquer la physiopathologie des troubles fonctionnels est long mais indispensable pour obtenir l’adhésion du patient.10
De l’utilité du raisonnement
La vignette clinique 4 illustre les limites des heuristiques de raisonnement qui n’ont pas permis d’aboutir au diagnostic. La réflexion présentée n’est pas compliquée mais il a été nécessaire de se l’imposer.
Test de Carnett
Chez un patient en décubitus dorsal, lorsque le point douloureux est identifié, le praticien demande au patient de contracter la paroi abdominale en maintenant la pression identique. Pour faciliter le test, il peut lui être demandé de lever les jambes tendues et/ou de rapprocher le menton du sternum en décollant les épaules du lit.
Le test est considéré comme positif si la douleur est exacerbée, suggérant l’implication du système sensitif somatique. Ce signe est particulièrement présent dans le syndrome du nerf cutané antérieur de l’abdomen. En revanche, si la douleur diminue, cela oriente vers une origine viscérale.
Vignette clinique 1
Une patiente d’une quarantaine d’années est adressée pour une douleur abdominale chronique fluctuante évoluant depuis deux ans. Les examens sanguins, l’échographie abdominale puis le scanner abdomino-pelvien précédemment réalisés sont tous normaux. Le scanner est refait six mois plus tard en raison de la persistance de la douleur, et la patiente est adressée en gastroentérologie. Des endoscopies sont proposées et apparaissent normales. La patiente désigne de manière précise sa douleur, du bout du doigt, au bord latéral d’un muscle grand droit. Un examen pariétal est conduit : reproduction de la douleur du bout du doigt, cellulalgie peu étendue, signe de Carnett positif. L’infiltration permet de faire disparaître la douleur.
Vignette clinique 2
Un patient de 27 ans consulte pour une douleur abdominale récurrente sus-ombilicale. Il a une hernie de la ligne blanche connue. Cette fois, la douleur est plus intense, sans autre signe associé. Une masse de petite taille, centimétrique, est palpée précisément à l’endroit douloureux. Le scanner n’ayant montré qu’un contenu graisseux, le patient n’est pas opéré. Il est traité par anti-inflammatoires non stéroïdiens et revu deux semaines plus tard. Il est finalement opéré, réglant son problème de douleur récurrente.
Vignette clinique 3
Un patient de 25 ans consulte aux urgences pour une douleur récurrente en fosse iliaque gauche. Le scanner montre une splénomégalie modeste. L’examen clinique splénique ne provoque aucune douleur. En revanche, le patient, au travail physiquement contraignant, a des points douloureux précis et une cellulalgie, évocateurs d’une origine pariétale de la douleur. Ces constatations conduisent à réaliser un examen rachidien mettant en évidence un syndrome de charnière thoracolombaire : contracture douloureuse des muscles paravertébraux ipsilatéraux à hauteur de T11 -L1, cellulalgie de l’aire rénale, points douloureux de la portion postérolatérale de la crête iliaque. Le traitement kinésithérapeutique du syndrome rachidien permet la disparition de la douleur abdominale.
Vignette clinique 4
Un patient de 20 ans se plaint d’une douleur abdominale chronique s’étant aggravée sur l’année, d’abord intermittente, puis permanente. Aucun facteur déclenchant n’est rapporté. L’intensité est moyenne à forte. La douleur est localisée au niveau du flanc droit et peut irradier en fosse iliaque droite. L’orthostatisme aggrave la douleur, et le repos physique la soulage. Il rapporte la palpation occasionnelle d’une masse au niveau du flanc droit. Il n’y a pas de symptôme associé tel que des troubles digestifs. Ni les analyses sanguines, ni les échographies abdominales, ni le scanner abdominopelvien ne permettent de poser un diagnostic.
L’examen physique n’est anormal qu’en orthostatisme : une masse profonde et sensible est effectivement palpée au niveau du flanc droit.
Un simple raisonnement fondé sur l’anatomie permet d’établir le diagnostic de ptose rénale, confirmée par échographie (en décubitus, puis en orthostatisme).
Que dire à vos patients ?
Les douleurs abdominales d’origine musculosquelettique sont fréquentes. Elles sont la conséquence des contraintes physiques exercées sur l’organisme.
Des gestes médicaux techniques sont possibles pour soulager, mais une prise en soins physique globale est indispensable : réduction pondérale en cas de surpoids, correction des postures, harmonisation des musculatures rachidienne et abdominale, règles d’économie rachidienne.
Un accompagnement par un kinésithérapeute peut être utile. Le patient doit être l’acteur principal de son bien-être.
2. Shian B, Larson ST. Abdominal wall pain: Clinical evaluation, differential diagnosis, and treatment. Am Fam Physician 2018;98(7):429-36.
3. Margalith J, Kehtari R. Douleurs abdominales d’origine pariétale : syndrome de compression de nerf cutané antérieur. Rev Med Suisse 2017;13(584):2054-6.
4. Perrin Barelli L, Guzman Dettori N. La face cachée des facettes. Lombalgies non spécifiques avec ou sans irradiations : les reconnaître pour mieux les traiter. Rev Med Suisse 2016;12(524):1222-4.
5. Mizumoto J, Shimizu T. Abdominal pain of spinal origin. J Hosp Gen Med 2024;6(6):161-3.
6. Corcos O, Mouri S. Ischémies mésentériques aiguës et chroniques. EMC – Gastro-entérologie [article 9-047-A-10], 2017.
7. Lukac S, Schmid M, Pfister K, et al. Extragenital endometriosis in the differential diagnosis of non-gynecological diseases. Dtsch Artzebl Int 2022;119(20):361-7.
8. Gerner-Rasmussen J, Burcharth J, Gögenur I. The efficacy of adhesiolysis on chronic abdominal pain: A systemic review. Langenbecks Arch Surg 2015;400(5):567-76.
9. Lukic S, Mijac D, Filipovic B, et al. Chronic abdominal pain: Gastroenterologist approach. Dig Dis 2022;40(2):181-6.
10. Pitron V, Ranque B, Vulser H, et al. Troubles somatiques fonctionnels : un modèle cognitif pour mieux les comprendre. Rev Med Interne 2019;40(7):466-73.

 Encadrés
Encadrés