Les sujets avec facteurs de risque hépatique, notamment un terrain métabolique ou une consommation à risque de boissons alcoolisées, sont très nombreux, mais, fort heureusement, seule une faible proportion d’entre eux développe une cirrhose et ses complications. Au vu du nombre très important de sujets à évaluer, l’identification des patients qui évoluent silencieusement vers la cirrhose nécessite de commencer par un test simple, sensible, acceptable et peu coûteux.
Formule et interprétation du FIB- 4
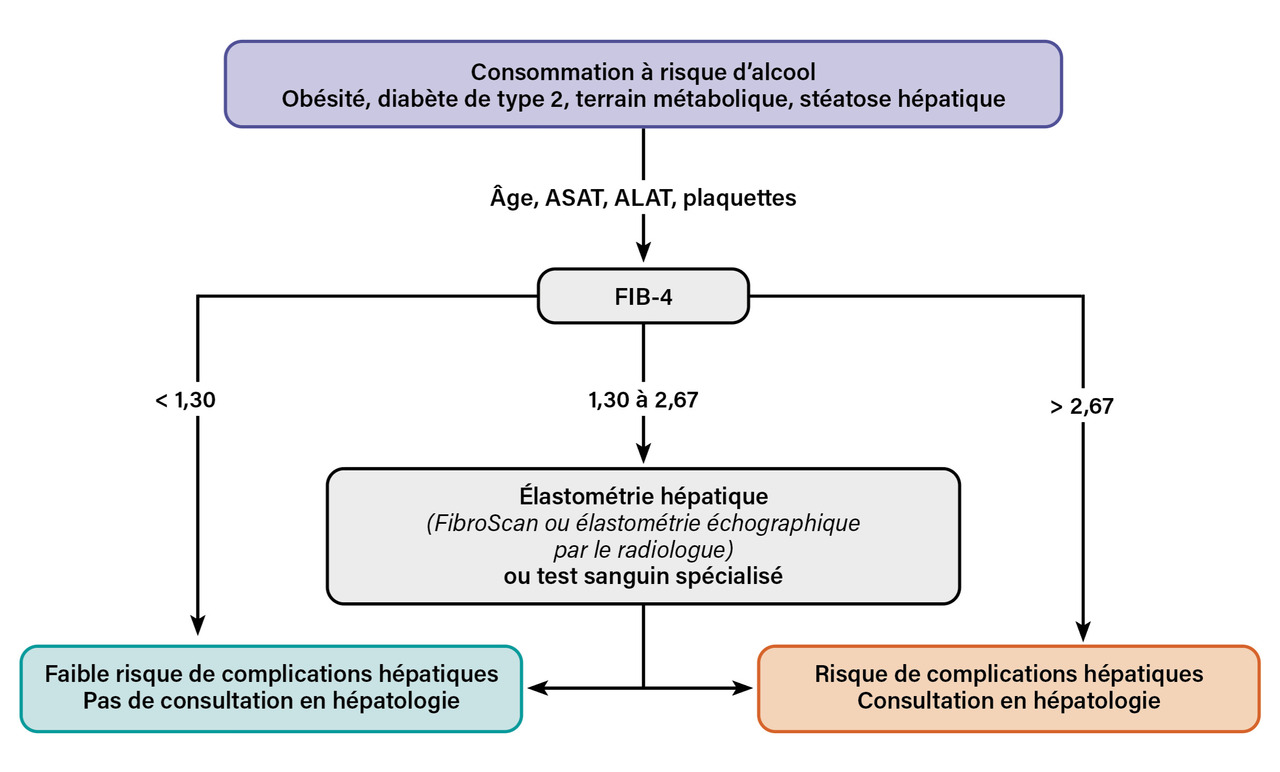
Le FIB- 4 (Fibrosis- 4) est un test sanguin simple développé pour le diagnostic de la fibrose hépatique avancée, qui précède la cirrhose. Le FIB- 4 inclut quatre paramètres : âge, aspartates aminotransférases (ASAT), alanines aminotransférases (ALAT) et plaquettes. Le FIB- 4 est calculé selon la formule suivante : (âge [années] × ASAT [UI/L])/(plaquettes [G/L] × ALAT [UI/L]1/2). De nombreux calculateurs en ligne gratuits sont disponibles.
Initialement développé dans une cohorte de 555 patients avec une co-infection hépatite C chronique et virus de l’immunodéficience humaine (VIH),1 le FIB- 4 a ensuite été validé dans les autres causes de maladie chronique du foie, notamment celles liées à l’alcool et la stéatose métabolique.2 - 4
Le FIB- 4 s’interprète avec deux seuils diagnostiques : un résultat inférieur à 1,30 signe un faible risque de fibrose hépatique avancée, alors qu’un résultat supérieur à 2,67 indique un haut risque, ces derniers patients nécessitant une prise en charge spécialisée (figure). Entre ces deux seuils (« zone grise » du test), le diagnostic est indéterminé et nécessite des explorations complémentaires (élastométrie hépatique et/ou test sanguin spécialisé).
Utilisation du FIB- 4 en pratique clinique
De nombreuses expériences de dépistage de la fibrose hépatique avancée avec le FIB- 4 ont été réalisées en soins primaires.5 Dans une étude anglaise, les médecins généralistes ont évalué un algorithme pour décider de l’adressage au médecin spécialiste hépatologue.6 Cet algorithme utilisait le FIB- 4 en première ligne, puis le test sanguin spécialisé ELF en seconde ligne si le résultat du FIB- 4 était dans la zone grise. Parmi les 1 452 patients inclus, 1 022 (70 %) avaient un FIB- 4 inférieur à 1,30. Les médecins qui appliquaient l’algorithme décisionnel divisaient par quatre le nombre de demandes futiles de consultation, définies comme les demandes de consultation spécialisée alors que le patient n’avait pas de fibrose hépatique avancée. Dans un autre travail, le FIB- 4 a été calculé de façon rétrospective dans un registre américain de soins primaires :7 20 556 patients avec facteur de risque hépatique ont été inclus, 64 % avaient un FIB- 4 inférieur à 1,30, 29 % un résultat dans la zone grise et 7 % un FIB- 4 supérieur à 2,67. Le taux de complications hépatiques au cours du suivi était faible dans les deux premiers groupes (respectivement 2 % et 4 %), alors qu’il était de 21 % chez les patients avec un FIB- 4 supérieur à 2,67. Ces résultats soulignent l’intérêt du FIB- 4 en soins primaires pour identifier les patients à risque de complication hépatique nécessitant une prise en charge spécialisée.
Un calcul automatique du FIB- 4 pour tous les patients en laboratoire de ville est-il pertinent ?
Parce qu’il inclut des paramètres biologiques largement prescrits, de nombreux laboratoires d’analyses médicales ont mis en place un calcul automatique du FIB- 4 dans leur système informatique, avec un rendu de résultat pour tous les patients, qu’ils aient ou non des facteurs de risque hépatiques. L’expérience marseillaise menée auprès de 29 707 patients dans 21 laboratoires a montré que 76,4 % des calculs automatiques de FIB- 4 concluaient à un faible risque hépatique.8 En revanche, le FIB- 4 était supérieur à 2,67 dans 7,3 % des cas, ce qui est bien plus élevé que la prévalence de la fibrose avancée en population générale (estimée à environ 1 à 2 %). De plus, 16,3 % des patients avaient un résultat dans la zone grise du FIB- 4 avec nécessité théorique d’effectuer des explorations complémentaires.
Cette approche de calcul automatique du FIB- 4 pour tous et sans sélection n’apparaît pas appropriée. Par exemple, un patient sous chimiothérapie peut avoir des transaminases élevées et des plaquettes basses à cause de son traitement mais sans aucune maladie chronique du foie sous-jacente. Il est ainsi absolument nécessaire de ne calculer le FIB- 4 que dans le bon contexte, à savoir chez les patients présentant des facteurs de risque hépatiques avérés. En effet, le calcul automatique sans sélection génère de nombreux faux positifs, des dépenses inappropriées (explorations complémentaires, consultations spécialisées) et surtout un stress inutile pour les patients qui reçoivent les résultats directement.
Test sanguin simple pour les patients à risque
Le FIB- 4 est un test sanguin simple, facile d’utilisation, fondé sur des paramètres largement prescrits en soins primaires. Utilisé chez les patients avec facteurs de risque hépatiques (consommation à risque d’alcool, obésité, diabète de type 2, syndrome métabolique), le FIB- 4 permet d’identifier les patients nécessitant des explorations complémentaires, voire d’emblée une consultation spécialisée. Le FIB- 4 constitue la première étape du processus d’identification des patients ayant une fibrose hépatique avancée asymptomatique, pour lesquels une prise en charge précoce permet d’éviter la survenue de complications hépatiques.
2. European Association for the Study of the Liver. EASL Clinical Practice Guidelines on non-invasive tests for evaluation of liver disease severity and prognosis - 2021 update. J Hepatol 2021;75(3):659-89.
3. Louvet A, Trabut JB, Moreno C, et al. Management of alcohol-related liver disease: The French Association for the Study of the Liver and the French Alcohol Society clinical guidelines. Liver Int 2022;42:1330-43.
4. European Association for the Study of the Liver. EASL-EASD-EASO clinical practice guidelines on the management of metabolic dysfunction-associated steatotic liver disease (MASLD). J Hepatol 2024;81(3):492-542.
5. Boursier J, Tsochatzis EA. Case-finding strategies in non-alcoholic fatty liver disease. JHEP Rep 2020;3(2):100219.
6. Srivastava A, Gailer R, Tanwar S, et al. Prospective evaluation of a primary care referral pathway for patients with non-alcoholic fatty liver disease. J Hepatol 2019;71(2):371-8.
7. Schreiner AD, Moran WP, Zhang J, et al. The association of fibrosis-4 index scores with severe liver outcomes in primary care. J Gen Intern Med 2022;37(13):3266-74.
8. Halfon P, Ansaldi C, Penaranda G, et al. Prospective screening of liver fibrosis in a primary care cohort using systematic calculation of fib-4 in routine results. PLoS One 2021;16(7):e0254939.