L’hypocalcémie est définie par une baisse de la concentration plasmatique du calcium total à un taux inférieur à 2,2 mmol/L, et à un taux inférieur à 1,15 mmol/L pour la calcémie ionisée. Il convient de distinguer l’hypocalcémie vraie – correspondant à la baisse de la fraction ionisée (fraction régulée) – de la fausse hypocalcémie – correspondant à la fraction couplée aux protéines. Les situations exposant à une hypoalbuminémie comme une dénutrition sévère ou un syndrome néphrotique aboutissent à une baisse de la calcémie totale sans diminution de la calcémie ionisée. En cas d’hypoalbuminémie, il faut donc utiliser la formule suivante : calcium corrigé = (40 – albumine) × 0,025 + Ca total.
Physiopathologie
L’homéostasie du calcium est un processus finement régulé qui assure le maintien des concentrations sériques de calcium à des niveaux constants. Elle est cruciale pour de nombreuses fonctions physiologiques, dont la contraction musculaire, la transmission nerveuse et la coagulation sanguine. Ce système repose sur l’interaction entre trois organes principaux : les os, les reins et les intestins, sous le contrôle hormonal de la parathormone (PTH), de la vitamine D active (1,25 -dihydroxyvitamine D3) et de la calcitonine.
La PTH, sécrétée par les glandes parathyroïdes, est le principal régulateur. Lors d’une hypocalcémie, elle stimule la résorption osseuse en activant les ostéoclastes, libérant ainsi du calcium dans la circulation sanguine. Parallèlement, elle augmente la réabsorption rénale de calcium et stimule la conversion de la vitamine D en sa forme active dans les reins, facilitant l’absorption intestinale du calcium.
La vitamine D active favorise également la minéralisation osseuse en maintenant l’apport calcique à travers l’intestin.
La calcitonine, produite par les cellules C de la thyroïde, joue un rôle antagoniste en inhibant la résorption osseuse lorsque les niveaux de calcium sont élevés, et en augmentant l’excrétion rénale de calcium.
Des symptômes au diagnostic
Les symptômes de l’hypocalcémie sont corrélés à son mode d’installation (l’hypocalcémie chronique étant mieux tolérée du fait d’une évolution lente) ainsi qu’à la profondeur de l’hypocalcémie (tableau).
Hypocalcémie d’installation aiguë
Lorsque l’hypocalcémie survient rapidement, les symptômes peuvent être sévères et nécessiter une intervention médicale urgente :
- spasmes musculaires et crampes (contractions involontaires et douloureuses, souvent au niveau des membres ou du visage) ;
- tétanie (spasmes musculaires soutenus et mouvements involontaires, souvent observés au niveau des mains [main d’accoucheur]) ;
- paresthésies (généralement autour des lèvres, dans les doigts ou les orteils) ;
- signes neurologiques (confusion, agitation, voire convulsions) ;
- allongement de l’intervalle QT (risque de torsades de pointe).
Hypocalcémie d’installation chronique
Dans le cas d’une hypocalcémie chronique, les signes sont moins francs mais peuvent affecter la qualité de vie du patient :
- fatigue et faiblesse musculaire, sans raison apparente ;
- douleurs osseuses ;
- signes cutanés (xérose) ;
- troubles dentaires (caries, problèmes de développement dentaire chez l’enfant).
Enquête étiologique
Les troubles responsables d’une hypocalcémie peuvent être classés en deux grandes catégories selon qu’ils sont, ou non, liés à l’action de la PTH.
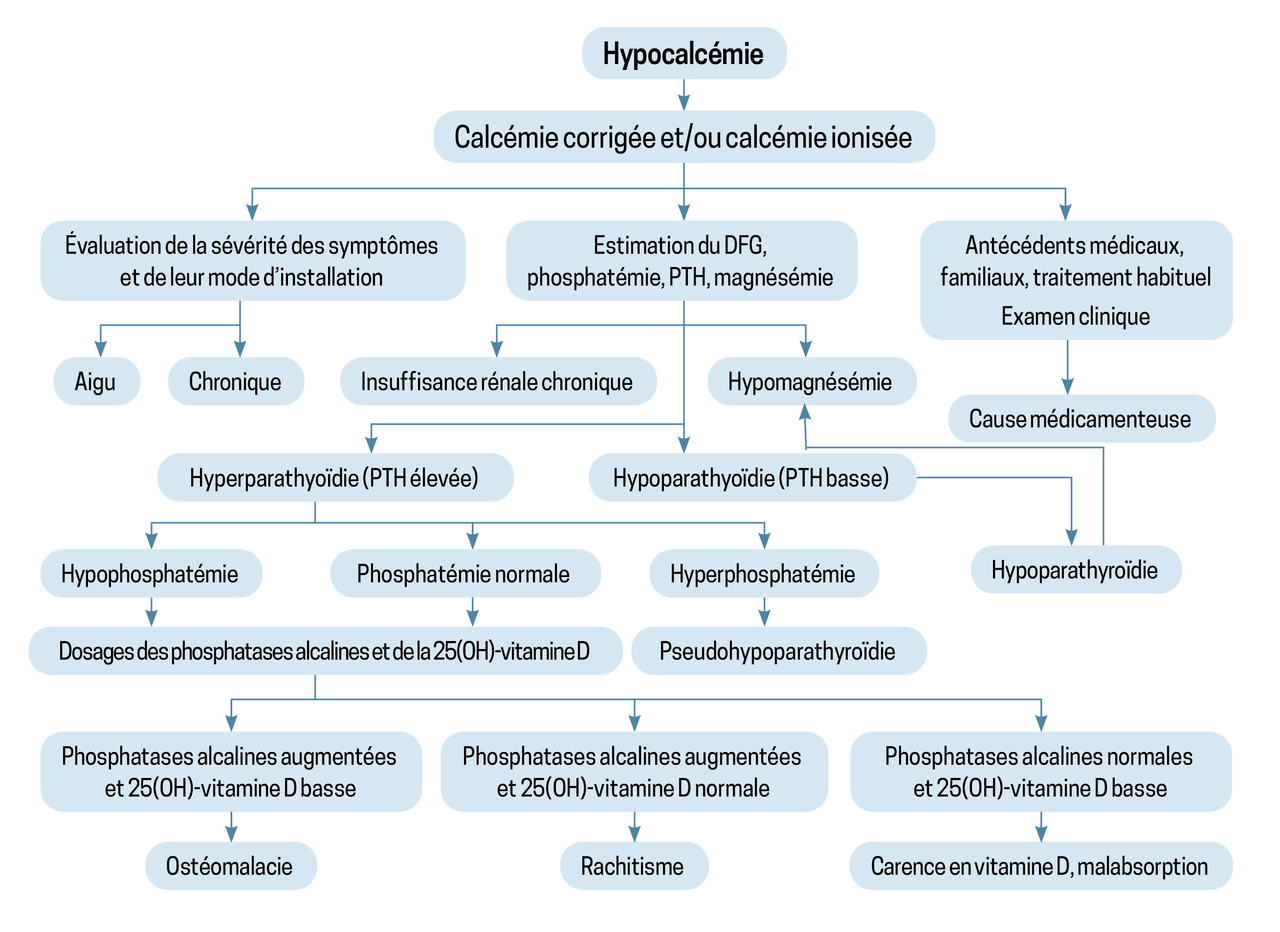
Un arbre diagnostique de l’hypocalcémie est proposé dans la figure.
Causes liées à l’action de la PTH
Les causes associées à la PTH découlent d’un dysfonctionnement des glandes parathyroïdiennes, entraînant une production insuffisante ou nulle de cette hormone.
Hypoparathyroïdie
Rare – la prévalence est de 5,3 à 37 cas pour 100 000 personnes par an –, l’hypoparathyroïdie est souvent d’origine chirurgicale. Elle peut être temporaire ou devenir permanente si elle persiste au-delà de six mois. La surveillance précoce des niveaux de calcium et de PTH après une chirurgie cervicale est utile afin de prédire le risque d’hypoparathyroïdie permanente. Sa fréquence après une intervention chirurgicale varie entre 1,4 et 22 cas pour 100 000 personnes par an. Les formes d’origine non chirurgicale sont encore moins fréquentes (1,3 à 2,3 pour 100 000 personnes par an).
Dysmagnésémie
L’hypomagnésémie, relativement fréquente, inhibe la sécrétion de PTH via la stimulation du récepteur sensible au calcium (CaSR).
L’hypermagnésémie est beaucoup plus rare.
Génétiques
Manifestions généralement pédiatriques, elles peuvent toutefois être observées chez l’adulte (syndrome de DiGeorge, mutation du gène PTH ou AIRE, responsable d’un syndrome auto-immun appelé APECED [autoimmune polyendocrinopathy candidiasis ectodermal dystrophy]).
Les mutations activatrices du CaSR sont, quant à elles, associées à une calcémie et une PTH basses et une calciurie anormalement élevée.
Causes infiltratives ou dégénératives
Dépôts de fer, de cuivre, infiltration parathyroïdienne tumorale, séquelles d’irradiation sont aussi potentiellement en cause.
Hypocalcémie non liée à la PTH
Les causes non liées à la PTH impliquent d’autres organes, tels que les reins, le foie, le squelette ou l’intestin, ainsi que des anomalies du métabolisme de la vitamine D, souvent accompagnées d’une augmentation compensatoire des taux de PTH.
Iatrogénie et carences
L’hypocalcémie liée à des médicaments est courante. Elle peut être provoquée par des diurétiques (favorisant l’excrétion du calcium), des anticonvulsivants (modifiant le métabolisme de la vitamine D) ou des inhibiteurs de la résorption osseuse comme les bisphosphonates et le dénosumab.
Une carence sévère en vitamine D, souvent due à des troubles d’absorption, comme la maladie cœliaque, ou après une chirurgie bariatrique, est également fréquente et s’accompagne souvent d’une hypophosphatémie et d’une hyperparathyroïdie secondaire. Cette carence peut aussi être en lien avec une production insuffisante de calcitriol secondaire à une insuffisance rénale.
Pseudohypoparathyroïdie
La pseudohypoparathyroïdie, autre cause rare, résulte d’une résistance des tissus à l’action de la PTH, caractérisée par des niveaux élevés de cette hormone, une hypocalcémie et une hyperphosphatémie.
Axe PTH-vitamine D
Des déséquilibres dans l’axe PTH-vitamine D peuvent survenir lors de pathologies graves, après une intervention chirurgicale majeure ou au cours d’une pancréatite aiguë, où le calcium se lie aux acides gras pour former des savons.
Comment traiter ?
Hypocalcémie aiguë
L’hypocalcémie aiguë peut être efficacement traitée par perfusion de calcium sous surveillance électrocardiographique.
Hypocalcémie chronique
La prise en charge à long terme de l’hypocalcémie vise à contrôler les symptômes tout en limitant les complications ; le but n’est pas de normaliser la calcémie. La gestion à long terme vise à prévenir l’hypercalciurie et à maintenir le produit calcium-phosphate en deçà de 55 mg²/dL² (4,4 mmol²/L²) afin d’éviter des complications comme la néphrolithiase et les calcifications extrasquelettiques. Des bilans biochimiques de surveillance tous les six mois sont recommandés.
La supplémentation en calcium et vitamine D3 réduit le risque d’hypocalcémie, notamment après une chirurgie thyroïdienne. Un apport alimentaire en calcium d’au moins 1 g/j est recommandé, mais souvent insuffisant chez les patients hypoparathyroïdiens, nécessitant une supplémentation orale (1 à 3 g/j en 3 ou 4 prises). Le citrate de calcium offre une meilleure absorption que le carbonate de calcium, surtout en cas d’achlorhydrie.
En cas d’hypomagnésémie associée, un supplément en magnésium est indiqué.
Le calcitriol (0,25 à 2 μg/j) et les diurétiques thiazidiques peuvent être ajoutés pour réduire l’excrétion urinaire de calcium (inférieure à 4 mg/kg/j).
Le cholécalciférol est conseillé en cas de carence en 25(OH)-vitamine D.
Formes graves et ou réfractaires
Les peptides de PTH (tériparatide et rhPTH[1 - 84]) sont utilisés chez les patients résistants au traitement conventionnel. Ces traitements réduisent les besoins en calcium et calcitriol tout en améliorant la qualité de vie, mais leur coût élevé les fait réserver aux patients avec hypocalcémie réfractaire, hypercalciurie ou risque de néphrolithiase. Le tériparatide a montré une efficacité à long terme, notamment chez les enfants avec hypoparathyroïdie génétique, mais nécessite une administration biquotidienne.
Les futurs développements thérapeutiques, notamment les médicaments à libération prolongée, pourraient transformer la prise en charge de l’hypocalcémie chronique.
Pepe J, Colangelo L, Biamonte F, et al. Diagnosis and management of hypocalcemia. Endocrine 2020;69(3):485-95.