La radiologie et l’imagerie médicale ont directement contribué à une profonde révolution dans les soins depuis leur découverte par Wilhelm Röntgen en 1895 et leurs premières applications en soins.1 Permettant de voir l’invisible, de concrétiser par des nuances « photographiques » des anomalies existantes mais cliniquement peu perceptibles, la radiologie a permis une transformation des stratégies diagnostiques, et plus encore aujourd’hui, le développement d’outils de traitement personnalisés mini-invasifs grâce à la radiologie interventionnelle.
La révolution numérique issue des développements informatiques de la fin des années 1970 et du début des années 1980 a encore accéléré ces développements. Le déploiement large des imageries de coupes, d’abord échographiques, puis tomodensitométriques (scanner), et enfin l’imagerie par résonance magnétique (IRM), a transformé les nuances « photographiques » en représentation des anomalies cliniques par des éléments d’information individuels, les voxels.
Et c’est désormais la nouvelle accélération digitale qui vient percuter ces développements technologiques, transformant les densités et signaux radiologiques en informations numériques digitalisées, que les outils algorithmiques appuyés par la génération de nouveaux réseaux de neurones – technologies d’intelligence artificielle – permettent d’optimiser, de décoder et d’améliorer. Il devient ainsi possible de voir « au-delà de l’image », en permettant une représentation numérique d’anomalies, étendant le champ de la radiologie vers le pronostic, la prédiction, et demain la prévention.
C’est dans ce champ scientifique nouveau, permis par le développement conjoint des outils informatiques et des technologies de l’imagerie médicale, appuyé par un besoin croissant de médecine personnalisée, prédictive et désormais préventive, que l’imagerie d’opportunité émerge. Promettant d’utiliser des données d’imagerie déjà acquises, pour permettre en un seul temps d’apprécier l’état de santé « globale » d’un patient, de prédire son devenir, elle fait entrevoir les développements toujours plus avancés des outils de la radiologie et de l’imagerie médicale pour l’amélioration des soins des patients et des populations.
Pour autant, ces stratégies d’imagerie d’opportunité posent question. Peut-on tout prédire ? Doit-on tout prédire ? Est-on en capacité de tout prédire ?
Principes de l’analyse des examens radiologiques par les médecins radiologues : que cherche-t-on dans l’image ?
Les actes de radiologie diagnostique, au cœur du métier de chaque médecin radiologue, reposent sur une suite de conduites indissociables combinant :
- l’analyse et la validation d’une prescription d’examen radiologique ;
- l’adaptation d’un acte radiologique à cette demande précise ainsi qu’aux informations recueillies en amont de sa réalisation ;
- la mise en œuvre d’un protocole d’acquisition adapté à la réponse attendue ;
- l’analyse des résultats et leur interprétation ;
- l’information directe du patient, son orientation vers une conduite à tenir et son suivi.
Chacune de ces étapes est sous-tendue par un principe de justification d’un acte radiologique directement relié à une question clinique précise, s’accompagnant de l’utilisation de rayonnements ionisants limités au strict nécessaire au bénéfice de la diminution des risques.
Dans ce cadre, comment positionner l’imagerie d’opportunité ?
L’imagerie d’opportunité se distingue d’abord d’une stratégie diagnostique finaliste telle qu’exposée plus haut, dès lors que les informations qui en sont attendues diffèrent de l’objectif initial de l’examen de radiologie conduit. En effet, il est maintenant accepté de définir l’imagerie d’opportunité comme l’obtention de données qualitatives ou quantitatives, recueillies de manière intentionnelle, mais qui sont sans lien avec l’objectif initial de l’examen d’imagerie.2
En ce sens, l’imagerie d’opportunité se distingue d’une stratégie de dépistage organisée, qui impose la réalisation de manière délibérée d’un examen d’imagerie, dont la finalité est justement de pouvoir détecter une maladie suspectée et de justifier l’acte réalisé.
Par ailleurs, l’imagerie d’opportunité se distingue de l’« incidentalome », néologisme initialement rapporté dans les années 1980, avec l’émergence des techniques de scanner3, qui décrivait la découverte fortuite ou secondaire d’une maladie lors d’un examen radiologique, nécessitant une prise en charge spécifique mais qui n’était pas anticipée sur la demande radiologique. Ainsi, la découverte d’un anévrisme aortique significatif sur un scanner abdominal réalisé pour la recherche de calcul du rein constitue un incidentalome. Sa découverte n’était pas attendue mais n’a pas fait non plus l’objet d’une recherche intentionnelle. Ainsi l’incidentalome dépend du « hasard des découvertes » tandis que l’imagerie d’opportunité constitue une recherche systématique de paramètres prédictifs de facteurs de risque, voire de maladies, sur un examen dont la justification ne reposait pas sur leur identification.
Quelles sont les applications actuelles de l’imagerie d’opportunité ?
La plupart des biomarqueurs d’imagerie d’opportunité visent à mieux prédire le devenir en santé d’un sujet par l’extraction d’un paramètre généralement quantitatif. Les données actuellement publiées dans la littérature sur ce sujet sont généralement dérivées d’acquisitions scanographiques.
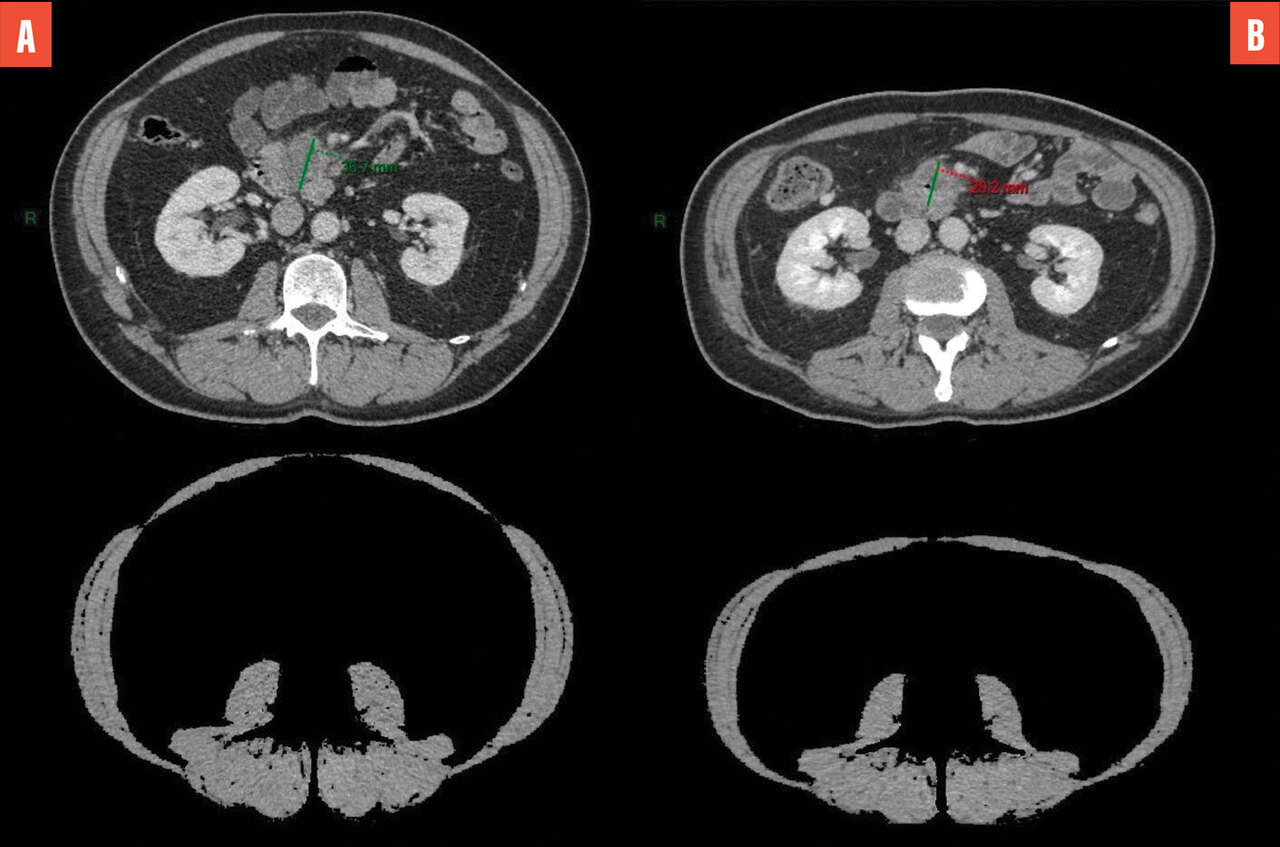
Les objectifs visés sont importants, consistant à optimiser la prédiction de la mortalité, de la morbidité, parfois l’apparition de lésions cancéreuses.2 De manière schématique, l’imagerie d’opportunité concerne principalement aujourd’hui les marqueurs de la maladie cardiovasculaire, les marqueurs d’ostéoporose et les marqueurs liés à la sarcopénie (figure). L’évaluation de la masse musculaire globale et l’identification « opportune » sur le scanner d’une potentielle sarcopénie permettent de prédire des évolutions péjoratives, notamment en cancérologie, indépendamment des traitements conduits.4,5 Dans une étude parue en 2023, les équipes de Pickhardt et al. ont rapporté leur expérience sur l’analyse rétrospective de 9 223 dossiers de patients ayant bénéficié d’un scanner abdominal et de l’extraction opportune de biomarqueurs quantitatifs (quantification des muscles en projection de L3, quantification de la graisse abdominale en L3 et quantification automatique du score de calcification de l’aorte abdominale).6 L’atténuation musculaire en L3 et la quantification des calcifications aortiques présentaient les meilleures performances pour prédire la survenue d’un décès dans les dix ans, avec un AUC (area under the curve ou aire sous la courbe) de 0,76 chez les hommes et de 0,72 chez les femmes, concernant l’atténuation musculaire.6
De la même façon, il est également possible d’identifier, de manière opportune, des sujets à risque de syndrome métabolique en utilisant des données extraites de scanners.7
Reste que les données médico-économiques disponibles pour apprécier la pertinence de ces stratégies d’imagerie d’opportunité sont peu nombreuses à ce jour.8 Si une première étude de modélisation semble montrer un rapport coût/efficacité important, et si cette approche d’imagerie d’opportunité pourrait être attendue également par les médecins de premier recours, comme le suggère une étude récente parue en 2024,9 une intégration prospective dans des stratégies de prévention reste à conduire ; des initiatives régionales sont en cours.
Quels enjeux pour l’imagerie d’opportunité ?
Avec environ 1 200 appareils de scanners disponibles sur le territoire français, la quantité d’informations disponibles qui pourraient faire l’objet d’une analyse « d’opportunité » est considérable. Mais cette stratégie de détection volontaire, par le médecin radiologue en charge d’analyser les images, d’anomalies prédictives d’une évolution d’un état de santé, ou de l’apparition d’un cancer, voire de la survenue d’un décès, n’est pas sans interroger.
Doit-on tout savoir dès lors que l’on passe un examen d’imagerie justifié par une indication clinique cadrée, dont le résultat attendu n’implique pas nécessairement des conséquences sur le devenir à long terme ?
Cette question est essentielle. Nos collègues spécialistes de la génétique médicale, confrontés depuis plusieurs années au potentiel du séquençage génomique complet, ont proposé plusieurs recommandations, qu’il devrait être possible d’adapter au domaine de l’imagerie d’opportunité. Le Collège américain de génomique et de médecine génétique (ACMG) a récemment recommandé que, lors de tout séquençage de génome ou d’exome réalisé, quelle qu’en soit l’indication, un nombre prédéfini de variants génomiques puissent être automatiquement et systématiquement détectés.10,11 Cette approche de détection automatique, complémentaire, d’anomalies génétiques, découvertes alors que le test génétique initial ne concernait pas la maladie potentiellement détectée ou le facteur de risque prédit, rejoint l’approche d’imagerie d’opportunité. La Société française de médecine prédictive et personnalisée (SFMPP) a ainsi défini des découvertes secondaires (SF) comme devant être systématiquement recherchées.12 Toutefois, cette recommandation concerne des gènes particuliers, reliés à des formes spécifiques de cancers de l’adulte. Par ailleurs, la SFMPP a insisté sur le nécessaire processus d’information et de consentement des patients, indispensables avant de conduire ces tests secondaires. Ainsi, il est convenu que ces tests ne doivent s’imposer que s’il existe également des stratégies préventives ou thérapeutiques qui permettent d’en limiter l’impact.
Ces problématiques doivent inspirer le secteur de la radiologie. L’application de l’imagerie d’opportunité ne saurait concerner des maladies pour lesquelles aucune perspective thérapeutique, aucune stratégie de réduction du risque par une approche préventive, n’existerait. En ce sens, une imagerie d’opportunité visant à prédire des troubles cognitifs, sans stratégie thérapeutique ultérieure, doit interroger. Le second point majeur soulevé par la génétique médicale concerne l’information au patient : la recherche d’anomalies génétiques secondaires est soumise à l’autorisation de réaliser cette analyse, complétée par une seconde autorisation de partager les résultats ensuite. Cette approche pourrait-elle s’imposer dans le domaine de la radiologie ? On pourrait imaginer que, sur le consentement de réaliser un acte de radiologie diagnostique pour exclure ou rechercher un diagnostic d’appendicite, soit mentionné que l’examen pourra fournir des paramètres quantitatifs concernant les facteurs de risque cardiovasculaire, ou les facteurs de risque fracturaire, par exemple. Mais ces résultats ne seraient rendus et restitués dans le compte-rendu que lorsque le patient lui-même consentirait, une deuxième fois, à recevoir ces résultats.
Équité ou médecine sélective ?
L’imagerie d’opportunité interroge également sur son intégration dans une dimension plus large, préventive, de la radiologie. Un dépistage organisé s’applique à une population sélectionnée, délibérément incluse dans un programme visant à détecter une anomalie précise. L’imagerie d’opportunité s’applique à une population par essence non définie mais exposée à un examen d’imagerie pour des raisons très variables. Dès lors, l’imagerie d’opportunité ne concerne plus une population définie par avance, ni une population invitée à en bénéficier. Par ailleurs et en conséquence, la prévalence des anomalies attendues par la mesure des paramètres quantitatifs de l’imagerie d’opportunité varie probablement davantage qu’au sein d’un programme de dépistage organisé. Cette prévalence variable des anomalies paramétriques observées implique nécessairement un taux non nul de « faux positifs », pouvant conduire à des explorations complémentaires, voire à des actes invasifs significatifs réalisés chez des patients indemnes de toute anomalie. Aussi est-il sans doute important de bien définir, dans le déploiement de l’imagerie d’opportunité, si celle-ci vise effectivement à s’intégrer dans des stratégies de prévention primaire, à cibler des populations qui seraient pertinentes pour en recevoir l’application, sur des critères d’âge ou sur des scores composites cliniques ou biologiques. La combinaison des informations numériques issues du dossier numérique patient – diabète, facteurs de risque cardiovasculaire, mode de vie – avec des éléments de l’anamnèse pourrait utilement être intégrée à des analyses algorithmiques, pour préciser s’il est opportun d’appliquer une extraction des paramètres quantitatifs d’imagerie. Le rôle des médecins référents, de proximité, impliqués dans les stratégies de prévention sera déterminant pour travailler de concert avec les radiologues afin d’expliquer, ensemble ou de manière asynchrone, les attendus des données d’opportunité extraites.
Il n’en demeure pas moins que les moyens qui seront mis en œuvre pour déployer cette imagerie d’opportunité devront être importants. Aujourd’hui, les modes de financement des logiciels qui seraient dans la plupart des cas nécessaires pour en réaliser l’analyse systématique ne sont pas connus.
Par ailleurs, chacun doit s’interroger sur les bénéficiaires directs de cette stratégie. S’agit-il finalement d’optimiser encore l’état de santé d’une population éclairée, informée, comprenant les enjeux de cette approche, insérée dans un circuit de soins, et pour laquelle le gain en matière de santé est plus limité que pour des populations qui restent encore éloignées des circuits de soins, et qui ne bénéficieront pas de l’ensemble de ces informations, vis-à-vis desquelles la connaissance et le consentement sont indispensables ?
L’impact de cette imagerie d’opportunité, à la fois à titre individuel, physique et psychologique mais également sociétal, reste inconnu. Beaucoup d’entre nous, radiologues, considérons que l’absence d’accès à des dépistages précoces de maladies doit être combattue. Il en va d’un enjeu de justice ou d’équité, comme rappelé récemment par une enquête sur la détection précoce de cancers de la prostate.13 Il n’en demeure pas moins que l’irruption d’un test positif dans une vie constitue une perturbation existentielle majeure, potentielle bascule d’un citoyen vers un parcours de soins où il devient patient. Ceci doit renforcer encore la nécessité d’une information a priori, et plus encore nous porter à vouloir déployer un programme de formation éducationnelle en population générale, pour s’approprier les enjeux scientifiques des préventions, pour lesquelles ces nouveaux outils sont désormais accessibles.
Par ailleurs, la garantie apportée à la protection des données numériques et, dans ce cas, aux données d’imagerie apparaît encore plus importante. Si les images contiennent des éléments pronostiques individuels, il faut en assurer la pleine sécurité, dans le respect du règlement général sur la protection des données (RGPD), afin de veiller à l’absence d’utilisations commerciales ou assurantielles non souhaitées de ces éléments.
Enfin, les professionnels de la radiologie, au premier rang desquels les radiologues, devront s’interroger sur le nécessaire engagement qu’ils devront avoir dans cette nouvelle ère préventive et prédictive. Cet engagement sera sans aucun doute encore plus fort dans les échanges directs avec les patients, en amont et après les examens radiologiques, mais également dans les soins, car la charge de travail augmentera de manière inéluctable malgré les promesses d’outils numériques et d’intelligence artificielle, promesses rarement tenues, en matière de temps médical rendu aux soignants.
Avancée considérable dans un cadre éthique à définir
L’imagerie d’opportunité constitue une avancée considérable, permise par le développement d’outils numériques et la capacité d’analyses informatiques. Les données actuelles permettent de penser que ces paramètres quantitatifs constituent des biomarqueurs importants dans la prédiction de la bonne santé, l’identification de facteurs de risque, la prédiction d’évolution vers des cancers, voire le développement d’une morbi-mortalité dans un parcours de soins.
Les préoccupations éthiques ouvertes par ce nouveau champ de la radiologie rejoignent celles déjà connues des médecins généticiens qui, par la détection d’anomalies génétiques insoupçonnées, ont pu permettre de prévenir l’apparition ou le développement de maladies cancéreuses. Mais, en phase avec les attendus du Comité consultatif national d’éthique du numérique, le contrôle humain à toutes les étapes du déploiement de cette imagerie d’opportunité doit également être constant : choix des populations ou des individus cibles, modes d’information, restitution de l’information, garantie d’un parcours de soins accompagné après la remise ou la transmission de l’information sur les biomarqueurs. Ces étapes sont essentielles pour assurer l’acceptabilité et le suivi de ces nouveaux outils et pour en garantir la bonne utilisation à des fins de bénéfice individuel direct pour chaque citoyen.
2. Pickhardt PJ, Summers RM, Garrett JW, et al. Opportunistic screening: Radiology scientific expert panel. Radiology 2023;307(5):e222044.
3. Berland LL, Silverman SG, Gore RM, et al. Managing incidental findings on abdominal CT: White paper of the ACR incidental findings committee. J Am Coll Radiol 2010;7:754-73.
4. Raynard B, Pigneur F, Di Palma M, et al. The prevalence of CT-defined low skeletal muscle mass in patients with metastatic cancer: a cross-sectional multicenter French study (the SCAN study). Support Care Cancer 2022;30:3119-29.
5. Parent P, Pigneur F, Hilmi M, et al. Muscle loss during first-line chemotherapy impairs survival in advanced pancreatic cancer despite adapted physical activity. J Cachexia Sarcopenia Muscle 2025;16:e13595.
6. Lee MH, Zea R, Garrett JW, et al. Abdominal CT body composition thresholds using automated AI tools for predicting 10-year adverse outcomes. Radiology 2023;306:e220574.
7. Pickhardt PJ, Graffy PM, Perez AA, et al. Opportunistic screening at abdominal CT: Use of automated body composition biomarkers for added cardiometabolic value. Radiographics 2021;41:524-42.
8. Pickhardt PJ, Correale L, Hassan C. AI-based opportunistic CT screening of incidental cardiovascular disease, osteoporosis, and sarcopenia: Cost-effectiveness analysis. Abdom Radiol (NY) 2023;48:1181-98.
9. Eltorai AEM, McKinney SE, Rockenbach MABC, et al. Primary care provider perspectives on the value of opportunistic CT screening. Clin Imaging 2024;112:110210.
10. Berg JS, Amendola LM, Eng C, et al. Processes and preliminary outputs for identification of actionable genes as incidental findings in genomic sequence data in the Clinical Sequencing Exploratory Research Consortium. Genet Med 2013;15:860-7.
11. Burke W, Antommaria AHM, Bennett R, et al. Recommendations for returning genomic incidental findings? We need to talk! Genet Med 2013;15:854-9.
12. Pujol P, Vande Perre P, Faivre L, et al. Guidelines for reporting secondary findings of genome sequencing in cancer genes: the SFMPP recommendations. Eur J Hum Genet 2018;26:1732-42.
13. Gellerstedt L, Langius-Eklöf A, Kelmendi N, et al. Men’s experiences of receiving a prostate cancer diagnosis after opportunistic screening-A qualitative descriptive secondary analysis. Health Expect 2022;25:2485-91.
Dans cet article
- Principes de l’analyse des examens radiologiques par les médecins radiologues : que cherche-t-on dans l’image ?
- Quelles sont les applications actuelles de l’imagerie d’opportunité ?
- Quels enjeux pour l’imagerie d’opportunité ?
- Équité ou médecine sélective ?
- Avancée considérable dans un cadre éthique à définir