Les mycoses invasives de la sphère ORL sont des pathologies rares mais graves qui touchent essentiellement les patients immunodéprimés et dans certains cas les patients diabétiques. Ces infections s’observent dans deux localisations : sinusiennes et otologiques, toutes deux pouvant ensuite se propager par contiguïté et s’étendre notamment à la base du crâne.
Sinusites fongiques invasives
Les rhinosinusites fongiques sont classées selon des critères cliniques, radiologiques et anatomopathologiques. On différencie, d’une part, les infections aiguës (évoluant depuis moins de quatre semaines) des infections chroniques (plus de douze semaines d’évolution) et, d’autre part, les infections non invasives (balle fongique ou aspergillome, et sinusite fongique allergique) des infections invasives (sinusites fongiques aiguës invasives et sinusites fongiques chroniques, granulomateuses ou non). Le caractère invasif est défini par la présence d’une invasion de la muqueuse, parfois étendue à l’os et aux tissus mous des régions adjacentes.1
Les sinusites fongiques invasives surviennent essentiellement chez le patient immunodéprimé. Les principaux agents retrouvés sont Aspergillus sp. chez les patients atteints d’hémopathies, et Mucorales chez les patients diabétiques, mais d’autres pathogènes sont possibles, notamment Fusarium sp., Scedosporium sp. ou Alternaria sp.
Sinusites fongiques aiguës invasives à Aspergillus
Aspergillus sp. est un champignon filamenteux ubiquitaire présent dans l’environnement tellurique. La contamination se fait par voie aérienne, par inhalation de spores, dont l’aérosolisation peut être favorisée par la présence de travaux ou de plantes dans l’environnement du patient. Il est normalement éliminé par les défenses immunitaires, mais en cas de baisse de l’immunité, et notamment de neutropénie, Aspergillus peut envahir les muqueuses, puis les vaisseaux et les organes adjacents.
En France, Aspergillus fumigatus est le plus souvent en cause dans les sinusites fongiques invasives devant Aspergillus niger et Aspergillus flavus.2
Du fait de la neutropénie profonde fréquemment présente chez les patients atteints de sinusite fongique invasive aspergillaire, le tableau clinique est peu symptomatique. Dans ce contexte, tout symptôme rhinosinusien, comme une épistaxis unilatérale, une douleur, une obstruction nasale ou encore une fièvre inexpliquée survenant sur un terrain immunodéprimé, doit conduire à un examen ORL et à la réalisation d’une imagerie sinusienne.
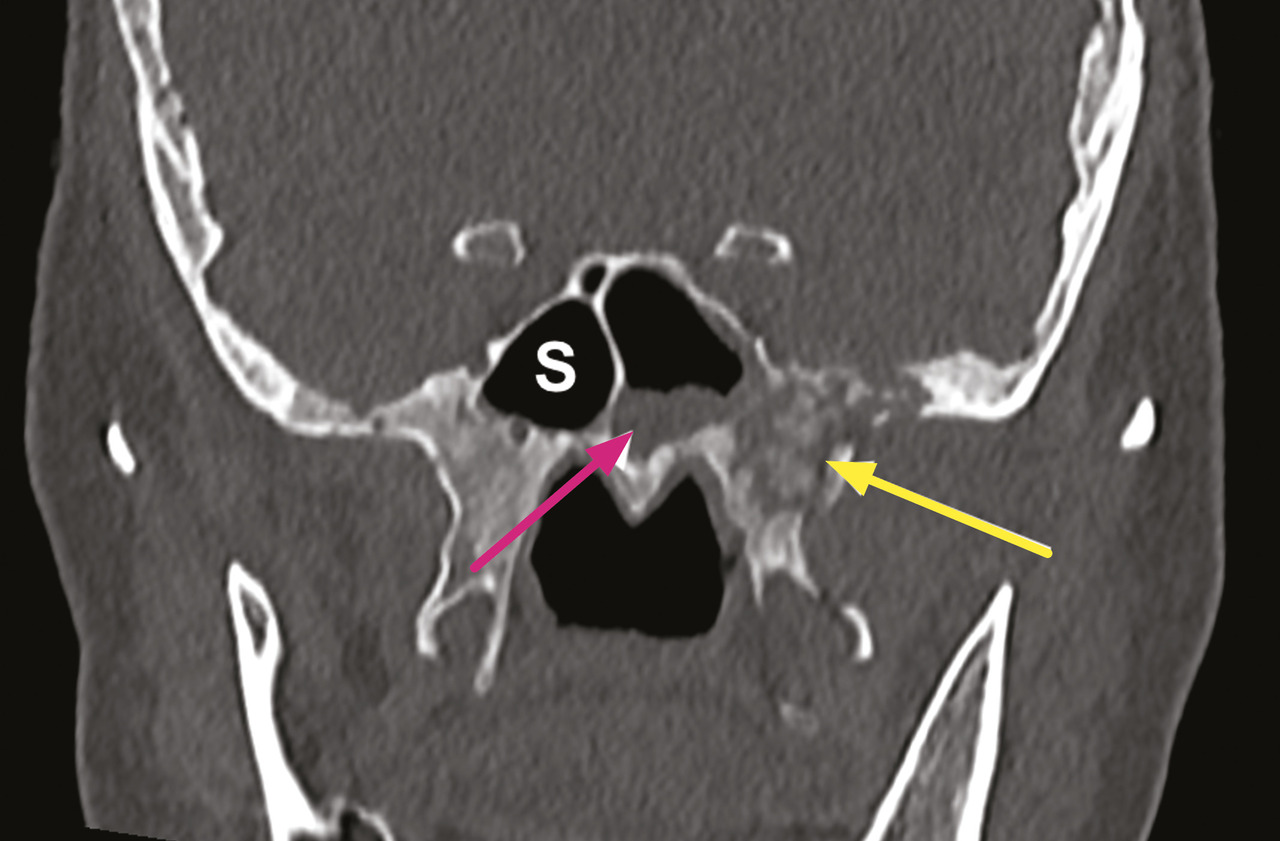
Le diagnostic d’aspergillose pulmonaire doit également faire pratiquer une imagerie sinusienne dans le bilan d’extension. L’examen d’imagerie de première intention est le scanner, qui met en évidence un épaississement muqueux sinusien associé à une ostéolyse de contact (fig. 1), qui peut cependant être inconstante dans les stades précoces de la maladie.
L’examen endoscopique nasal réalisé par l’ORL permet de rechercher Aspergillus dans les sécrétions prélevées, et surtout dans les biopsies muqueuses réalisées, et d’éliminer une mucormycose. L’antigène galactomannane sérique, marqueur fongique indirect, ou encore la PCR Aspergillus sur prélèvement sanguin ou sur les biopsies peuvent être des outils diagnostiques supplémentaires. En anatomopathologie, on retrouve dans la muqueuse des filaments réguliers, septés, avec des branchements à angle aigu, associés à un infiltrat inflammatoire neutrophile avec nécrose muqueuse. En pratique, l’examen anatomopathologique est indispensable, car il permet bien souvent de confirmer le diagnostic et de signer le caractère invasif.
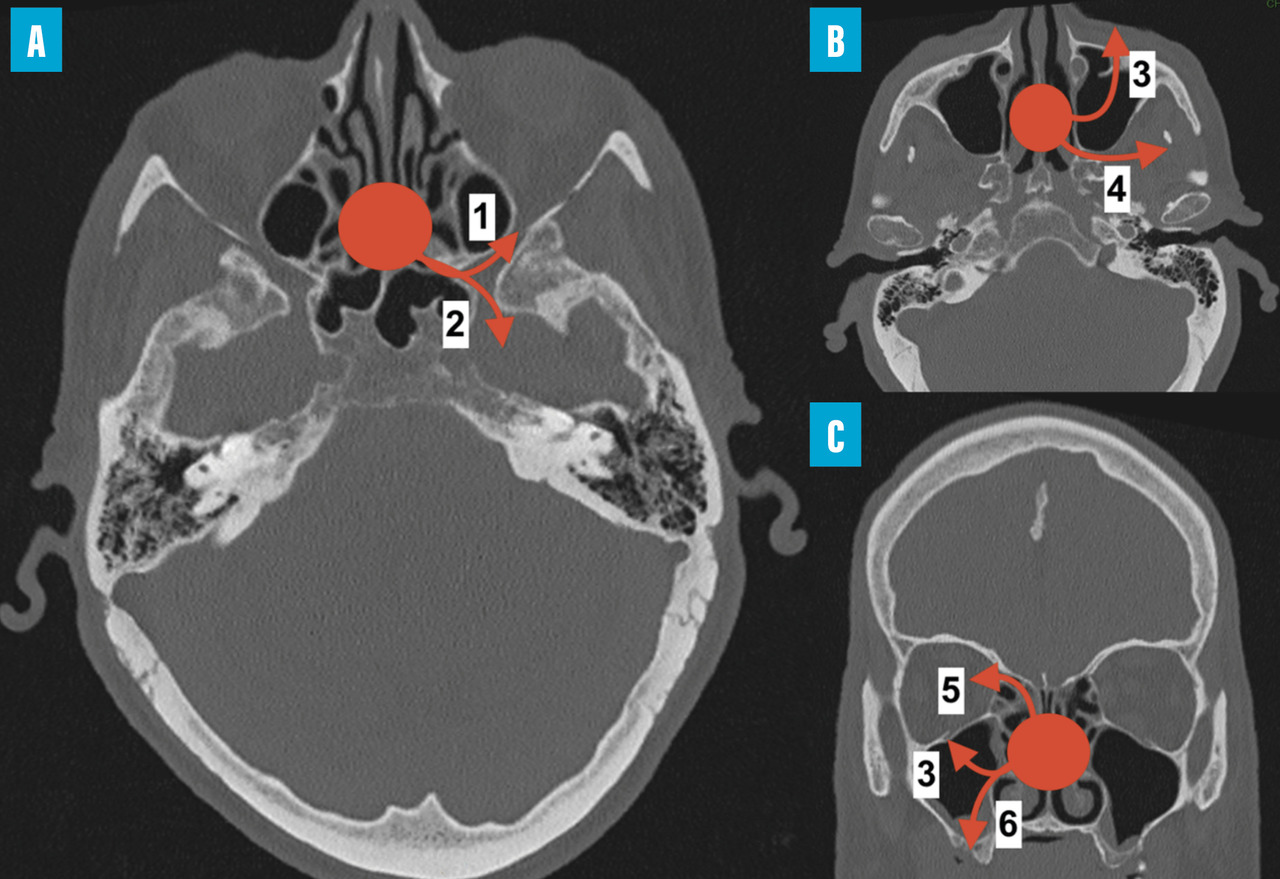
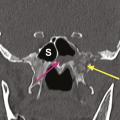
Le bilan comprend une imagerie par résonance magnétique (IRM) pour l’évaluation des tissus mous et une angio-tomodensitométrie (angio-TDM) pour rechercher une atteinte vasculaire. L’évolution de l’infection est en effet marquée par un angiotropisme. L’envahissement du sinus caverneux est une complication fréquente qui peut aboutir à un anévrisme mycotique de la carotide interne. L’envahissement de l’artère sphénopalatine peut entraîner l’invasion de la fosse infratemporale. L’extension depuis l’ethmoïde peut se faire vers l’orbite – induisant baisse d’acuité visuelle, ophtalmoplégie et exophtalmie – et/ou vers le compartiment intra-crânien (fig. 2).
Le traitement de référence est fondé sur certains antifongiques de la famille des azolés, en particulier le voriconazole. La chirurgie est, pour certains, associée au traitement médical, mais son indication et son étendue restent débattues :3 elle est parfois considérée comme un traitement de deuxième ligne à discuter en cas de reliquat persistant après thérapie antifongique prolongée. Une discussion médico-chirurgicale est de toute façon indispensable, initialement et lors du suivi prolongé.
Le pronostic dépend à la fois du terrain et de l’extension des lésions ; il est particulièrement péjoratif en cas d’envahissement intracrânien.
Mucormycoses rhino-orbito-cérébrales
Les Mucorales sont aussi des champignons filamenteux ubiquitaires présents dans l’environnement tellurique. Dans la mucormycose rhino-orbito-cérébrale, l’espèce la plus souvent retrouvée est Rhizopus arrhizus. La contamination se fait par voie aérienne chez un patient immunodéprimé. Il s’agit d’un patient diabétique (deux tiers des cas), ou d’un patient porteur d’une hémopathie maligne (un quart des cas).4
Plusieurs cas de mucormycose rhino-orbito-cérébrale ont aussi été décrits dans le mois suivant une infection par le SARS-CoV- 2, le plus souvent chez des patients diabétiques ayant reçu une corticothérapie.5
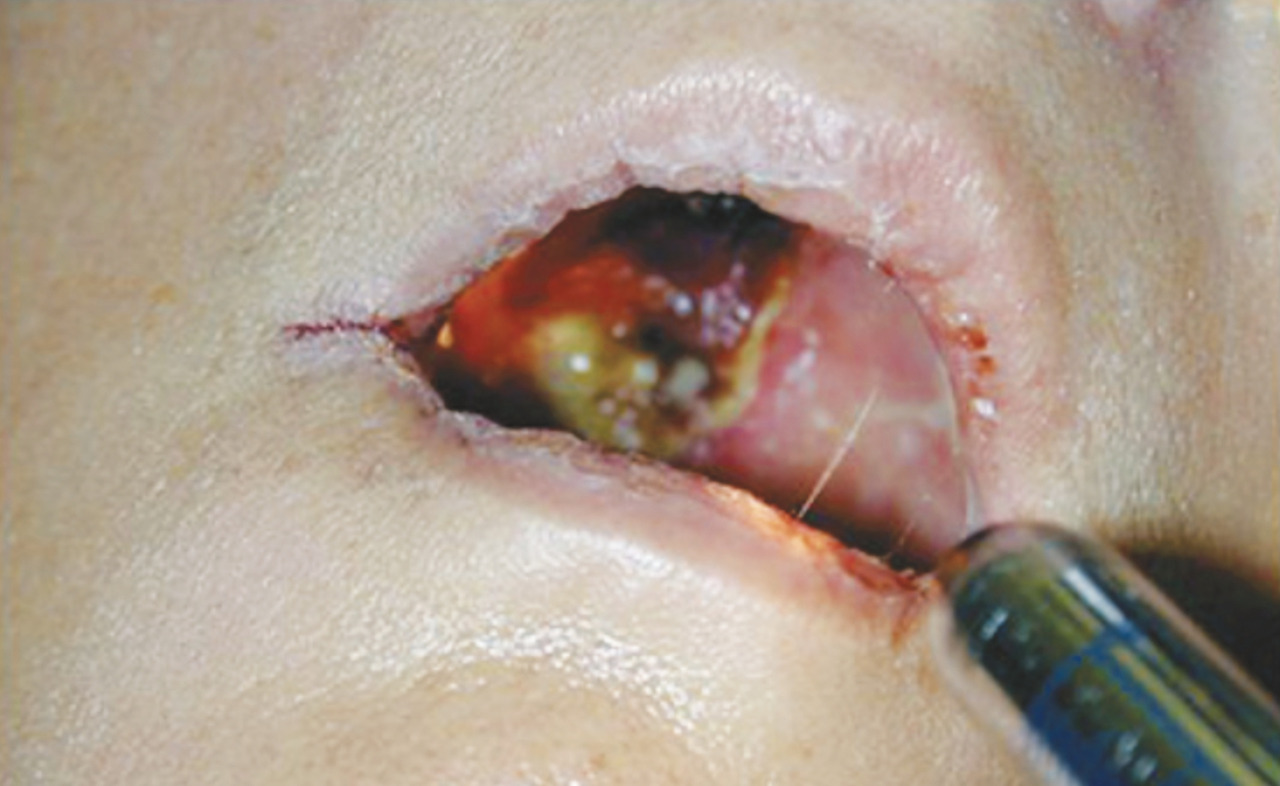
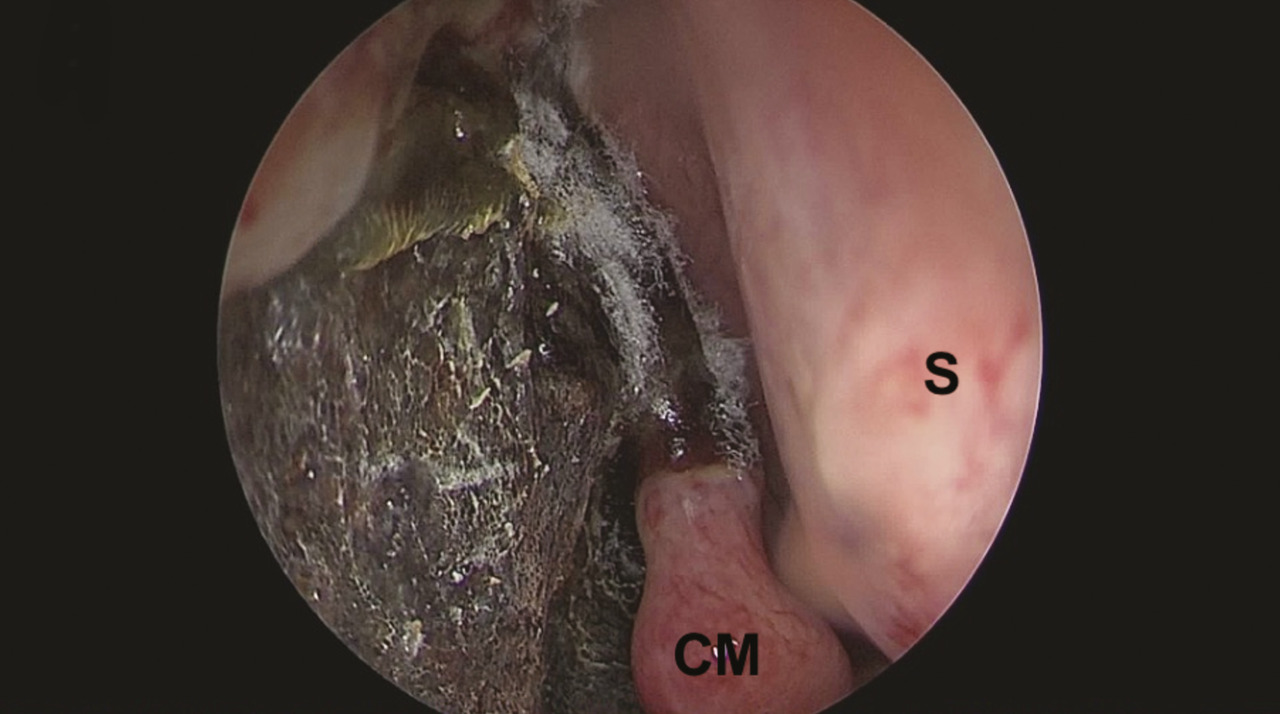
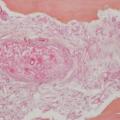
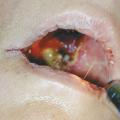
Les premiers symptômes de l’infection sont, là encore, peu spécifiques, marqués par une douleur sinusienne unilatérale associée à une rhinorrhée et/ou une obstruction nasale. L’important angiotropisme des Mucorales entraîne la formation de thrombi intravasculaires extensifs (fig. 3) et peut engendrer par diffusion une nécrose muqueuse intranasale, palatine (fig. 4), cutanée, orbitaire, voire intracrânienne (fig. 2). Une exophtalmie, un chémosis, des troubles de l’oculomotricité et une baisse d’acuité visuelle sont possibles en cas d’atteinte du sinus caverneux ou de l’orbite. L’envahissement de la base du crâne se traduit par des signes neuroméningés.
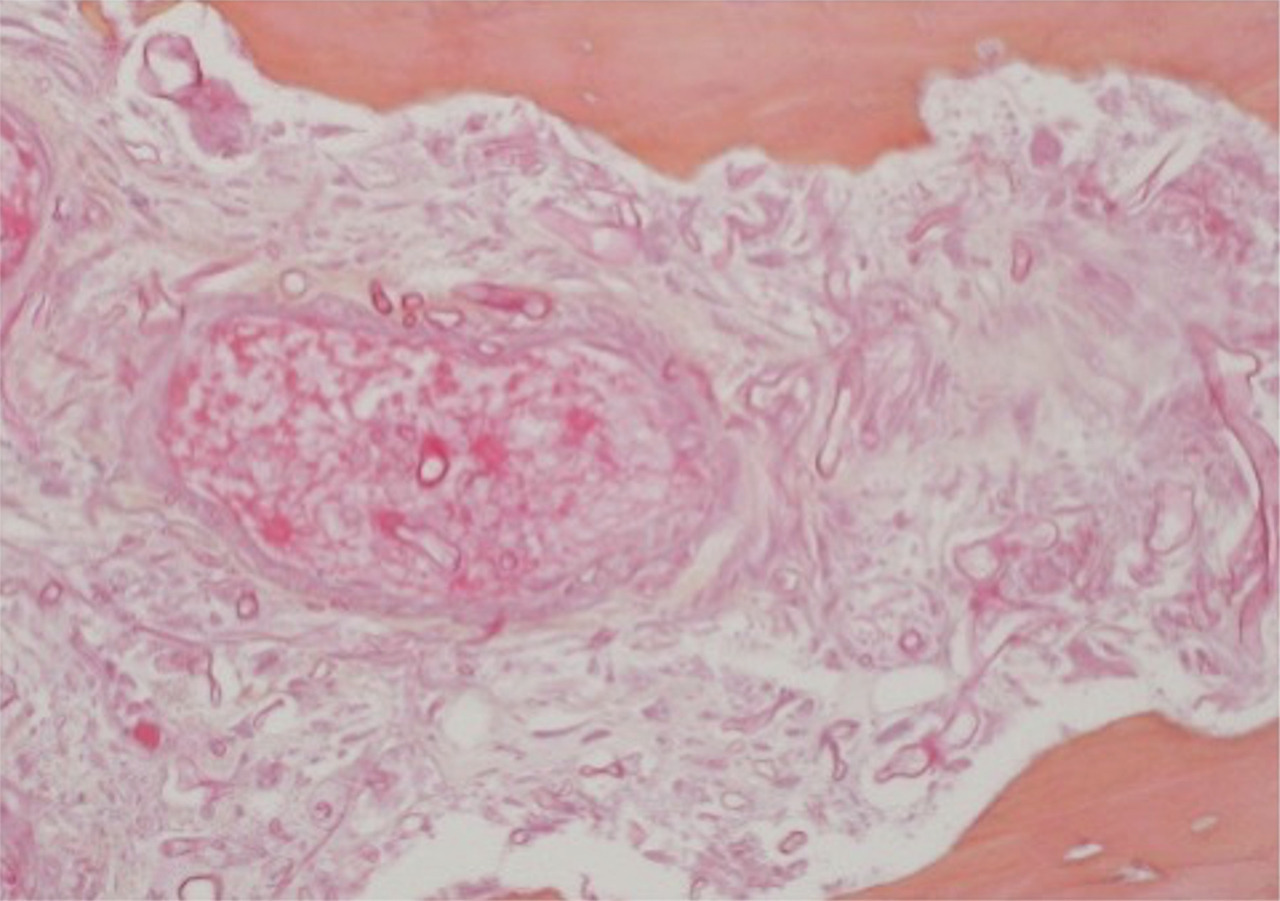
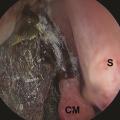
L’examen endoscopique de la fosse nasale doit être réalisé en urgence devant toute suspicion clinique. Il recherche un aspect atone, voire nécrotique, des muqueuses, typique des mucormycoses (fig. 5). Il permet de confirmer le diagnostic, par la réalisation de biopsies pour analyses mycologiques et anatomopathologiques. L’examen direct mycologique réalisé en urgence avec un microscope à fluorescence peut établir le diagnostic en identifiant les filaments mycéliens évocateurs. L’examen anatomopathologique retrouve des filaments larges, non septés, associés à un infiltrat fongique périnerveux, avec une réponse inflammatoire neutrophilique et surtout des images d’angio-invasion fongique avec thrombose et nécrose (fig. 3). La culture mycologique est négative dans plus de la moitié des cas dans une série française.4 La PCR Mucorales sur les biopsies et sur prélèvement sanguin peut être une aide au diagnostic puis dans le suivi.6,7
Les examens d’imagerie (scanner et IRM) peuvent être normaux au début de la pathologie et ne doivent pas retarder l’endoscopie et la prise en charge. Le scanner recherche une lyse osseuse, qui n’est pas systématique, notamment à la phase précoce de l’infection. Injecté, le scanner permet de rechercher une atteinte vasculaire. L’IRM est l’examen de référence pour l’extension locorégionale et le suivi, en permettant une analyse plus fine de l’atteinte de la muqueuse et des tissus mous.
Le traitement est pluridisciplinaire et le plus précoce possible. Il associe un médicament antifongique intraveineux (amphotéricine B liposomale à forte dose en première intention), une correction maximale des facteurs favorisants (en particulier le contrôle du diabète) et un traitement chirurgical élargi, potentiellement répété, permettant l’excision large des tissus nécrosés.8,9 La chirurgie, qui implique parfois des gestes mutilants (exentération, maxillectomie avec sacrifice cutané), doit être discutée de façon collégiale en prenant en compte le terrain et le pronostic général de la pathologie sous-jacente.
Malgré un traitement bien conduit, la mortalité de cette pathologie reste d’environ 40 %. Elle est moindre en cas d’atteinte sinusienne isolée, soulignant l’importance d’un diagnostic précoce.10
Sinusite fongique chronique invasive
Cette entité, rare dans les pays occidentaux, est principalement due à Aspergillus sp. et compliquerait une sinusite chronique non invasive (classiquement l’aspergillome sinusien) chez un patient diabétique mal équilibré ou à l’occasion d’un traitement par corticoïdes, par exemple. Elle est parfois possible chez le patient immunocompétent.
L’évolution est lente, marquée initialement par des symptômes sinusiens non spécifiques : obstruction nasale, douleurs sinusiennes, céphalées, anosmie. À un stade plus avancé, l’infection détruit la paroi muqueuse et osseuse sinusienne et peut envahir l’orbite et le cerveau. Du fait de l’atteinte fréquente de la partie supérieure de l’orbite, le syndrome de l’apex orbitaire est classiquement rattaché à cette pathologie. Il associe une baisse d’acuité visuelle, une exophtalmie, une ophtalmoplégie et une anesthésie du territoire de la branche ophtalmique du nerf trijumeau (V1).
L’imagerie met en évidence une lyse osseuse ethmoïdale et du toit de l’orbite avec un envahissement des tissus de proximité. Le diagnostic repose sur les examens microbiologiques et sur l’analyse histologique des biopsies par endoscopie sinusienne, qui confirme l’envahissement muqueux et osseux par des champignons filamenteux, associé à un infiltrat inflammatoire chronique et une angio-invasion filamenteuse.
Le traitement repose sur le voriconazole en première intention. La place de la chirurgie est discutée et tend à être de plus en plus limitée.11,12
Sinusite fongique chronique granulomateuse
Cette forme de sinusite fongique chronique invasive s’observe chez le patient immunocompétent et est principalement due à Aspergillus flavus. C’est une forme rare en Europe, qui se retrouve surtout dans des zones avec une forte charge fongique aérienne (Moyen-Orient, Afrique du Nord, Inde, Pakistan).
Le tableau clinique est celui d’une sinusite chronique résistante au traitement médical, évoluant sur plusieurs mois, voire plusieurs années, mais restant peu symptomatique, ce qui peut entraîner un retard diagnostique. L’extension se fait progressivement vers l’orbite ou le parenchyme cérébral et induit un déficit neurologique d’aggravation progressive et/ou une exophtalmie, souvent unilatérale.
L’imagerie met en évidence une masse hétérogène pouvant contenir des tonalités calciques en tomodensitométrie, lysant les parois sinusiennes et envahissant les organes de voisinage, notamment l’orbite. Le diagnostic est histologique et retrouve des granulomes sans nécrose caséeuse, associés à une fibrose importante. Les filaments mycéliens sont peu nombreux et s’observent à l’intérieur des cellules géantes ; il n’y a pas d’angio-invasion, contrairement à la forme chronique non granulomateuse.
Le traitement est avant tout médical et prolongé, reposant sur le voriconazole en première intention. La chirurgie est indiquée en cas d’échec du traitement médical, avec une exérèse des tissus mous infectés tout en restant aussi conservatrice que possible.
La mortalité de ces infections est très faible, mais l’évolution est marquée par des récidives fréquentes.13
Otites fongiques invasives
L’otite externe nécrosante (anciennement appelée otite externe maligne) est une infection grave survenant chez le patient immunodéprimé ou, plus souvent, diabétique.14 Elle débute au niveau de la peau du conduit auditif externe puis s’étend à l’os pétreux et à la base du crâne pour donner une ostéomyélite de la base du crâne. Ces otites sont majoritairement bactériennes, causées par Pseudomonas aeruginosa, mais dans environ 10 % des cas elles sont d’origine fongique, le plus souvent dues à Aspergillus flavus.14,15
Le tableau clinique est celui d’une otite externe résistante au traitement local, avec une otalgie au premier plan, volontiers associée dans l’otite externe nécrosante fongique à une atteinte des nerfs crâniens (paralysie faciale, atteinte des nerfs mixtes). L’examen otoscopique retrouve une sténose du conduit auditif externe plus ou moins marquée, avec une otorrhée et parfois un polype du conduit.
L’imagerie permet de confirmer le diagnostic. La TDM met en évidence une lyse osseuse plus ou moins étendue. L’IRM permet l’analyse les tissus mous et recherche notamment une extension vers les fosses crâniennes moyenne et postérieure, ou vers la fosse infratemporale. Une imagerie métabolique (tomographie par émission de positons [TEP-TDM], scintigraphie aux leucocytes marqués) est réalisée à la phase initiale de la prise en charge pour servir de référence et permettre le monitorage de la réponse au traitement.16
Les examens mycologiques et bactériologiques réalisés sur l’otorrhée ou idéalement sur une biopsie permettent le diagnostic étiologique. Ils peuvent nécessiter la réalisation d’une fenêtre thérapeutique avant réalisation de biopsies profondes sous anesthésie générale, guidées par l’imagerie, pour examens microbiologiques et histologiques, notamment en cas de négativité des premiers résultats. Les co-infections sont possibles.
Le traitement repose sur le traitement antifongique par voie systémique adapté au champignon retrouvé, et prolongé pour une durée en règle supérieure à six mois. Une réévaluation fondée sur la clinique, la biologie et l’imagerie métabolique objective la persistance de signes d’activité de l’infection et guide la durée du traitement. La chirurgie n’a pas de place en première intention mais peut parfois être indiquée dans la gestion de certaines complications (décompression du nerf facial, canaloplastie en cas de sténose persistante du conduit auditif externe, etc.).15
Les otites externes nécrosantes fongiques ont un moins bon pronostic que les formes bactériennes et nécessitent un traitement prolongé sous peine de récidive, mais la mortalité de ces infections reste très faible.15
Identifier les formes invasives
Chez les patients avec des symptômes rhinosinusiens ou d’otite, les atteintes invasives d’origine fongique doivent être évoquées, en les distinguant bien des formes non invasives comme l’aspergillome et la sinusite fongique allergique. Il existe un risque d’invasion des tissus adjacents, notamment osseux, vasculaire et cérébral.
Elles nécessitent une prise en charge spécialisée, avec concertation entre les chirurgiens ORL, les infectiologues et le médecin référent du patient (diabétologue, hématologue), car le contrôle des facteurs favorisants est un élément clé de la prise en charge. Pour les atteintes aspergillaires, le traitement repose essentiellement sur les antifongiques de la famille des azolés, en particulier le voriconazole. Ce dernier est administré de façon souvent prolongée, justifiant un suivi pharmacologique et de tolérance (hépatique, neurologique, cutané) régulier.
2. Lortholary O, Gangneux JP, Sitbon K, et al. Epidemiological trends in invasive aspergillosis in France: The SAIF network (2005-2007). Clin Microbiol Infect 2011;17(12):1882‑9.
3. Patterson TF, Thompson GR, Denning DW, et al. Practice guidelines for the diagnosis and management of aspergillosis: 2016 update by the Infectious Diseases Society of America. Clin Infect Dis 2016;63(4):e1‑e60.
4. Lanternier F, Dannaoui E, Morizot G, et al. A global analysis of mucormycosis in France: The RetroZygo Study (2005-2007). Clin Infect Dis 2012;54 Suppl 1:S35-43.
5. Hoenigl M, Seidel D, Carvalho A, et al. The emergence of COVID-19 associated mucormycosis: A review of cases from 18 countries. Lancet Microbe 2022;3(7):e543‑52.
6. Alanio A, Garcia-Hermoso D, Mercier-Delarue S, et al. Molecular identification of Mucorales in human tissues: Contribution of PCR electrospray-ionization mass spectrometry. Clin Microbiol Infect 2015;21(6):594.e1-5.
7. Millon L, Caillot D, Berceanu A, et al. Evaluation of serum Mucorales polymerase chain reaction (PCR) for the diagnosis of mucormycoses: The MODIMUCOR prospective trial. Clin Infect Dis 2022;75(5):777‑85.
8. Vironneau P, Verillaud B, Tran H, et al. Rhino-orbito-cerebral mucormycosis, surgical treatment, state of the art. Med Sci (Paris) 2013;29 Spec No 1:31‑5.
9. Cornely OA, Alastruey-Izquierdo A, Arenz D, et al. Global guideline for the diagnosis and management of mucormycosis: An initiative of the European Confederation of Medical Mycology in cooperation with the Mycoses Study Group Education and Research Consortium. Lancet Infect Dis 2019;19(12):e405‑21.
10. Cag Y, Erdem H, Gunduz M, et al. Survival in rhino-orbito-cerebral mucormycosis: An international, multicenter ID-IRI study. Eur J Intern Med 2022;100:56‑61.
11. Morgand M, Rammaert B, Poiree S, et al. Chronic invasive Aspergillus sinusitis and otitis with meningeal extension successfully treated with voriconazole. Antimicrob Agents Chemother 2015;59(12):7857‑61.
12. D’Anza B, Stokken J, Greene JS, et al. Chronic invasive fungal sinusitis: Characterization and shift in management of a rare disease. Int Forum Allergy Rhinol 2016;6(12):1294‑300.
13. Rupa V, Peter J, Michael JS, et al. Chronic granulomatous invasive fungal sinusitis in patients with immunocompetence: A review. Otolaryngol Head Neck Surg 2023;168(4):669-80.
14. Marchionni E, Parize P, Lefevre A, et al. Aspergillus spp. invasive external otitis: Favourable outcome with a medical approach. Clin Microbiol Infect 2016;22(5):434‑7.
15. Le Clerc N, Verillaud B, Duet M, et al. Skull base osteomyelitis: Incidence of resistance, morbidity, and treatment strategy. Laryngoscope 2014;124(9):2013‑6.
16. Vion PA, Verillaud B, Paycha F, et al. 99m Tc-HMPAO-leucocyte scintigraphy and [18F]FDG-PET/CT for diagnosis and therapy monitoring in eleven patients with skull base osteomyelitis. Clin Otolaryngol 2020;45(4):591‑4.