La douleur provoquée par les soins agresse d’abord les plus vulnérables. Tout en étant prévisible, elle nuit aux conditions de réalisation et à la qualité même du soin et s’interpose dans la relation entre le soigné et le soignant qu’elle pénalise l’un et l’autre. Des stratégies de prévention efficaces, collectives et/ou individuelles existent et nécessitent d’être diffusées et mises en œuvre. Il en va donc de l’éthique la plus élémentaire comme de la qualité du système de santé.1
Identifier les différentes causes de la douleur
Il faut bien distinguer la douleur provoquée lors d’une manœuvre diagnostique en secteur de soins ou de recherche au laboratoire, la douleur iatrogénique survenant au décours d’un traitement pourtant bien conduit et la douleur – que l’on peut anticiper – d’un geste (ou sa répétition) réalisé dans le cadre du soin. Cette dernière étant tantôt dénommée douleur procédurale (procedural pain du thésaurus MeSH, 2018), douleur induite ou douleur liée aux soins, nous préférons ici le vocable « douleur provoquée par les soins » (DPS), éliminant tout caractère inopiné de sa survenue (hors urgence vitale) et soulignant la responsabilité du professionnel de santé dans la mise en œuvre de sa prévention, en parallèle du soin en question.
À l’heure actuelle, les gestes identifiés comme les plus invasifs, dont la réalisation nécessite un environnement technique spécifique et la disponibilité totale du patient comme en médecine interventionnelle, sont protocolisés et font intervenir l’anesthésie locorégionale, voire générale, avec monitorage.2 La douleur postopératoire et sa chronicisation font l’objet de démarches spécifiques.
Cet article cible les gestes de soins plus simples, parfois quotidiens, dans les services d’urgence ou d’hospitalisation, en médecine de cabinet ou en institution. Ces gestes sont considérés indûment comme ordinaires et peu douloureux par la plupart, et la formation initiale comme l’expérience des personnels médicaux et paramédicaux sont souvent happées par les habitudes des services au détriment de stratégies antalgiques.
Quels sont les mécanismes physiopathologiques en jeu ?
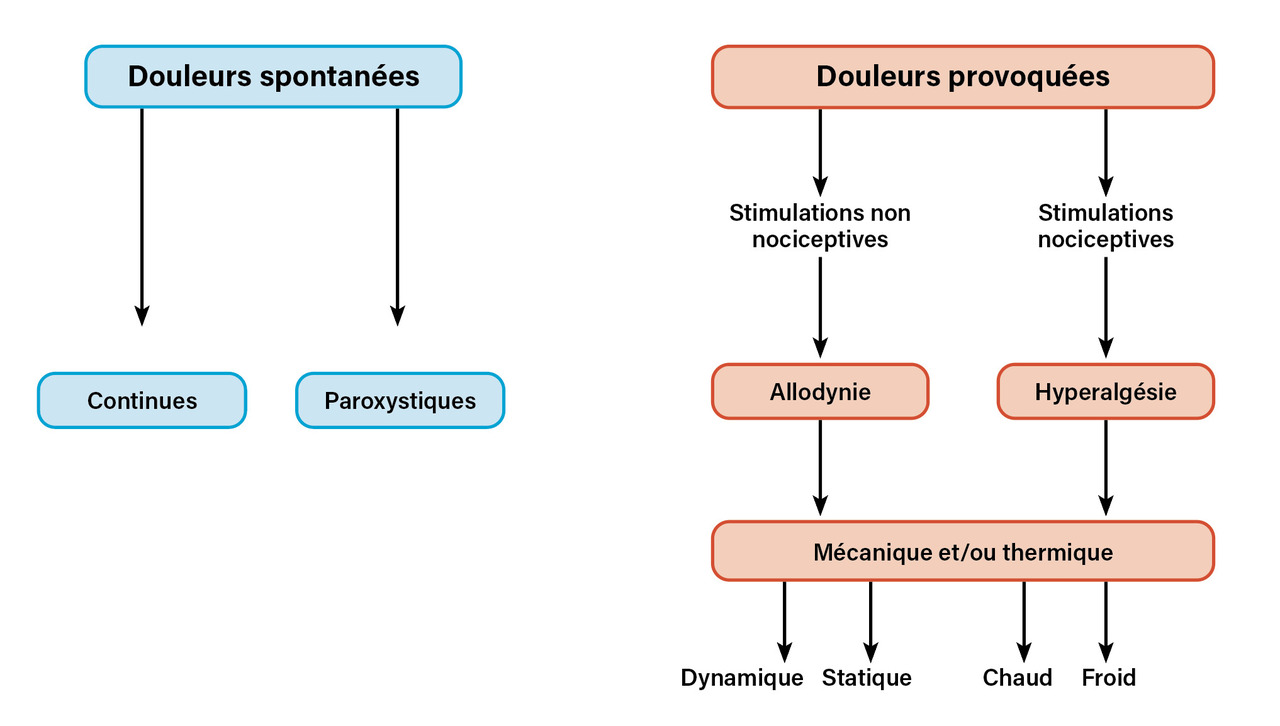
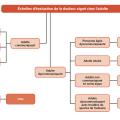
La douleur provoquée par les soins correspond le plus généralement à un accès de douleur aiguë liée au stimulus créé au site du soin sur les nocicepteurs périphériques : il s’agit alors d’un mécanisme par excès de nociception. Lorsque le soin est réalisé dans un territoire correspondant à la distribution neuro-atomique d’une lésion (ou maladie) du système somato-sensoriel, le mécanisme de la douleur provoquée peut être neuropathique. Dans ce cas, si le stimulus est nociceptif, la perception douloureuse peut être amplifiée (hyperalgésie) ; si le stimulus n’est pas nociceptif, une perception douloureuse peut pourtant exister (allodynie), que le stimulus soit mécanique (statique ou dynamique) et/ou thermique (chaud ou froid) [fig. 1].
L’allodynie et l’hyperalgésie accompagnent la plupart des syndromes douloureux chroniques et relèvent des phénomènes de sensibilisation centrale, c’est-à-dire une augmentation de la réactivité des neurones nociceptifs du système nerveux à des influx afférents normaux ou inférieurs au seuil d’activation. Cette notion est importante à connaître, car on estime qu’au moins un quart de la population française est porteuse de douleurs chroniques et 7 % de douleurs neuropathiques, lesquels ont une probabilité élevée de côtoyer le système de soins.3
Sur fond de douleur chronique ou non, un événement douloureux aigu n’est jamais anodin, en particulier chez les plus vulnérables : aux âges extrêmes de la vie, au cours d’une maladie chronique, en cas de difficulté à communiquer. Lorsqu’ils sont répétés, il est démontré que les épisodes douloureux s’engramment dans le système nerveux4 et que la mise en jeu des composantes émotionnelles et cognitives lors d’un premier soin conditionne leur expression lors des suivants.5 Il est également admis que des émotions comme l’anxiété et la peur sont prédictives de l’intensité douloureuse tandis que des croyances négatives et du catastrophisme sont prédictives de la tolérance à la douleur.6
Pourquoi la douleur provoquée par les soins peut-elle être intense ?
La nature même du soin est un facteur d’influence, par l’intensité du stimulus, sa localisation sur un site corporel plus ou moins riche en nocicepteurs et la sensation de menace qu’il génère. Une augmentation d’intensité douloureuse au cours d’un soin est associée à sa durée7 et la récurrence d’un soin douloureux crée une anticipation anxieuse.
L’état psychologique du patient, fortement influencé par la représentation qu’il a du soin, est déterminant. Les attentes et croyances négatives sont susceptibles de générer un effet nocebo.8 Le vécu douloureux antérieur, en cas de maladie chronique, sensibilise de façon cumulative à la perception de la douleur. La compréhension de la nécessité d’un soin dépend d’une information loyale et adaptée délivrée au patient, en particulier pour les enfants et les personnes âgées, en fonction de la fatigue, de la disponibilité, de la barrière de la langue.
Le comportement professionnel du soignant, qui comprend avec empathie la situation du patient et se montre attentif et disponible, conditionne son attitude positive face au patient qui la perçoit en retour. La qualité de l’organisation et la maîtrise du geste conditionnent également la confiance du patient et une bonne réalisation. En cas d’échecs répétés, savoir passer la main à un collègue est légitime et raisonnable. Enfin, la maîtrise des moyens d’évaluation de la douleur et de son soulagement sont des parties intégrantes du savoir-faire. Afin de favoriser une bonne relation soigné-soignant, le lieu de soin, souvent inconnu du patient, doit permettre une installation confortable pour les deux, la présence d’un proche, dans un endroit calme et respectant l’intimité.
La problématique de la douleur provoquée par les soins reste-t-elle un tabou ?
Bien que matériellement simple à prévenir, la DPS reste pourtant un sujet de non-dits et de conflits. Il est salutaire d’interroger les attitudes des uns et des autres. Cette douleur, souvent anticipée, trouve son absurdité dans l’inutilité de sa survenue (il n’y a nul besoin d’alarme) lors d’une démarche pourtant censée être favorable au patient et qui fait dès lors figure d’agression : « Est-ce pour mon bien ? » ; « Est-ce normal ? » ; « Dois-je me plaindre ? » ; « En ai-je le droit ? » ; « Ne va-t-on pas me délaisser ? »…
Porté par les habitudes de travail et par les pratiques du groupe dont il fait partie et qu’il a intériorisées, le soignant est confronté à l’embarras d’un soin compliqué par le comportement douloureux du soigné. Volontiers en proie au déni, la douleur provoquée par les soins le met en situation de dissonance cognitive où ce qu’il vit contrarie ses valeurs et génère de la culpabilité et/ou de la conflictualité, si ce n’est de réelles difficultés à réaliser le soin. Les fausses croyances encouragent les réticences à la prévention de la DPS, certaines justifications sont évoquées : « Ce soin n’est pas douloureux habituellement » ; « D’ailleurs, le patient ne se plaint pas » ; « C’est une perte de temps » ; « Nous ne sommes pas assez nombreux » ; « Nous n’avons pas les moyens »…
Dans le cadre de la contention lors des soins en pédiatrie a émergé le concept de « cécité empathique transitoire » dont le soignant serait l’objet, le temps d’un soin marqué par l’opposition du patient.9 Empêcher chez un patient l’évitement, voire la phobie du soin douloureux relève ici, outre les obligations légales, d’une démarche clairvoyante de modification des pratiques individuelles et/ou collectives.
Prévention de la douleur provoquée par les soins adaptée selon le contexte et le secteur de soins
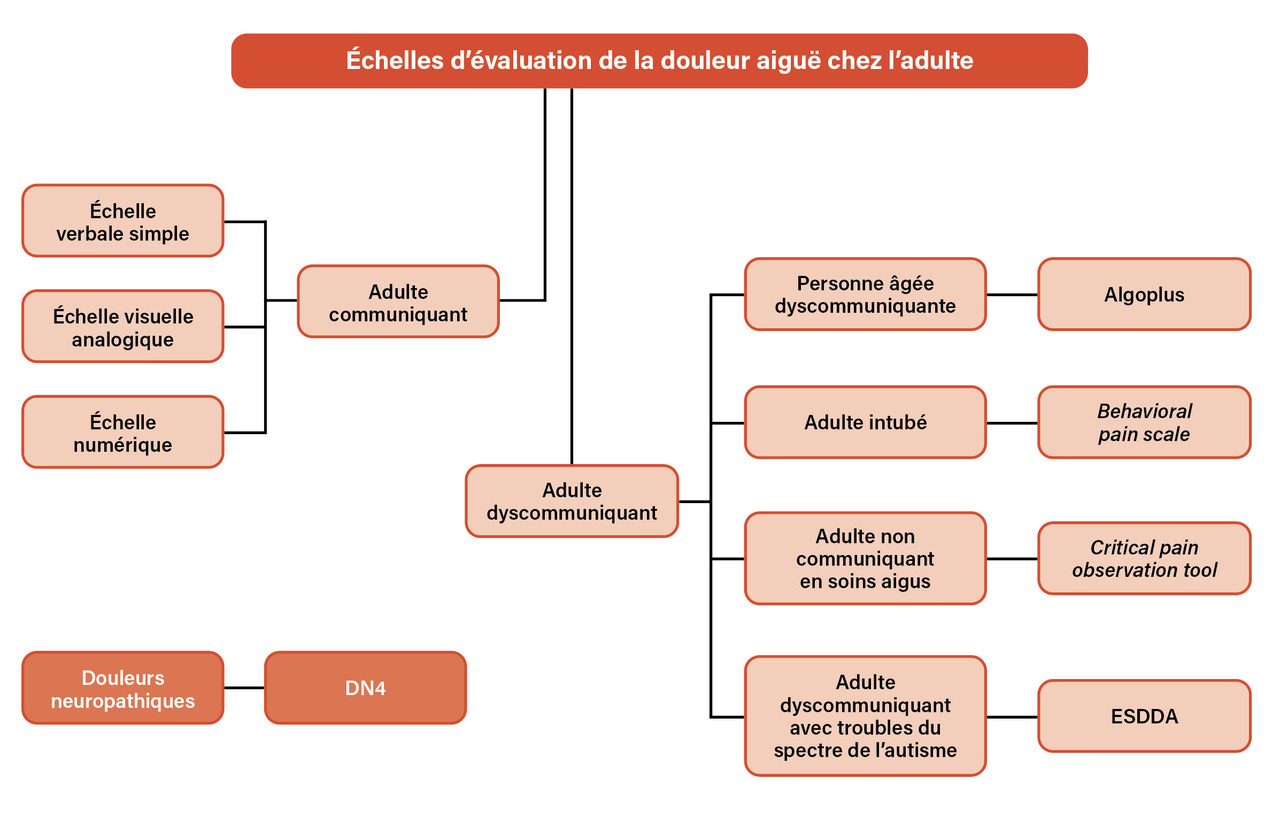
En ville10,11 comme à l’hôpital, souvent à l’initiative des comités de lutte contre la douleur (CLUD), les soins les plus fréquemment responsables de douleur provoquée ont pu être identifiés par des audits de situation, voire des études observationnelles. La réflexion collective sur l’organisation entourant un soin problématique, aiguisée par « l’effet étude », a permis d’abord de questionner la pertinence et le caractère systématique de certains gestes, puis de mettre en place des protocoles de prévention de la douleur provoquée par les soins. Les données épidémiologiques concernant la douleur provoquée par les soins sont encore peu nombreuses au regard de la prise de conscience relativement récente de leur impact et elles concernent prioritairement la pédiatrie. En France, quelques études observationnelles ont été menées chez des adultes hospitalisés, rapportant globalement des soins douloureux chez plus d’un patient sur deux, avec des douleurs intenses pour plus d’un tiers à la moitié des cas.12,13 Le Centre national ressources douleur (CNRD) a diffusé sur son site internet les résultats de plusieurs enquêtes14,15 et deux ouvrages traitent du sujet (encadré Ressources). Ce type d’études est à promouvoir dans tous les secteurs de soin, avec des méthodes adaptées pour le recueil de l’information (au mieux en temps réel), le choix des outils de mesure (échelles d’évaluation de la douleur validées [fig. 2]) et la formation des investigateurs.16 Une réalité épidémiologique se cache derrière la notion de satisfaction globale couramment rencontrée dans les enquêtes rétrospectives fondées sur les déclarations des sujets inclus.
Stratégies de prévention de la douleur provoquée par les soins
La relation de confiance, les moyens non médicamenteux et les antalgiques constituent les clés d’une bonne prévention de la douleur provoquée par les soins.
Relation de confiance
La congruence entre le soigné et le soignant est l’édifice du plan de prévention des douleurs provoquées par les soins, qui doit être multimodal :
- admettre et anticiper l’existence d’une douleur lors d’un soin instaure une dialectique constructive. Informer sur le geste à venir, en employant un vocabulaire descriptif sans minimiser ou exagérer la douleur envisageable. Il n’y a pas de « petites piqûres » ; éviter de dire : « Vous ne sentirez rien, ça va aller très vite ». Employer des termes moins connotés : « Nous réalisons un prélèvement sanguin » ou « Nous mettons en œuvre des moyens antalgiques » ;
- aider le soigné à se représenter le geste grâce à des supports informatifs (brochures, vidéos, démonstrations) ;
- entendre ce que le geste douloureux signifie pour le soigné, tant sur l’aspect sensoriel, cognitivo-comportemental qu’émotionnel (anxiété) ; le soignant doit intégrer ces aspects dans ses choix thérapeutiques ;
- valider l’état émotionnel du soigné, en le reconnaissant verbalement (« J’ai entendu vos appréhensions… »). Dans les situations d’anxiété très envahissante, il est envisageable de prescrire un anxiolytique (en plus des moyens antalgiques).
Lors de la réalisation du geste, les termes employés doivent suggérer des sensations agréables tout en maintenant un narratif réaliste. Il est reconnu, depuis les travaux sur la communication thérapeutique, que les suggestions négatives activent les réseaux de la douleur.17 L’écoute attentive des appréhensions et de la douleur avant, pendant et après le geste permet au soignant de réajuster sa communication, ses stratégies de prévention, de faire des pauses si besoin.
Il est primordial de valoriser les ressources efficaces du soigné pour faire face à la douleur afin de renforcer le coping positif*.18
Moyens non médicamenteux
L’offre d’un éventail varié de méthodes individualisées permet à chaque soigné de s’en approprier certaines ou d’en proposer lui-même.
Méthodes physiques
L’utilisation du gate control**19 modifie la composante sensori-discriminative et offre de multiples applications : l’application de froid provoque une hypoalgésie (avant une effraction cutanée par exemple), le chaud peut également être appliqué ; le toucher-massage ou les frottements sur une partie du corps en marge de la zone de soin (contre-stimulation) activent les contrôles inhibiteurs descendants et réduisent le message douloureux.
Pratiques psychocorporelles
Distraction
Détourner l’attention de l’acte de soin diminue la dimension émotionnelle. Le soignant peut, par exemple, mobiliser les canaux de communication du soigné et si possible plusieurs sens (visuel, auditif, kinesthésique, olfactif, gustatif), faire écouter de la musique (auditif), regarder une vidéo (auditif et visuel), souffler dans un ballon (kinesthésique), pétrir une balle anti-stress (kinesthésique), vivre une expérience de réalité virtuelle (auditif, visuel et kinesthésique).
Hypno-analgésie
La communication hypnotique lors du soin induit une dissociation entre le message nociceptif et les composantes émotionnelle et cognitive.
Les patients ayant une pratique de relaxation , de méditation ou d’auto-hypnose peuvent par eux-mêmes accéder à ces états de conscience modifiée.20
Antalgiques
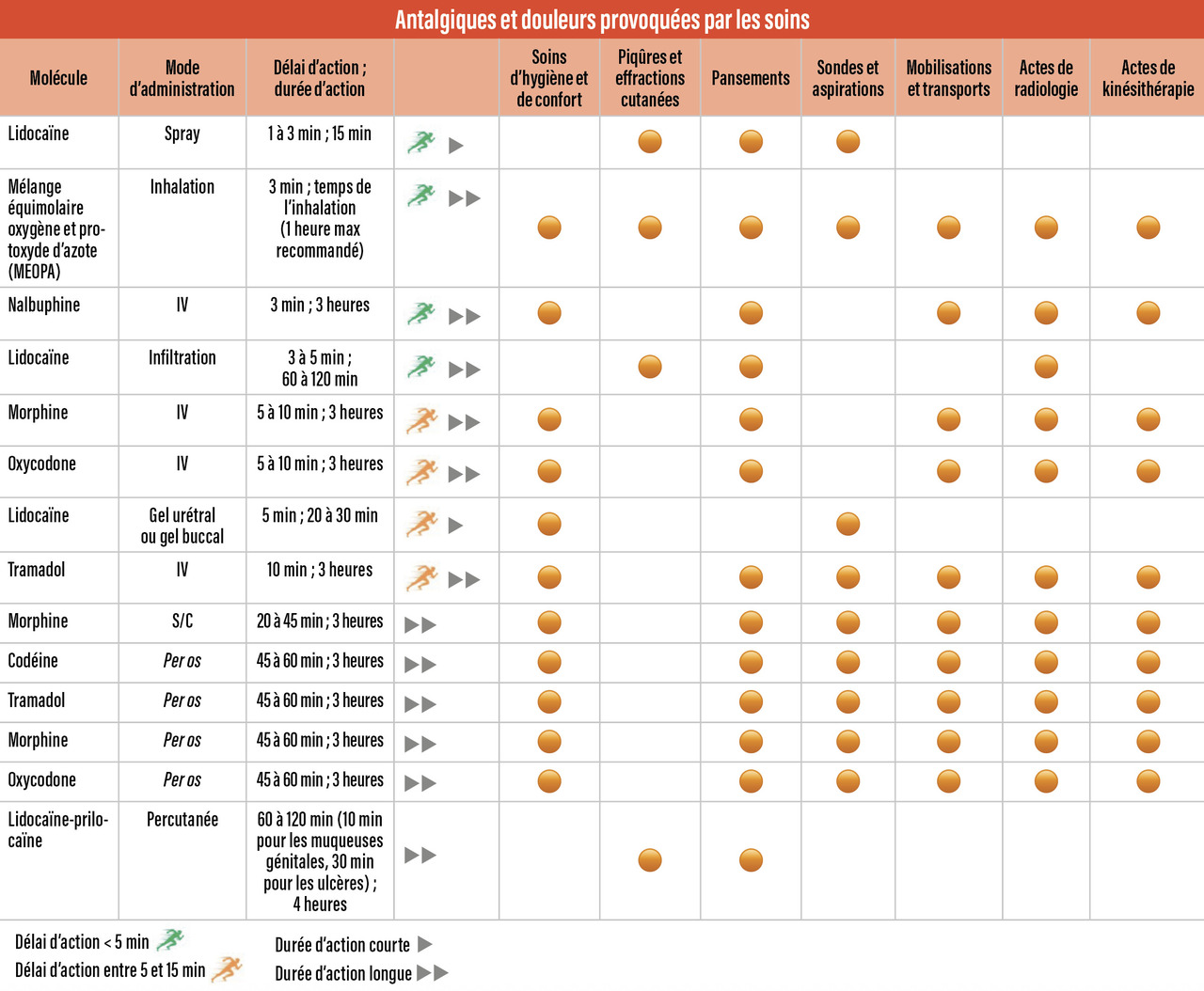
L’anticipation est la clé d’une bonne stratégie de prévention des douleurs provoquées par les soins. La figure 3 présente les différentes molécules pouvant être prescrites, en tenant compte des délais et durées d’action. À l’heure actuelle, il n’existe aucune alternative antalgique aussi efficace, sûre et facile à déployer, dans cette indication prioritaire, que le mélange équimolaire d’oxygène et de protoxyde d’azote (MEOPA). Son délai d’action est court (trois minutes), ses effets sont réversibles à court terme et son utilisation est simple (encadré).21,22
Les premières études observationnelles avaient permis d’identifier les antalgiques les plus adaptés aux douleurs provoquées par les soins parmi des catégories distinctes de soins (tableau). Une bibliographie spécialisée est disponible (encadré Ressources utiles).
Situations particulières
Soins d’hygiène et de confort
Leur fréquence et leur nécessité contribuent à en intensifier la douleur.23 Le matériel doit être adapté (fauteuil, lève-malade, drap de glisse, ceinture d’aide à la verticalisation), l’environnement rassurant (température ambiante, respect de l’intimité, aide à l’autonomie). Le MEOPA et/ou les morphiniques peuvent être proposés, ainsi qu’une méthode distractive individualisée. Le dépistage des douleurs neuropathiques (DN4) est primordial. En cas d’allodynie, le toucher doit être ferme et paume à plat.
Piqûres et effractions cutanées
Pour toute ponction (veineuse, artérielle, médullaire) ou injection, la pose d’un patch de lidocaïne/prilocaïne est recommandée ou, à défaut, une application de froid. Pendant le soin, proposer du MEOPA et une technique de distraction ou d’hypno-analgésie.
Pour les ponctions osseuses, il peut être proposé une infiltration d’anesthésique et du MEOPA.
Concernant les ponctions lombaires, il est maintenant recommandé d’utiliser des aiguilles atraumatiques.24
Réfection de pansements
Leur répétition est un facteur de risque de douleur. La prévention doit être mise en place d’emblée, en évaluant régulièrement les stratégies et en les ajustant si besoin. On peut envisager des anesthésiques locaux, du MEOPA, des morphiniques à libération immédiate, un environnement sécurisant (confort) et une méthode non pharmacologique. Les blocs nerveux périphériques sont indiqués dans le cas de douleurs rebelles aux traitements de première ligne.25
Une attention particulière doit être portée au retrait des adhésifs et au choix de ceux-ci. L’utilisation d’eau savonneuse, teinture de benjoin ou spray anti-adhésif permet le retrait en limitant les excès de nociception.
Sondes et aspirations
L’intrusion d’un corps étranger est anxiogène par nature. L’information sur le geste doit être la plus précise possible, le matériel de démonstration est une bonne stratégie pour désamorcer le stress (par exemple, le soigné qui manipule une sonde urinaire constate la souplesse et la légèreté du matériel). Les applications locales de lidocaïne sont recommandées, comme les techniques de distraction, toucher-massage ou hypno-analgésie. Pour les ablations de drains, le tamponnage de lidocaïne est efficace.26
Mobilisations et transport
Préserver l’autonomie du soigné et sa participation active limite la douleur.27
Le MEOPA est un excellent antalgique à proposer pour les mobilisations difficiles, seul ou associé à un morphinique. Le matériel de mobilisation doit par ailleurs être adapté et les délais d’attente optimisés.
Séances de kinésithérapie
L’observance et l’efficacité de la kinésithérapie sont facilitées par une couverture antalgique.28
Une évaluation régulière des douleurs provoquées par les soins lors des séances est nécessaire pour réajuster la prescription. Si certains sportifs souhaitent conserver « l’alarme » douleur au cours de leur rééducation, pour d’autres, elle peut devenir un obstacle. Les douleurs à la suite des séances doivent également être considérées et traitées, notamment pour les porteurs de douleurs chroniques.
Examens de radiologie
Le caractère anxiogène de l’examen est à prendre en compte. La proposition de topique lidocaïne/prilocaïne est recommandée en cas d’effraction cutanée ainsi que l’utilisation du MEOPA pour les mobilisations et certains sondages. Toutes les techniques psychocorporelles et de distraction sont adaptées.
Lutter contre les idées reçues
Outre la nécessité de former à la prévention et au soulagement de la douleur provoquée par les soins, un certain nombre d’idées reçues qui entravent la prise en charge doivent être démenties : non, le paracétamol n’est pas efficace pour les douleurs provoquées par les soins dynamiques ; en revanche, il est utile pour les douleurs prolongées à la suite du geste ; non, traiter l’anxiété ne se substitue pas à un antalgique.
Modalités d’utilisation du MEOPA
Le mélange équimolaire d’oxygène et de protoxyde d’azote (MEOPA) est administré par un personnel de santé formé, sur prescription (ou dans le cadre d’un protocole) ; la présence du médecin n’est pas nécessaire. Son utilisation est autorisée en ambulatoire.
Contre-indications
Pneumothorax non drainé, occlusion digestive, hypertension intracrânienne, toute situation vitale précaire, tout trouble de conscience évolutif, traumatisme crânien non évalué, toute accumulation de gaz ou d’air dans une cavité close de l’organisme (chirurgie oculaire avec gaz SF6, C3F8, C2F6), accident de plongée, fracture de la face, situation exigeant une oxygénothérapie de plus de 50 %.
Indications
Soin ou examen douloureux ou anxiogène de courte durée (suture, pansement, effraction cutanée, pose de sonde, ponction lombaire mais aussi toilette douloureuse, mobilisation, réalisation de radiographie).
Ne convient pas seul pour des gestes très invasifs (fracture, abcès, brûlures graves…), penser alors à l’approche multimodale médicamenteuse ou non.
Administration
Le jeûne n’est pas nécessaire.
L’auto-administration est à privilégier.
Effets indésirables
Effets indésirables réversibles en quelques minutes après l’arrêt de l’inhalation. Contrôler et supplémenter en vitamine B12 en cas d’administrations quotidiennes répétées (plus de dix jours).
Toxicité exceptionnelle en cas de respect des précautions d’emploi et des contre-indications (inhalations répétées non ou mal tracées).
Absence d’addiction (ne pas confondre avec le N2O pur en vente libre).
Précautions d’emploi
Pollution atmosphérique du N2O : gaz à effet de serre, éviter le gaspillage.
Exposition professionnelle : si aucune preuve de risque pour la santé n’existe dans un contexte clinique*, l’Agence nationale de sécurité sanitaire, de l’alimentation, de l’environnement et du travail (ANSES) a émis en 2024 une recommandation de valeur limite d’exposition.**
Depuis l’harmonisation des réglementations européennes concernant l’utilisation du protoxyde d’azote en milieu professionnel (2 avril 2025), il est recommandé des locaux ventilés et une valve à la demande associée à un masque à double enveloppe. Les employeurs doivent respecter certaines obligations (https ://urls.fr/oowqOL).
La grossesse de la patiente n’est pas une contre-indication***.
Ressources utiles
Site du Centre national ressources douleur (CNRD). https ://urls.fr/dJnrIs
Wanquet Thibault P. Douleurs liées aux soins. Malakoff : Lamarre, coll. Soigner et accompagner, 2015. 165 p.
Wrobel J, Donnadieu S, Annequin D, et al. Les douleurs induites. Rueil-Malmaison : Institut UPSA de la douleur 2007. 192 p.
2. Steib A, Hausberger D, Robillart A, et al. Anesthésie pour imagerie interventionnelle. Ann Fr Anesth Reanim 2006;25(6):615‑25.
3. Chenaf C, Delorme J, Delage N, et al. Prevalence of chronic pain with or without neuropathic characteristics in France using the capture-recapture method: A population-based study. Pain 2018;159(11):2394‑402.
4. Laferriere A, Pitcher MH, Haldane A, et al. PKMζ is essential for spinal plasticity underlying the maintenance of persistent pain. Mol Pain 2011;7:99.
5. Noel M, Chambers CT, McGrath PJ, et al. The role of state anxiety in children’s memories for pain. J Pediatr Psychol 2012;37(5):567‑79.
6. Cimpean A, David D. The mechanisms of pain tolerance and pain-related anxiety in acute pain. Health Psychol Open 2019;6(2):2055102919865161.
7. Lang EV, Benotsch EG, Fick LJ, et al. Adjunctive non-pharmacological analgesia for invasive medical procedures: A randomised trial. Lancet 2000;355(9214):1486‑90.
8. Woo KY. Unravelling nocebo effect: The mediating effect of anxiety between anticipation and pain at wound dressing change. J Clin Nurs 2015;24(13‑14):1975‑84.
9. Lombart B. De la cécité empathique transitoire à la prudence dans les soins. Au sujet de la contention lors des soins en pédiatrie [Internet]. Thèse de doctorat. Université Paris-Est ; 2016.https://theses.fr/2016PESC0054
10. Talour K, Schollhammer M, Garlantezec R, et al. Facteurs prédictifs de la douleur dans les gestes techniques dermatologiques. Ann Dermatol Venereol 2013;140(1):5‑14.
11. Malacarne K, Manoliu A, Maillard F, et al. Soins infirmiers douloureux à domicile : enquête de terrain DOLASI. Faculté de médecine des Saint-Pères, Paris; 2014. p. 10. https://urls.fr/InhEG9
12. Coutaux A, Salomon L, Rosenheim M, et al. Care related pain in hospitalized patients: A cross-sectional study. Eur J Pain 2008;12(1):3‑8.
13. Ambrogi V, Tezenas du Montcel S, Collin E, et al. Care-related pain in hospitalized patients: Severity and patient perception of management. Eur J Pain 2015;19(3):313‑21.
14. Cimerman P, Galinski M, Thibault P, et al. Étude REGARDS (Recueil épidémiologique en gériatrie des actes ressentis comme douloureux et stressants), 2011. www.cnrd.fr
15. Maillard F, Cimerman P, Thibaut M, et al. Statut de performance et douleur des soins : résultats préliminaires de l’étude SPdol. www.cnrd.fr
16. Maillard F, Cimerman P, Thibaut M, et al. Douleur provoquée par les soins. In: SFETD, éditeur. Livre blanc de la douleur 2017. État des lieux et propositions pour un système de santé éthique, moderne et citoyen. Paris: Med-Line; 2017. p. 87‑90. http://www.sfetd-douleur.org/autres-productions
17. Derbyshire SWG, Whalley MG, Stenger VA, et al. Cerebral activation during hypnotically induced and imagined pain. NeuroImage 2004;23(1):392‑401.
18. Lazarus RS. Toward better research on stress and coping. Am Psychol 2000;55(6):665‑73.
19. Melzack R, Wall PD. Pain mechanisms: A new theory. Science 1965;150(3699):971‑9.
20. Gueguen J, Barry C, Hassler C, et al. Évaluation de l’efficacité de la pratique de l’hypnose. https://urls.fr/wAnNH0/
21. Lay F, Maillard F. MEOPA. Outils pratiques, dispositifs pour diminuer la pollution des locaux lors de son utilisation. CNRD 2023. https://urls.fr/cYCPTC
22. Annequin D. Protoxyde d’azote et traitement de la douleur. Presse Medicale Form 2021;2(6):561‑6.
23. Lombart B, Cimerman P, Guiot C, et al. NursPainPrevent: A prospective observational study on pain during a bed bath. Pain Manag Nurs 2025;26(0):e66‑73.
24. HAS, SFAR. Fiche mémo. Prévention et prise en charge des effets indésirables pouvant survenir après une ponction lombaire 2019. https://urls.fr/r_655j
25. Bures E, Schneider L, Rivet P, et al. Prise en charge de la douleur chronique rebelle des malades artéritiques par cathéters péri-nerveux et infusion continue d’anesthésique local de longue durée. Douleurs 2007;8(3):174‑80.
26. Guiraud-Chaumeil V, Goussault H, Boudjemaa A, et al. DOULAPLUX : efficacité de l’anesthésie locale à la xylocaïne tamponnée (AL) dans le contrôle de la douleur induite par les gestes pleuraux. Rev Mal Respir Actual. 2024;16(1):16.
27. Nebbak JM, Vignozzi A, Bussy C, et al. Mesures concrètes de prévention des douleurs provoquées par les opérations de brancardage dans un institut de cancérologie. Bull Cancer 2013;100(7-8):679‑87.
28. Perrot S, Rondeau V, Chartier I, et al. Stratégies de prévention de la douleur induite par la kinésithérapie ostéoarticulaire en médecine générale en France : le registre Alto. Kinesithérapie Rev 2013;13(134):29‑30.
29. Payen JF, Bru O, Bosson JL, et al. Assessing pain in critically ill sedated patients by using a behavioral pain scale. Crit Care Med 2001;29(12):2258-63.
30. Bouhassira D, Attal N. Douleurs neuropathiques, 2e édition, Arnette, Rueil-Malmaison, 2012.
31. Attal N, Alchaar H, Boureau F, et al. Comparison of pain syndromes associated with nervous or somatic lesions and development of a new neuropathic pain diagnostic questionnaire (DN4). Pain 2005;114(1‑2):29‑36.
32. Gelinas C, Fillion L, Puntillo KA, et al. Validation of the critical-care pain observation tool in adult patients. Am J Crit Care Off Publ Am Assoc Crit-Care Nurses 2006;15(4):420‑7.
33. Rat P, Jouve E, Pickering G, et al. Validation of an acute pain-behavior scale for older persons with inability to communicate verbally: Algoplus. Eur J Pain Lond Engl 2011;15(2):198.e1-198.e10.
34. Mytych I, Mercier C, Da Silva S, et al. Expression de la douleur dans les troubles du spectre autistique. Douleurs. Évaluation-Diagnostic-Traitement 2018;19(6):255‑7.
Dans cet article
- Identifier les différentes causes de la douleur
- Quels sont les mécanismes physiopathologiques en jeu ?
- Pourquoi la douleur provoquée par les soins peut-elle être intense ?
- La problématique de la douleur provoquée par les soins reste-t-elle un tabou ?
- Prévention de la douleur provoquée par les soins adaptée selon le contexte et le secteur de soins
- Stratégies de prévention de la douleur provoquée par les soins
- Situations particulières
- Lutter contre les idées reçues

 Encadrés
Encadrés