La radiothérapie fait partie des traitements incontournables dans le domaine de l’oncologie : aujourd’hui, au moins un patient sur deux atteint d’un cancer bénéficie d’un tel traitement. En urologie, et notamment dans le traitement du cancer de la prostate, la radiothérapie s’est imposée, avec la chirurgie, comme un des traitements de référence, que ce soit pour les cancers de stade intermédiaire ou pour les cancers plus localement avancés, pour lesquels elle reste le traitement de choix. Sans cesse en évolution, que ce soit dans la modernisation du matériel ou des techniques, elle a vu petit à petit les traitements traditionnels, comportant jusqu’à 40 séances et dits normofractionnés, être remplacés par des traitements plus courts dit hypofractionnés modérés, avec des séances délivrant davantage de dose par fraction, permettant une réduction du nombre de séances, voire des traitements hypofractionnés extrêmes de type stéréotaxique.
Modernisation du matériel et des techniques de radiothérapie
Pour le traitement des cancers de la prostate, la radiothérapie en trois dimensions a été abandonnée, au profit de la radiothérapie en modulation d’intensité par ARC-thérapie. L’appareil de traitement effectue une rotation à 360 degrés autour du patient tout en délivrant le rayonnement, tandis que la forme du faisceau est modifiée en temps réel grâce à un collimateur multilame, permettant de se conformer à la forme de la prostate, tout en évitant les organes de voisinage afin de les protéger au mieux.
La planification dosimétrique est dite inversée, c’est-à-dire que les paramètres de protection des organes de voisinage sont directement intégrés à la planification.
Les imageries traditionnelles de repositionnement fondé sur les structures osseuses ont, elles aussi, été remplacées par des cone beam CT (CBCT) ou scanner embarqué, permettant à chaque séance de se repositionner au mieux sur la cible prostatique et d’appréhender les modifications anatomiques (remplissage de vessie et de rectum, perte ou prise de poids). Ce mode de repositionnement est nommé Image-guided radiation therapy (IGRT).
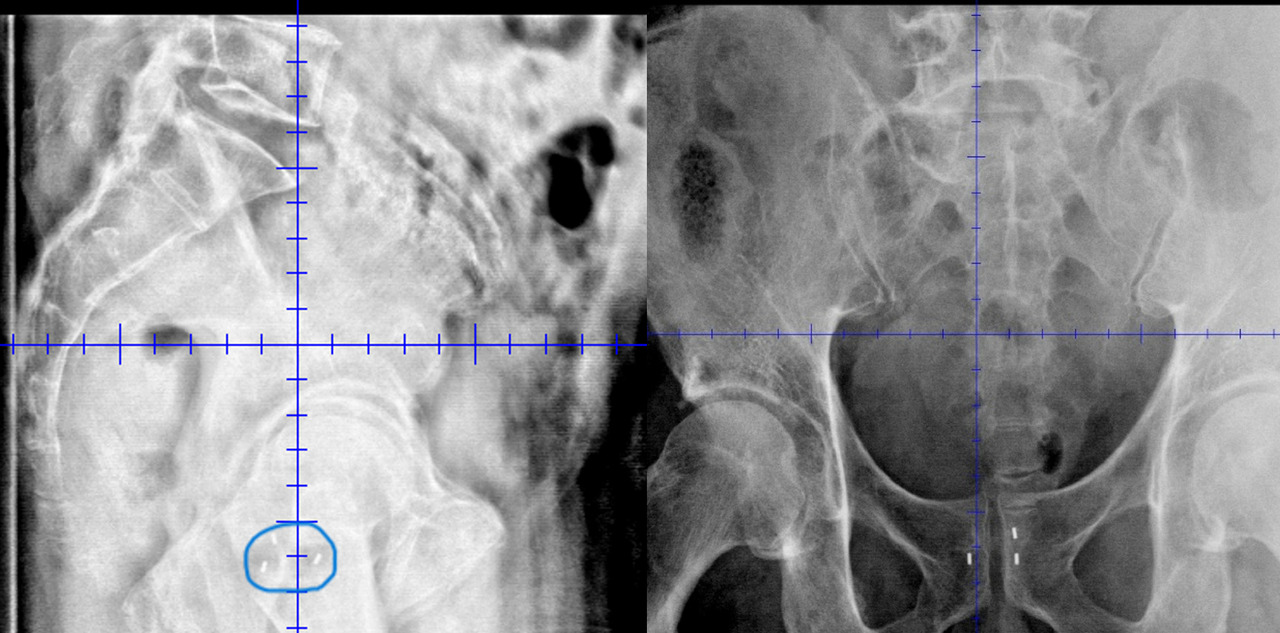
Il est également possible d’effectuer, avant la radiothérapie, une mise en place de fiduciaires, ou grains d’or, se figeant de manière définitive dans la prostate, et d’appréhender les mouvements de cette dernière pendant les traitements par un suivi de ces grains d’or, soit avant chaque séance, soit pendant la séance en direct (figure).
Hypofractionnement modéré de bénéfice équivalent à la radiothérapie classique
Parmi les cancers, celui de la prostate semble être particulièrement sensible aux doses plus élevées par fractions, en raison de la nature de son tissu cancéreux. Ainsi, alors qu’il avait été montré dans plusieurs études que la majoration de dose totale délivrée dans des traitements en fractionnement classique avait un impact sur leur efficacité, poussant à réaliser des irradiations délivrant 78 à 80 Gy en 39 ou 40 séances, les études d’hypofractionnement se sont multipliées dans les vingt dernières années, permettant d’envisager des traitements plus courts, avec un meilleur confort pour le patient et un impact médico-économique non négligeable.
En 2016, les résultats de l’étude RTOG 0415 ont été publiés dans le Journal of Clinical Oncology1, montrant que, dans les cancers à risque faible, une radiothérapie de 70 Gy en 28 séances de 2,5 Gy permettait une survie sans maladie à cinq ans parfaitement identique à celle obtenue avec un traitement de 73,8 Gy en 41 séances, au prix d’un léger sur-risque d’effets indésirables tardifs de type gastro-intestinal.
La même année, Dearnaley et al. publiaient les résultats de l’étude britannique CHIPP,2 montrant qu’un fractionnement de 60 Gy en 20 séances permet d’obtenir une survie sans récidive biochimique équivalente à celle d’un traitement de 74 Gy en 37 séances dans des cancers de tout stade. Ces données ont été confirmées par un essai français3 montrant une survie sans récidive à cinq ans identique dans deux groupes comparant 60 Gy en 20 fractions à 78 Gy en 39 fractions dans des cancers de stade intermédiaire.
Aucune étude n’a, en revanche, permis de démontrer une supériorité des schémas hypofractionnés en matière de bénéfice de survie. Pour autant, l’équivalence seule avec une toxicité finalement bien maîtrisée a suffi à faire de ce schéma un standard dans les traitements de radiothérapie prostatique. Le Groupe d’étude des tumeurs urogénitales a d’ailleurs publié ses recommandations sur ce fractionnement de 60 Gy en 20 séances, considéré maintenant comme un standard.4
Il est désormais acquis que la toxicité des traitements hypofractionnés est maîtrisée, même s’il convient d’être prudent, notamment chez les patients ayant des prostates de gros volume ou des troubles urinaires importants, pouvant nécessiter un premier traitement par résection transurétrale afin d’éviter tout risque de rétention pendant les traitements de radiothérapie.
Hypofractionnement extrême ou stéréotaxie pour les cancers de stade intermédiaire en France
Les traitements modérément hypofractionnés ayant montré leur bénéfice équivalent, il est logique que les essais suivants aient étudié la possibilité de recourir à des traitements hypofractionnés, dits extrêmes, avec des doses par fractions de plus de 5 Gy. En effet, cette irradiation dite stéréotaxique, délivrant de plus grosses doses par séance avec une précision majorée, est devenue un standard dans bon nombre d’autres localisations (poumon, os, cerveau…).
L’essai HYPO-RT-PC5 a comparé, dans une étude de phase III, une radiothérapie classique (78 Gy en 39 fractions) à une radiothérapie ultrahypofractionnée (42,7 Gy en 7 fractions de 6,1 Gy). Il s’agissait d’un essai de non-infériorité incluant 1 180 patients dont 80 % avaient un cancer de stade intermédiaire.
Le taux de contrôle biochimique à cinq ans était équivalent dans les deux bras, de même que la toxicité (15 à 20 % de toxicité urinaire de grade 2 et 10 % de toxicité digestive de grade 2). Les données de suivi en matière de qualité de vie ont montré que les toxicités post-stéréotaxie dans cette étude s’amenuisaient fortement après un an de suivi.
L’actualisation récente des données à dix ans, présentée au congrès de l’European Society for Medical Oncology (ESMO) 2024, confirme ces données.
L’essai PACE-B6 a montré, chez 874 patients porteurs d’un cancer de la prostate de stade intermédiaire favorable ou bas risque, une équivalence (avec une médiane de suivi à six ans) entre un traitement normofractionné de 78 Gy en 39 séances, un traitement modérément hypofractionné de 62 Gy en 20 séances et un traitement stéréotaxique de 36,25 Gy en 5 séances. Le taux de survie sans récidive à cinq ans se situait autour de 95 %, la toxicité urinaire supérieure à un grade 2 était de 5,5 % dans le groupe stéréotaxie.
Les recommandations de l’Association française d’urologie 2024 - 2026 répertorient l’irradiation prostatique avec un fractionnement extrême comme une possibilité thérapeutique pour les cancers de stade intermédiaire, tandis que les recommandations américaines ouvrent cette possibilité quel que soit le stade du cancer.
Pour le futur, plusieurs essais tentent de démontrer l’efficacité d’une irradiation prostatique en une fraction unique, notamment PROSINT. Dans cette étude de phase II, les patients bénéficient d’une séance unique de 24 Gy pour des cancers de la prostate de stade intermédiaire. Les données de tolérance semblent plutôt encourageantes,7 avec une toxicité semblant équivalente entre le groupe en 5 fractions et le groupe en une fraction. Ces résultats sur un faible effectif nécessitent cependant des confirmations à plus grande échelle et avec davantage de recul.
Un frein à l’utilisation de la radiothérapie stéréotaxique étendue à toutes les indications de radiothérapie prostatique pourrait être l’irradiation pelvienne ganglionnaire prophylactique. En effet, plusieurs études tendent à démontrer qu’elle a un intérêt pour l’irradiation des cancers à haut risque dans les irradiations normofractionnés. Des essais de faisabilité et d’efficacité sont néanmoins en cours, étudiant la possibilité d’irradiation pelvienne en 5 fractions de 5 Gy en parallèle de l’irradiation prostatique.
Études de majoration de dose
L’essai FLAME, publié en 2021, a étudié la faisabilité d’un boost intégré dans la lésion index repérée sur l’imagerie par résonance magnétique (IRM) lors d’un traitement en fractionnement classique.8 Ce boost permettait une majoration de la survie sans récidive et sans majoration de la toxicité.
L’essai Hypo Flame, non encore publié, étudie ce concept, cette fois appliqué à un traitement de stéréotaxie en 5 séances, avec une irradiation de 35 Gy sur la prostate et une majoration de dose entre 40 et 50 Gy sur la lésion cible prostatique repérée en IRM. Les résultats préliminaires semblent en faveur d’une tolérance acceptable ; l’efficacité reste à démontrer avec un recul plus important, mais les résultats sont attendus avec impatience.
2. Dearnaley D, Syndikus I, Mossop H, et al. Conventional versus hypofractionated high-dose intensity-modulated radiotherapy for prostate cancer: 5-year outcomes of the randomised, non-inferiority, phase 3 CHHiP trial. Lancet Oncol 2016;17(8):1047-60.
3. Supiot S, de Laroche G, Latorzeff I, et al. PROstate Fractionated Irradiation Trial (PROFIT) : résultats d’une étude internationale randomisée comparant deux schémas d’irradiation des cancers de prostate de risque intermédiaire. Cancer Radiother 2016;20(6-7):710.
4. Langrand-Escure J, de Crevoisier R, Llagostera C, et al. Dose constraints for moderate hypofractionated radiotherapy for prostate cancer: The French genito-urinary group (GETUG) recommendations. Cancer Radiother 2018;22(2):193-8.
5. Widmark A, Gunnlaugsson A, Beckman L, et al. Ultra-hypofractionated versus conventionally fractionated radiotherapy for prostate cancer: 5-year outcomes of the HYPO-RT-PC randomised, non-inferiority, phase 3 trial. Lancet 2019;394(10196):385-95.
6. Van As N, Tree A, Patel J, et al. 5-Year Outcomes from PACE B: An international phase III randomized controlled trial comparing stereotactic body radiotherapy (SBRT) vs conventionally fractionated or moderately hypo fractionated external beam radiotherapy for localized prostate cancer. Int J Radiat Oncol Biol Phys 2023;117(4):E2-3.
7. Greco C, Pares O, Pimentel N, et al. Safety and efficacy of virtual prostatectomy with single-dose radiotherapy in patients with intermediate-risk prostate cancer: Results from the PROSINT phase 2 randomized clinical trial. JAMA Oncol 2021;7(5):700-8.
8. Kerkmeijer LGW, Groen VH, Pos FJ, et al. Focal boost to the intraprostatic tumor in external beam radiotherapy for patients with localized prostate cancer: Results from the FLAME randomized phase III trial. J Clin Oncol 2021;39(7):787-96.