La cardiotoxicité induite par les traitements anticancéreux constitue une complication majeure pouvant mener à la suspension, voire à l’arrêt, d’une prise en charge oncologique pourtant efficace. Sa survenue peut compromettre non seulement la poursuite du traitement, et donc le pronostic du cancer, mais aussi être directement responsable de morbi-mortalité. Les manifestations cliniques incluent l’insuffisance cardiaque, la dysfonction ventriculaire asymptomatique, les arythmies, la myocardite et les syndromes coronariens. Ces effets indésirables peuvent être réversibles ou laisser des séquelles irréversibles.
Cet article se focalise sur la cardiotoxicité de type insuffisance cardiaque ou dysfonction ventriculaire.
En 2021, la Société internationale de cardio-oncologie (International Cardio-Oncology Society [IC-OS]) et la Heart Failure Association (HFA) ont conjointement proposé des scores de risque de cardiotoxicité,1 notamment de risque de dysfonction ventriculaire ou d’insuffisance cardiaque. Ces scores ont été largement repris par la Société européenne de cardiologie (ESC) à l’occasion des premières recommandations de cardio-oncologie.2
L’intérêt pour les méthodes de diagnostic précoce, avant l’apparition de symptômes cardiovasculaires, est croissant. L’évaluation repose principalement sur l’imagerie cardiaque par échographie, enrichie désormais par les biomarqueurs sériques, l’imagerie multimodale3 et l’analyse fine de l’électrocardiogramme de surface.4,5 Une fois identifiée la population à risque de développer une cardiotoxicité, la mise en place de stratégies de cardioprotection primaire, qu’elles soient pharmacologiques ou comportementales, pourrait être envisagée.2 Les données de la littérature demeurent cependant parcellaires pour recommander une approche pharmacologique de cardioprévention primaire.
Définition évolutive de la cardiotoxicité des traitements anticancéreux
Les définitions de la cardiotoxicité ont évolué ces dernières années. Celle liée à l’insuffisance cardiaque ou à la dysfonction systolique du ventricule gauche reste la plus étudiée. Les valeurs seuils de fraction d’éjection ventriculaire gauche (FEVG) varient selon les sources. Le tableau récapitule les différentes définitions proposées par les sociétés savantes. Celles de l’ESC (2022) sont les plus couramment utilisées : FEVG inférieure à 50 % (quelle que soit la modalité d’imagerie utilisée) avec une baisse d’au moins 10 % par rapport à la valeur préthérapeutique ; baisse du strain global longitudinal (SGL) échocardiographique supérieure à 15 % par rapport à la valeur de référence (préthérapeutique oncologique) et/ou augmentation des biomarqueurs cardiaques sériques (troponinine supérieure au 99e percentile).2
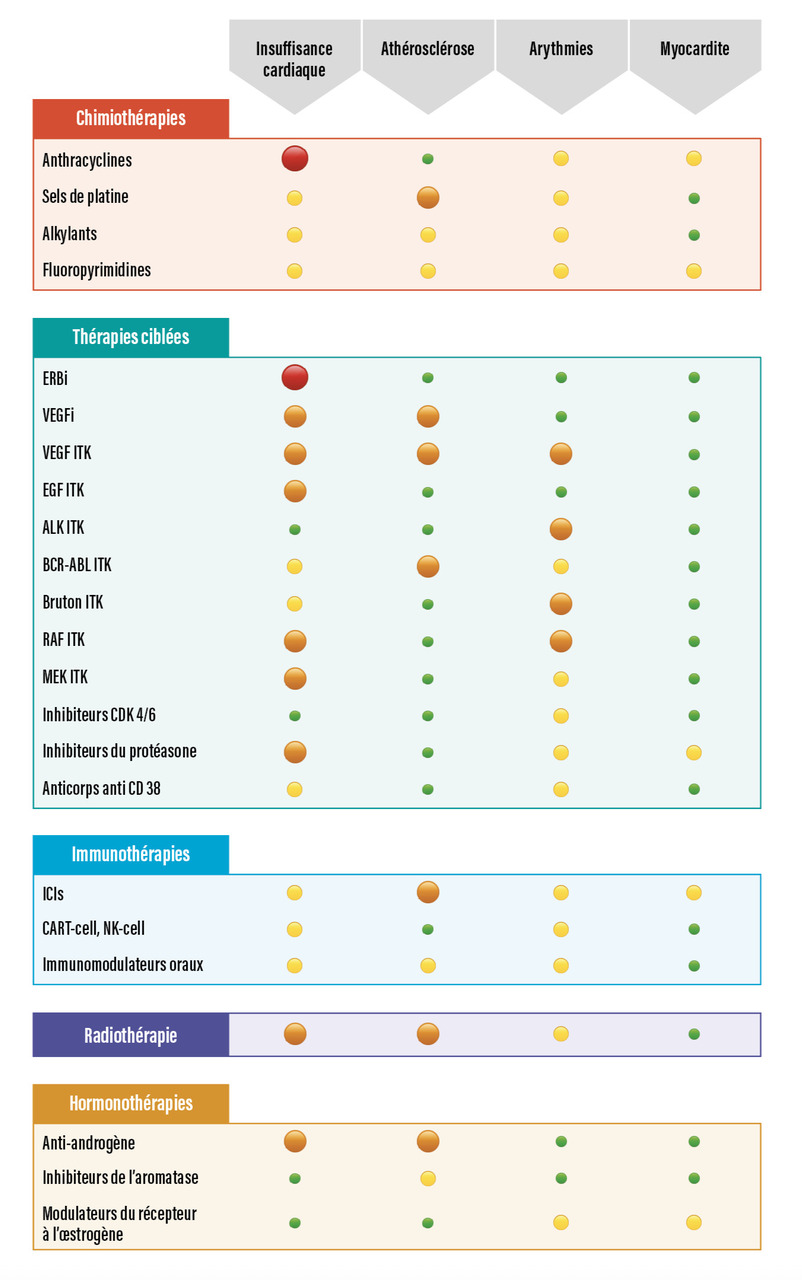
Le diagnostic des toxicités cardiovasculaires induites par les traitements du cancer peut être complexe. Outre les facteurs de risque communs, l’interaction entre cancer et maladies cardiovasculaires, ainsi que la sophistication croissante des traitements, complexifient la discipline de la cardio-oncologie. La figure présente les traitements oncologiques classiquement responsables de cardiotoxicité de type insuffisance cardiaque ou dysfonction ventriculaire asymptomatique.
Prédiction de la cardiotoxicité grâce à des scores
L’identification des facteurs de risque est cruciale pour anticiper la survenue d’une cardiotoxicité. Les principaux facteurs sont de deux types :
- liés au patient : âge (à la fois les enfants et adolescents6,7 et les patients âgés8,9), antécédents de maladies cardiovasculaires, hypertension artérielle, diabète, dyslipidémie, obésité et tabagisme.9 Ces derniers correspondent aux facteurs de risque cardiovasculaire d’athérosclérose du patient ;
- liés au traitement : type d’agent anticancéreux, dose totale cumulée,6,10 mode d’administration et association avec d’autres traitements potentiellement cardiotoxiques. Par exemple, les anthracyclines, telles que la doxorubicine, sont connues pour leur potentiel cardiotoxique dose-dépendant, avec un risque accru d’insuffisance cardiaque au-delà de certaines doses cumulées, et ce dès 100 mg/m2. Le risque augmente lors de la combinaison avec une radiothérapie médiastinale incluant le myocarde. Il s’agit ici du risque de cardiotoxicité attribuable à la molécule ou à la classe thérapeutique anticancéreuse.
Des scores de risque de cardiotoxicité de type insuffisance cardiaque ont été établis pour les grandes classes thérapeutiques,1 incluant les anthracyclines, les thérapies ciblées (inhibant ERB2, VEGF, etc.), les inhibiteurs du protéasome (figure). Ces scores n’étaient que des propositions, car à leur publication ils n’avaient pas fait l’objet de validation par des cohortes indépendantes. Ils ont ensuite été testés, avec une performance variable, par différentes équipes, le plus fréquemment de façon rétrospective.
Le score HFA/IC-OS est performant pour stratifier le risque sous inhibiteurs de tyrosine kinase BCR-ABL,11 anthracyclines,12 et dans la population oncologique générale.13 La capacité du score HFA/IC-OS à discriminer la probabilité de cardiotoxicité s’est avérée modérée sous thérapie ciblant ERB2.14
Il ne s’agit pas à proprement parler de modèles prédictifs9 d’événement cardiovasculaire majeur avec un chiffrage individuel à un délai donné, mais ces scores permettent de classer aisément le patient en risque faible, modéré, élevé ou très élevé de cardiotoxicité.
L’utilisation des scores est facilitée par l’application téléchargeable de l’ESC (https ://urls.fr/cZpSDY).
Détection précoce de la cardiotoxicité
Le diagnostic précoce de cardiotoxicité, avant l’apparition de symptômes et avant la survenue d’événement cardiovasculaire majeur, nécessite le recours à des outils de mesure, que l’on appelle des biomarqueurs.
Quels examens complémentaires ?
En pratique clinique courante, l’échocardiographie transthoracique par la mesure de la FEVG (préférentiellement par méthode tridimensionnelle)15 - 17 et celle du strain global longitudinal18 se situe au premier rang de la cardiodétection chez les patients recevant des traitements de type anthracyclines (doxorubicine, épirubicine, idarubicine), thérapies ciblées anti-ERB2, anciennement appelés anti-HER2 (trastuzumab, pertuzumab, lapatinib). La réalisation d’un électrocardiogramme (ECG) est également recommandée avant l’initiation de tout traitement potentiellement cardiotoxique.2 Les biomarqueurs sériques prennent une place prépondérante, surtout chez les patients à haut risque de cardiotoxicité.1,2
Surveillance variable selon les molécules et le profil du patient
Les dernières recommandations de l’ESC de 2022 établissent des algorithmes de surveillance du risque en utilisant le score HFA/IC-OS.1 À titre d’exemple, un patient à faible risque de cardiotoxicité des anthracyclines ne nécessite qu’une échocardiographie préthérapeutique renouvelée à douze mois du début du traitement, sans recours aux biomarqueurs sériques. En revanche, si le patient est estimé à haut risque ou à très haut risque de cardiotoxicité, une surveillance rapprochée s’avère nécessaire, avec échocardiographie préthérapeutique, puis après deux cures d’anthracyclines, combinée avec des biomarqueurs sériques.2 Le niveau de preuve est faible, cependant, pour recommander fortement ces rythmes de surveillance.
La surveillance échocardiographique sous thérapie ciblée anti-ERB2 (anciennement anti-HER2) est trimestrielle, tel qu’inscrit dans le résumé des caractéristiques du produit (RCP) du médicament en France, mais sans étude qui corrobore ce rythme rapproché. Chez des patients à faible risque de toxicité, sans nocivité par le passé, recevant un traitement anti-ERB2 pour des durées prolongées (par exemple dans le cas du cancer du sein métastatique surexprimant ERB2), la surveillance peut être espacée tous les quatre mois.2
La surveillance est différente chez des patients recevant des inhibiteurs du protéasome pour myélome multiple, essentiellement guidée par des scores de risque différents, axés sur la présence ou non d’amylose cardiaque AL.2
Imagerie de recours : IRM cardiaque
Enfin, en cas d’échogénicité insuffisante, le recours à l’imagerie par résonance magnétique (IRM) est indiqué pour la quantification de la FEVG et de la FEVD.19 L’accélération des séquences d’acquisition et l’amélioration de l’interprétation grâce aux progrès d’algorithmes ayant utilisé l’intelligence artificielle rendent l’accès à la technique plus facile. L’injection de produits gadolinés n’est donc pas nécessaire pour une quantification de la fonction biventriculaire, réduisant la durée de l’examen, et rendant ainsi la technique plus accessible.
Qu’en est-il de la radiothérapie ?
La cardiotoxicité des traitements ionisants (radiothérapie) devrait diminuer nettement grâce à des stratégies de préservation des organes sains. Les patients ayant été traités pour un cancer antérieur peuvent néanmoins présenter une cardiopathie compliquant la radiothérapie, comme une insuffisance cardiaque à FEVG préservée, une coronaropathie, une valvulopathie et/ou une péricardite chronique.
Trois modalités de surveillance
En résumé, la surveillance régulière des patients sous traitement anticancéreux est essentielle pour détecter précocement la cardiotoxicité, selon plusieurs modalités :
- imagerie cardiaque : l’échocardiographie est l’outil de référence pour évaluer la fonction systolique et diastolique du ventricule gauche. La mesure du SGL permet de détecter des altérations infracliniques de la fonction myocardique avant la diminution de la FEVG ;
- biomarqueurs : les dosages de la troponine et du peptide natriurétique de type B (BNP ou NT-pro-BNP) sont utiles pour détecter des lésions myocardiques précoces. Une élévation de ces biomarqueurs peut précéder les modifications observées en imagerie ;
- surveillance électrocardiographique : l’ECG permet de détecter des anomalies de la conduction et des arythmies potentielles induites par les traitements ; la survenue d’anomalies à l’ECG permet de prédire la survenue ultérieure de cardiotoxicité de type insuffisance cardiaque. Les progrès apportés par l’intelligence artificielle permettraient de généraliser l’utilisation de l’ECG pour le dépistage de la cardiotoxicité.
Une détection précoce permet une intervention rapide, telle que l’ajustement du traitement oncologique ou l’introduction de thérapies cardioprotectrices, afin de prévenir l’évolution vers une insuffisance cardiaque symptomatique.
Prévention et traitement de la cardiotoxicité
Équilibration de la cardiopathie ou des facteurs de risque cardiovasculaire préexistants
Les recommandations de prévention primaire cardiovasculaire doivent être appliquées chez tous les patients ayant un cancer, surtout s’ils sont à risque de développer une cardiotoxicité sous traitement oncologique. Seuls les patients avec une espérance de vie limitée, recevant des soins palliatifs de confort, ne font pas l’objet d’une optimisation thérapeutique cardiovasculaire globale avant traitement oncologique.2
La base de la prévention de la cardiotoxicité des traitements oncologiques est un contrôle des facteurs de risque cardiovasculaire classiques, encore largement sous-estimés en pratique clinique. L’équilibration de l’hypertension artérielle préexistante est essentielle pour limiter le risque de cardiotoxicité ultérieure. L’optimisation thérapeutique en cas d’antécédent de cardiopathie ou d’insuffisance cardiaque avec le recours aux quatre classes thérapeutiques (bloqueurs du système rénine-angiotensine, bêtabloquants, gliflozines, spironolactone) est essentielle en cas d’insuffisance cardiaque à FEVG altérée. Il faut s’assurer de la récupération au moins partielle (FEVG supérieure à 40 %) et de l’absence de décompensation récente avant d’initier un traitement oncologique potentiellement cardiotoxique.
Pour les patients diabétiques, l’introduction de gliflozines (SGLT2i) avant un traitement potentiellement cardiotoxique paraît fondamentale. Une récente méta-analyse portant sur 13 études et plus de 80 000 participants a démontré que les gliflozines chez des patients ayant un cancer avaient un effet protecteur contre la survenue d’insuffisance cardiaque et d’hospitalisation pour insuffisance cardiaque. La population qui en bénéficiait le plus était les femmes traitées par anthracyclines pour cancer du sein.20
Pour les patients présentant un SCORE2 (outil de référence européen pour l’évaluation du risque cardiovasculaire) élevé,21 l’introduction de statines en prévention primaire cardiovasculaire devrait être appliquée. De surcroît, une récente étude suggère l’intérêt des statines en prévention primaire de la dysfonction ventriculaire gauche chez les patients traités par anthracyclines.22
Enfin, l’hygiène de vie, notamment le sevrage d’une intoxication tabagique, la minoration de la consommation d’alcool, une alimentation équilibrée et l’exercice physique, devrait être encouragée. Et ce quel que soit le type de cancer, si l’espérance de vie attendue est supérieure à un an. Plusieurs études ont démontré l’intérêt de l’activité physique, de loisirs ou médicalement encadrée, pendant et après la prise en charge multimodale du cancer, notamment pour le cancer du sein et le cancer du côlon.
Modification des protocoles thérapeutiques oncologiques
Le recours à un traitement anticancéreux aussi efficace mais moins cardiotoxique doit être privilégié de façon systématique, notamment chez les patients à haut risque ou à très haut risque de cardiotoxicité. À titre d’exemple, la réduction des doses cumulées d’anthracyclines, les techniques de préservation des organes sains en radiothérapie, le fractionnement des doses ainsi que la durée d’infusion de la chimiothérapie potentiellement cardiotoxique peuvent être mis en place pour l’ensemble des patients et réduire ainsi le risque de cardiotoxicité à l’échelle de la population.
Le recours à un traitement moins cardiotoxique mais moins efficace sur le plan oncologique n’est envisageable qu’après la survenue d’une cardiotoxicité aiguë avec des signes de gravité (FEVG inférieure à 40 %, sans récupération, hospitalisation pour insuffisance cardiaque).
La réduction des doses cumulées d’agents cardiotoxiques, l’utilisation de schémas d’administration fractionnée et la substitution par des médicaments moins toxiques lorsque cela est possible sont aussi importantes pour réduire la cardiotoxicité.
Intérêt de la cardioprotection pharmacologique en prévention primaire de la cardiotoxicité ?
Le recours au traitement classique de l’insuffisance cardiaque a été étudié chez des patients non hypertendus en prévention primaire, notamment lors de l’administration d’anthracyclines. Les classes thérapeutiques les plus étudiées ont été les bloqueurs du système rénine-angiotensine (inhibiteur de l’enzyme de conversion ou bloqueur du récepteur de l’angiotensine) et les bêtabloquants, avec des données discordantes. Aujourd’hui, il n’est pas recommandé de façon robuste d’entreprendre un traitement pharmacologique en prévention primaire, surtout chez les patients classés comme étant à faible risque de toxicité.
Le recours aux inhibiteurs du SGLT2 (patients diabétiques de type 2) ou aux statines (dyslipidémie et/ou haut risque cardiovasculaire), lorsqu’il existe une indication en prévention primaire, demeure néanmoins indiqué chez le patient avec cancer.
Des traitements spécifiques peuvent aussi être administrés en oncologie pour limiter la toxicité des anthracyclines, surtout si les doses totales cumulées sont importantes, notamment pour un deuxième cancer. Le recours au dexrazoxane, chélateur du fer, est possible.
Activité physique et réadaptation cardiaque
Les traitements systémiques anticancéreux réduisent la capacité cardiorespiratoire. L’activité physique est bénéfique en matière de risque cardiovasculaire, de qualité de vie et de survenue de cancer, notamment du sein.23 Les modalités d’activité physique, supervisée ou non, ont varié d’une étude à l’autre. L’American Heart Association préconise la mise en place de programmes de réhabilitation cardiaque dédiés aux patients ayant été traités pour cancer, et non uniquement pour le cancer du sein ou du côlon.24 Actuellement, il existe suffisamment de données dans la littérature pour valider l’intérêt de la réadaptation cardiologique au décours du traitement par cancer du sein, à l’instar des protocoles de réadaptation après syndrome coronarien aigu ou pour insuffisance cardiaque.
Suivi après le cancer
La prise en charge holistique du patient avec cancer ne se termine pas à la fin du traitement systémique ou par radiothérapie. Les traitements par des cardiotoxiques potentiels augmentent le risque cardiovasculaire pour le reste de la vie, qu’il s’agisse de survenue d’insuffisance cardiaque ou de pathologie coronarienne. Les adultes ayant été traités au cours de leur enfance ou adolescence par des traitements potentiellement cardiotoxiques sont ainsi à haut risque de pathologie cardiovasculaire prématurée.7 De tels antécédents doivent alerter les praticiens, pour un adressage rapide en cas de point d’appel clinique.
Identifier les patients à risque
La cardiotoxicité liée aux traitements anticancéreux constitue une complication sérieuse qui nécessite une attention particulière. Une approche multidisciplinaire impliquant les médecins généralistes, les oncologues, les cardiologues et les autres professionnels de santé est essentielle pour une prise en charge optimale. L’identification des patients à risque, la mise en œuvre de stratégies préventives efficaces – au premier rang desquelles le contrôle des facteurs de risque cardiovasculaire, y compris la sédentarité – et une surveillance étroite permettent de minimiser les effets indésirables cardiovasculaires et d’améliorer la qualité de vie des patients atteints de cancer tout au long de leur vie.
2. Lyon AR, Lopez-Fernandez T, Couch LS, et al. 2022 ESC Guidelines on cardio-oncology developed in collaboration with the European Hematology Association (EHA), the European Society for Therapeutic Radiology and Oncology (ESTRO) and the International Cardio-Oncology Society (IC-OS): Developed by the task force on cardio-oncology of the European Society of Cardiology (ESC). Eur Heart J 2022;43(41):4229-361.
3. Baldassarre LA. Ganatra S, Lopez-Mattei J, et al. Advances in multimodality imaging in cardio-oncology. J Am Coll Cardiol 2022;80(16):1560-78.
4. Attia ZI, Kapa S, Lopez-Jimenez F, et al. Screening for cardiac contractile dysfunction using an artificial intelligence–enabled electrocardiogram. Nat Med 2019;25(1):70-4.
5. Jacobs JEJ, Greason G, Mangold KE, et al. Artificial intelligence electrocardiogram as a novel screening tool to detect a newly abnormal left ventricular ejection fraction after anthracycline-based cancer therapy. Eur J Prev Cardiol 2024;31(5):560-6.
6. Haddy N, Diallo S, El-Fayech C,et al. Cardiac diseases following childhood cancer treatment: Cohort study. Circulation 2016;133(1):31-8.
7. Leerink JM, van der Pal HJH, Kremer LCM, et al. Refining the 10-Year prediction of left ventricular systolic dysfunction in long-term survivors of childhood cancer. JACC CardioOncol 2021;3(1):62-72.
8. Saiki H, Petersen IA, Scott CG, et al. Risk of heart failure with preserved ejection fraction in older women after contemporary radiotherapy for breast cancer. Circulation 2017;135(15):1388-96.
9. Abdel-Qadir H, Thavendiranathan P, Austin PC, et al. Development and validation of a multivariable prediction model for major adverse cardiovascular events after early stage breast cancer: A population-based cohort study. Eur Heart J 2019;40(48):3913-20.
10. Feijen EAM, Font-Gonzalez A, Van der Pal HJH, et al. Risk and temporal changes of heart failure among 5‐Year childhood cancer survivors: A DCOG‐LATER study. J Am Heart Assoc 2019;8(1):e009122.
11. Di Lisi D, Moreo A, Casavecchia G, et al. Atrial strain assessment for the early detection of cancer therapy-related cardiac dysfunction in breast cancer women (The STRANO study: Atrial strain in cardio-oncology). J Clin Med 2023;12(22):7127.
12. Rivero-Santana B, Saldana-Garcia J, Caro-Codon J, et al. Anthracycline-induced cardiovascular toxicity: Validation of the Heart Failure Association and International Cardio-Oncology Society risk score. Eur Heart J 2025;46(3):273-84.
13. Gynnild M, Vinje V, Holtrop J, et al. External validation of the HFA-ICOS risk stratification tool for prediction of cardiovascular complications after cancer treatment. Eur Heart J 2024;45(1):ehae666.2693.
14. Cronin M, Crowley A, Davey MG, et al. Heart Failure Association-International Cardio-Oncology Society risk score validation in HER2-positive breast cancer. J Clin Med 2023;12(4):1278.
15. Walker J, Bhullar N, Fallah-Rad N, et al. Role of three-dimensional echocardiography in breast cancer: Comparison with two-dimensional echocardiography, multiple-gated acquisition scans, and cardiac magnetic resonance imaging. J Clin Oncol 2010;28(21):3429-36.
16. Lambert J, Lamacie M, Thampinathan B, et al. Variability in echocardiography and MRI for detection of cancer therapy cardiotoxicity. Heart 2020;106(11):106:817-23.
17. Nazir MS, Okafor J, Murphy T, et al. Echocardiography versus cardiac MRI for measurement of left ventricular ejection fraction in individuals with cancer and suspected cardiotoxicity. Radiol Cardiothorac Imaging 2024;6(1):e230048.
18. Sawaya H, Sebag IA, Plana JC, et al. Assessment of echocardiography and biomarkers for the extended prediction of cardiotoxicity in patients treated with anthracyclines, taxanes, and trastuzumab. Circ Cardiovasc Imaging 2012;5(5):596-603.
19. Addison D, Neilan TG, Barac A, et al. Cardiovascular imaging in contemporary cardio-oncology: A scientific statement from the American Heart Association. Circulation 2023;148(16):1271-86.
20. Bhalraam U, Veerni RB, Paddock S, et al. Impact of sodium–glucose cotransporter-2 inhibitors on heart failure outcomes in cancer patients and survivors: A systematic review and meta-analysis. Eur J Preventive Cardiol 2026;33:214-26.
21. SCORE2 working group and ESC Cardiovascular risk collaboration, et al. SCORE2 risk prediction algorithms: New models to estimate 10-year risk of cardiovascular disease in Europe. Eur Heart J 2021;42(25):2439-54.
22. Neilan TG, Quinaglia T, Onoue T, et al. Atorvastatin for anthracycline-associated cardiac dysfunction: The STOP-CA randomized clinical trial. JAMA 2023;330(6):528-36.
23. Kehm RD, Genkinger JM, MacInnis RJ, et al. Recreational physical activity is associated with reduced breast cancer risk in adult women at high risk for breast cancer: A cohort study of women selected for familial and genetic risk. Cancer Res 2020;80(1):116-25.
24. Gilchrist SC, Barac A, Ades PA, et al. Cardio-oncology rehabilitation to manage cardiovascular outcomes in cancer patients and survivors: A scientific statement from the American Heart Association. Circulation 2019;139(21):e997-e1012.
25. Plana JC, Galderisi M, Barac A, et al. Expert consensus for multimodality imaging evaluation of adult patients during and after cancer therapy: A report from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. J Am Soc Echocardiogr 2014;27(9):911-39.
26. Armenian SH, Laccetti C, Barac A, et al. Prevention and monitoring of cardiac dysfunction in survivors of adult cancers: American Society of Clinical Oncology clinical practice guideline. J Clin Oncol 2017;35(8):893-911.
27. Curigliano G, Lenihan D, Fradley M, et al. Management of cardiac disease in cancer patients throughout oncological treatment: ESMO consensus recommendations. Ann Oncol 2020;31(2):171-90.
28. Travers S, Alexandre J, Baldassarre LA, et al. Diagnosis of cancer therapy-related cardiovascular toxicities: A multimodality integrative approach and future developments. Arch Cardiovasc Dis 2025;118(3):185-98.