Les douleurs chroniques sont fréquentes en population générale. Parmi elles, les douleurs neuropathiques peuvent représenter un véritable défi tant diagnostique que thérapeutique. Si les bons outils sont utilisés, il n’est cependant pas si complexe, en réalité, de reconnaître ces douleurs, même quand le contexte ne s’y prête pas. Il est également tout à fait possible de les prendre en charge en médecine de ville, tout au moins pour l’initiation et le suivi des traitements de première, voire de seconde intention.
Un diagnostic souvent tardif
La douleur est définie comme une expérience sensorielle et émotionnelle désagréable associée ou ressemblant à celle associée à une lésion tissulaire réelle ou potentielle. La douleur est dite neuropathique lorsqu’elle est causée par une lésion ou une maladie du système somato-sensoriel. Il peut s’agir d’une atteinte du système nerveux périphérique ou central.1
Fréquence accrue chez les femmes et après 50 ans
Estimer l’incidence et la prévalence de la douleur neuropathique en population générale a longtemps été complexe, en raison de l’absence de critères diagnostiques universels applicables à grande échelle. En soins primaires, le diagnostic est souvent tardif après le début des troubles.2 En 2008, la prévalence en population générale, en France, a été estimée à 7 % (5 % pour les douleurs d’intensité modérée à sévère).3,4 Une large étude française plus récente, fondée sur les données de l’Assurance maladie, a confirmé ces résultats.5 Ces douleurs sont plus fréquentes chez les femmes (8 % contre 6 % chez les hommes) et les personnes âgées de plus de 50 ans (9 % contre 6 % avant l’âge de 50 ans). Elles ont un impact significatif sur la qualité de vie, entraînant des troubles du sommeil, de l’humeur et une diminution de la capacité physique. Elles constituent une charge importante pour le système de santé,2 car les patients souffrant de douleurs neuropathiques chroniques consultent plus fréquemment des spécialistes et utilisent davantage de traitements médicamenteux que ceux atteints de douleurs chroniques non neuropathiques.
Deux types de cause : périphérique ou centrale
Pour les lésions nerveuses périphériques, les causes les plus souvent rencontrées en France sont les suivantes :
- douleurs neuropathiques consécutives à la lésion d’un nerf périphérique (souvent causée par un traumatisme ou une intervention chirurgicale) ;
- polyneuropathies douloureuses (diabétiques et non diabétiques) ;
- douleurs post-zostériennes ;
- radiculopathies (sciatalgies, névralgies cervico-brachiales) ;
- névralgie du trijumeau.
Concernant les lésions du système nerveux central, les causes les plus fréquentes sont les douleurs liées à :
- la sclérose en plaques ;
- des lésions médullaires ;
- un accident vasculaire cérébral ;
- un traumatisme crânien.
Les médecins de ville sont en première ligne pour repérer et initier un traitement afin de prendre en charge précocement le patient douloureux.
Les principales causes des douleurs neuropathiques rencontrées en médecine de ville sont présentées dans le tableau 1.
Quand évoquer le diagnostic ?
La douleur neuropathique a des caractéristiques cliniques bien particulières. Elle est décrite le plus souvent comme une sensation de brûlure, de piqûre, de décharges électriques, d’étau ou de froid douloureux. Elle est souvent associée à des sensations anormales, désagréables (dysesthésies) ou non (paresthésies). Elle peut être spontanée, survenant en l’absence de stimulus, ou provoquée par un stimulus sensitif (toucher, froid…), la douleur provoquée étant souvent associée aux douleurs spontanées.7
À l’examen clinique peuvent être notamment mises en évidence une hypoesthésie à diverses modalités (thermique, mécanique, vibratoire) dans la zone douloureuse, une allodynie (douleur en réponse à un stimulus habituellement non douloureux) et une hyperalgésie (augmentation de la réponse à un stimulus habituellement douloureux).
Pour dépister aisément les douleurs neuropathiques, notamment en soins primaires, plusieurs questionnaires diagnostiques ont été développés depuis environ vingt ans. Le plus largement utilisé et recommandé en France, validé sur une cohorte de patients français en 2005, est le questionnaire DN4 (douleur neuropathique en 4 questions),8 qui comporte 10 items cliniques (symptômes et signes) et dont la sensibilité et la spécificité sont excellentes (tableau 2). Une version plus courte ne comprenant pas d’examen clinique (DN4 interrogatoire) a également été validée et permet son utilisation par des non-médecins, par le patient lui-même et sur de larges cohortes de patients.9
Pour compléter le bilan lésionnel d’une douleur neuropathique et aboutir à un diagnostic de certitude, les questionnaires peuvent s’avérer insuffisants. Ainsi, le contexte d’apparition de la douleur (par exemple, le diabète dans le cadre d’une neuropathie sensitive, la chirurgie ayant précédé la douleur, la notion d’accident vasculaire cérébral…), son territoire cutané (qui correspond le plus souvent à l’aire neuro-anatomique du nerf, de la racine lésée ou au territoire correspondant à une lésion centrale), la mise en évidence d’une lésion à l’origine de la douleur qui dépend du contexte (électromyogramme, biopsie cutanée, potentiels évoqués, image-rie…) peuvent être nécessaires pour confirmer la lésion ou la maladie du système nerveux somato-sensoriel expliquant la douleur.
Quel traitement proposer en médecine de ville et à quels patients ?
Les douleurs neuropathiques sont difficiles à traiter et répondent habituellement peu aux analgésiques courants (paracétamol, anti-inflammatoires non stéroïdiens, codéinés).11,12 En médecine de ville, il est tout à fait possible de combiner des approches pharmacologiques et non pharmacologiques.
Traiter la cause, quand c’est possible
En premier lieu, il convient, après le diagnostic, de tenter de déterminer si la cause de la douleur peut être traitée. Ceci est possible, par exemple, dans les neuropathies associées à certaines maladies de système, dans les douleurs de la sclérose en plaques ou dans la neuropathie diabétique douloureuse. Cependant, la plupart du temps, le traitement de la cause est impossible ou n’a aucun impact sur la douleur. La prise en charge des douleurs neuropathiques est donc avant tout symptomatique.
Traitement symptomatique d’effet souvent partiel
Les classes thérapeutiques les plus efficaces dans les douleurs neuropathiques périphériques et centrales recommandées en première intention sont certains antidépresseurs et antiépileptiques. Contrairement à la douleur aiguë, ces traitements n’ont que rarement un effet complet sur l’intensité douloureuse et ne réduisent pas nécessairement tous les symptômes douloureux (brûlure, décharges électriques, etc.). Ils ne sont pas non plus efficaces chez tous les patients, mais pour environ la moitié d’entre eux. Il est impératif de les initier à doses faibles et d’augmenter les doses par paliers, environ tous les quatre à sept jours selon la tolérance et l’efficacité, jusqu’à obtenir un effet analgésique (pour les doses, voir le tableau 3). Il peut être nécessaire de les combiner pour optimiser leur efficacité. En général, il est nécessaire d’attendre au moins un mois avant de juger de leur effet. Si l’efficacité est bonne (au moins 50 % d’effet sur la douleur), ces traitements doivent être maintenus au moins six mois aux mêmes doses, puis il est possible de tenter de réduire progressivement les posologies pour trouver la dose minimale efficace, voire les arrêter. Dans tous les cas, il ne faut jamais interrompre ces traitements brutalement.
Antidépresseurs à doses progressives
Les antidépresseurs n’ont pas tous la même efficacité : les principales molécules efficaces sont les inhibiteurs de la recapture de la sérotonine et de la noradrénaline (IRSNa) et les antidépresseurs tricycliques. La duloxétine et la venlafaxine sont les deux antidépresseurs IRSNa les plus prescrits dans le traitement des douleurs neuropathiques. Leur efficacité antalgique est indépendante de leur effet sur l’humeur et porte sur les douleurs continues et paroxystiques (décharges électriques, coups de couteau). Seule la duloxétine dispose d’une autorisation de mise sur le marché (AMM) en analgésie (tableau 3). Cependant, ces traitements étant aussi proposés pour le traitement de la dépression et des troubles anxieux, leur prescription en ville pour les douleurs neuropathiques est facilitée, dans la mesure où ces patients ont très souvent des comorbidités anxieuses ou dépressives. Les effets indésirables de la duloxétine sont surtout digestifs, et il est préférable de ne pas la prendre à jeun et de débuter à doses faibles. Certaines interactions médicamenteuses sont à prendre en compte, comme la prise d’anticoagulants oraux. La venlafaxine peut provoquer des augmentations tensionnelles à fortes doses. Les troubles sexuels et de la libido sont également fréquents. Une hyponatrémie est possible, surtout chez la personne âgée polymédiquée.
Les antidépresseurs tricycliques les plus utilisés en analgésie sont l’amitriptyline et la clomipramine, qui disposent toutes deux d’une AMM pour les douleurs neuropathiques. Leur intérêt est d’agir également sur d’autres pathologies douloureuses : traitement de fond de la migraine pour l’amitriptyline et effet anxiolytique (notamment antipanique) pour la clomipramine à faibles doses. Les doses efficaces en analgésie sont le plus souvent nettement inférieures aux doses antidépressives (tableau 3). La somnolence est fréquente : il faut donc prescrire une prise tardive le soir (après 20 h), notamment pour l’amitriptyline. Ces traitements ont de nombreux autres effets indésirables (tableau 3), et il convient d’éviter d’utiliser des doses élevées (supérieures à 75 mg/j) chez la personne âgée ou fragile.
Antiépileptiques dans des cas bien définis
Les antiépileptiques gabapentine et prégabaline sont efficaces dans le traitement des douleurs neuropathiques et possèdent une AMM dans cette indication. Leur efficacité concerne les douleurs continues et paroxystiques, ainsi que l’allodynie. Leur grand avantage par rapport aux antidépresseurs, et notamment à la duloxétine, est l’absence d’interactions pharmacologiques. En revanche, ils peuvent induire somnolence, impression vertigineuse et prise de poids, ainsi que des œdèmes périphériques, dose-dépendants. Leur élimination étant rénale, leur posologie doit être réduite en cas d’insuffisance rénale, même modérée (risques de surdosage notamment chez les personnes âgées qui présentent souvent une insuffisance rénale fonctionnelle) ; une vérification de la clairance de la créatinine, si elle n’est pas obligatoire, est donc recommandée. Ces dernières années, de nombreux cas de mésusage ont été rapportés avec ces traitements, notamment concernant la prégabaline. De ce fait, elle doit être prescrite sur une ordonnance sécurisée et est désormais recommandée en seconde intention par la Société française d’étude et de traitement de la douleur depuis 2020 en France (sa place reste de première intention dans les recommandations internationales).11
Outre ces antiépileptiques, la carbamazépine est le traitement de première intention de la névralgie essentielle du trijumeau, une douleur neuropathique bien particulière, dont le traitement diffère de celui des autres douleurs, du fait de ses mécanismes spécifiques.
Topiques anesthésiques locaux si la zone douloureuse est bien délimitée
Si la douleur est neuropathique périphérique et la zone douloureuse bien limitée, il est possible de recourir à des topiques anesthésiques locaux. Le traitement de référence consiste en des emplâtres de lidocaïne 5 %, qui bénéficient d’une AMM dans la douleur neuropathique post-zostérienne. Cependant, ce traitement est également efficace dans d’autres douleurs neuropathiques périphériques, en particulier post-chirurgicales. L’avantage de ce traitement est une innocuité presque absolue, permettant son utilisation en gériatrie ou chez les patients fragiles et polymédiqués. La durée d’application est d’environ douze heures, avec un maximum de trois emplâtres par jour. Le risque essentiel est celui d’une irritation ou d’une allergie cutanée.
Traitements non pharmacologiques en complément
Les traitements pharmacologiques ne sont pas toujours suffisants, surtout si la douleur est très chronique et s’accompagne de comorbidités psychologiques ou psychiatriques, ou d’un déconditionnement musculaire d’effort. Ainsi, les psychothérapies et l’activité physique adaptée (APA) ont leur place très précocement dans le traitement d’une douleur neuropathique, souvent en complément des traitements pharmacologiques.
Il existe un large consensus sur l’intérêt majeur de l’APA dans la douleur chronique, quelle qu’elle soit.13 Sa prescription concerne en réalité un grand nombre de patients souffrant de pathologies chroniques et en affection de longue durée (ALD).
Les psychothérapies, telles que les thérapies psycho-comportementales, sont recommandées, notamment en présence de comorbidités anxiodépressives mais aussi en cas de focalisation excessive sur la douleur, ou quand les répercussions fonctionnelles et sociales de la douleur sont très importantes.14
Quelles sont les autres options thérapeutiques ?
Plusieurs autres options thérapeutiques peuvent être envisagées, mais jamais en première ligne.
Opiacés en dernier recours
Les opiacés forts sont recommandés par les sociétés savantes en dernière intention dans les douleurs neuropathiques.11 Il est préférable de les éviter en médecine de ville, sauf cas particulier (douleurs neuropathiques associées à un cancer évolutif) ou de les prescrire en dernier recours sous forme de morphine retard ou de patchs de fentanyl, à doses faibles, et en tenant compte du profil des patients. Le risque addictif est majeur au long cours, surtout si les doses sont élevées, si le patient est de sexe masculin, jeune, aux antécédents d’abus ou de dépendance à d’autres substances psychoactives (y compris tabac et alcool) et avec une pathologie psychiatrique.
Les morphiniques d’action rapide, notamment le fentanyl transmuqueux, sont à proscrire en médecine de ville dans les douleurs non cancéreuses. En cas de douleur paroxystique, il est préférable de traiter les patients par antidépresseurs ou antiépileptiques et de ne pas chercher à traiter les crises elles-mêmes.
Les opiacés faibles (tramadol, codéine, poudre d’opium) ne sont généralement pas efficaces sur les douleurs neuropathiques, sauf le tramadol du fait d’un effet spécifique sur la recapture des monoamines, à l’instar des antidépresseurs. Ces traitements sont tous à risque addictif.
L’association tramadol-paracétamol, qui contient des doses faibles de tramadol, peut cependant être utile pour soulager certaines crises douloureuses si celles-ci sont peu fréquentes (moins d’une par jour), afin d’éviter le risque d’abus.
La neurostimulation électrique transcutanée réduit la perception de la douleur
La neurostimulation électrique transcutanée (transcutaneous electrical nerve stimulation [TENS]) est une méthode de gestion de la douleur qui utilise des impulsions électriques pour soulager le patient. Des électrodes sont placées sur la peau près de la zone douloureuse et un appareil envoie des signaux électriques pour stimuler les nerfs. Cela peut aider à réduire la perception de la douleur en bloquant les signaux nerveux ou en libérant des endorphines. Sa prescription, qui peut être réalisée en première intention avec ou sans traitement pharmacologique associé, est limitée aux structures spécialisées dans la prise en charge des douleurs chroniques.
Patchs de capsaïcine et toxine botulinique A
La capsaïcine est le principe actif du piment. Utilisée sous forme de patchs de haute concentration (8 %), ce traitement agit en se fixant sur des récepteurs spécifiques (TRPV1) situés sur les fibres nociceptives. Lorsque la capsaïcine est appliquée sur la peau, elle provoque initialement une sensation de chaleur, suivie d’une réduction de la douleur, qui peut durer pendant environ trois mois.
La toxine botulinique A peut être utilisée (en l’absence d’AMM, mais avec autorisation de prescription compassionnelle délivrée en avril 2024 par l’Agence nationale de sécurité du médicament et des produits de santé [ANSM]) pour traiter des douleurs neuropathiques périphériques localisées.
Ces deux traitements, recommandés en deuxième ou troisième intention, font partie de la réserve hospitalière et leur prescription est du ressort du spécialiste.
Cannabinoïdes, pas d’efficacité démontrée
Même si les cannabinoïdes ont fait récemment l’objet d’une expérimentation française coordonnée par l’ANSM, ils ne sont pas à ce jour officiellement recommandés par les sociétés savantes et ne font pas partie de l’algorithme de prise en charge des douleurs neuropathiques, du fait d’études cliniques randomisées contrôlées contre placebo le plus souvent négatives.11 On ne peut cependant exclure qu’un sous-groupe de patients puisse en bénéficier.
Stimulation magnétique transcrânienne répétitive dans des cas de douleurs très réfractaires
La stimulation magnétique transcrânienne répétitive (repetitive transcranial magnetic stimulation [rTMS]) est une technique de neurostimulation centrale non invasive qui, en analgésie, consiste à stimuler le cortex moteur sans déclencher de mouvements. Son effet analgésique est obtenu par la modulation de plusieurs régions cérébrales distantes impliquées dans le traitement ou le contrôle des signaux nociceptifs. L’effet analgésique peut durer plusieurs semaines après la réalisation de plusieurs séances. Ce traitement, qui n’a pas d’AMM ni de reconnaissance d’acte thérapeutique à ce jour en France, s’effectue dans certaines structures de prise en charge de la douleur chronique, pour des patients ayant des douleurs neuropathiques très réfractaires.
Stimulation médullaire, réduction de la perception de la douleur
La stimulation médullaire semble influencer les mécanismes de contrôle segmentaires et descendants de la douleur. Cette technique est utilisée pour soulager la douleur chronique en appliquant des impulsions électriques à la moelle épinière, via une électrode implantée. Cette stimulation modifie la transmission des signaux de douleur au cerveau, réduisant ainsi la perception de la douleur. Elle est recommandée pour des patients vivant avec une douleur neuropathique réfractaire, en particulier ceux avec une neuropathie diabétique douloureuse ou une lomboradiculalgie chronique.
Techniques complémentaires de lutte contre la douleur
Ces techniques, dont le niveau de preuve est moindre dans les douleurs neuropathiques que celui des autres traitements, incluent notamment hypnose, relaxation, yoga, méditation de pleine conscience et acupuncture. Elles ont l’avantage d’une bonne tolérance et d’un faible coût. Elles sont proposées par certaines structures de prise en charge de la douleur chronique, notamment pour des patients dont la douleur est très chronique, qui se révèlent souvent intolérants ou non-répondeurs aux autres approches thérapeutiques.
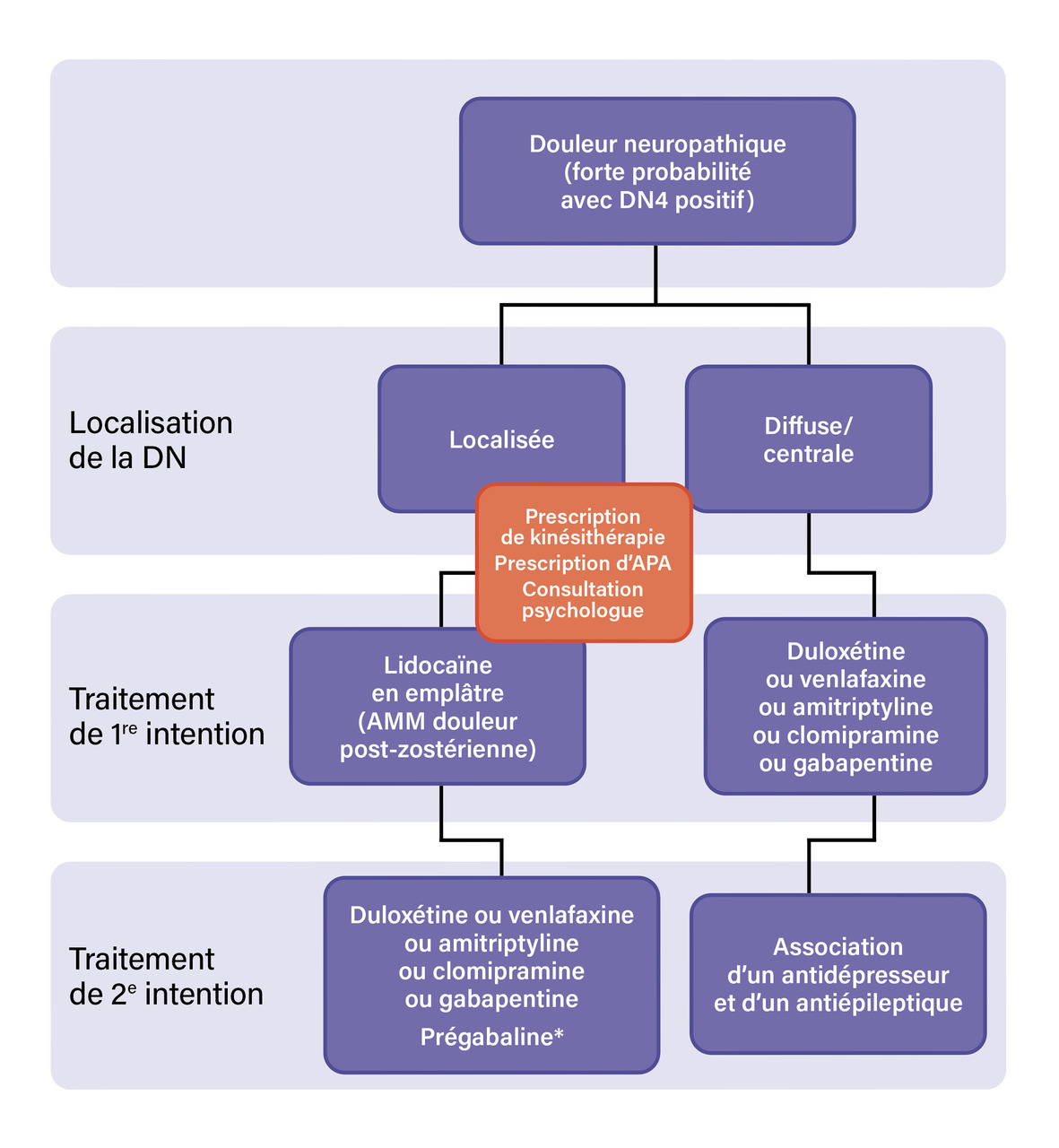
Prise en charge des douleurs neuropathiques en ville en première intention
La prise en charge des douleurs neuropathiques chroniques est tout à fait possible en soins primaires (figure).
Comme pour toute douleur chronique, elle peut intégrer des traitements pharmacologiques et non pharmacologiques.
Le développement de recommandations thérapeutiques fondées sur les preuves cliniques permet de guider les praticiens dans le choix des traitements les plus appropriés pour chaque patient.
L’orientation vers un médecin de la douleur ou vers une structure spécialisée dans la prise en charge de la douleur chronique peut être proposée après échec d’un traitement de deuxième intention.
Messages des médecins de la douleur
Les nombreuses causes (tableau 1) et la fréquence des douleurs neuropathiques impliquent qu’elles soient observées en médecine de ville bien plus souvent que supposé.
Il ne faut pas hésiter à débuter un traitement devant un faisceau d’arguments en faveur d’une douleur neuropathique. Le diagnostic vient souvent par la suite, avec parfois plusieurs années de délai pour certaines lésions.
Il est tout à fait possible de combiner traitement topique et traitement par voie orale.
Il existe maintenant un vaccin remboursé contre le zona aigu et la douleur post-zostérienne (réduction du risque de zona de 80 % environ et de douleurs post-zostériennes de près de 90 % [Cunningham, NEJM 2016]). Cette vaccination est recommandée pour les personnes immunodéprimées âgées de 18 ans et plus, ainsi que pour tous les adultes âgés de 65 ans et plus (y compris ceux qui ont déjà présenté un ou plusieurs épisodes de zona).
Il est relativement aisé de prescrire des antidépresseurs dans le traitement de la douleur neuropathique, malgré l’absence d’AMM pour certains, du fait de la prévalence importante de la dépression et des troubles anxieux chez ces patients.
Les posologies moyennes des traitements de la douleur neuropathique sont rarement à dépasser en médecine de ville ; en cas d’effet insuffisant à ces doses, un relais par un spécialiste ou une structure douleur chronique est souhaitable.
Le rôle souvent très bénéfique de la psychothérapie, de la rééducation fonctionnelle ainsi que de l’activité physique adaptée ne doit pas être négligé.
Il ne faut pas méconnaître le contexte de la crise des opiacés, toujours en cours aux États-Unis, véritable épidémie de dépendance et de surdosage liée à l’usage excessif d’analgésiques opioïdes (oxycodone en majorité), largement prescrits à partir des années 1990. Cette crise a été exacerbée par des pratiques médicales laxistes et une publicité agressive de la part des fabricants. Elle a conduit à l’émergence de millions de personnes dépendantes et à des centaines de milliers de décès. Les efforts pour y remédier incluent des initiatives de prévention, des traitements de désintoxication et des poursuites judiciaires contre les entreprises pharmaceutiques.
Cas clinique
Mme T., âgée de 76 ans, a pour antécédents essentiels une hypertension artérielle traitée par irbésartan, un diabète de type 2 traité par metformine et une gonarthrose bilatérale sévère pour laquelle une intervention chirurgicale est envisagée. Elle pèse 88 kg pour 159 cm. Elle consulte pour des douleurs hémithoraciques gauches.
Elle a présenté une éruption vésiculaire thoracique alors qu’elle était dans sa maison de campagne il y a trois mois, dans un contexte de stress, ayant appris que sa sœur avait un cancer. Elle a cru initialement à des piqûres de moustique et n’a consulté que tardivement (après une semaine) un médecin généraliste dans la région. Celui-ci a fait le diagnostic de zona. Il n’a, à juste titre, pas proposé d’antiviraux compte tenu du délai trop long écoulé après le début du zona (supérieur à soixante-douze heures) et a débuté un traitement par paracétamol et poudre d’opium, puis a revu la patiente après quelques jours. L’effet de ce traitement ayant été insuffisant sur la douleur, il l’a remplacé par de faibles doses de morphine retard, traitement poursuivi pendant trois mois, malgré une efficacité insuffisante.
De retour de la campagne après trois mois, la patiente consulte. La douleur, malgré la cicatrisation de l’éruption et le traitement morphinique, reste insomniante, permanente, décrite comme une brûlure, associée à des démangeaisons insupportables et aggravées par le moindre effleurement de la peau. La patiente n’arrive pas à porter de soutien-gorge. Les caractéristiques de la douleur sont fortement en faveur d’une douleur neuropathique, ce qui, dans le contexte du zona, évoque clairement une douleur post-zostérienne. La patiente dit ne plus supporter la morphine, responsable d’une somnolence diurne et d’une constipation malgré un traitement laxatif, qui ne la soulage que très insuffisamment (10 % d’efficacité). Elle se dit épuisée par la douleur persistante et souhaite éviter des traitements à risque de somnolence et de prise de poids. L’intensité douloureuse est de 7 sur une échelle de 0 à 10.
Un traitement par emplâtres de lidocaïne 5 % (AMM douleur neuropathique post-zostérienne) est envisageable, dans la mesure où la zone douloureuse n’est pas trop étendue. En parallèle, il s’agit de diminuer progressivement la dose de morphine jusqu’à l’arrêt. Si la douleur n’est pas suffisamment soulagée par le traitement local et reste très insomniante, il est possible d’associer au traitement topique de très faibles doses de tricycliques le soir au coucher, par exemple amitriptyline en débutant par trois à cinq gouttes puis en augmentant par paliers de cinq gouttes tous les quatre jours environ, selon la tolérance et l’efficacité sur la douleur. À doses faibles, il y a peu de risques de somnolence et de prise de poids sous amitriptyline.
Avec le traitement par emplâtres de lidocaïne 5 % (deux par jour, laissés en place pendant douze heures dans la journée sur la zone douloureuse) associé à douze gouttes d’amitriptyline le soir au coucher, la douleur n’a pas disparu, mais elle a été améliorée de plus de 50 %. Mme T. reste très affectée par la maladie de sa sœur et accepte un suivi psychologique en ville.
2. Perrot S, Pickering G, Lanteri-Minet M, et al. Real-life management pathways for chronic peripheral neuropathic pain at tertiary pain clinics in France. Pain Med 2021;22(4):875-82.
3. Hall GC, Carroll D, Parry D, et al. Epidemiology and treatment of neuropathic pain: The UK primary care perspective. Pain 2006;122(1‑2):156‑62.
4. Hall GC, Morant SV, Carroll D, et al. An observational descriptive study of the epidemiology and treatment of neuropathic pain in a UK general population. BMC Fam Pract 2 2013;14:28.
5. Attal N, Lanteri-Minet M, Laurent B, et al. The specific disease burden of neuropathic pain: Results of a French nationwide survey. Pain 2011;152(12):2836‑43.
6. Di Stefano G, Falco P, Galosi E, et al. A systematic review and meta‐analysis of neuropathic pain associated with coronavirus disease 2019. Eur J Pain 2023;27(1):44‑53.
7. Colloca L, Ludman T, Bouhassira D, et al. Neuropathic pain. Nat Rev Dis Primer 2017;3(1):1‑19.
8. Attal N, Bouhassira D, Baron R. Diagnosis and assessment of neuropathic pain through questionnaires. Lancet Neurol 2018;17(5):456‑66.
9. Attal N. Pharmacological treatments of neuropathic pain: The latest recommendations. Rev Neurol (Paris) 2019;175(1‑2):46‑50.
10. Bouhassira D, Attal N, Alchaar H, et al. Comparison of pain syndromes associated with nervous or somatic lesions and development of a new neuropathic pain diagnostic questionnaire (DN4). Pain 2005;114(1‑2):29‑36.
11. Moisset X, Bouhassira D, Couturier JA, et al. Traitements pharmacologiques et non pharmacologiques de la douleur neuropathique : une synthèse des recommandations françaises. Douleur et Analgésie 2020;33(2):101‑12.
12. Tosti G, Attal N. Traitement pharmacologique des douleurs neuropathiques. EM Consulte. 22 février 2021. https://urls.fr/UtJyXx
13. Ray BM, Kelleran KJ, Eubanks JE, et al. Relationship between physical activity and pain in U.S. adults. Med Sci Sports Exerc 2023;55(3):497‑506.
14. Williams ACDC, Fisher E, Hearn L, et al. Psychological therapies for the management of chronic pain (excluding headache) in adults. Cochrane Database Syst Rev 2020;8(8):CD007407.

 Encadrés
Encadrés