L’hyponatrémie est définie par une concentration plasmatique en sodium inférieure à 135 mmol/L.
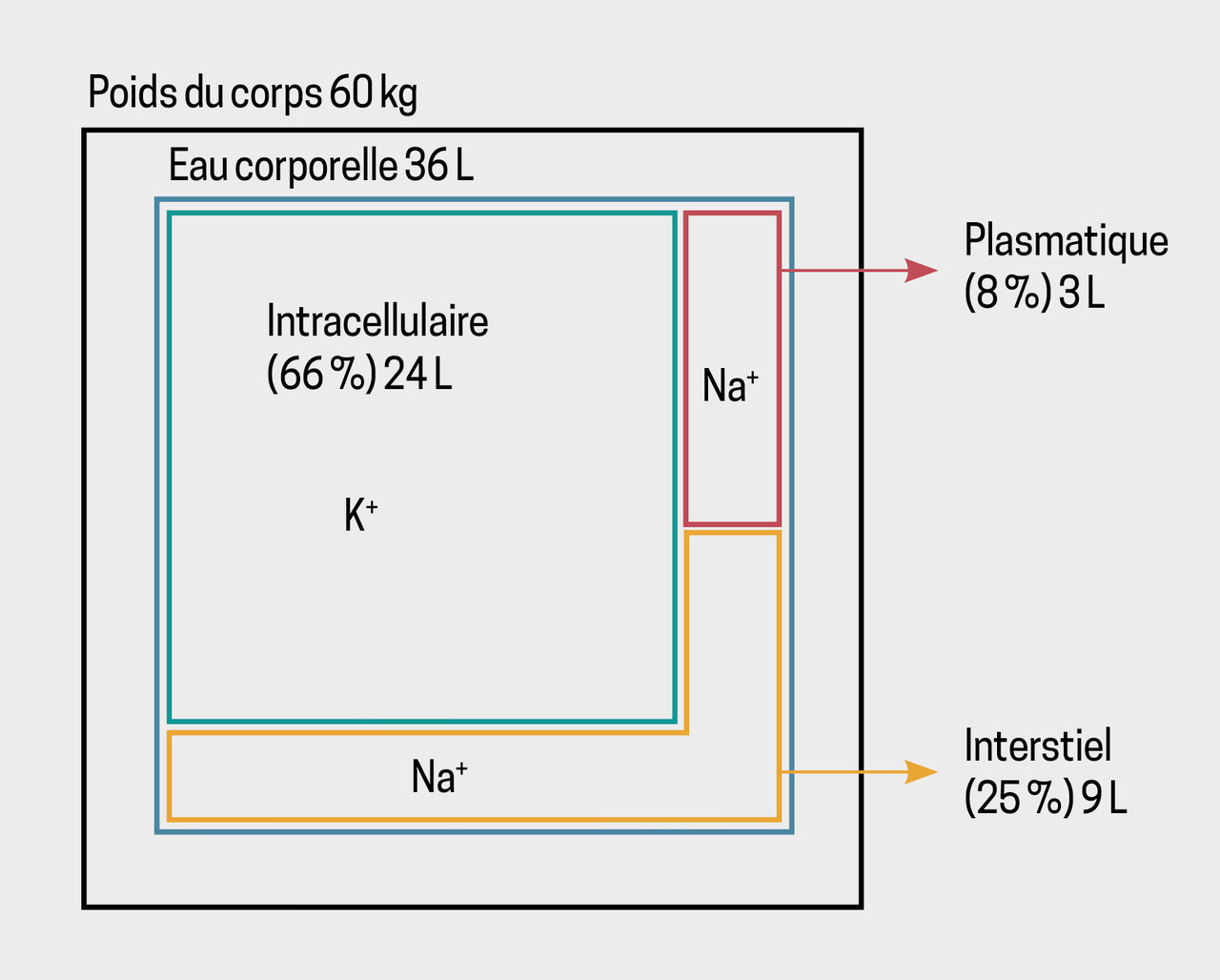
Le corps contient en moyenne 60 % d’eau chez l’homme et 50 % chez la femme, avec la répartition suivante (fig. 1) :1
- 66 % dans le secteur intracellulaire ;
- 33 % dans le secteur extracellulaire, lui-même divisé en compartiments interstitiel (25 % de l’eau corporelle totale) et intravasculaire (8 % de l’eau corporelle totale).
L’osmolalité (quantité d’électrolytes par litre) est identique entre les secteurs. Elle repose principalement sur le sodium en extracellulaire et le potassium en intracellulaire.
L’osmolalité plasmatique, normale entre 275 et 290 mOsmol/L, peut s’estimer grâce à la formule : natrémie (mmol/L) × 2 + glycémie (mmol/L).
La concentration en ions intracellulaires étant stable, une diminution de l’osmolalité reflète une augmentation de l’eau intracellulaire. Ainsi, l’hyponatrémie révèle une hyperhydratation intracellulaire, sauf dans de rares exceptions :
- hyperglycémie avec état hyperosmolaire ;
- hypertriglycéridémies ou hyperprotidémies extrêmes faussant les mesures de quantité de plasma, et donc de natrémie.
L’équilibre hydrosodé se fait au moyen de plusieurs systèmes hormonaux (rénine-angiotensine-aldostérone, hormone antidiurétique [ADH]), du système nerveux sympathique et des peptides natriurétiques (ANP et BNP).
La vasopressine (ADH) permet d’augmenter la réabsorption rénale d’eau et de concentrer les urines. En l’absence de sécrétion d’ADH, les urines sont diluées entre 40 et 100 mOsmol/L. L’ADH est sécrétée en cas de déshydratation intracellulaire et/ou d’hypoperfusion tissulaire.
Repérer les signes cliniques
L’hyponatrémie hypo-osmolaire entraîne des manifestations principalement neurologiques centrales, les neurones étant particulièrement sensibles à l’œdème intracellulaire.2 Leur sévérité dépend de la rapidité d’installation et de la profondeur de l’hyponatrémie.
En cas d’installation aiguë, les nausées et la sensation de malaise apparaissent à partir de 130 mmol/L ; céphalées, obnubilation, coma, convulsions ou engagement cérébral apparaissent à partir de 120 mmol/L.
En cas d’installation chronique, ces signes sont plus rarement présents, même avec des natrémies plus profondes. En effet, en quelques jours, les cellules cérébrales s’adaptent en perdant des électrolytes intracellulaires. Dans ce cas, des signes moins spécifiques apparaissent pour des natrémies inférieures à 120 mmol/L : asthénie, nausées, vomissements, troubles de la marche, troubles cognitifs, crampes, chutes chez la personne âgée. Les complications graves sont beaucoup plus rares.
À l’inverse, le risque clinique, dans ce contexte, est lié à la correction trop rapide de l’hyponatrémie. Il s’agit d’une complication neurologique grave appelée syndrome de démyélinisation osmotique, survenant dans les deux à six jours après correction. Il peut aller de la confusion à la myélinolyse centropontine, évoluant vers un locked-in syndrome (syndrome d’enfermement), qui est alors irréversible.
L’hyponatrémie est associée à une surmortalité chez les patients hospitalisés.3
Principales causes
L’enquête étiologique distingue deux types de situation.4
Hypovolémie efficace avec hypoperfusion tissulaire
Elle peut être liée à :
- une déshydratation extracellulaire ;
- une anasarque (insuffisance cardiaque, cirrhose).
Secteur extracellulaire normal
Dans ce contexte, l’excrétion rénale d’eau peut être :
- adaptée : un excès d’apports hydriques est en cause (potomanie, hydratation intraveineuse, urétroscopie ou hystéroscopie thérapeutique [transurethral resection of the prostate ou TURP syndrome]) ;
- ou inadaptée, du fait :
- de la prise de diurétiques thiazidiques ;
- d’une insuffisance rénale sévère ;
- d’une hypothyroïdie profonde ;
- d’une insuffisance surrénalienne ;
- d’un syndrome d’antidiurèse inappropriée.
Ce dernier peut être dû à :
- une sécrétion inappropriée d’ADH (SIADH) : lésion du système nerveux central (accident vasculaire cérébral, hémorragie, traumatisme, infection) ; lésion pulmonaire (pneumopathie, asthme, tuberculose, insuffisance respiratoire) ;
- un cancer (pulmonaire à petite cellules, ORL, cérébral, neuroblastome olfactif, digestif, génito-urinaire) ;
- des médicaments (inhibiteurs de recapture de la sérotonine, tricycliques, halopéridol, carbamazépine, valproate de sodium, cyclophosphamide, méthotrexate, sels de platine, anti-inflammatoires non stéroïdiens, amiodarone, ciprofloxacine) ;
- des drogues (cathinones et amphétamines) ;
- une chirurgie récente ;
- une origine néphrogénique (mutation activatrice des récepteurs rénaux à l’ADH).
Démarche diagnostique
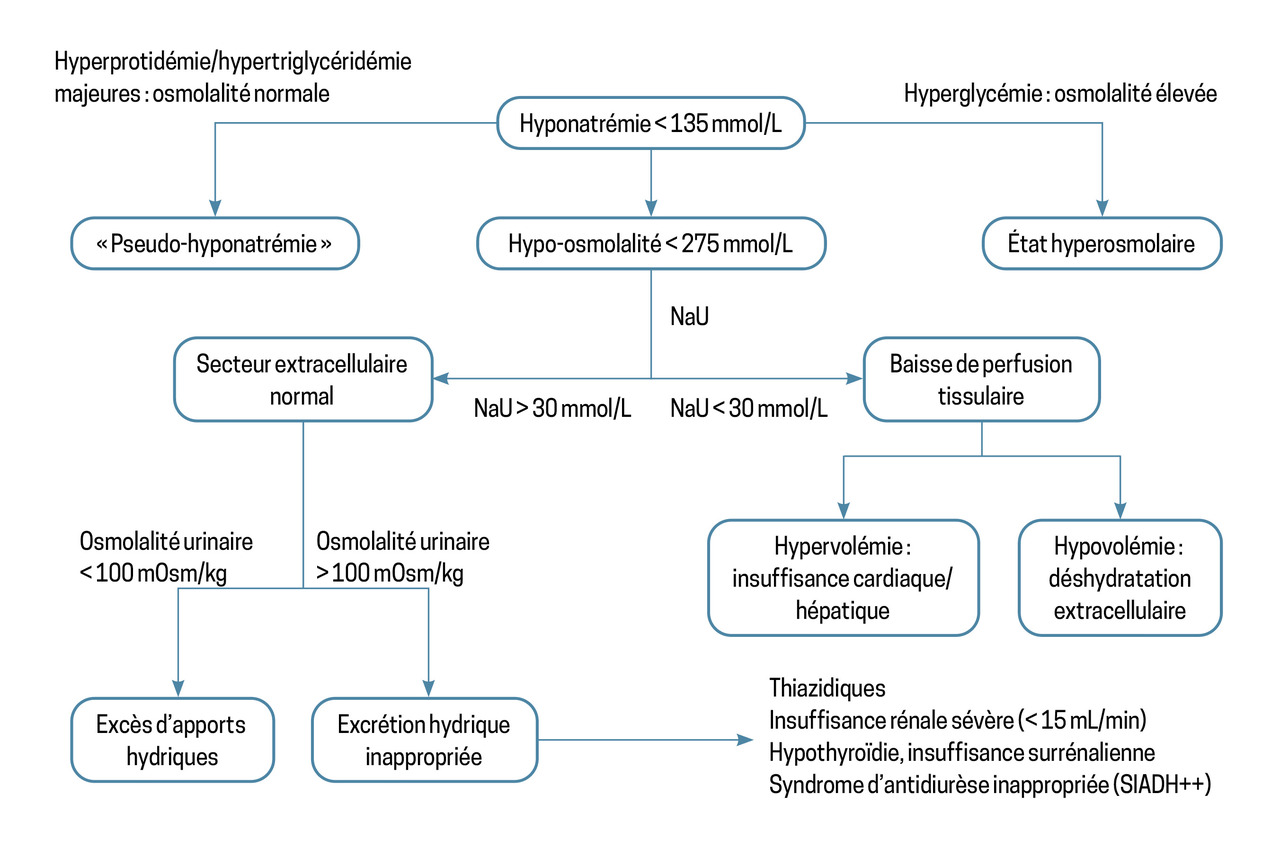
La fig. 2 propose un algorithme à suivre.
En cas d’hyponatrémie inférieure à 135 mmol/L, il est nécessaire de confirmer l’hypo-osmolalité. Un dosage de l’osmolalité plasmatique peut être demandé, mais les causes d’hyponatrémie sans hypo-osmolalité sont rares et facilement identifiables : il peut s’agir d’une hyperglycémie majeure ou d’une hypertriglycéridémie ou hyperprotidémie (pic monoclonal).
Dans les autres cas, l’osmolalité est inférieure à 275 mOsmol/L et il existe une hyperhydratation intracellulaire. L’évaluation du secteur extracellulaire permet de repérer une hypoperfusion tissulaire en recherchant un syndrome œdémateux ; une cause de déshydratation (diarrhée, vomissements), des signes de déshydratation extracellulaire (tachycardie, hypotension, sécheresse muqueuse), une hémoconcentration biologique (protides, hémoglobine) ou une insuffisance rénale aiguë ; un sodium urinaire inférieur à 30 mmol/L.
En l’absence d’hypoperfusion tissulaire, il convient de rechercher une prise excessive d’eau à l’interrogatoire et de mesurer ou calculer l’osmolalité urinaire, qui est alors inférieure à 100 mOsm/L : 2 × (Na urinaire + K urinaire) + urée urinaire (mmol/L).
En l’absence d’apports hydriques excessifs, l’hyponatrémie est liée à une excrétion hydrique inadaptée, dont les causes ont été décrites précédemment.
Ne pas corriger trop rapidement !
La correction d’une hyponatrémie ne doit pas se faire trop rapidement, le risque étant l’apparition du syndrome de démyélinisation osmotique.
Les patients symptomatiques ou avec une hyponatrémie profonde, c’est-à-dire inférieure à 120 mmol/L, doivent être hospitalisés, du fait des risques de complications liées à l’hyponatrémie ou à sa correction.5
Le but du traitement est d’augmenter la natrémie sans dépasser 10 mmol/L par 24 heures à J1 et 8 mmol/L par 24 heures à J2.4
En cas de symptômes sévères (coma, convulsions), la perfusion de NaCl 3 % (150 mL sur 20 minutes) est recommandée, à répéter pour un objectif de 4 à 6 mmol/L d’augmentation.
En l’absence de symptômes sévères, le traitement varie selon la cause :
- perfusion de sérum physiologique (500 à 1 000 mL par 24 heures) en cas d’hypovolémie ;
- déplétion en cas d’anasarque ;
- restriction hydrique (500 mL par 24 heures) en cas d’hyponatrémie isolée ;
- en cas de SIADH et si échec de la restriction hydrique, prescrire furosémide (20 à 60 mg) + apports sodés per os ou prise d’urée per os ;
- si échec, privilégier l’antagoniste spécifique des récepteurs V2 de l’ADH, le tolvaptan (15 à 60 mg/j).
Pour éviter une correction trop rapide de la natrémie, une surveillance biologique rapprochée est nécessaire. Si la correction est trop rapide, l’administration d’un soluté hypotonique et/ou de desmopressine peut être réalisée.
2. Sterns RH. Disorders of plasma sodium--causes, consequences, and correction. N Engl J Med 2015;372(1):55‑65.
3. Holland-Bill L, Christiansen CF, Heide-Jørgensen U, et al. Hyponatremia and mortality risk: A Danish cohort study of 279 508 acutely hospitalized patients. Eur J Endocrinol 2015;173(1):71‑81.
4. Spasovski G, Vanholder R, Allolio B, et al. Clinical practice guideline on diagnosis and treatment of hyponatraemia. Nephrol Dial Transplant 2014;29 Suppl 2:i1‑39.
5. Sterns RH. Treatment of Severe Hyponatremia. Clin J Am Soc Nephrol 2018;13(4):641-9.