Le diabète est devenu depuis quelques années un problème majeur de santé publique, avec un doublement attendu du nombre de patients dans le monde d’ici à 2040. En France, ce sont actuellement 3,3 millions de personnes atteintes. Parmi elles, on estime qu’un tiers développera une rétinopathie diabétique (RD). Son apparition est corrélée à la durée d’évolution du diabète, au niveau de l’hémoglobine glyquée (HbA1c) et à la pression artérielle (PA).
La RD et ses complications potentiellement graves (première cause de cécité avant 50 ans) sera assurément un réel défi pour des médecins déjà surchargés. Des recommandations existent déjà depuis plusieurs années concernant le dépistage et le traitement de la RD. Ces recommandations vont sans doute évoluer rapidement avec l’apparition de nouvelles technologies, en particulier l’intelligence artificielle.
La RD et ses complications potentiellement graves (première cause de cécité avant 50 ans) sera assurément un réel défi pour des médecins déjà surchargés. Des recommandations existent déjà depuis plusieurs années concernant le dépistage et le traitement de la RD. Ces recommandations vont sans doute évoluer rapidement avec l’apparition de nouvelles technologies, en particulier l’intelligence artificielle.
Dépistage
Le dépistage de la rétinopathie chez les patients diabétiques est fondamental pour éviter la survenue de complications pouvant mettre en jeu le pronostic visuel. Des recommandations pour le dépistage et la surveillance des complications oculaires du patient diabétique ont été formulées en 2011 par la Haute Autorité de santé et en 2016 par la Société francophone du diabète et la Société française d’ophtalmologie.1
En pratique, quand dépister la rétinopathie diabétique ?
Un examen ophtalmologique complet doit être réalisé au moment de la découverte du diabète, quel que soit son type.
Chez le diabétique de type 1, le dépistage est ensuite annuel et débuté après la cinquième année de la maladie.
Chez le diabétique de type 2, le dépistage est annuel. Si le patient n’a pas de RD initiale, ne prend pas d’insuline, respecte les objectifs de contrôle glycémique et de pression artérielle, la surveillance peut être effectuée tous les deux ans. Au dernier congrès Euretina, il a même été proposé d’allonger le délai de surveillance à trois ans pour ces patients. En effet, des études récentes ont montré qu’en l’absence de RD et de facteurs de risque, l’évolution vers une forme grave est peu probable avant trois ans.
Chez le diabétique de type 1, le dépistage est ensuite annuel et débuté après la cinquième année de la maladie.
Chez le diabétique de type 2, le dépistage est annuel. Si le patient n’a pas de RD initiale, ne prend pas d’insuline, respecte les objectifs de contrôle glycémique et de pression artérielle, la surveillance peut être effectuée tous les deux ans. Au dernier congrès Euretina, il a même été proposé d’allonger le délai de surveillance à trois ans pour ces patients. En effet, des études récentes ont montré qu’en l’absence de RD et de facteurs de risque, l’évolution vers une forme grave est peu probable avant trois ans.
Comment dépister la rétinopathie diabétique ?
Même si le fond d’œil par biomicroscopie indirecte avec dilatation pupillaire reste pertinent car il s’inscrit dans un bilan ophtalmologique complet, l’accent est mis sur la réalisation de photographies du fond d’œil avec ou sans dilatation pupillaire. Deux rétinographies couleur sur chaque œil, d’au moins 45 °, centrées sur la macula et sur la papille sont recommandées. Ces clichés peuvent être pris lors de campagnes de dépistage par des techniciens non médecins et interprétés de manière différée par un ophtalmologiste (exemple du réseau OPHDIAT en Île-de-France depuis 2008). Cet acte de prise de rétinographie et de lecture à distance du cliché est le premier acte de télémédecine pris en charge par l’Assurance maladie. Il s’adresse aux patients diabétiques âgés de moins de 70 ans, sans RD connue. En présence d’anomalie plus importante qu’une rétinopathie diabétique non proliférante (RDNP) minime (microanévrismes seuls) sur les clichés de dépistage, le patient est adressé chez un ophtalmologue dans un délai réglementaire de deux mois.
Ce mode de dépistage permet de diminuer le nombre de consultations en ophtalmologie mais nécessite toujours du temps médical pour l’interprétation des images. Une solution réside peut-être dans les nouvelles technologies d’intelligence artificielle et d’analyse automatisée de clichés du fond d’œil fondées sur le deep learning. Une étude publiée en novembre 2019 a montré que l’algorithme EyeArt avait une sensibilité et une spécificité de 91 % pour diagnostiquer une RDNP au moins minime.2 Il existe d’autres logiciels de reconnaissance d’images et d’aide au dépistage tels que IDx-DR, ADCIS, OphtAI… Cependant, ces logiciels ont un coût de fonctionnement pour l’instant non pris en charge par l’Assurance maladie.
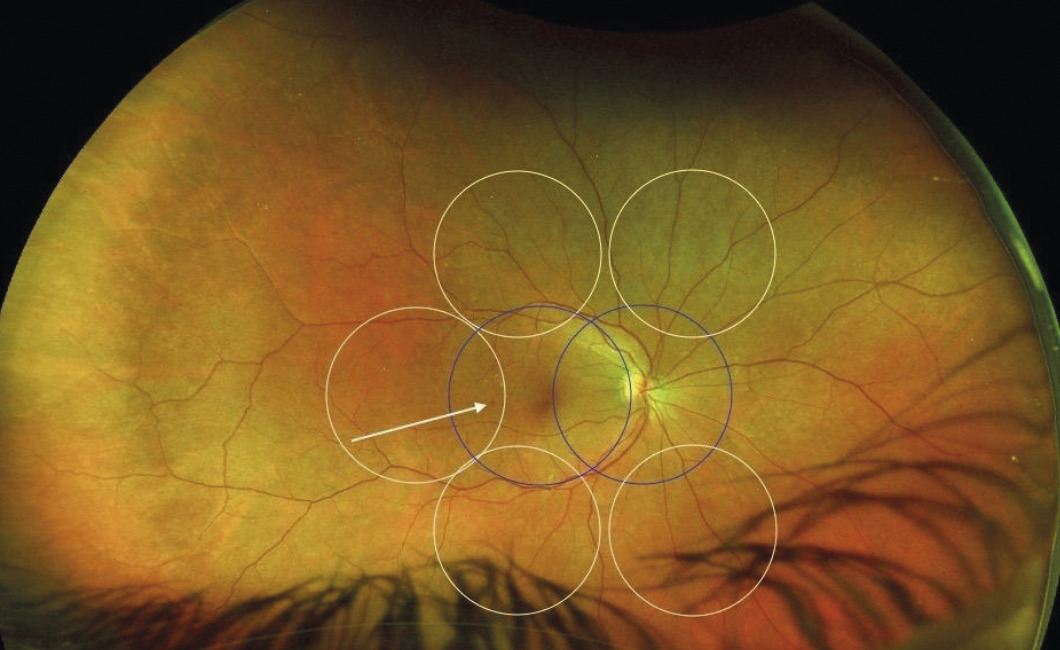
Depuis quelques années, l’utilisation de rétinographes ultra-grand champ pouvant prendre des clichés allant jusqu’à 200 ° se démocratise. Des études ont montré que ce mode d’imagerie est aussi performant pour grader la RD que les sept champs de référence de l’ETDRS (figure ). De plus, il pourrait détecter des lésions rétiniennes périphériques non visibles autrement et ainsi dépister un plus grand nombre de patients atteints de RD.3 Le prix important de ces appareils reste un frein à leur diffusion, et leur utilisation en dépistage reste à préciser.
Ce mode de dépistage permet de diminuer le nombre de consultations en ophtalmologie mais nécessite toujours du temps médical pour l’interprétation des images. Une solution réside peut-être dans les nouvelles technologies d’intelligence artificielle et d’analyse automatisée de clichés du fond d’œil fondées sur le deep learning. Une étude publiée en novembre 2019 a montré que l’algorithme EyeArt avait une sensibilité et une spécificité de 91 % pour diagnostiquer une RDNP au moins minime.2 Il existe d’autres logiciels de reconnaissance d’images et d’aide au dépistage tels que IDx-DR, ADCIS, OphtAI… Cependant, ces logiciels ont un coût de fonctionnement pour l’instant non pris en charge par l’Assurance maladie.
Depuis quelques années, l’utilisation de rétinographes ultra-grand champ pouvant prendre des clichés allant jusqu’à 200 ° se démocratise. Des études ont montré que ce mode d’imagerie est aussi performant pour grader la RD que les sept champs de référence de l’ETDRS (
Surveillance
Chez les patients atteints d’une RD plus importante qu’une RDNP minime, la surveillance doit être effectuée par l’ophtalmologiste dans le cadre d’une coopération pluridisciplinaire.
Dans ce cas, la surveillance s’effectue par examen du fond d’œil après dilatation pupillaire, rétinographies et si besoin angiographie à la fluorescéine et OCT (Optical Coherence Tomography) maculaire, à la recherche d’un œdème maculaire diabétique (OMD) [tableau ].
Dans ce cas, la surveillance s’effectue par examen du fond d’œil après dilatation pupillaire, rétinographies et si besoin angiographie à la fluorescéine et OCT (Optical Coherence Tomography) maculaire, à la recherche d’un œdème maculaire diabétique (OMD) [
Certains cas particuliers imposent une surveillance rapprochée
Chez les enfants et adultes jeunes, le dépistage de la RD doit commencer à partir de 12 ans et devenir annuel à partir de 15 ans.
Les adolescents diabétiques de type 1 mal équilibrés sur le plan glycémique doivent être surveillés au moins tous les six mois en raison du risque de RD floride, c’est-à-dire une évolution rapide d’une RDNP minime ou modérée à une forme proliférante, très ischémique, au pronostic visuel sombre.
Chez la femme enceinte diabétique, un dépistage de la RD est nécessaire avant la conception, puis tous les trois mois pendant la grossesse. En cas de RD même minime, une surveillance mensuelle est nécessaire.
En cas de rééquilibration rapide de la glycémie (mise sous pompe à insuline, optimisation thérapeutique, greffe pancréatique, chirurgie bariatrique), un examen du fond d’œil doit être effectué avant l’intensification thérapeutique puis tous les trois mois pendant douze mois.
Les adolescents diabétiques de type 1 mal équilibrés sur le plan glycémique doivent être surveillés au moins tous les six mois en raison du risque de RD floride, c’est-à-dire une évolution rapide d’une RDNP minime ou modérée à une forme proliférante, très ischémique, au pronostic visuel sombre.
Chez la femme enceinte diabétique, un dépistage de la RD est nécessaire avant la conception, puis tous les trois mois pendant la grossesse. En cas de RD même minime, une surveillance mensuelle est nécessaire.
En cas de rééquilibration rapide de la glycémie (mise sous pompe à insuline, optimisation thérapeutique, greffe pancréatique, chirurgie bariatrique), un examen du fond d’œil doit être effectué avant l’intensification thérapeutique puis tous les trois mois pendant douze mois.
Traitement de la rétinopathie diabétique et de l’œdème maculaire diabétique
La prise en charge du patient diabétique repose sur l’équilibre glycémique (HbA1c autour de 6,5 à 7 %), tensionnel (PA systolique proche de 130 mmHg et diastolique proche de 80 mmHg en cas de RD), lipidique et la prise en charge d’un éventuel syndrome d’apnées du sommeil.
La photocoagulation panrétinienne (PPR) reste le traitement de référence de la rétinopathie diabétique proliférante (RDP). Elle est également indiquée en cas de RDNP sévère avec risque d’évolution rapide de la RD (équilibration glycémique rapide, grossesse, chirurgie de cataracte, suivi aléatoire).
Récemment a été émise l’idée, notamment aux États-Unis, de traiter la RDP par des injections intravitréennes (IVT) d’anti-VEGF (vascular endothelial growth factor). En effet, le protocole S du DRCR.net (Diabetic Retinopathy Clinical Research Network) a montré une bonne efficacité des IVT de ranibizumab (Lucentis) pour réduire l’aggravation de la RDP.4 En France, cette prise en charge est beaucoup plus discutée. En effet, les anti-VEGF n’empêchent pas l’ischémie rétinienne, et l’arrêt des injections peut conduire à la reprise de la prolifération néovasculaire. Ceci peut mener vers une cécité rapide chez des patients atteints d’une RDP et perdus de vue chez qui, sans les injections, une évolution vers un décollement de rétine tractionnel ou un glaucome néovasculaire est probablement inévitable. En revanche, lorsqu’il existe une RDP associée à un OMD, on peut dans un premier temps traiter par des injections d’anti-VEGF, le temps de pouvoir faire une PPR sur quelques mois.
Concernant l’OMD, le traitement historique consistait en la photocoagulation laser de la macula. Aujourd’hui, le traitement de l’OMD repose essentiellement sur les IVT d’anti-VEGF. Deux traitements ont obtenu l’AMM en France dans cette indication en première intention : le ranibizumab (Lucentis) depuis 2012 et les résultats des études RISE et RIDE, et l’aflibercept (Eylea) depuis 2014 et les études VIVID et VISTA.
En avril 2019, les résultats du protocole V du DRCR.net montrent que le traitement de l’OMD n’est pas nécessaire tant que l’acuité visuelle est conservée (supérieure à 20/25, soit 8/10e), une surveillance reste nécessaire, de même que l’initiation d’un traitement si l’acuité visuelle baisse.5
La pratique actuelle est de réaliser un nombre important d’injections et d’initier le traitement avec une injection par mois pendant six mois. En cas de mauvaise réponse aux anti-VEGF, l’utilisation de corticoïdes (dexaméthasone) en IVT est envisageable.
À noter que le laser focal garde sa pertinence pour un OMD extrafovéolaire localisé.
De nouveaux anti-VEGF (brolucizumab, conbercept, abicipar pegol) sont actuellement en cours de développement dans la dégénérescence maculaire liée à l’âge (DMLA). Peut-être apporteront-ils également une aide dans la prise en charge de l’OMD en diminuant le nombre d’injections nécessaires.
La photocoagulation panrétinienne (PPR) reste le traitement de référence de la rétinopathie diabétique proliférante (RDP). Elle est également indiquée en cas de RDNP sévère avec risque d’évolution rapide de la RD (équilibration glycémique rapide, grossesse, chirurgie de cataracte, suivi aléatoire).
Récemment a été émise l’idée, notamment aux États-Unis, de traiter la RDP par des injections intravitréennes (IVT) d’anti-VEGF (vascular endothelial growth factor). En effet, le protocole S du DRCR.net (Diabetic Retinopathy Clinical Research Network) a montré une bonne efficacité des IVT de ranibizumab (Lucentis) pour réduire l’aggravation de la RDP.4 En France, cette prise en charge est beaucoup plus discutée. En effet, les anti-VEGF n’empêchent pas l’ischémie rétinienne, et l’arrêt des injections peut conduire à la reprise de la prolifération néovasculaire. Ceci peut mener vers une cécité rapide chez des patients atteints d’une RDP et perdus de vue chez qui, sans les injections, une évolution vers un décollement de rétine tractionnel ou un glaucome néovasculaire est probablement inévitable. En revanche, lorsqu’il existe une RDP associée à un OMD, on peut dans un premier temps traiter par des injections d’anti-VEGF, le temps de pouvoir faire une PPR sur quelques mois.
Concernant l’OMD, le traitement historique consistait en la photocoagulation laser de la macula. Aujourd’hui, le traitement de l’OMD repose essentiellement sur les IVT d’anti-VEGF. Deux traitements ont obtenu l’AMM en France dans cette indication en première intention : le ranibizumab (Lucentis) depuis 2012 et les résultats des études RISE et RIDE, et l’aflibercept (Eylea) depuis 2014 et les études VIVID et VISTA.
En avril 2019, les résultats du protocole V du DRCR.net montrent que le traitement de l’OMD n’est pas nécessaire tant que l’acuité visuelle est conservée (supérieure à 20/25, soit 8/10e), une surveillance reste nécessaire, de même que l’initiation d’un traitement si l’acuité visuelle baisse.5
La pratique actuelle est de réaliser un nombre important d’injections et d’initier le traitement avec une injection par mois pendant six mois. En cas de mauvaise réponse aux anti-VEGF, l’utilisation de corticoïdes (dexaméthasone) en IVT est envisageable.
À noter que le laser focal garde sa pertinence pour un OMD extrafovéolaire localisé.
De nouveaux anti-VEGF (brolucizumab, conbercept, abicipar pegol) sont actuellement en cours de développement dans la dégénérescence maculaire liée à l’âge (DMLA). Peut-être apporteront-ils également une aide dans la prise en charge de l’OMD en diminuant le nombre d’injections nécessaires.
Références
1. Massin P, Feldman-Billard S. Référentiel pour le dépistage et la surveillance des complications oculaires du patient diabétique – 2016. Médecine des maladies Métaboliques. Elsevier Masson SAS. Décembre 2016.
2. Bhaskaranand M, et al. The Value of Automated Diabetic Retinopathy Screening with the EyeArt System: A Study of More Than 100,000 Consecutive Encounters from People with Diabetes. Diabetes Technol Ther 2019;21(11):635-43.
3. Aiello L, et al. Comparison of Early Treatment Diabetic Retinopathy Study Standard 7-Field Imaging With Ultrawide-Field Imaging for Determining Severity of Diabetic Retinopathy. JAMA Ophthalmol 2019 1;137(1):65-73.
4. Sun J. et al. Rationale and Application of the Protocol S Anti-Vascular Endothelial Growth Factor Algorithm for Proliferative Diabetic Retinopathy. Ophthalmology 2019;126(1):87-95.
5. Baker C. et al. Effect of Initial Management With Aflibercept vs Laser Photocoagulation vs Observation on Vision Loss Among Patients With Diabetic Macular Edema Involving the Center of the Macula and Good Visual Acuity: A Randomized Clinical Trial. JAMA. 2019;321(19):1880-94.
2. Bhaskaranand M, et al. The Value of Automated Diabetic Retinopathy Screening with the EyeArt System: A Study of More Than 100,000 Consecutive Encounters from People with Diabetes. Diabetes Technol Ther 2019;21(11):635-43.
3. Aiello L, et al. Comparison of Early Treatment Diabetic Retinopathy Study Standard 7-Field Imaging With Ultrawide-Field Imaging for Determining Severity of Diabetic Retinopathy. JAMA Ophthalmol 2019 1;137(1):65-73.
4. Sun J. et al. Rationale and Application of the Protocol S Anti-Vascular Endothelial Growth Factor Algorithm for Proliferative Diabetic Retinopathy. Ophthalmology 2019;126(1):87-95.
5. Baker C. et al. Effect of Initial Management With Aflibercept vs Laser Photocoagulation vs Observation on Vision Loss Among Patients With Diabetic Macular Edema Involving the Center of the Macula and Good Visual Acuity: A Randomized Clinical Trial. JAMA. 2019;321(19):1880-94.