Les prémices de la robotique remontent aux années 1950, lorsque le premier robot industriel a été développé. Il ouvre alors la voie à une nouvelle ère technologique dans laquelle les machines peuvent être programmées pour effectuer des tâches répétitives avec une précision et une efficacité sans précédent. Pourtant, ce n’est que dans les années 1980 que la possibilité d’appliquer ces technologies à la chirurgie a émergé. Pionnier dans ce domaine, le robot Puma 560 a été utilisé pour effectuer des biopsies cérébrales stéréotaxiques en 1985, marquant ainsi le début de l’exploration de la robotique dans le domaine médical.1
Dans les années qui ont suivi, plusieurs autres prototypes de robots chirurgicaux ont vu le jour. En 1992, Robodoc est utilisé pour faciliter la mise en place de prothèses totales de hanche en améliorant la précision du fraisage du fût fémoral. L’apparition, en 1994, du système robotique Zeus, développé par Computer-Motion, est une évolution notable : il est composé d’une console de travail physiquement séparée de trois bras robotiques fixés à la table d’opération, réalisant ainsi un système télémanipulé selon la configuration « maître-esclave ». Initialement utilisé en chirurgie cardiovasculaire pour réaliser des pontages aortocoronariens, il permet une avancée majeure dans la téléchirurgie par la réalisation transatlantique d’une cholécystectomie robotique à New York, pilotée par le chirurgien Jacques Marescaux depuis Strasbourg, le 7 septembre 2001.
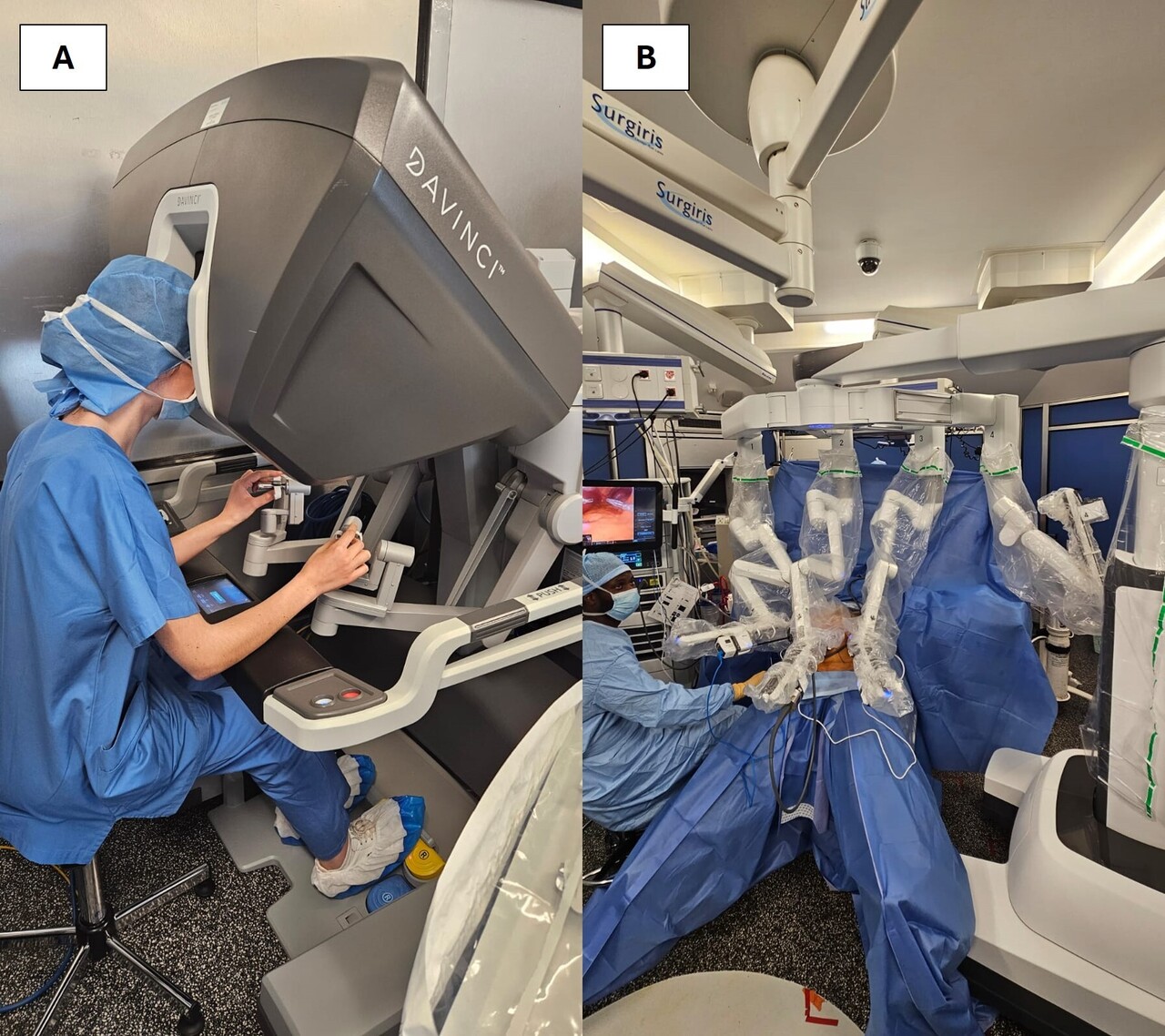
Le système Da Vinci, robot chirurgical développé par la firme américaine Intuitive Surgical, est rapidement devenu le fer de lance de la chirurgie robotique sur le plan international, utilisant le même principe de bras robotiques physiquement séparés d’une console de travail (figure). Son utilisation se porte d’abord essentiellement sur la chirurgie cardiovasculaire, digestive (cholécystectomie), puis du reflux gastro-œsophagien, pour s’étendre progressivement à la chirurgie colorectale et bariatrique ainsi qu’à la chirurgie gynécologique et urologique. Les similitudes entre les robots Da Vinci et Zeus conduisent à un conflit entre les deux entreprises, porté en justice, pour aboutir à leur fusion en 2003. La production de Zeus a rapidement été arrêtée pour laisser la place à Da Vinci.
Depuis la fin des années 2000, la robotique chirurgicale est en perpétuelle évolution, bouleversant les normes chirurgicales et ouvrant la voie à de nouvelles avancées technologiques offertes par la miniaturisation et l’apport futur de l’intelligence artificielle. La place de la robotique en chirurgie digestive est étroitement liée au développement du système Da Vinci : avec plus de 7 500 robots implantés dans le monde, Intuitive Surgical est le leader incontesté dans le secteur. La France se classe au quatrième rang mondial en nombre de systèmes Da Vinci installés, après les États-Unis, l’Allemagne et le Japon. Depuis sa création, plus de 12 millions de procédures ont été réalisées dans le monde avec ce système, dont 1,8 million uniquement en 2022. En France, c’est plus de 250 000 opérations qui ont été effectuées à ce jour.
Avantages de la chirurgie robotique
Comparée à la vision bidimensionnelle de la cœlioscopie (l’opérateur regardant l’écran d’un téléviseur en deux dimensions), la vision tridimensionnelle offerte par les systèmes robotiques permet une perception spatiale améliorée, une meilleure appréciation des profondeurs, des surfaces et une vision plus précise des structures anatomiques. Elle est permise grâce à la présence d’un système à deux caméras, qui transmettent respectivement à chaque œil une image différente sur la console du chirurgien, elle-même constituée d’un système de vision binoculaire.
En outre, les gestes chirurgicaux, réalisés à l’aide des joysticks depuis la console, possèdent un module de filtration permettant la suppression du tremblement physiologique. Plusieurs instruments sont également capables de mouvements articulés complexes avec sept degrés de liberté, non réalisables par le poignet humain, facilitant ainsi les sutures ou dissections dans des endroits confinés. Enfin, l’opérateur principal étant assis, la chirurgie robotique offre une ergonomie améliorée, réduisant la fatigue physique et les tensions pour les chirurgiens lors d’interventions prolongées.
Inconvénients de la chirurgie robotique
Une des limites techniques du robot est l’absence de retour de force de la tension exercée sur les tissus, ce qui peut conduire, notamment en début d’expérience, à des déchirures tissulaires. Cette absence de retour de force est cependant partiellement compensée par la vision en trois dimensions, qui permet une évaluation précise de la déformation des tissus par l’œil du chirurgien. Dans les futures générations de robots, des interfaces permettant à l’utilisateur d’avoir ce retour de force devraient être intégrées.
Par ailleurs, d’éventuels conflits entre les bras du robot peuvent limiter certaines actions et endommager le matériel. Il est important de garder en tête que, comme toutes machines, des défaillances techniques imprévues peuvent survenir et mener à des complications.
Évaluation des techniques chirurgicales robotiques
La chirurgie mini-invasive par cœlioscopie a fait ses preuves dans la plupart des pathologies de chirurgie digestive, démontrant une diminution de la morbidité, de la durée d’hospitalisation, de la mortalité, avec des résultats oncologiques au moins équivalents à ceux la voie ouverte. Les robots chirurgicaux utilisés actuellement sont des aides à la réalisation de cœlioscopies dans de meilleures conditions.
Si la première phase a consisté à évaluer avec succès la faisabilité et la sécurité de leur utilisation pour la réalisation de procédures chirurgicales, il leur faut aujourd’hui démontrer leur intérêt (voire leur supériorité) par rapport à la cœlioscopie. S’agissant d’une voie d’abord similaire, cette dernière étape apparaît plus difficile à obtenir. Ces évaluations doivent prendre en compte en premier lieu le patient mais également le chirurgien et la société, avec notamment le rapport coûts/bénéfices.
Chirurgie œsogastrique
L’intérêt de la robotique chirurgicale varie selon les indications.
Reflux gastro-œsophagien : le robot n’a pas d’intérêt
La réalisation de fundoplicatures pour le traitement chirurgical du reflux gastro-œsophagien a été l’une des premières évaluations de la chirurgie digestive robotique, et près d’une dizaine d’essais contrôlés randomisés ont été publiés. Il n’a pas été mis en évidence d’intérêt de la chirurgie robotique par rapport à la cœlioscopie, qu’il s’agisse des résultats per- ou postopératoires, du traitement des symptômes de reflux, ou même de l’ergonomie de l’équipe chirurgicale.
Cancer de l’œsophage : à préciser
En ce qui concerne la chirurgie œsophagienne, la réalisation du temps abdominal par cœlioscopie du cancer de l’œsophage fait aujourd’hui référence, comparée à la laparotomie. L’utilisation du robot dans cette indication a été évaluée dans un essai de phase III rapporté par l’équipe de Van der Sluis en 2019,2 comparant la chirurgie du cancer de l’œsophage par voie robot-assistée et par voie ouverte. Les résultats étaient en faveur de la chirurgie robotique, notamment sur les complications chirurgicales et la récupération fonctionnelle postopératoire, avec néanmoins une durée opératoire plus longue. Le taux de fistules anastomotiques, le taux de mortalité à trente et quatre-vingt-dix jours et les résultats oncologiques étaient identiques. Ces résultats sont similaires à ceux obtenus quelques années plus tôt par cœlioscopie. Il reste donc à préciser l’intérêt de la chirurgie robotique comparativement à la cœlioscopie par les essais prospectifs randomisés en cours.
Gastrectomie : rôle non encore défini
Le contexte est différent pour la gastrectomie : bien que des études aient démontré les bénéfices de la cœlioscopie par rapport à la voie ouverte, sans impact négatif sur le pronostic oncologique, la laparotomie reste en France une alternative validée. Cela peut s’expliquer par les limites de la cœlioscopie (degré de mobilité des instruments, vision en deux dimensions et ergonomie sous-optimale).
Le rôle de la robotique n’est pas encore défini, et il n’existe pas à ce jour d’essai prospectif randomisé concernant la gastrectomie robotique pour cancer. L’approche robotique dans cette indication semble néanmoins être une technique sûre et équivalente sur le plan oncologique à la laparoscopie ou à la laparotomie, quoique plus longue et plus coûteuse.
Chirurgie bariatrique
L’avènement de la chirurgie cœlioscopique a joué un rôle crucial dans le développement de la chirurgie bariatrique, permettant une réduction majeure de la morbi-mortalité postopératoire. L’apprentissage de certaines techniques de chirurgie bariatrique comme le bypass gastrique reste toutefois difficile et nécessite une formation prolongée. Même si ces chirurgies sont courtes (moins de deux heures en moyenne), les caractéristiques anatomiques des patients peuvent être à l’origine de difficultés ergonomiques pour l’opérateur. L’introduction de la robotique a permis de surmonter les défis posés par l’importance du tissu adipeux périviscéral et l’épaisseur de la paroi abdominale qui, en augmentant les contraintes, peuvent compromettre la précision des interventions et accroître la fatigue du chirurgien.
Une méta-analyse de Wang et son équipe en 2018 ne trouvait pas de différence significative dans la survenue de complications entre le groupe opéré par cœlioscopie et celui ayant eu une chirurgie robot-assistée. Plus récemment, dans une étude rétrospective publiée en 2023, Caiazzo et ses collaborateurs rapportaient une durée de séjour plus courte comme seul bénéfice du robot, aussi bien pour la sleeve gastrectomie que lors du bypass gastrique.3 Il n’y avait, en revanche, aucune amélioration dans la survenue des complications postopératoires, voire une augmentation du risque de complications à la suite d’une sleeve gastrectomie. Afin d’étayer ces résultats, des études prospectives randomisées doivent être effectuées.
Chirurgie colorectale
L’engouement pour l’approche robotique en chirurgie colorectale existe particulièrement pour celle du rectum et, dans une moindre mesure, celle du côlon droit. L’approche par cœlioscopie est actuellement le traitement de référence, et le robot doit montrer sa supériorité en matière de rapport coût-efficacité.
Dans la chirurgie du côlon droit, il n’existe pour l’heure qu’un seul essai randomisé publié en 2012 : Park et ses collaborateurs rapportaient des résultats à court terme équivalents sur la morbidité et les résultats oncologiques entre la cœlioscopie et le robot.4 En 2019, la même équipe a publié des résultats à cinq ans, avec un taux de survie globale et sans récidive comparable. La méta-analyse la plus récente, publiée par Genova et son équipe en 2022, est en faveur de la chirurgie robot-assistée : elle permet une diminution des pertes sanguines peropératoires, des complications postopératoires et de la durée d’hospitalisation. Le temps opératoire est en revanche plus long, et le taux de fistules anastomotiques n’est pas différent. Ces résultats doivent être mis en balance avec le surcoût important du robot, en comparaison à la cœlioscopie.
Dans la chirurgie du côlon gauche, la sécurité du robot est également démontrée, avec des résultats comparables en matière de morbidité et de mortalité chirurgicales, associée ici aussi à une durée opératoire plus longue.
L’apport technique du robot semble plus important dans la chirurgie du rectum. En effet, du fait de sa localisation anatomique dans la concavité sacrée et de ses nombreux rapports anatomiques viscéraux et nerveux, la chirurgie du rectum par cœlioscopie reste un défi pour le chirurgien, responsable d’un taux de conversion non négligeable.5 Les méta-analyses comparant la chirurgie robot-assistée à la cœlioscopie rapportent une diminution significative du taux de conversion avec le robot, associée à une augmentation de la durée opératoire. La majorité des études ne trouvent aucune différence sur la quantité de saignement peropératoire, la morbidité, la durée d’hospitalisation ou les résultats oncologiques.
La publication d’études randomisées de phase III doit permettre de préciser l’intérêt et l’apport de l’utilisation du robot dans la chirurgie colorectale en comparaison à la cœlioscopie.
Chirurgie hépato-bilio-pancréatique
En chirurgie hépatique, la cœlioscopie a pris une place croissante liée à une diminution des pertes sanguines, de la morbidité, de la durée d’hospitalisation et des résultats oncologiques équivalents en comparaison à la laparotomie. Le robot apparaît donc comme une option dans le développement de la prise en charge minimale invasive. En effet, les méta-analyses montrent, comme pour la cœlioscopie, que la chirurgie robotique, comparativement à la laparotomie, est associée à une diminution de la morbidité et de la durée d’hospitalisation.6 En revanche, par rapport à la cœlioscopie, il est rapporté un temps opératoire plus long, excepté pour les hépatectomies majeures. La mortalité postopératoire, la morbidité, la durée d’hospitalisation et les résultats oncologiques sont équivalents.
La chirurgie pancréatique suscite davantage de réserves quant à la sécurité opératoire et les résultats oncologiques des approches mini-invasives par rapport à la laparotomie. Si la place de la cœlioscopie s’est imposée dans la chirurgie du pancréas gauche, la chirurgie de la tête du pancréas est, à l’inverse, particulièrement discutée. En effet, malgré des résultats initiaux encourageants, l’essai LEOPARD II étudiant la duodénopan-créatectomie céphalique par cœlioscopie a été arrêté en raison d’un taux élevé de morbi-mortalité.7 Ainsi, il existe en France et en Europe un intérêt mitigé pour une partie de la chirurgie pancréatique par cœlioscopie et, par défaut, par chirurgie robotique.
Chirurgie pariétale
Actuellement, la chirurgie cœlioscopique est fréquemment utilisée pour traiter les hernies de l’aine ou de la ligne blanche ainsi que pour certaines cures d’éventration. Cependant, en quelques années, l’utilisation de l’assistance robotique a permis de repousser les indications de la chirurgie mini-invasive de la paroi abdominale. Grâce à une amélioration des capacités de mouvement, il est possible de travailler dans des conditions très favorables directement dans la paroi, ce qui permet de réaliser des dissections étendues, une fermeture rigoureuse des orifices pariétaux et la mise en place de larges prothèses pariétales. Le robot offre la possibilité de préserver tous les bénéfices de la chirurgie cœlioscopique traditionnelle (réduction des douleurs, de la morbidité, reprise plus rapide de l’activité...) tout en effectuant un renforcement pariétal de manière anatomique et solide, ce qui était autrefois presque impossible. Une récente (2024) et large méta-analyse (64 études et plus de 300 000 patients) de De Angelis et son équipe a observé des résultats en faveur de l’assistance robotique en comparaison à la cœlioscopie avec moins de récidive, de conversions en laparotomie et de plaies digestives, au prix, une fois de plus, d’une durée opératoire augmentée.8 Il faut cependant noter que les études incluses étaient très majoritairement rétrospectives.
Limites de l’évaluation de la chirurgie robotique
De manière générale, il semble établi que la chirurgie robotique est fiable, sécurisée et offre un confort pour le chirurgien. À ce jour, le rapport coût/bénéfices du robot est plutôt défavorable, en particulier face à l’alternative moins onéreuse et tout aussi sûre que constitue la cœlioscopie. S’agissant d’une voie d’abord chirurgicale relativement similaire, la démonstration d’une supériorité significative de la robotique par rapport à la cœlioscopie reste difficile à établir.
Ces résultats ne mettent toutefois pas en valeur la progression des chirurgiens dans la maîtrise de cette nouvelle technologie, ni les évolutions rapides des robots déjà disponibles (apparition de nouveaux instruments, de nouveaux logiciels de guidage chirurgical faisant appel à la réalité augmentée…) qui amélioreront probablement, dans le futur, les résultats obtenus.
Quelles formations initiale et continue ?
La nécessité d’une formation dédiée à la pratique de la chirurgie robotique est indispensable.
Plusieurs méthodes pédagogiques ont été développées : e-learning, simulateurs avec images virtuelles, simulateurs sur modèles en silicone ou sur modèles anatomiques humains, « proctoring » par la venue d’un chirurgien expert lors d’interventions programmées, installation d’un robot à double console permettant au mentor de superviser et d’intervenir depuis une autre console en cas de besoin.
Il est probable que le rapport de l’Agence nationale de sécurité du médicament (ANSM) publié en 2014 et révélant le nombre d’effets indésirables graves liés à la chirurgie robotique ait favorisé la généralisation de ces formations. En effet, sur plus de 17 000 interventions, une trentaine d’effets indésirables graves ont été rapportés, la majorité étant des hémorragies ou des perforations d’organes. On compte également un décès lié à une erreur de manipulation du robot. La principale cause rapportée (45 %) est le manque d’expérience et de formation du chirurgien.
Il n’existe pas, à ce jour, de certification autorisant l’utilisation du robot en chirurgie. La principale formation est délivrée par Intuitive Surgical après l’acquisition d’un robot Da Vinci au sein d’un établissement hospitalier. En Europe, ces formations sont réalisées à l’Orsi Academy en Belgique et à l’Institut de recherche contre les cancers de l’appareil digestif (Ircad) à Strasbourg.
À titre d’exemple, on estime à vingt le nombre d’interventions nécessaires pour que le chirurgien atteigne le plateau de sa courbe d’apprentissage dans le cancer du bas rectum. Il existe également plusieurs diplômes interuniversitaires, le plus souvent ouverts aux chirurgiens et infirmiers de bloc, qui permettent d’acquérir les compétences de base en chirurgie robotique.9 - 10
Prise en charge et coût
La présence de systèmes robotisés au sein des établissements de soins est un atout majeur, d’une part pour la renommée, d’autre part pour l’attractivité. Néanmoins, le coût élevé d’acquisition et de maintenance des systèmes robotiques peut être un obstacle pour de nombreux établissements. À l’avenir, l’apparition de firmes concurrentes pourrait permettre une diminution des coûts. En outre, il n’existe actuellement pas de tarif de remboursement de l’acte chirurgical par l’Assurance maladie spécifique à la chirurgie robotique. Ainsi, le remboursement étant identique que l’intervention soit réalisée avec ou sans l’assistance d’un système robotisé, sa rentabilité est généralement défavorable. S’ajoutent également, en raison de la taille et du poids parfois importants de certains systèmes, des travaux d’aménagement pour obtenir des salles d’intervention adaptées.
Et demain ?
Plusieurs systèmes concurrents du robot Da Vinci sont en cours de développement ou ont été développés. Leur effet sur le marché international reste cependant encore anecdotique. Citons, par exemple, pour la chirurgie digestive : Hugo RAS développé par Medtronic, Senhance développé par TransEnterix, Versius développé par CMR Surgical. Chacun de ces systèmes tente d’apporter sa particularité à la chirurgie robotique.
De nombreuses innovations techniques devraient accompagner le développement de ces nouvelles plateformes. Parmi elles, la mise au point d’interfaces permettant à l’utilisateur d’avoir un retour de force du robot lors de la manipulation des tissus mais aussi des systèmes intégrés de réalité augmentée. Ces derniers assurent une projection, sur l’écran du chirurgien, de représentations tridimensionnelles des organes opérés, ainsi que des tumeurs et vaisseaux qu’ils contiennent, avec la capacité de s’adapter en temps réel aux déformations imposées par la chirurgie afin de guider au mieux la procédure.
S’ils peuvent sembler être des inventions de films de science-fiction, il ne faut pas oublier que les robots chirurgicaux ne fonctionnent pas en autonomie mais en tant qu’extension des compétences et de la précision du chirurgien. Le rôle du chirurgien reste central et irremplaçable : c’est bien lui qui guide et réalise l’ensemble du processus chirurgical. Cependant, il est très probable qu’apparaissent à plus long terme des robots pouvant réaliser de manière autonome (mais sous contrôle du chirurgien) certaines parties bien précises et standardisées d’une procédure, comme les sutures digestives.
Que dire à vos patients ?
La chirurgie robotique est une innovation chirurgicale en plein essor.
Les robots chirurgicaux sont des dispositifs conçus pour assister le chirurgien lors des interventions. Le principe fondamental de fonctionnement repose sur le concept de « maître-esclave ». Le chirurgien, assis à la console, contrôle les mouvements des bras robotisés à l’aide de joysticks et de pédales. Ces mouvements sont transmis de manière précise aux instruments chirurgicaux situés à l’intérieur du corps du patient.
Durant l’intervention, le système permet une vision en trois dimensions de haute résolution grâce à des caméras miniaturisées, offrant ainsi une visualisation détaillée de la zone opératoire.
En dépit des avancées, il est important de souligner que l’indication d’une chirurgie robotique doit être soigneusement évaluée en fonction des besoins spécifiques du patient et des compétences du chirurgien. La décision d’utiliser un robot chirurgical doit être partagée entre le chirurgien et le patient, en tenant compte des bénéfices potentiels et des risques associés à cette technologie.
2. Van Der Sluis PC, Van Der Horst Sylvia, May AM, et al. Robot-assisted Minimally Invasive Thoracolaparoscopic Esophagectomy Versus Open Transthoracic Esophagectomy for Resectable Esophageal Cancer: A Randomized Controlled Trial. Ann Surg 2019;269(4):621‑30.
3. Caiazzo R, Bauvin P, Marciniak C, et al. Impact of Robotic Assistance on Complications in Bariatric Surgery at Expert Laparoscopic Surgery Centers: A Retrospective Comparative Study With Propensity Score. Ann Surg 2023;278(4):489‑96.
4. Park JS, Choi GS, Park SY, et al. Randomized clinical trial of robot-assisted versus standard laparoscopic right colectomy. Br J Surg 2012;99(9):1219‑26.
5. Jayne D, Pigazzi A, Marshall H et al. Effect of Robotic-Assisted vs Conventional Laparoscopic Surgery on Risk of Conversion to Open Laparotomy Among Patients Undergoing Resection for Rectal Cancer: The ROLARR Randomized Clinical Trial. JAMA 2017;318(16):1569.
6. Ciria R, Berardi G, Alconchel F, et al. The impact of robotics in liver surgery: A worldwide systematic review and short-term outcomes meta-analysis on 2,728 cases. J Hepatobiliary-Pancreat Sci 2022;29(2):181‑97.
7. Van Hilst J, De Rooij T, Bosscha K, et al. Laparoscopic versus open pancreatoduodenectomy for pancreatic or periampullary tumours (LEOPARD-2): A multicentre, patient-blinded, randomised controlled phase 2/3 trial. Lancet Gastroenterol Hepatol 2019;4(3):199‑207.
8. De Angelis N, Schena CA, Moszkowicz D, et al. Robotic surgery for inguinal and ventral hernia repair: A systematic review and meta-analysis. Surg Endosc 2024;38(1):24‑46.
9. Cooper MA, Ibrahim A, Lyu H, et al. Underreporting of Robotic Surgery Complications. J Healthc Qual 2015;37(2):133‑8.
10. Hubert J, Vouhe P, Poitout D, et al. Rapport 21-13. Formation des chirurgiens/des équipes chirurgicales à la chirurgie robot-assistée. État de la situation actuelle. Propositions d’améliorations. Bull Academie Natl Medecine 2022;206(2):167‑78.

 Encadrés
Encadrés