Une thrombocytose correspond à un taux de plaquettes supérieur ou égal à 450 giga par litre (G/L), la normale se situant entre 150 et 400 G/L.
Une cause réactionnelle et une fausse thrombocytose doivent d’abord être recherchées. Après les avoir éliminées, un avis hématologique s’impose afin de poser le diagnostic au moyen d’examens de biologie moléculaire. Parmi les hémopathies malignes, la thrombocytémie essentielle est la cause la plus fréquente de thrombocytose. Une évaluation du risque thrombotique est primordiale.
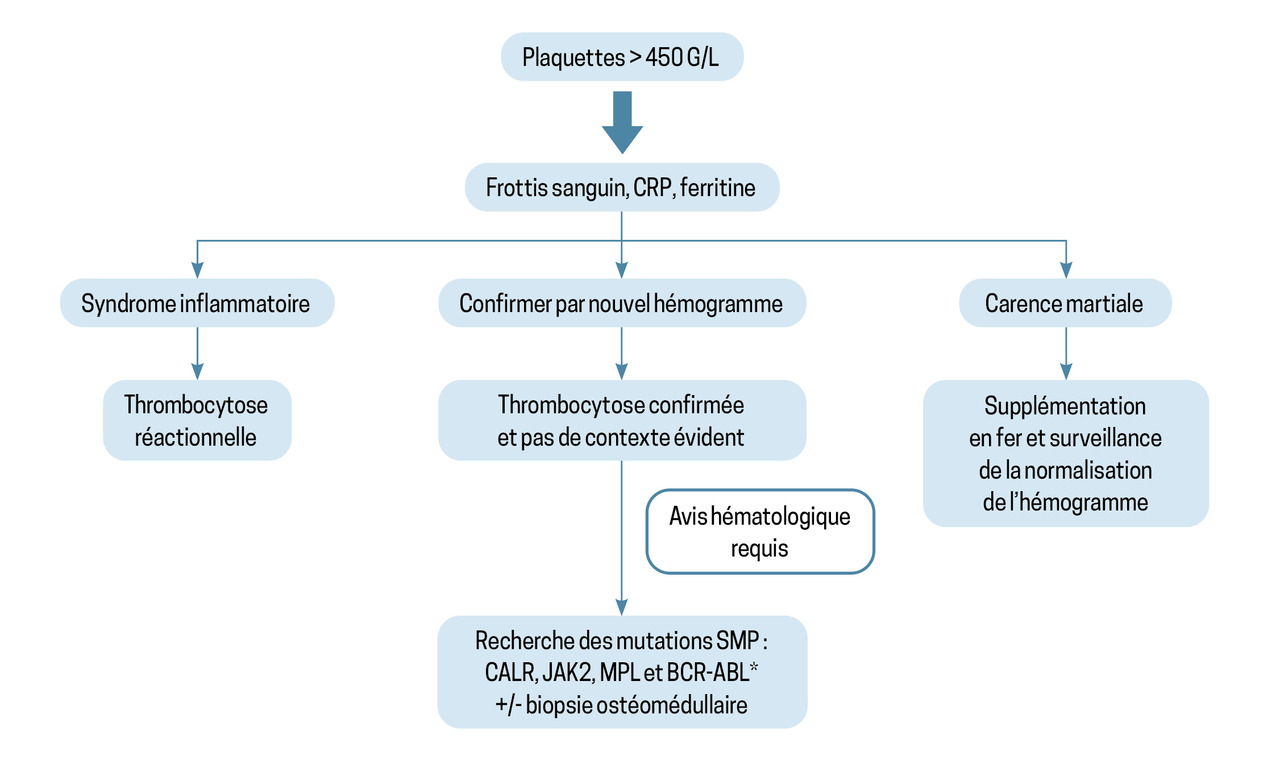
La démarche étiologique est résumée dans la figure.
Éliminer une thrombocytose réactionnelle
La thrombocytose réactionnelle correspond à 90 % de l’ensemble des cas de thrombocytose. Les trois causes fréquentes en sont l’inflammation, la carence martiale et la période postopératoire.
Syndrome inflammatoire
Les infections ou pathologies inflammatoires chroniques, telles qu’une maladie de système ou un cancer, peuvent être à l’origine d’un syndrome inflammatoire.
Le cancer peut entraîner une thrombocytose en raison de l’inflammation, mais aussi par des phénomènes d’interactions entre la tumeur et les plaquettes dans les processus de tumorigenèse et d’angiogenèse. La thrombocytose associée aux cancers est un facteur de mauvais pronostic.1
Une hyperleucocytose est souvent associée à ces thrombocytoses réactionnelles.
Carence martiale
La carence martiale se manifeste typiquement par une anémie microcytaire arégénérative qui peut s’associer à une thrombocytose. Le taux de fer sérique est bas, ainsi que la ferritinémie et le coefficient de saturation de la transferrine.
En cas de syndrome inflammatoire associé, la ferritinémie peut être « faussement normale ».
La supplémentation en fer permet généralement de corriger ces anomalies. En dehors d’une cause évidente (règles abondantes, saignement récent...), un bilan étiologique digestif et/ou gynécologique doit être réalisé.
En post-chirurgie
La splénectomie entraîne typiquement une thrombocytose, mais tout autre acte chirurgical important peut être responsable d’une élévation du taux de plaquettes.
Ces situations sont généralement transitoires, le risque thromboembolique devant être prévenu. Il n’est généralement pas nécessaire de prescrire un traitement pour diminuer le taux de plaquettes (cytoréducteur), excepté en cas de persistance et/ou si le taux de plaquettes est supérieur à 1 000 G/L ; dans ce cas, un avis hématologique doit être pris.
Les graves traumatismes peuvent également être responsables de thrombocytose réactionnelle.
Éliminer une fausse thrombocytose
Cette situation, bien que rare, peut être due à la présence d’une cryoglobuline (maladie de Waldenström, infection par le virus de l’hépatite C) ou de certains micro-organismes (Candida, par exemple), entraînant alors des interférences analytiques.
Thrombocytose d’origine hématologique
La thrombocytose d’origine hématologique peut résulter de différentes causes, qui peuvent être acquises ou constitutionnelles.2
Formes acquises
Les formes acquises de thrombocytose correspondent à des syndromes myéloprolifératifs ou myélodysplasiques.
Syndromes myéloprolifératifs
Trois types de syndrome myéloprolifératif se distinguent : thrombocytémie essentielle, polyglobulie de Vaquez et leucémie myéloïde chronique.
Thrombocytémie essentielle
La thrombocytémie essentielle est la principale hémopathie pouvant être à l’origine d’une thrombocytose. Trois mutations sont retrouvées dans la majorité des cas : CALR, JAK2 ou MPL. Un suivi hématologique est requis, le risque principal étant thrombotique. Une acutisation en leucémie aiguë myéloblastique est possible.2
Polyglobulie de Vaquez
Dans cette pathologie, la polyglobulie est généralement prédominante, mais elle peut être masquée par une carence martiale. La mutation de JAK2 est retrouvée dans l’immense majorité des cas. Les risques et les traitements ressemblent à ceux de la thrombocytémie essentielle, même s’il existe quelques différences.
Leucémie myéloïde chronique
Hémopathie maligne, la leucémie myéloïde chronique est caractérisée par la présence d’une translocation entre les chromosomes 9 et 22 (appelé chromosome Philadelphie) donnant naissance à un transcrit de fusion BCR-ABL à l’origine d’une prolifération de la lignée myéloïde. La présentation habituelle est celle d’une hyperleucocytose à polynucléaires neutrophiles avec hyperéosinophilie et basophilie, associée à une myélémie, mais une thrombocytose isolée est possible. Depuis 2000, cette pathologie est prise en charge par une thérapie ciblée, et précisément par les inhibiteurs de tyrosine kinase, qui en ont révolutionné le pronostic.
Syndrome myélodysplasique et autres hémopathies
Le sous-type, appelé syndrome myélodysplasique 5q-, est fréquemment révélé par une anémie et une thrombocytose.
Formes constitutionnelles
Les thrombocytoses familiales sont rares et apparaissent en général dès l’enfance.
Évaluer le risque thrombotique
L’évaluation du risque thrombotique chez les patients ayant une thrombocytose constitue une étape clé de la prise en charge.
Thrombocytose réactionnelle
Le risque thrombotique est plus faible et plus difficile à évaluer dans cette situation car il dépend du contexte qui peut, en lui-même, être thrombogène (immobilisation post-chirurgicale, cancer). Il n’y a pas de prise en charge spécifique de la thrombocytose, le traitement est avant tout celui de la cause.
Toutefois, la cytoréduction (traitement visant à diminuer le taux de plaquettes) peut se discuter si le taux de plaquettes est supérieur à 1 000 G/L, en tenant compte toutefois des autres facteurs de risque thrombotiques (tabac, obésité, antécédent de thrombose, pilule œstroprogestative, thrombophilie).
Hémopathie maligne
En premier lieu, il convient de citer la thrombocytémie essentielle, qui est l’une des hémopathies les plus à risque thrombotique. Il existe des scores pour prédire ce risque.3 Dans la grande majorité des cas, il est nécessaire de prescrire un traitement antiagrégant plaquettaire.
Si une indication de traitement cytoréducteur est posée, l’objectif thérapeutique est d’obtenir un taux de plaquettes inférieur à 400 G/L.
À noter qu’un risque hémorragique peut toujours survenir, notamment dans les grandes thrombocytoses,4 avec possibilité d’acquisition de troubles de l’hémostase associés (maladie de Willebrand acquise). Cette situation contre-indique, au moins temporairement, le traitement antiagrégant plaquettaire.
Le type de traitement cytoréducteur utilisé dépend de l’âge, des antécédents thrombotiques et du type de mutations retrouvé.5
2. Schafer AI. Thrombocytosis. N Engl J Med 2004;350(12):1211-9.
3. Barbui T, Vannucchi AM, Buxhofer-Ausch V, et al. Practice-relevant revision of IPSET-thrombosis based on 1019 patients with WHO-defined essential thrombocythemia. Blood Cancer J 2015;5(11):e369.
4. Venkat RK, Redd RA, Harris AC, et al. Risk of bleeding in patients with essential thrombocythemia and extreme thrombocytosis. Blood Adv 2024;8(23):6043-54.
5. Tefferi A, Pardanani A. Essential thrombocytemia. N Engl J Med 2019;381(22):2135-44.