La prise en charge des pathologies orthopédiques traumatiques ou programmées a été modifiée par l’évolution des techniques mini-invasives, permettant des gestes majeurs moins agressifs et des alternatives à l’hospitalisation classique (récupération améliorée après chirurgie1 et prise en charge ambulatoire). Ces évolutions confrontent les médecins généralistes à des situations qui étaient jusque-là l’apanage des chirurgiens ou des rééducateurs. Le but est ici de décrire les suites habituelles et les principales complications précoces ou tardives après chirurgie orthopédique (hors chirurgies rachidienne et tumorale) et leur prise en charge en médecine générale.
Principales interventions en orthopédie et traumatologie
En orthopédie (chirurgie réglée), il existe deux types d’intervention :
les interventions conservatrices, permettant de réparer ou de corriger des lésions de l’appareil locomoteur ;
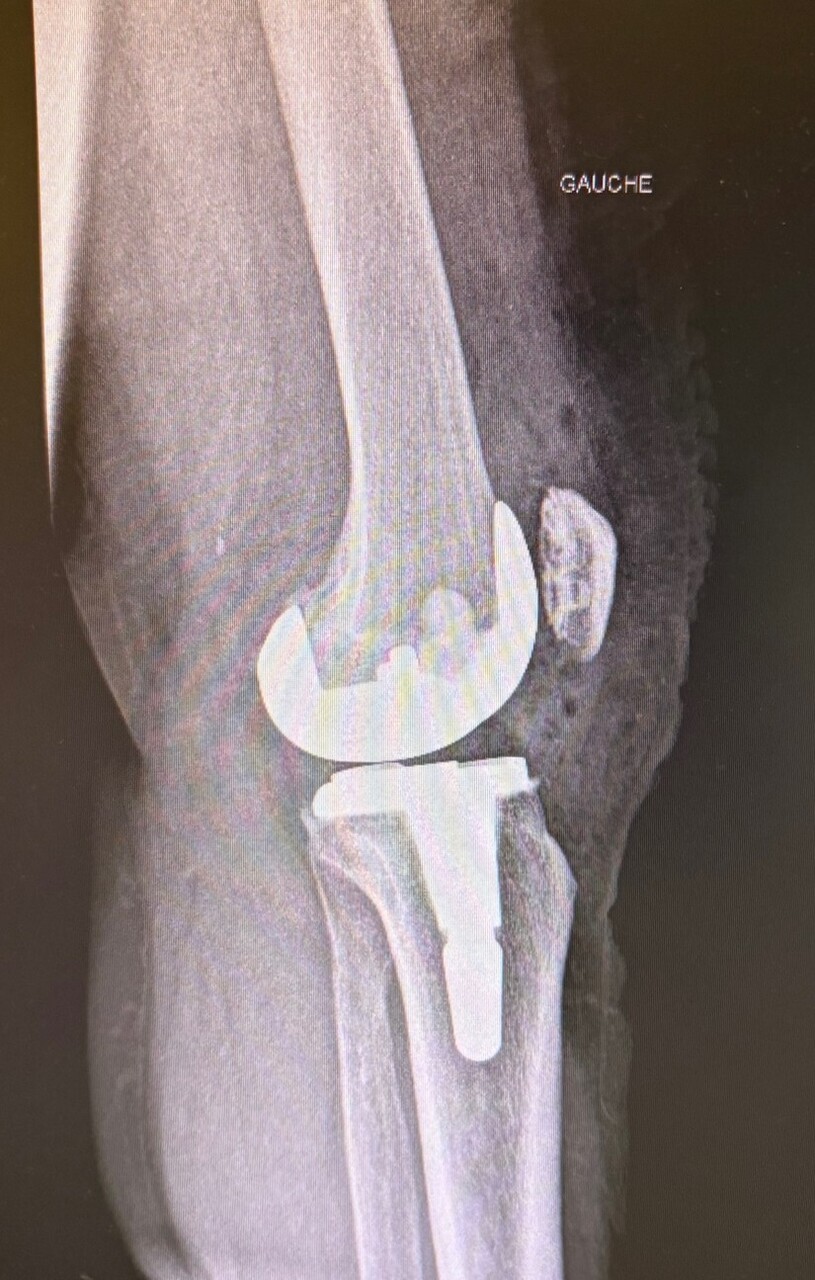
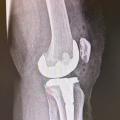
les interventions prothétiques non conservatrices (fig. 1).
En traumatologie, il convient de distinguer :
le traitement fonctionnel ne comportant pas d’immobilisation ou à visée antalgique ;
le traitement orthopédique, fréquent en pédiatrie, impliquant une immobilisation et une éventuelle réduction orthopédique. Il impose une surveillance régulière (généralement hebdomadaire) s’assurant de l’absence de complication de la fracture jusqu’à la consolidation ;
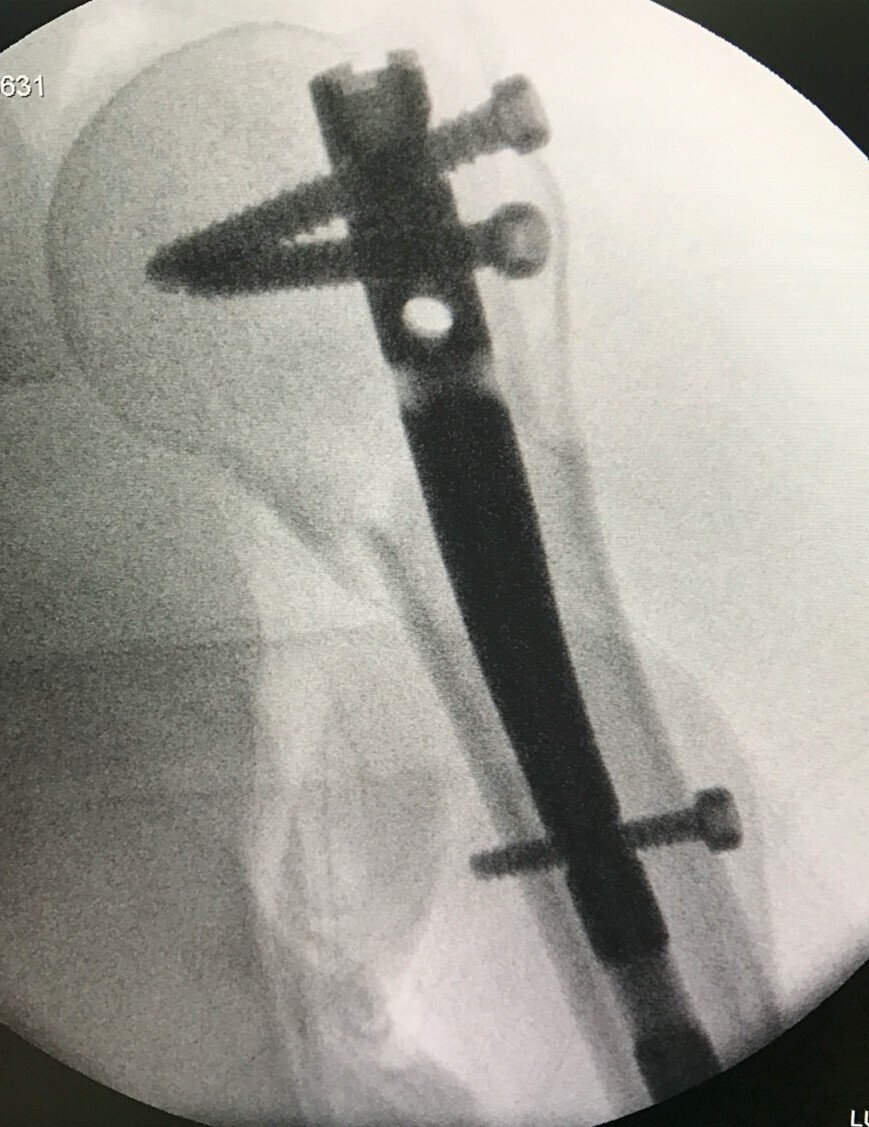
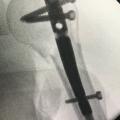
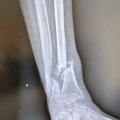
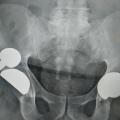
l’ostéosynthèse consistant en une réduction directe ou indirecte de la fracture, puis en son immobilisation par du matériel intra-osseux (broche, clous, vis, plaques), ou parfois à l’extérieur du membre (fixateur externe), notamment en cas de fracture ouverte grave (fig. 2). Une immobilisation complémentaire par attelle ou plâtre peut être associée.
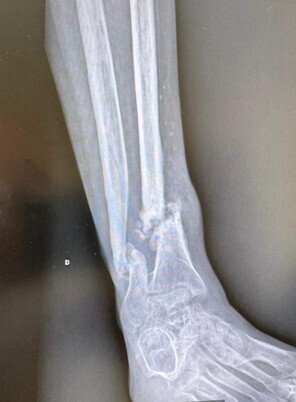
L’évolution normale d’une fracture conduit à sa consolidation et au rétablissement de la fonction du membre. Cette évolution peut être compliquée par un déplacement secondaire, un retard de consolidation, une non-consolidation (pseudarthrose) ou une consolidation non anatomique (cal vicieux) [fig. 3], pouvant nécessiter des chirurgies complémentaires.
Gestion des suites normales
Dès la sortie d’hospitalisation, une lettre de liaison accompagnée, le cas échéant, d’un compte rendu opératoire décrivent le motif de prise en charge et les gestes réalisés. Ces documents sont capitaux pour préciser les suites : possibilité ou non de rééducation et d’appui ; mouvements interdits et durée ; traitements médicamenteux nécessaires, notamment antalgiques et traitements anticoagulants ; soins des plaies chirurgicales éventuelles (type de fermeture, date d’ablation, soins de pansement et rythme) ; éventuelles complications ou difficultés lors de la prise en charge.
En l’absence de complications, il est le plus souvent demandé au médecin généraliste d’assurer le suivi d’un traitement anticoagulant préventif par héparine de bas poids moléculaire et/ou la surveillance d’un traitement anticoagulant curatif ou son équilibration. Des adaptations individuelles sont parfois décidées en fonction du rapport bénéfice/risque établi par le chirurgien et l’anesthésiste, par exemple une reprise volontairement retardée des nouveaux anticoagulants oraux en dépit d’une arythmie complète par fibrillation atriale.
En cas de traitement orthopédique ou d’une immobilisation complémentaire, il convient de vérifier le plâtre : il ne doit pas présenter de zones de faiblesse, être compressif ou douloureux, ni être souillé en cas de geste chirurgical associé. Le temps de séchage varie entre une heure pour les résines et vingt-quatre à quarante-huit heures pour les plâtres classiques. Un temps d’adaptation de vingt-quatre à soixante-douze heures lié à la présence de l’œdème post-traumatique est fréquent, mais sans aucun signe de gravité neurologique ou vasculaire. Il ne faut pas hésiter à rappeler les conseils pratiques pour éviter les complications ou désagréments, qui se résument à surélever la main ou le pied au repos, effectuer des contractions isométriques et mobiliser les articulations libres dans les secteurs autorisés, éviter de mouiller le plâtre (ou le protéger, car même en résine, un jersey mouillé entraîne une macération cutanée au contact), ne pas introduire d’objet en cas de prurit en raison du risque de blessure (un traitement médicamenteux peut être proposé en cas de prurit sévère). Enfin, il convient d’informer le patient du risque de survenue d’une amyotrophie et d’une hypertrichose localisée secondaire à l’immobilisation.
Gestion des suites compliquées
Plusieurs complications peuvent apparaître au décours d’une chirurgie orthopédique et doivent être connues du médecin traitant.
Complications liées au plâtre
En cas d’immobilisation plâtrée, un motif fréquent de consultation est la mauvaise tolérance du plâtre. Les signes de gravité sont neurologiques (paralysie, hypoesthésie, dysesthésie ou déficit sensitif non signalés lors de la prise en charge initiale) ou vasculaires (œdème majeur, signes d’ischémie). Apparus à distance de la confection du plâtre et notamment après réduction orthopédique, un éventuel syndrome des loges doit être évoqué : il s’agit d’une urgence qui doit conduire idéalement à une consultation spécialisée immédiate. À défaut, le plâtre doit être fendu, jersey compris, voire bivalvé.
Une douleur devenant lancinante et localisée traduit le plus souvent un conflit entre le plâtre et un relief osseux ou articulaire. Un avis rapide et une réfection du plâtre limitent le risque d’escarre sous plâtre et d’infection secondaire. Il en est de même si le patient s’est blessé en se grattant.
Ne pas banaliser une impotence fonctionnelle
Après une chirurgie prothétique ou une ostéosynthèse, une impotence fonctionnelle brutale dégradant les suites simples fait évoquer une complication de la chirurgie ; elle ne doit jamais être minimisée.
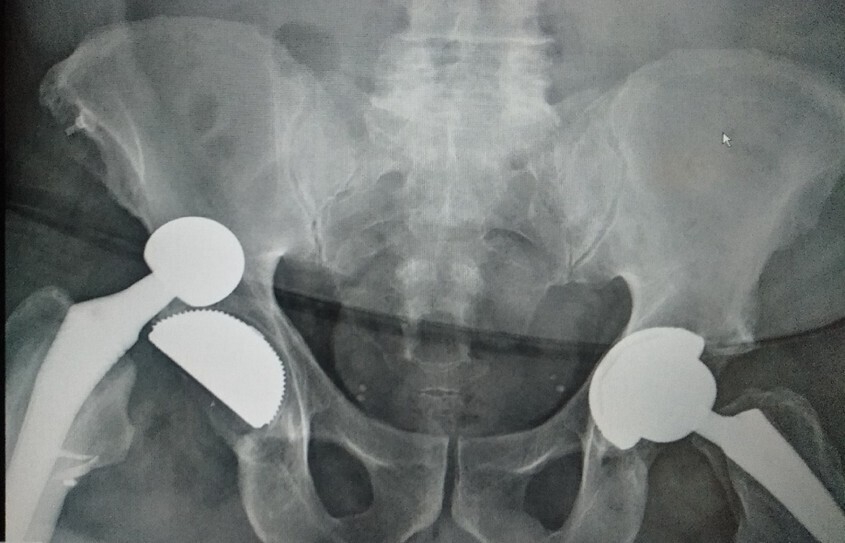
Les causes sont variables : hématome, lésion des parties molles, infection débutante, démontage de l’ostéosynthèse, luxation ou fracture périprothétique (fig. 4). Un avis chirurgical urgent doit être sollicité, parfois précédé d’un bilan d’imagerie radiologique simple et d’un bilan biologique (hémogramme, protéine C réactive [CRP]).
Attention à la réapparition des douleurs après une phase d’amélioration
Les douleurs postopératoires restent fréquentes même si leur gestion s’est améliorée. Certaines sont prévisibles, comme les rebonds douloureux entre J + 2 et J + 5 après pose de prothèse. Un examen général et du site opéré permet d’éliminer une complication cicatricielle ou thromboembolique.
Le médecin généraliste doit encourager la prise régulière d’antalgiques à la phase initiale, malgré les réticences de certains patients, notamment en expliquant l’intérêt d’avoir un seuil de douleur bas plutôt que des pics de douleur aiguë.
La réapparition de douleurs après une phase d’amélioration est un signal d’alarme. Isolées et d’horaire mécanique, elles évoquent une complication locale de la chirurgie (mobilisation du matériel, hématome...) ; d’horaire inflammatoire et associées à de la fièvre ou à un trouble cicatriciel, elles orientent vers une complication thromboembolique ou une infection.
Survenue d’un œdème : éliminer une thrombose
Un œdème du membre opéré est fréquent, notamment après une pose de prothèse, et peut se prolonger plusieurs mois ; certains proposent le port de bas ou de bandes de contention. Les phlébites distales asymptomatiques ne sont pas rares, mais leur traitement systématique doit être mis en balance avec les risques d’hématome au niveau du site opéré. Les phlébites poplitées ou proximales doivent être traitées.
La fréquence des embolies pulmonaires a diminué en raison des traitements anticoagulants préventifs et d’une rééducation, avec appui précoce, notamment après prothèse.
Fièvre isolée fréquente
En postopératoire immédiat, une fièvre isolée, supérieure à 38 °C, est fréquente et n’est pas inquiétante. Elle doit céder dans la semaine postopératoire. Néanmoins, elle doit faire dépister une complication précoce (infectieuse ou thromboembolique) ou une infection concomitante (respiratoire, digestive ou urinaire).
Les troubles cicatriciels orientent vers une complication infectieuse
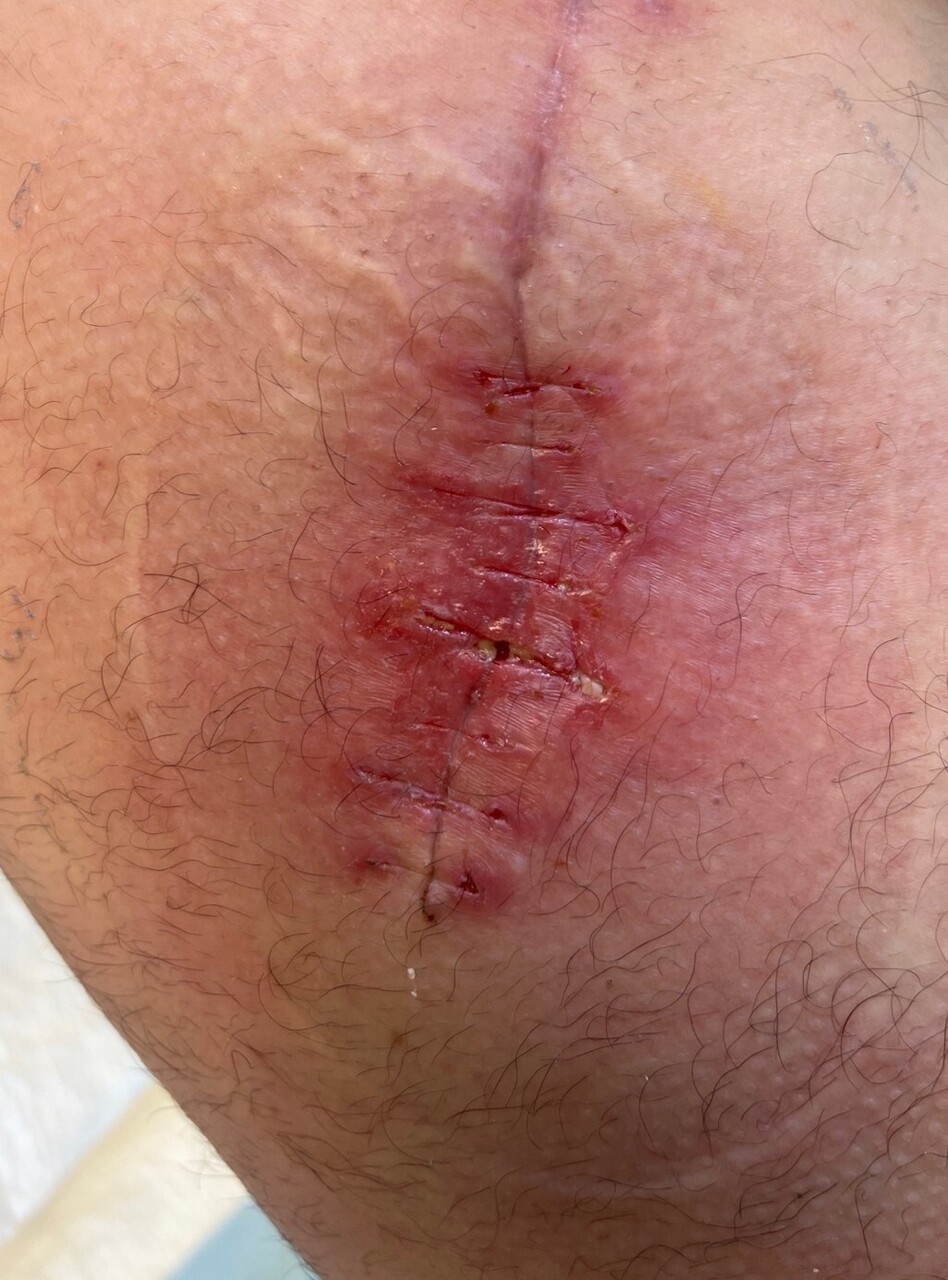
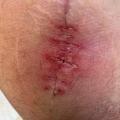
Les troubles cicatriciels sont fréquents. Un écoulement sanglant ou sérosanglant est possible pendant sept à dix jours. Sa persistance, et surtout sa survenue alors que la plaie était initialement sèche, fait évoquer une complication infectieuse (fig. 5).
Les infections, plus graves en présence de matériel, compliquent en moyenne 1 % des interventions en orthopédie. Leur taux de guérison est variable selon la situation clinique, l’état général du patient, le délai et les modalités de leur prise en charge.
Même pour un chirurgien entraîné, différencier un accident cicatriciel à traiter par soins locaux et une infection à son début peut être difficile.
Constater un accident cicatriciel doit faire demander en urgence un avis chirurgical, physique ou distanciel et faire prescrire un bilan biologique (hémogramme, CRP). Si une surveillance est décidée, fréquence et type de pansements sont modifiés.
En cas d’infection, le traitement est médico-chirurgical. La prescription isolée d’une antibiothérapie est une erreur majeure, voire une faute, compromettant la prise en charge et les chances de guérison de l’infection.
Le traitement de ces infections associe, en effet, un nettoyage local à une antibiothérapie prolongée, secondairement adaptée (3 mois en cas de présence de matériel).
En cas d’infection sur prothèse, la chirurgie conservatrice (lavage-synovectomie ou DAIR [débridement, antibiotiques et sauvetage de l’implant]) n’est possible que trente jours après la chirurgie initiale. Au-delà, l’implant recouvert d’un biofilm doit impérativement être changé (tableau).2
Ces infections doivent être prises en charge par une équipe associant orthopédiste et infectiologue et, dans les cas les plus graves, dans un centre spécialisé (Centre de référence des infections ostéoarticulaires complexes [CRIOAC]).3 Les complications liées au traitement antibiotique (intolérance digestive, allergie, interactions médicamenteuses) sont fréquentes. Toute modification thérapeutique sans avis de l’infectiologue doit être proscrite, car source d’échec du traitement.
La survenue d’une complication grave (anomalie sanguine sévère, allergie cutanée…) doit conduire à un avis spécialisé en urgence.
Autres complications et perturbations biologiques
L’anémie est fréquente, mais les protocoles de blood management* peuvent limiter l’usage des transfusions. Les perfusions de fer peuvent permettre une augmentation prolongée de la ferritine.
La CRP est un marqueur d’inflammation non spécifique de l’infection, qui peut augmenter fortement après chirurgie. En règle générale, elle se normalise en un mois environ. Son interprétation doit inclure sa cinétique et les éléments cliniques (cicatrice, fonction, douleur). Une seule valeur de CRP n’a pas de signification en elle-même.
Prise en charge globale du patient
La prise en charge du patient, au-delà de l’aspect chirurgical et thérapeutique, doit comporter la reprise des activités, l’accompagnement psychologique et la gestion des attentes pour une récupération globale et personnalisée.
Activités professionnelle et sportive : quand reprendre ?
La durée de l’arrêt de travail varie selon le traitement initial, notamment ses contraintes de rééducation et son évolution. Elle doit être individualisée en tenant compte des possibilités réelles d’effectuer une activité ou de s’y rendre. Le chirurgien rédige le premier arrêt mais peut parfois demander au médecin généraliste de le prolonger entre deux consultations orthopédiques.
La reprise du sport peut nécessiter, selon les activités, la mise en place de conditions ou précautions particulières (récupération musculaire, ablation de matériel, interdiction temporaire ou définitive de certaines activités), qui sont du ressort du chirurgien. En pédiatrie, il est souvent proposé, pour éviter une fracture itérative, un délai double de celui de l’immobilisation.
Un syndrome de stress post-traumatique est possible
Lorsque le geste opératoire fait suite à un accident, le patient a pu développer un syndrome de stress post-traumatique, qu’il s’agit de ne pas minimiser. Si la prise en charge n’a pas été débutée en phase hospitalière, elle doit être proposée au décours.
Insatisfaction du patient en postopératoire
Le médecin traitant peut être interrogé sur un résultat jugé insuffisant par le patient, après (ou non) avis du chirurgien. Cette situation n’est pas rare, notamment après prothèse articulaire : 2 % environ pour les prothèses de hanche et jusqu’à 20 % pour les prothèses de genou. Les plaintes sont variables et parfois associées (douleurs persistantes, mobilité incomplète, gênes fonctionnelles ou sportives). Le médecin peut se trouver alors en position délicate entre son patient et le chirurgien. Il est important de reprendre les échanges de courrier, notamment l’examen et l’information préopératoire. Les suites chirurgicales peuvent également expliquer ces difficultés. Le résultat fonctionnel complet s’obtient généralement après six mois pour une pose de prothèse de hanche et un an après la pose d’une prothèse de genou, et certains dysfonctionnements sont de diagnostic difficile. Le plus souvent, des explications répétées suffisent. Toutefois, dans certains cas, un second avis chirurgical peut être pertinent. En revanche, il convient d’éviter la prescription de bilans d’imagerie, parfois inappropriés, comme une scintigraphie précoce moins d’un an après la pose de prothèse. En effet, des images ambiguës et non spécifiques peuvent orienter vers un diagnostic erroné et favoriser l’évolution vers un conflit médico-légal.
Prise en charge à distance du traitement initial
À distance du traitement initial, il convient de mettre en place un suivi clinique et radiologique constant afin de détecter précocement les complications infectieuses, mécaniques et évolutives, et adapter la stratégie thérapeutique.
Infection secondaire
La survenue d’une infection secondaire, notamment sur prothèse, est possible. Il peut s’agir d’une infection dite de contiguïté – par exemple, après une plaie en regard d’une prothèse – ou d’une infection à distance à partir d’un foyer infectieux non orthopédique. Il importe donc de diagnostiquer et de traiter toute infection bactérienne, notamment chez les porteurs de prothèse articulaire.
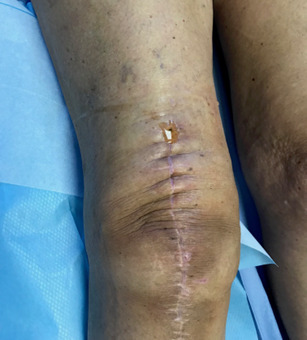
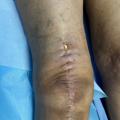
Toute altération cicatricielle au-delà d’un mois après la chirurgie évoque une complication infectieuse, qui est certaine en cas de fistule sur – ou à proximité – de la cicatrice (fig. 6).
La survenue de douleurs et d’une impotence fonctionnelle sur un membre opéré porteur de matériel d’ostéosynthèse ou de prothèse dans le cadre d’une infection à distance peut orienter vers un diagnostic d’infection secondaire. L’examen clinique, associé à une ponction articulaire, confirme le diagnostic. Seul un traitement rapide, initié dans les quinze jours, peut conduire à un sauvetage de l’implant ; au-delà, il doit être changé (tableau).4
Surveillance et durée de vie d’une prothèse
Une dégradation fonctionnelle tardive peut traduire une évolution de la pathologie initiale ou la dégradation du traitement (descellement de prothèse, arthrose après ligamentoplastie…). Si une prothèse est présente, même en cas de pathologie de voisinage, comme une cruralgie, un bilan radiologique de l’implant doit être effectué.
Les prothèses articulaires doivent être revues à intervalles réguliers car elles peuvent montrer des signes d’usure et/ou un descellement, initialement révélé par des radiographies et conduisant, en l’absence de signes cliniques, à une surveillance plus rapprochée. En cas de signes cliniques et selon l’état général, le changement de prothèse est souvent possible, avec une morbidité actuelle moindre.
La durée de vie d’une prothèse ne peut pas être prédite individuellement. Mais hors complications (infections, fracture…), elle est en moyenne de vingt ans. Cette durée varie en fonction de l’indication initiale, des antécédents locaux et généraux et de l’activité du patient.
La survenue tardive d’une première luxation de prothèse de hanche après un geste banal traduit une usure de la pièce cotyloïdienne, une fracture tardive sur implant céramique ou une altération musculaire des fessiers. Dans ce contexte, une reprise uni- ou bipolaire doit être évoquée, sans attendre une récidive de la luxation.
Évolution de la pathologie initiale
Un autre mode de dégradation est la reprise évolutive de la pathologie initiale après une phase d’amélioration, par exemple, sous forme d’arthrose après méniscectomie. Un nouveau bilan clinique du retentissement des troubles associé à un bilan d’imagerie, privilégiant les radiographies, affirme le diagnostic évolutif. Si la gêne fonctionnelle le permet, le traitement médical doit être privilégié.
Que dire à vos patients ?
La chirurgie orthopédique et traumatologique est fiable quand l’indication est bien posée.
Le taux d’infections postopératoires est bas et le pronostic est bon après un traitement médico-chirurgical bien conduit et sans retard.
Les modalités d’hospitalisation actuelles (ambulatoire, récupération améliorée après chirurgie...) sont sûres et reposent sur une complémentarité entre chirurgien, médecin traitant et adhésion du patient.
À long terme, une dégradation du résultat peut survenir par reprise évolutive de la pathologie ou pour des causes mécaniques. Quand elle est correctement dépistée et diagnostiquée, des solutions existent, qui ne sont pas toutes chirurgicales.
2. Haute Autorité de santé. Prothèse de hanche ou de genou : diagnostic et prise en charge de l’infection dans le mois suivant l’implantation. Mars 2014. https://bit.ly/49csEXa
3. Ministère de la Santé. Infections ostéoarticulaires complexes – Centres de référence interrégionaux pour la prise en charge des Infections ostéoarticulaires complexes. 10 septembre 2025. https://bit.ly/4jlQ9BO
4. Iza K, Foruria X, Moreta J, et al. DAIR (Debridement, Antibiotics and Implant Retention) less effective in hematogenous total knee arthroplasty infections. J Orthop Surg Res 2019;14(1):278.

 Encadrés
Encadrés