Un patient âgé de 34 ans, sans antécédent pathologique notable, est suivi dans le service de gastroentérologie pour des vomissements post-prandiaux associés à des douleurs épigastriques chroniques, aggravés par la prise alimentaire, et évoluant dans un contexte d’apyrexie et d’amaigrissement évalué à 12 kg en un an. L’examen clinique révèle un abdomen souple, associé à un clapotage au niveau épigastrique, sans empâtement ni masse palpable. L’indice de masse corporelle (IMC) est de 16,7 kg/m². Le bilan biologique est sans anomalie. La fibroscopie œsogastroduodénale montre une gastrite érythémateuse antropylorique et une dilatation de la première et deuxième portion du duodénum sans obstacle intrinsèque visible, avec un reflux bilieux au niveau gastrique. L’étude anatomopathologique des biopsies réalisées met en évidence une gastrite chronique et une duodénite non spécifiques.
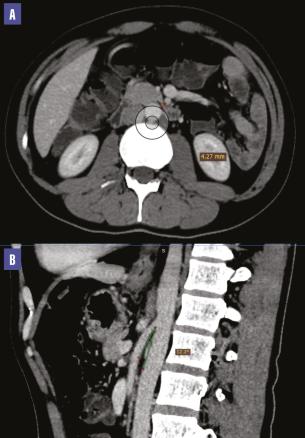
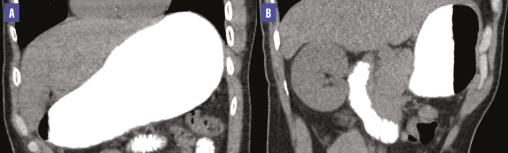
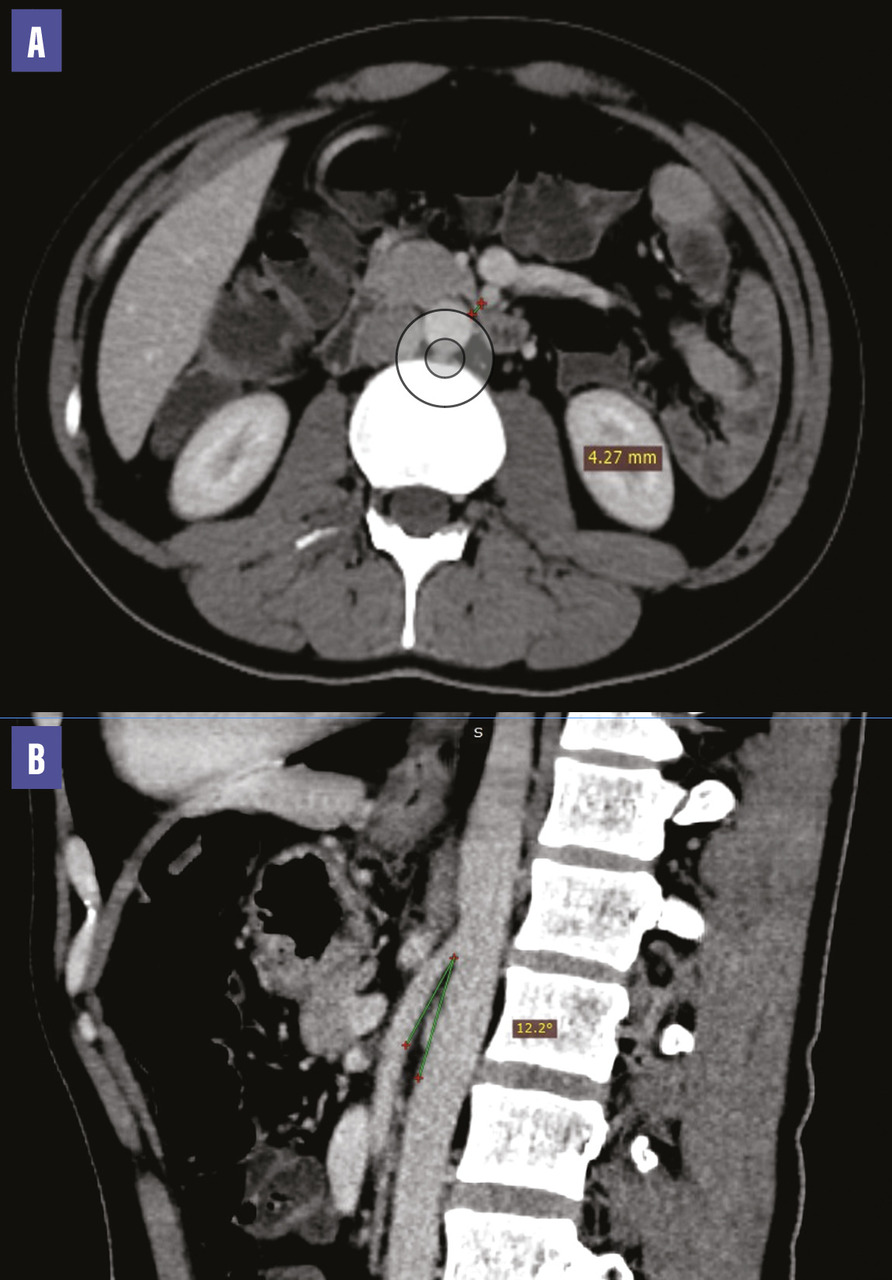
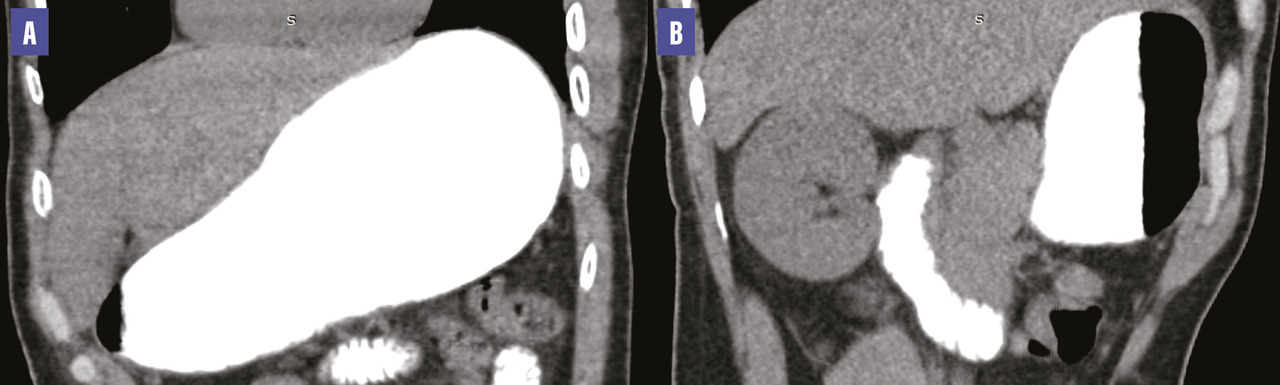
Une tomodensitométrie (TDM) abdominale met en évidence une compression de la troisième portion du duodénum par l’artère mésentérique supérieure associée à une importante dilatation de l’estomac et des deux premières portions du duodénum. L’angle aortomésentérique est mesuré à 12,2° et la distance aorte-artère mésentérique supérieure atteint 4,27 mm (fig. 1 et 2 ), ce qui a permis de poser le diagnostic du syndrome de la pince aortomésentérique.
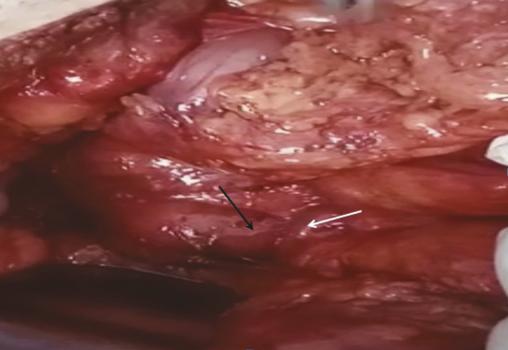
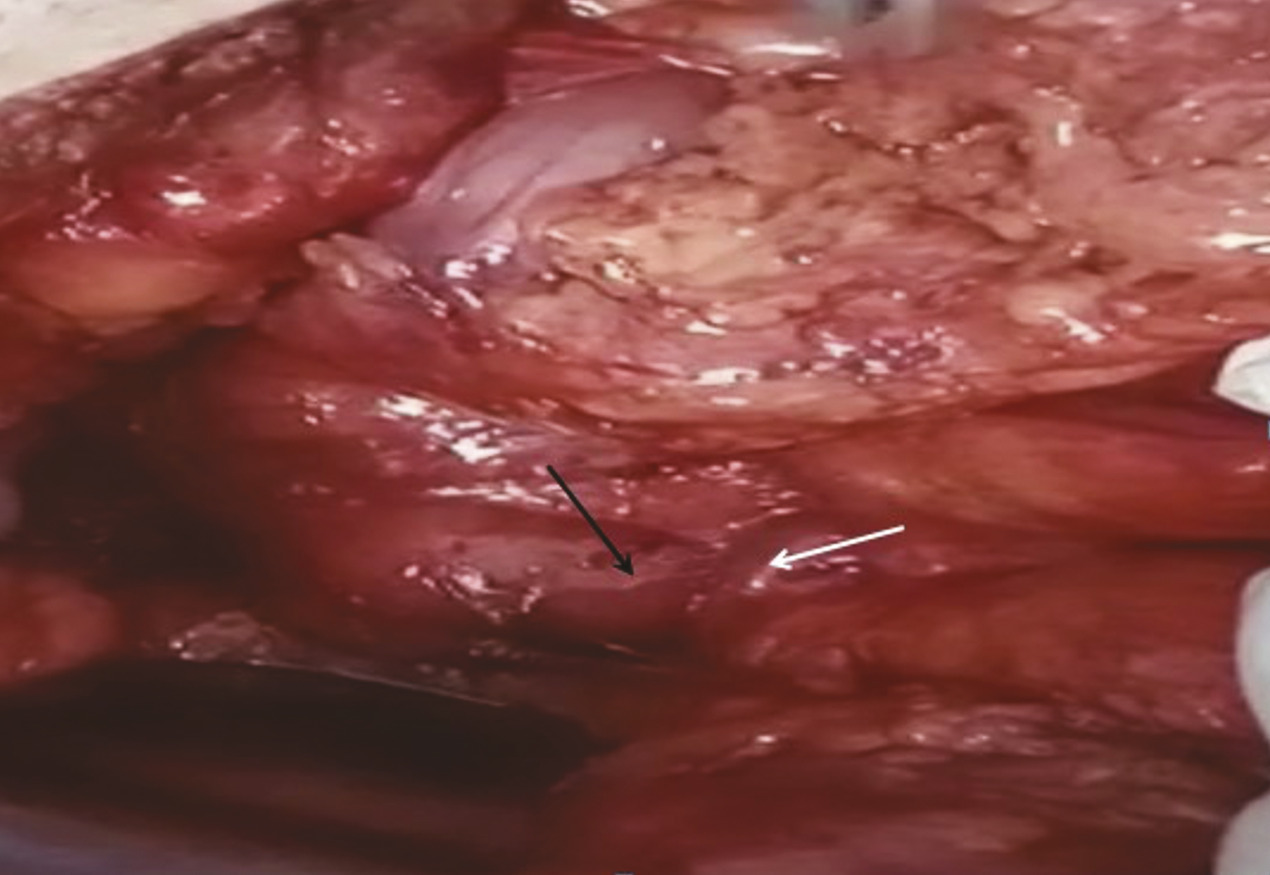
Le traitement médical initial a associé la mise en place d’une sonde nasogastrique et l’administration de solutions hydroélectrolytiques et métaboliques par voie parentérale. Cependant, après quinze jours de traitement, aucune amélioration clinique significative n’a été observée, la sonde gastrique a continué à drainer en moyenne 1 300 mL par jour. Face à cette situation, une intervention chirurgicale a été décidée. Lors de l’exploration chirurgicale réalisée par une incision médiane, une distension importante de l’estomac et du duodénum en amont de l’empreinte de l’artère mésentérique supérieure a été constatée ; en aval de cette empreinte, les anses grêles étaient aplaties (fig. 3 ). Une anastomose gastrojéjunale transmésocolique a été effectuée. Les suites postopératoires ont été normales. Les contrôles à un mois et à trois mois ont montré une nette amélioration des symptômes.
Une tomodensitométrie (TDM) abdominale met en évidence une compression de la troisième portion du duodénum par l’artère mésentérique supérieure associée à une importante dilatation de l’estomac et des deux premières portions du duodénum. L’angle aortomésentérique est mesuré à 12,2° et la distance aorte-artère mésentérique supérieure atteint 4,27 mm (
Le traitement médical initial a associé la mise en place d’une sonde nasogastrique et l’administration de solutions hydroélectrolytiques et métaboliques par voie parentérale. Cependant, après quinze jours de traitement, aucune amélioration clinique significative n’a été observée, la sonde gastrique a continué à drainer en moyenne 1 300 mL par jour. Face à cette situation, une intervention chirurgicale a été décidée. Lors de l’exploration chirurgicale réalisée par une incision médiane, une distension importante de l’estomac et du duodénum en amont de l’empreinte de l’artère mésentérique supérieure a été constatée ; en aval de cette empreinte, les anses grêles étaient aplaties (
Le syndrome de la pince aortomésentérique (SPAM) résulte de la compression du duodénum par l’aorte et l’artère mésentérique supérieure (AMS). En conditions normales, le duodénum est protégé par le tissu graisseux périvasculaire. Les causes du SPAM comprennent une prédisposition résultant de divers facteurs tels que la perte de poids, induisant un rétrécissement de l’angle aortomésentérique à la suite d’un amaigrissement rapide dans un contexte de maladies chroniques, de situations d’anorexie mentale, de malabsorption ou d’états cataboliques. Des anomalies anatomiques ou congénitales, telles que l’insertion haute du ligament de Treitz, la mal-rotation intestinale, une origine courte de l’AMS, ou une lordose lombaire, peuvent également contribuer à la prédisposition au SPAM. Des situations postopératoires, comme la chirurgie de la scoliose, la chirurgie bariatrique, ou la réparation chirurgicale d’un anévrisme de l’aorte, sont également des facteurs de risque.1
Cliniquement, le SPAM se manifeste par des symptômes tels que des douleurs épigastriques post-prandiales, des nausées, des vomissements et une sensation de satiété. Les patients peuvent ressentir un soulagement en adoptant des positions spécifiques, comme la position couchée, genou-poitrine, ou le décubitus latéral gauche. Dans certains cas, la symptomatologie peut être plus chronique, caractérisée par des plénitudes post-prandiales répétées et des vomissements intermittents. Le SPAM est plus fréquent chez les femmes.1,2
Ce syndrome implique l’utilisation de modalités d’imagerie spécifiques. Les examens de référence sont le transit œsogastroduodénal (TOGD) suivi d’un scanner injecté. En fluoroscopie, les signes distinctifs sont les suivants : dilatation des première et deuxième parties du duodénum, éventuellement associée à une dilatation gastrique, et rétrécissement brusque de la troisième partie du duodénum, caractérisé par un défaut vertical linéaire en forme de bande recouvrant la colonne vertébrale. Le flux antipéristaltique de baryte proximal à l’obstruction est mieux visualisé en position couchée, genou-poitrine, ou en décubitus latéral gauche. Le scanner injecté permet de visualiser une compression en bec de la troisième partie du duodénum entre l’AMS et l’aorte, avec des critères spécifiques tels qu’un angle aorto-AMS inférieur à 22 à 25° dans le plan sagittal et une distance aorto-AMS inférieure à 8 mm.
Les diagnostics différentiels incluent d’autres causes d’obstruction duodénale, nécessitant une gastroduodénoscopie pour éliminer les causes intraluminales, ainsi que des conditions telles que la sclérodermie intestinale et les sténoses duodénales qui ont des caractéristiques distinctes.1
Le traitement du SPAM est essentiellement médical en première ligne. Il consiste à décharger l’estomac et le duodénum à l’aide d’une sonde nasogastrique, tout en plaçant le patient en décubitus latéral gauche. Une attention particulière est accordée à la correction des déséquilibres hydroélectrolytiques et une alimentation hypercalorique double est instaurée, combinant une nutrition entérale par sonde naso-jéjunale et une nutrition parentérale. Bien que ce traitement médical atteigne un taux de succès d’environ 72 %, les récidives surviennent chez environ 30 % des patients traités. En cas d’inefficacité de la prise en charge médicale, caractérisée par l’absence d’amélioration des symptômes, après deux à douze jours, une approche chirurgicale peut être envisagée. Les interventions possibles incluent la création d’une dérivation par gastro- jéjunostomie ou duodéno-jéjunostomie, réalisables par voie laparoscopique. Alternativement, la modification des conditions anatomiques peut être entreprise, impliquant la mobilisation et le décroisement de l’angle duodéno-jéjunal, avec le positionnement du jéjunum à droite de l’aorte mésentérique supérieure après la section du muscle de Treitz.2
Cliniquement, le SPAM se manifeste par des symptômes tels que des douleurs épigastriques post-prandiales, des nausées, des vomissements et une sensation de satiété. Les patients peuvent ressentir un soulagement en adoptant des positions spécifiques, comme la position couchée, genou-poitrine, ou le décubitus latéral gauche. Dans certains cas, la symptomatologie peut être plus chronique, caractérisée par des plénitudes post-prandiales répétées et des vomissements intermittents. Le SPAM est plus fréquent chez les femmes.1,2
Ce syndrome implique l’utilisation de modalités d’imagerie spécifiques. Les examens de référence sont le transit œsogastroduodénal (TOGD) suivi d’un scanner injecté. En fluoroscopie, les signes distinctifs sont les suivants : dilatation des première et deuxième parties du duodénum, éventuellement associée à une dilatation gastrique, et rétrécissement brusque de la troisième partie du duodénum, caractérisé par un défaut vertical linéaire en forme de bande recouvrant la colonne vertébrale. Le flux antipéristaltique de baryte proximal à l’obstruction est mieux visualisé en position couchée, genou-poitrine, ou en décubitus latéral gauche. Le scanner injecté permet de visualiser une compression en bec de la troisième partie du duodénum entre l’AMS et l’aorte, avec des critères spécifiques tels qu’un angle aorto-AMS inférieur à 22 à 25° dans le plan sagittal et une distance aorto-AMS inférieure à 8 mm.
Les diagnostics différentiels incluent d’autres causes d’obstruction duodénale, nécessitant une gastroduodénoscopie pour éliminer les causes intraluminales, ainsi que des conditions telles que la sclérodermie intestinale et les sténoses duodénales qui ont des caractéristiques distinctes.1
Le traitement du SPAM est essentiellement médical en première ligne. Il consiste à décharger l’estomac et le duodénum à l’aide d’une sonde nasogastrique, tout en plaçant le patient en décubitus latéral gauche. Une attention particulière est accordée à la correction des déséquilibres hydroélectrolytiques et une alimentation hypercalorique double est instaurée, combinant une nutrition entérale par sonde naso-jéjunale et une nutrition parentérale. Bien que ce traitement médical atteigne un taux de succès d’environ 72 %, les récidives surviennent chez environ 30 % des patients traités. En cas d’inefficacité de la prise en charge médicale, caractérisée par l’absence d’amélioration des symptômes, après deux à douze jours, une approche chirurgicale peut être envisagée. Les interventions possibles incluent la création d’une dérivation par gastro- jéjunostomie ou duodéno-jéjunostomie, réalisables par voie laparoscopique. Alternativement, la modification des conditions anatomiques peut être entreprise, impliquant la mobilisation et le décroisement de l’angle duodéno-jéjunal, avec le positionnement du jéjunum à droite de l’aorte mésentérique supérieure après la section du muscle de Treitz.2
Références
1. Federle MP, Raman SP. Chapitre « Syndrome de l’AMS » dans Imagerie abdominale. 2020. Ed. Elsevier Masson:324-5
2. Tidjane A, Tabeti B, Benmaarouf N, Boudjenan N, Bouziane C, Kessai N. Le syndrome de la pince aorto-mésentérique: rare, mais pensez-y. Pan Afr Med J 2014;17:47.
2. Tidjane A, Tabeti B, Benmaarouf N, Boudjenan N, Bouziane C, Kessai N. Le syndrome de la pince aorto-mésentérique: rare, mais pensez-y. Pan Afr Med J 2014;17:47.
Une question, un commentaire ?