Les troubles vésico-sphinctériens sont fréquents dans les pathologies neurologiques, et leur type diffère selon la localisation et l’étendue lésionnelle. Ces troubles, lorsqu’ils ne sont pas pris en charge, exposent le patient à de potentielles complications urologiques (lithiases rénale et vésicale, infections urinaires récidivantes, insuffisance rénale) et extra-urologiques ; ils peuvent altérer significativement la qualité de vie et parfois compromettre l’autonomie du patient.1,2 Si les centres spécialisés en neuro-urologie jouent un rôle essentiel dans le parcours de soins, le médecin généraliste occupe également une place primordiale, tant pour la prise en charge initiale que pour le suivi de ces patients.
Physiopathologie
L’appareil vésico-sphinctérien comprend la vessie, l’urètre, ainsi que le complexe sphinctérien (sphincter lisse et sphincter strié). Chez l’homme, la prostate se situe entre le sphincter lisse, situé au niveau du col vésical, et le sphincter strié, situé au niveau de l’apex prostatique.
Fonctionnement vésico-sphinctérien normal
L’appareil vésico-sphinctérien assure à la fois un rôle social et de confort – en transformant une sécrétion rénale lente et continue en une miction brève, facile et complète – et un rôle de sécurité – en maintenant un régime de basse pression au sein du bas et du haut appareil urinaire. Pour cela, l’appareil vésico-sphinctérien alterne entre une phase de « remplissage » vésical et une phase de « vidange » vésicale. C’est ce qu’on appelle le cycle mictionnel.
Au cours de la phase de remplissage, la vessie joue un rôle de réservoir et se laisse distendre à basse pression au fur et à mesure que les urines sont sécrétées par les reins. Le maintien des basses pressions permet d’éviter les épisodes d’incontinence urinaire et de préserver la fonction rénale. Au cours de cette phase de remplissage, le complexe sphinctérien augmente progressivement en contraction, et ce, de manière réflexe, afin de parfaire la continence urinaire. Au cours de la phase de vidange vésicale, la vessie se contracte et l’appareil sphinctérien se relâche de manière synergique, afin de permettre une vidange vésicale brève, facile, complète et à basse pression.
Contrôle neurologique de l’appareil vésico-sphinctérien
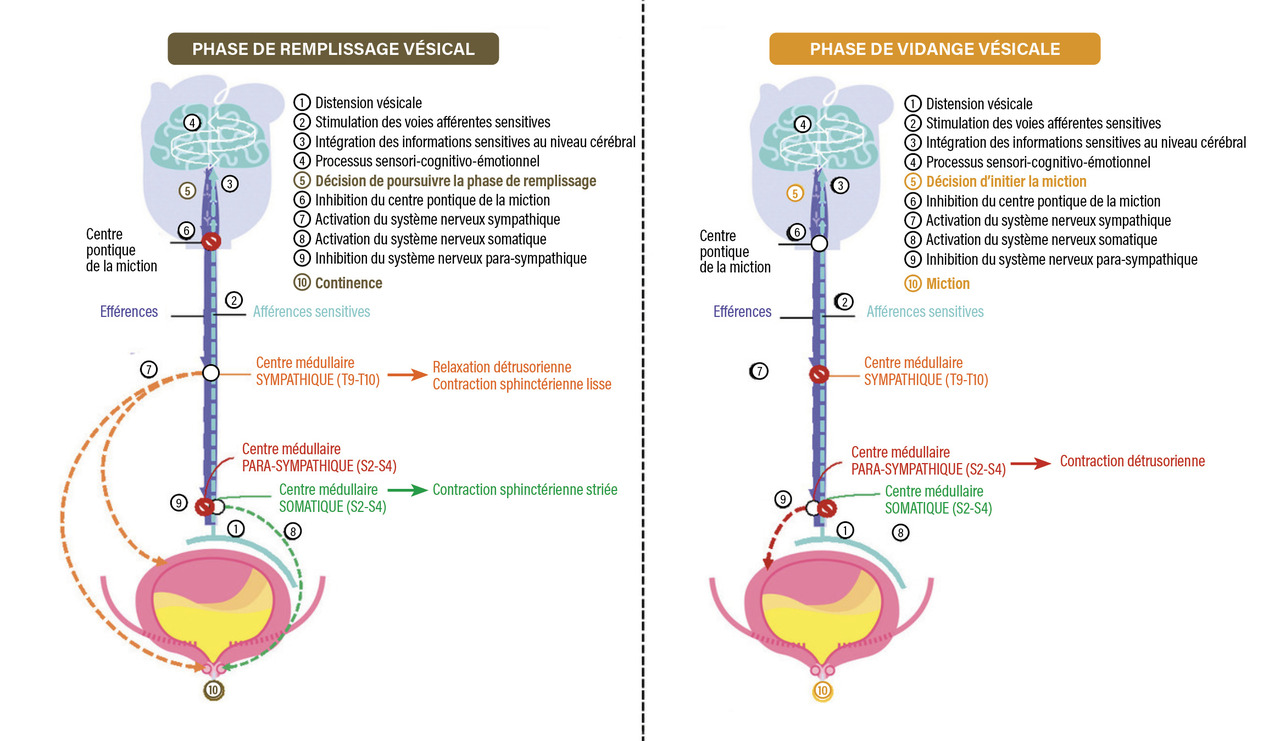
Le contrôle du cycle mictionnel est sous l’influence des systèmes nerveux périphérique et central, comprenant les voies afférentes sensitives et les voies efférentes somatiques et sympathiques, favorisant le maintien de la continence urinaire ; et les voies efférentes parasympathiques, favorisant l’initiation et le maintien de la miction (fig. 1).2 Au niveau cérébral, de multiples réseaux neuronaux sont impliqués dans la régulation du cycle mictionnel et permettent, en traitant les informations contextuelles sensori-cognitivo-émotionnelles, de proposer à chaque instant la réponse la plus adaptée : poursuivre la phase de remplissage ou initier la phase de vidange.
Dysfonctionnements vésico-sphinctériens associés aux lésions neurologiques
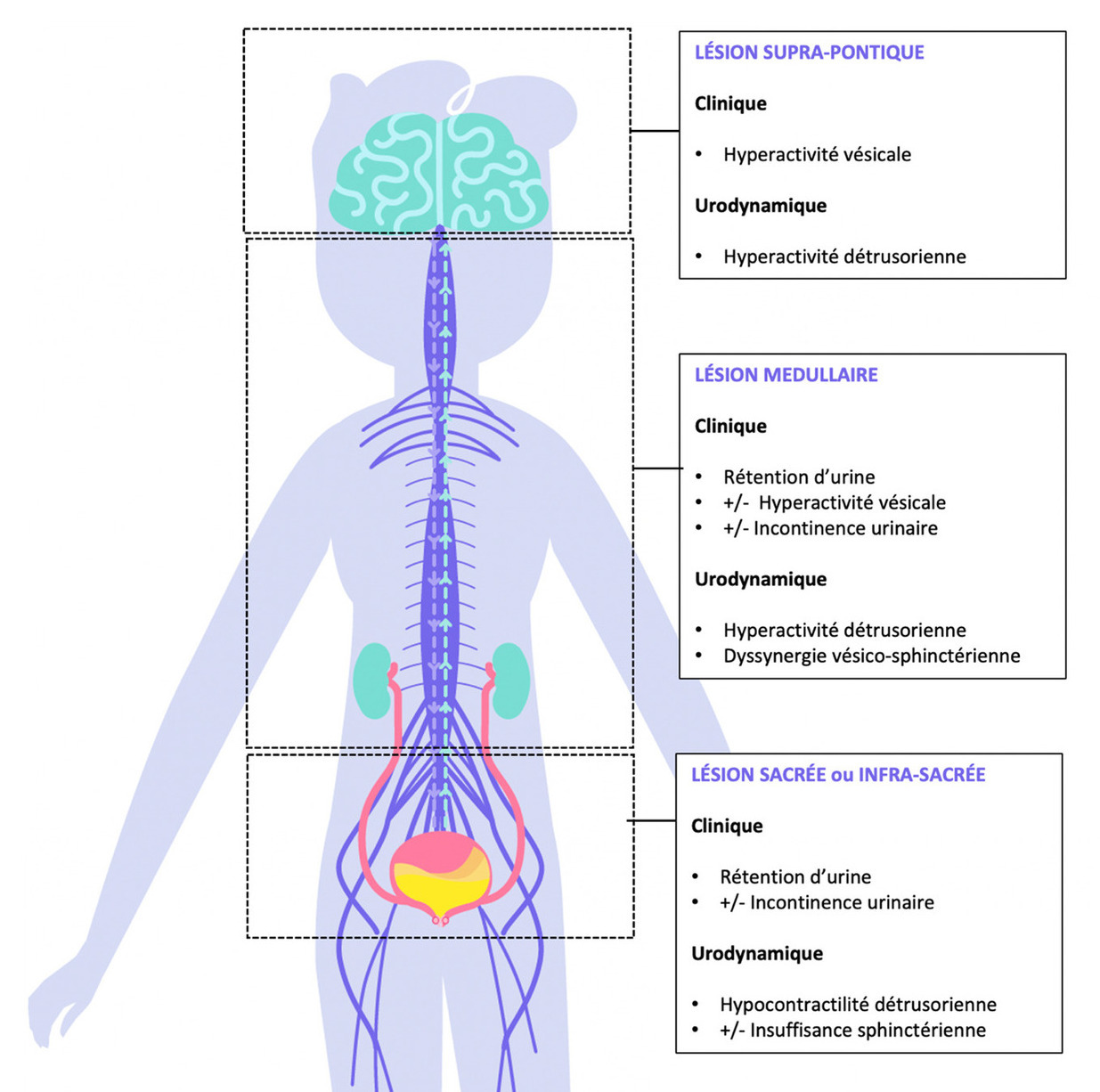
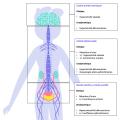
Les conséquences des atteintes neurologiques sur le cycle mictionnel dépendent de la localisation et de l’étendue lésionnelle. Ainsi, ces atteintes sont classées en lésions cérébrales (suprapontiques), lésions médullaires (infrapontiques et suprasacrées) et lésions périphériques (sacrées ou infrasacrées) [fig. 2].
L’épidémiologie et les caractéristiques des troubles vésico-sphinctériens des atteintes neuro-urologiques les plus fréquentes sont résumées dans le tableau.
Évaluation minutieuse
Les objectifs de la prise en charge d’une vessie neurologique comprennent : la prévention des complications urologiques (infections urinaires récidivantes, lithiases rénales et vésicales, dégradation de la fonction rénale) et extra-urologiques (escarre périnéale, hyperréflexie autonome, constipation, dysfonction sexuelle, infertilité), l’amélioration de la qualité de vie (incontinence urinaire) et la promotion de l’autonomie du patient.1
L’évaluation des troubles vésico-sphinctériens neurogènes est aujourd’hui bien codifiée. Elle doit s’attacher à apprécier successivement la phase de vidange puis la phase de remplissage vésical et à rechercher systématiquement les complications pouvant survenir au niveau du bas et du haut appareil urinaire.
En médecine générale, cette évaluation consiste en la réalisation d’un calendrier mictionnel (sur trois jours) et en l’observation morphologique et fonctionnelle du bas et du haut appareil urinaire par une échographie rénovésicale et par le dosage de la créatininémie. En cas de sarcopénie, le dosage de la créatininémie est associé à un dosage de la créatininurie des vingt-quatre heures ou, à défaut, à un dosage sanguin de la cystatine C.
La prise en charge au sein de centres spécialisés en neuro-urologie, faisant intervenir neuro-urologues et médecins rééducateurs, permet la réalisation d’un bilan urodynamique, seul à même d’objectiver l’équilibre vésico-sphinctérien. En fonction du contexte, la réalisation d’une urétrocystoscopie ou d’une urétrocystographie rétrograde et mictionnelle (UCRM) peut aussi être proposée. L’utilisation de scores de symptômes, comme le score Urinary Symptom Profile (USP) et de scores de qualité de vie liée aux symptômes urinaires, comme le Qualiveen Short Form, peuvent aider à préciser la plainte fonctionnelle.3,4 Pour l’ensemble des patients, il est en outre nécessaire de rechercher systématiquement des épines irritatives pouvant exacerber les troubles vésicosphinctériens : constipation, escarre, douleur, infection. Les facteurs extra-urologique pouvant influer sur la prise en charge (cognition, dextérité, vision, spasticité, contexte social, évolutivité de la pathologie) doivent aussi être évalués systématiquement.
Situations particulières
Trouble de la vidange chez l’homme
Un trouble de la vidange vésical peut coexister avec une pathologie neurologique, en particulier chez les hommes de plus de 50 ans. Chez les hommes atteints d’une pathologie neurologique, il n’est pas toujours aisé de faire la part entre les troubles vésicosphinctériens neurogènes et ceux dus à un obstacle sous-vésical anatomique, comme l’hypertrophie bénigne de la prostate (HBP). Il est donc nécessaire, avant toute prise en charge chirurgicale de l’HBP, que ces patients soient évalués en centre spécialisé de neuro-urologie.
Myéloméningocèles
Avec une incidence estimée entre 1,3 et 1,6/100 000 naissances,5 le spina bifida est souvent associé à des troubles vésicosphinctériens complexes avec classiquement une hyperactivité détrusorienne, un trouble de compliance vésicale, une incontinence urinaire et un trouble de la vidange vésicale.1 Le suivi doit être réalisé au sein de centres de référence ou de compétence.
Prise en charge thérapeutique
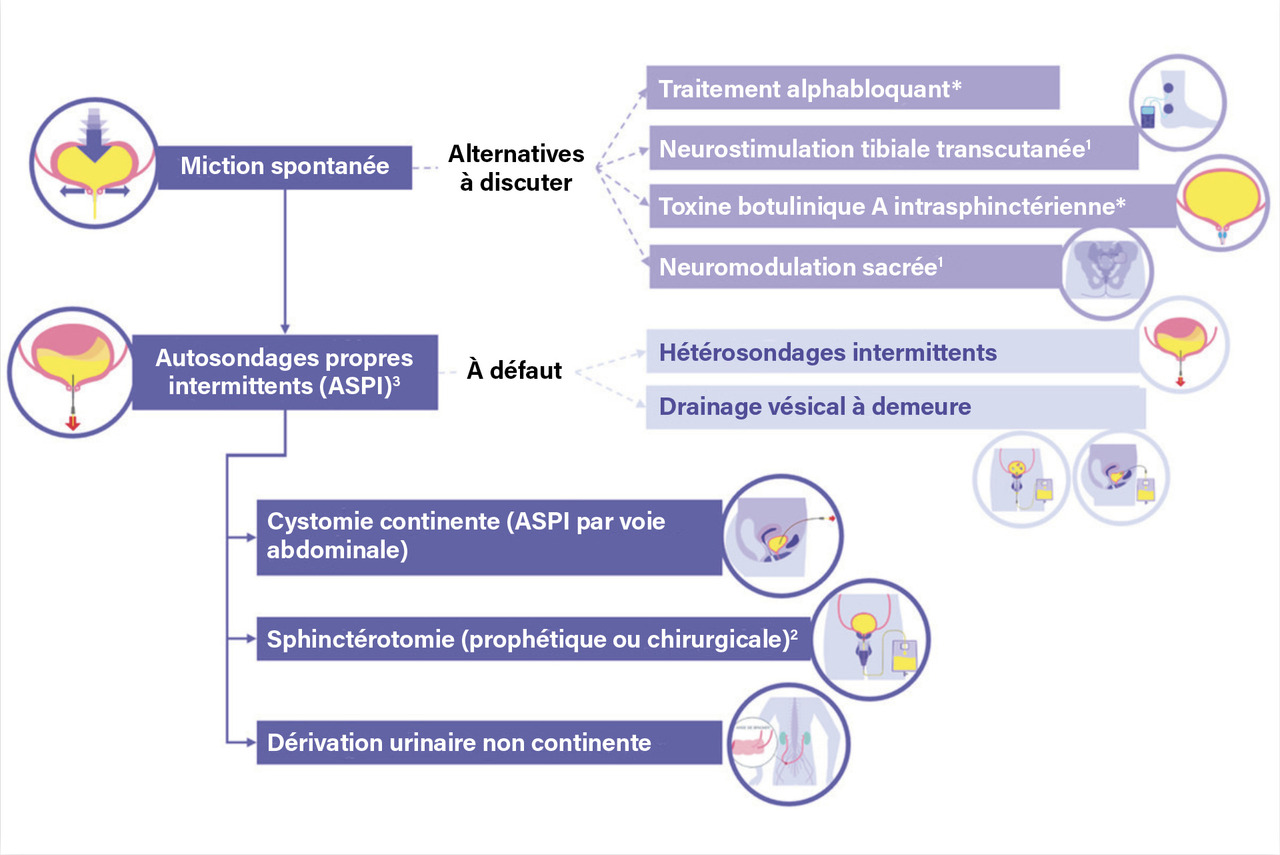
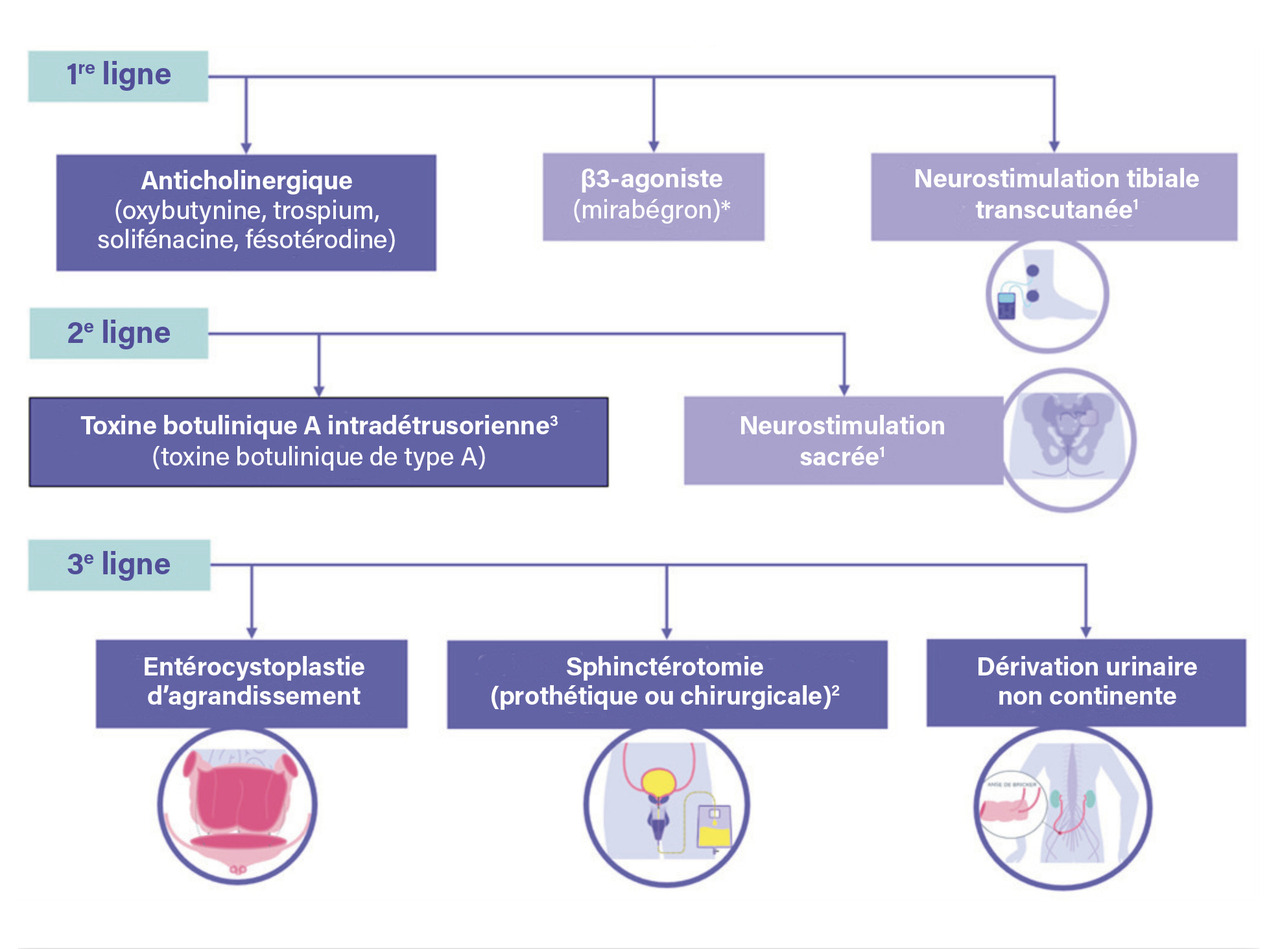
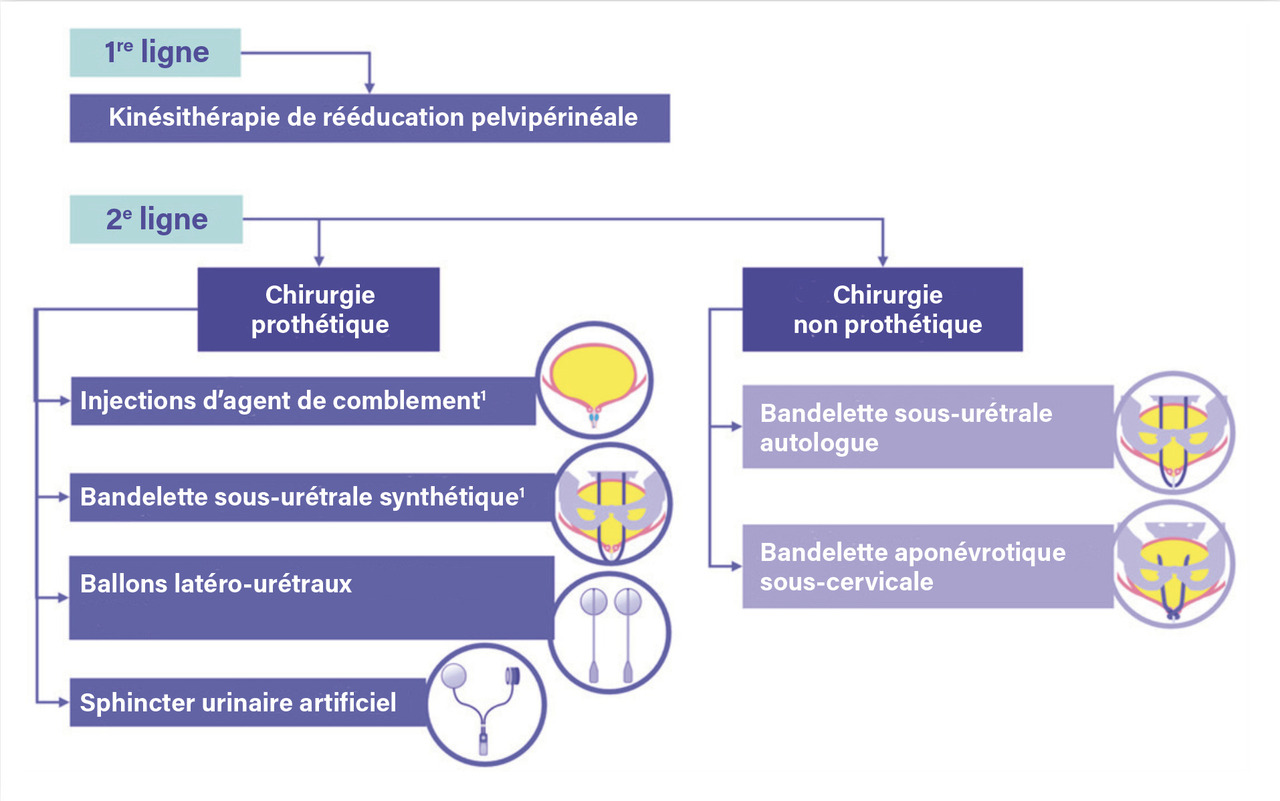
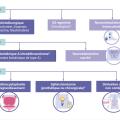
Le but du traitement est de rétablir l’équilibre entre vidange et réservoir vésical. Les figures 3, 4 et 5 détaillent l’algorithme thérapeutique de la vessie neurologique.
Choix du mode mictionnel
La prise en charge d’une vessie neurologique doit toujours débuter par le choix du mode mictionnel le plus adapté, c’est-à-dire permettant une vidange vésicale complète, rapide, régulière et à basse pression. Si la miction spontanée est possible, elle doit être privilégiée.
Autosondages propres intermittents
Dans le cas contraire, les autosondages propres intermittents (ASPI) constituent le mode mictionnel de référence, sous réserve que le patient ait les capacités fonctionnelles et cognitives pour les réaliser.6 Les ASPI doivent être initiés dans le cadre d’une éducation thérapeutique dédiée afin d’assurer leur bonne réalisation et leur pérennité sur le long terme.
Alphabloquants
En alternative, chez les patients le souhaitant et en fonction du bilan initial réalisé en centre spécialisé de neuro-urologie, peut être proposé de manière plus marginale un traitement par alphabloquant – hors autorisation de mise sur le marché (AMM) –, l’implantation d’une neuromodulation sacrée ou des injections intrasphinctériennes de toxine botulinique A (hors AMM).
Cystostomie continente
Lorsque les ASPI ne peuvent être réalisés par les voies naturelles (altération de la dextérité, spasticité des membres inférieurs, difficulté aux transferts), la réalisation d’une cystostomie continente, consistant en la confection d’un conduit entre la vessie et la paroi abdominale – à partir de l’appendice (Mitrofanoff) ou d’un segment d’intestin grêle (Monti, Casale) – peut permettre la réalisation des ASPI par voie abdominale.
Chirurgie de dérivation urinaire non continente
À l’extrême, une chirurgie de dérivation urinaire non continente (dérivation cutanée transiléale selon Bricker), associée à un geste de cystectomie, peut être discutée.
Sondage à demeure en dernier recours
Le sondage à demeure, par sonde vésicale ou cathéter sus-pubien, expose le patient à des infections urinaires récidivantes (court terme), à une altération morphologique et fonctionnelle du haut appareil urinaire (moyen terme) ainsi qu’au risque de tumeur vésicale (long terme).1,2 En outre, la sonde vésicale positionnée par voie transurétrale se complique souvent de lésions, voire de lacérations péniennes (chez l’homme) et périnéales (chez la femme). Le drainage à demeure prolongé ne doit donc être envisagé qu’en l’absence d’alternative raisonnable.
Obtention d’un réservoir vésical se remplissant à basse pression
La prise en charge d’une vessie neurologique doit ensuite permettre d’obtenir un réservoir vésical se remplissant à basse pression.
Anticholinergiques et agoniste ß3 -adrénergique
En cas d’hyperactivité détrusorienne, les anticholinergiques constituent le traitement de première ligne. Xérophtalmie, xérostomie et constipation en sont des effets indésirables les plus fréquents.
Le mirabégron, agoniste ß3 -adrénergique, semble avoir une efficacité similaire sur les symptômes d’hyperactivité vésicale, en évitant les effets indésirables associés aux anticholinergiques (hors AMM). En revanche, son efficacité sur l’hyperactivité détrusorienne neurogène semble limitée. En 2025, ce médicament n’est pas remboursé en France.1
Neurostimulation du nerf tibial par voie transcutanée
La neurostimulation du nerf tibial par voie transcutanée, à raison d’une séance de vingt minutes auto-administrée quotidiennement, se positionne comme un traitement non médicamenteux et non invasif. Cette thérapie, remboursée par l’Assurance maladie, a montré son efficacité sur l’hyperactivité vésicale neurogène.
Toxine botulinique en deuxième ligne
En cas d’échec des traitements de première ligne, les injections intradétrusoriennes de toxine botulinique A – réalisées par voie endoscopique sous anesthésie locale en consultation – ont l’AMM dans le traitement de l’hyperactivité détrusorienne neurogène avec incontinence urinaire non contrôlée par un traitement anticholinergique, chez les patients blessés médullaires et les patients atteints de sclérose en plaques. En outre, elles sont parfois proposées hors AMM dans d’autres pathologies neurologiques. Compte tenu du risque élevé de trouble de la vidange vésicale iatrogène, les patients doivent être en capacité et doivent avoir accepté de réaliser des ASPI avant la première injection. La toxine botulinique A en injection intradétrusorienne a une efficacité temporaire et doit être répétée régulièrement, tous les six à douze mois selon les patients.
Neuromodulation sacrée en cours d’évaluation
La neuromodulation sacrée, consistant en l’implantation unilatérale d’un stimulateur au niveau d’une racine sacrée S3, est encore en cours d’évaluation pour le traitement de l’hyperactivité vésicale neurogène ; il n’y a pas encore aujourd’hui de données robustes quant à son efficacité urodynamique à court ou moyen terme.
Chirurgie en troisième intention
En cas d’échec des traitements de deuxième ligne, une chirurgie d’agrandissement vésical par entérocystoplastie peut être proposée chez des patients sélectionnés.
Chez l’homme ayant une lésion médullaire suprasacrée, la sphinctérotomie, consistant en la section du sphincter strié par voie endoscopique, constitue une alternative permettant de rétablir des mictions réflexes à basse pression, mais nécessite le port permanent d’un étui pénien.
En dernier recours, une chirurgie de dérivation urinaire non continente (dérivation cutanée transiléale selon Bricker) associée à un geste de cystectomie peut être discutée.
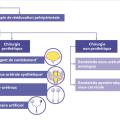
Résistances urétrales : que faire en cas d’incontinence urinaire d’effort persistante ?
En cas d’incontinence urinaire d’effort – le plus souvent en lien avec une insuffisance sphinctérienne – persistant après équilibre de la vidange et du réservoir vésical, une kinésithérapie pelvipérinéale peut être proposée.
Elle n’a cependant de sens que chez les patients n’ayant pas d’altération cognitive trop importante et ayant un contrôle et une sensibilité périnéaux préservés.
En cas d’échec ou d’impossibilité à réaliser une rééducation pelvi-périnéale, plusieurs techniques chirurgicales peuvent être proposées, en fonction des attentes et des capacités fonctionnelles et cognitives du patient (injection péri-urétrale d’agent de comblement : gel de polyacrylamide), implantation de ballons latéro-urétraux, pose d’une bandelette sous-urétrale autologue ou synthétique, implantation d’un sphincter urinaire artificiel péricervical.7
Suivi en médecine de ville
Le suivi d’un patient présentant une vessie neurologique consiste à vérifier que les objectifs de prise en charge sont atteints, en particulier le maintien de basses pressions au sein du réservoir vésical. En médecine de ville, cette surveillance repose principalement sur le calendrier mictionnel sur trois jours, le relevé de la fréquence des infections urinaires, l’échographie rénovésicale (recherchant une urétéro-hydronéphrose, la trophicité rénale, des lithiases rénales et vésicales, un résidu post-mictionnel) et la mesure de la fonction rénale. L’infection urinaire doit toujours être distinguée de la colonisation urinaire ; celle-ci (présente chez plus de 80 % des patients réalisant des ASPI et correspondant à la présence d’une ou de plusieurs bactéries dans les urines ne s’associant à aucune symptomatologie) ne doit être ni recherchée ni traitée (en dehors du cas particulier des femmes enceintes et dans le contexte de geste réalisé au contact de l’urine : bilan urodynamique [BUD], injection intradétrusorienne de toxine botulinique A…).
Chez les patients présentant une hyperactivité détrusorienne, en cas de modification des symptômes ou en cas d’échec d’un traitement de première ligne, un bilan urodynamique doit être réalisé dans un centre spécialisé en neuro-urologie et répété à intervalles réguliers.1
Le suivi doit être au moins annuel, mais sa fréquence est à adapter selon l’évaluation du risque uronéphrologique du patient. L’aggravation brutale des symptômes urologiques, la survenue d’infections urinaires récidivantes, l’apparition d’une hématurie macroscopique et/ou la dégradation de la fonction rénale constituent des drapeaux rouges qui doivent amener à une prise en charge urgente dans un centre spécialisé en neuro-urologie.8
Prévenir les complications et améliorer la qualité de vie
Les pathologies neurologiques sont fréquemment responsables de troubles vésico-sphinctériens, dépendant à la fois de la localisation et de l’étendue lésionnelle. Le diagnostic et la prise en charge des vessies neurologiques imposent d’évaluer et de prendre en compte le mode mictionnel et le fonctionnement du réservoir vésical ainsi que l’état des résistances urétrales, afin de prévenir à la fois les complications urologiques et extra-urologiques, d’améliorer la qualité de vie et de promouvoir l’autonomie du patient.
2. Abrams P, Cardozo L, Wagg A, et al. Incontinence, 6th Edition. Bristol UK: ICI-ICS. International Continence Society, 2017.
3. Haab F, Richard F, Amarenco G, et al. Comprehensive evaluation of bladder and urethral dysfunction symptoms: Development and psychometric validation of the Urinary Symptom Profile (USP) questionnaire. Urology 2008;71(4):646‑56.
4. Bonniaud V, Bryant D, Parratte B, et al. Development and validation of the short form of a urinary quality of life questionnaire: SF-Qualiveen. J Urol 2008;180(6):2592‑8.
5. Peyronnet B, Gao F, Brochard C, et al. Épidémiologie du spina bifida en France. Progrès en Urologie 2016;26(13):721.
6. Game X, Phe V, Castel-Lacanal E, et al. Intermittent catheterization: Clinical practice guidelines from Association française d’urologie (AFU), Groupe de neuro-urologie de langue française (GENULF), Société française de médecine physique et de réadaptation (SOFMER) and Société interdisciplinaire francophone d’urodynamique et de pelvi-périnéologie (SIFUD-PP). Progrès en Urologie 2020;30(5):232‑51.
7. Chartier Kastler E, Genevois S, Game X, et al. Treatment of neurogenic male urinary incontinence related to intrinsic sphincter insufficiency with an artificial urinary sphincter: A French retrospective multicentre study. BJU Int 2011;107(3):426‑32.
8. Drake MJ, Apostolidis A, Cocci A, et al. Neurogenic lower urinary tract dysfunction: Clinical management recommendations of the neurologic incontinence committee of the Fifth International Consultation on Incontinence 2013. Neurourol Urodyn 2016;35(6):657‑65.