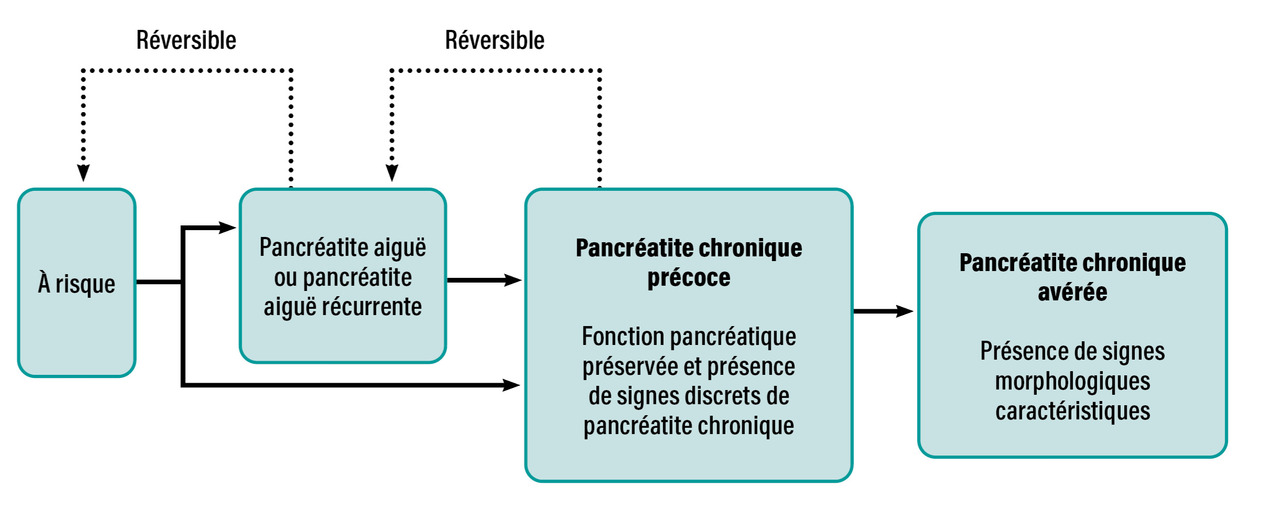
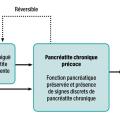
La pancréatite chronique se caractérise par des altérations morphologiques irréversibles du tissu exocrine et endocrine, associant inflammation et fibrose.1 Mais cette définition se heurte à l’absence habituelle de preuve histologique. Les sociétés savantes (International Association of Pancreatology, American Pancreatic Association, Japan Pancreas Society et European Pancreatic Club) intègrent maintenant le continuum pancréatite aiguë, pancréatites aiguës récidivantes, pancréatite chronique débutante et pancréatite chronique avérée, sur la base de critères cliniques et morphologiques (fig. 1).2,3
La définition d’une pancréatite chronique ne préjuge pas de sa cause.4 L’alcool est identifié comme la cause la plus fréquente de pancréatite chronique dans les pays occidentaux, représentant 60 à 80 % des cas. Le tabac est également un facteur de risque indépendant et synergique, présent chez plus de 60 % des patients atteints de pancréatite chronique. La combinaison alcool-tabac a un effet multiplicatif sur le risque et la progression de la maladie.3
La découverte de mutations de gènes de prédisposition aux pancréatites chroniques (PRSS1, CFTR, SPINK1, TRPV6…) a néanmoins marqué un tournant dans la pancréatologie et a permis de sortir du schéma classique de la pancréatite chronique alcoolique. Enfin, dans 5 à 10 % des cas, aucune cause n’est mise en évidence et on parle alors de pancréatite chronique idiopathique.
Les objectifs d’une définition appropriée de la pancréatite chronique sont multiples :
- apporter aux patients une approche thérapeutique holistique adaptée ;
- établir un diagnostic à un stade précoce pour agir sur l’histoire naturelle de la pancréatite chronique ;
- définir un cadre nosologique pour les études scientifiques.
Signes variés et peu caractéristiques
La présentation de la pancréatite chronique est variée : découverte fortuite, manifestations douloureuses aiguës ou chroniques, diarrhée par insuffisance pancréatique exocrine, diabète. Dans 30 à 65 % des cas, le diagnostic de pancréatite chronique est établi chez un patient n’ayant jamais eu d’épisode de pancréatite aiguë.2 Parfois, c’est lors du diagnostic de cancer du pancréas que l’on découvre une pancréatite chronique sous-jacente.
La prévalence de la pancréatite chronique est de 25 à 98/100 000 et son incidence de 5 à 10/100 000 par an, mais ces chiffres sont probablement sous-évalués du fait de la difficulté diagnostique des formes précoces.3
Le diagnostic de pancréatite chronique s’appuie sur la tomodensitométrie et l’imagerie par résonance magnétique
Les signes histologiques de la pancréatite chronique sont une inflammation, une fibrose inter- puis intralobulaire, une perte de cellules acineuses et des îlots de Langerhans avec une atrophie glandulaire et des calcifications parenchymateuses ou intracanalaires. Ces lésions peuvent être focales ou diffuses, leur répartition dans le pancréas est hétérogène. À l’exception de la pancréatite auto-immune, ces signes n’ont pas de spécificité orientant vers la cause de la pancréatite chronique.
La mise en évidence de ces lésions et donc le diagnostic de la pancréatite chronique reposent sur l’imagerie.
Tomodensitométrie pour identifier des lésions caractéristiques
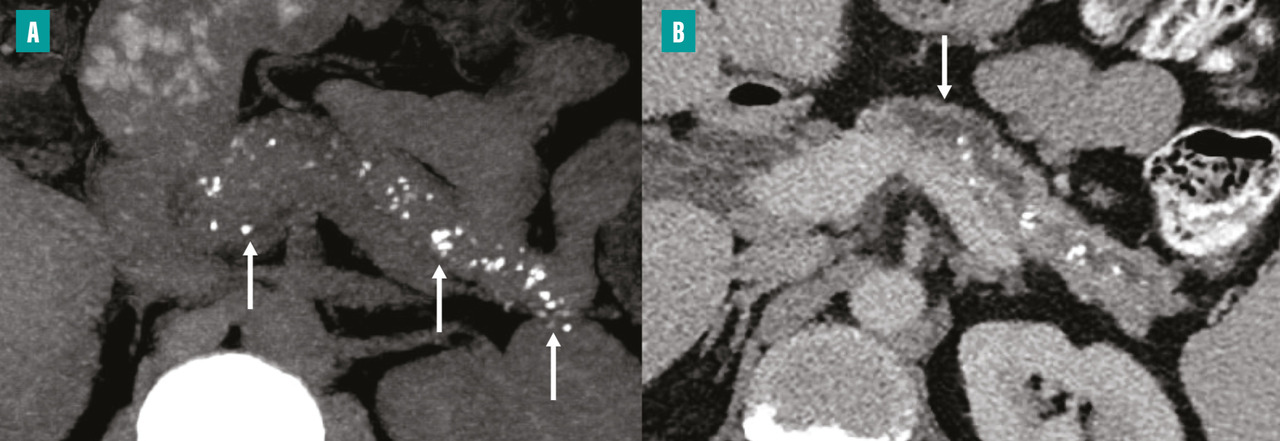
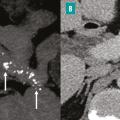
La tomodensitométrie (TDM) est l’examen initial le plus approprié en cas de suspicion de pancréatite chronique, car elle permet d’identifier des lésions caractéristiques telles que les calcifications parenchymateuses ou des conduits pancréatiques, ainsi que l’atrophie du parenchyme pancréatique. Un protocole TDM optimal comprend des acquisitions sans injection de produit de contraste, une phase artérielle pancréatique (environ 35 à 40 secondes après l’injection) et une phase veineuse (70 à 80 secondes après l’injection). Les calcifications sont facilement détectées sous forme d’hyperdensités spontanées sur les acquisitions sans injection. Elles peuvent être de taille variable. Dans les formes avancées de pancréatite chronique, la TDM peut montrer une dilatation irrégulière du conduit pancréatique principal (fig. 2) et d’éventuelles complications, notamment les pseudokystes et les atteintes vasculaires. La TDM est en revanche moins performante dans les formes précoces de pancréatite chronique, en particulier en l’absence de calcifications. La taille et le nombre des calcifications pancréatiques doivent être évalués, car le degré de calcification dans la pancréatite chronique peut refléter l’évolution et la gravité la maladie.5 La présence de grosses calcifications constitue un signe très évocateur de pancréatite chronique. Cependant, certaines calcifications parenchymateuses pancréatiques liées au vieillissement, généralement ponctiformes (de 1 à 3 mm), ne traduisent pas nécessairement une pancréatite chronique.6
Imagerie par résonance magnétique et cholangio-pancréatographie-IRM, examens de référence
L’imagerie par résonance magnétique (IRM) en particulier lorsqu’elle est associée à la cholangio-pancréatographie-IRM (CP-IRM), est considérée comme l’examen d’imagerie diagnostique de référence pour la pancréatite chronique. Elle permet de détecter des calcifications, l’atrophie pancréatique, ainsi qu’une obstruction ou une dilatation des conduits.
La CP-IRM, fondée sur des séquences fortement pondérées en T2, permet une visualisation dédiée et non invasive des conduits biliopancréatiques en deux et trois dimensions et elle est plus sensible que la TDM pour l’évaluation des anomalies canalaires.
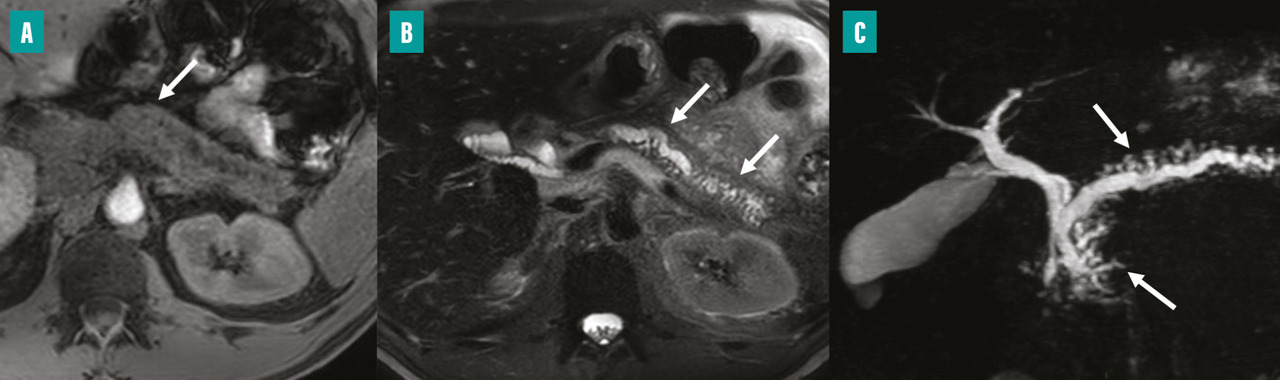
Dans les formes précoces de pancréatite chronique, l’IRM peut révéler une hypo-intensité du signal pancréatique sur les séquences pondérées en T1 avec suppression du signal graisseux (perte de l’hypersignal T1 physiologique de la glande), un retard et un aspect hétérogène de rehaussement du parenchyme pancréatique (lié à la présence de fibrose) ainsi qu’une dilatation des conduits secondaires.
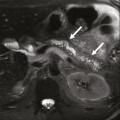
Dans les formes plus avancées, la CP-IRM met en évidence une atrophie plus marquée de la glande pancréatique, avec aspect en hyposignal T1, des dilatations irrégulières moniliformes du conduit pancréatique principal et des dilatations en « flammèches » des conduits secondaires (fig. 3).
Indications réduites pour l’endoscopie
Avant qu’elle ne soit définitivement supplantée par la CP-IRM pour le diagnostic de pancréatite chronique, la cholangio-pancréatographie rétrograde endoscopique (CPRE), avait démontré une excellente sensibilité et une spécificité proche de 100 % en décrivant les anomalies canalaires qui ont permis d’aboutir à la classification de Cambridge.7
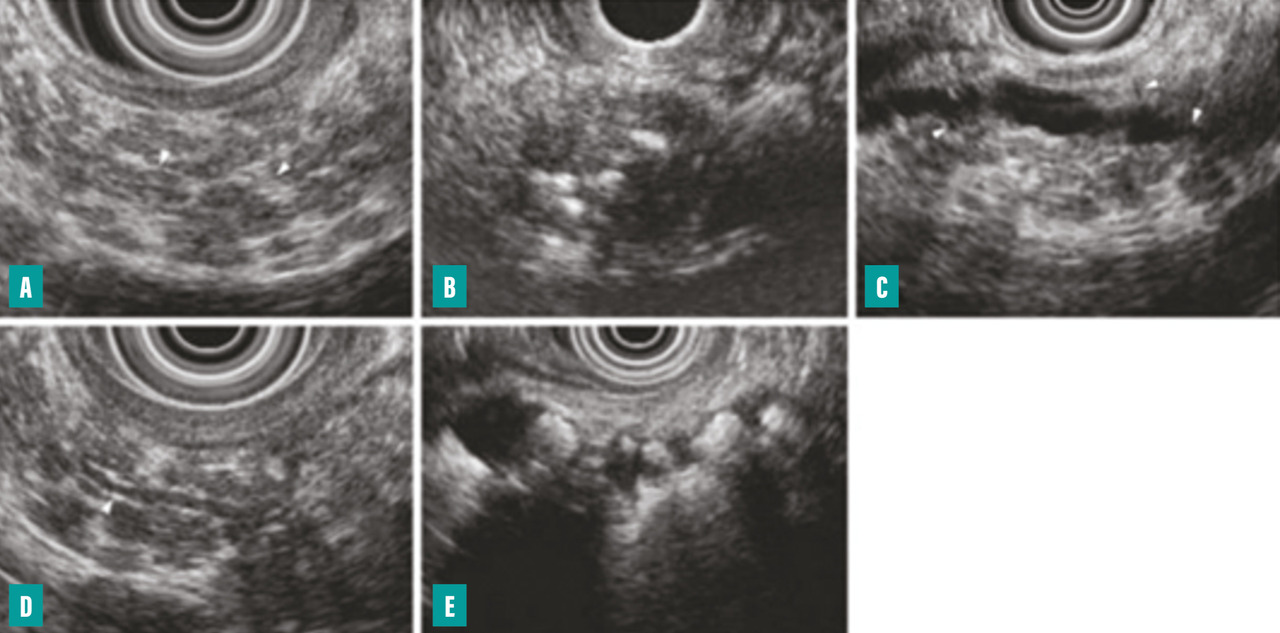
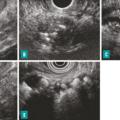
L’écho-endoscopie, apparue dans les années 1990, s’est positionnée comme l’examen de choix pour le diagnostic des pancréatites chroniques débutantes pour lesquelles la TDM et l’IRM manquent de sensibilité. La classification de Rosemont a défini des critères majeurs et mineurs concernant le parenchyme pancréatique et les canaux (fig. 4).8 Mais cet examen se heurte à deux limites : son manque de spécificité pour le diagnostic de pancréatite chronique et son caractère opérateur-dépendant.
Les nouvelles techniques (élastographie et écho-endoscopie de contraste) n’ont pas fait la preuve de leur intérêt pour le diagnostic de pancréatite chronique.
L’intérêt de l’écho-endoscopie est l’obtention d’une preuve histologique par la ponction (à l’aide d’une aiguille coupante) dans les formes focales (pseudomasses) pour le diagnostic de pancréatite auto-immune et le diagnostic différentiel de cancer pancréatique. En revanche, si l’imagerie est évocatrice d’une simple pancréatite chronique, il n’y a aucune indication à réaliser une ponction pour confirmation histologique de ce diagnostic.
Analyses biologiques restreintes à la recherche de complications
Jusque dans les années 1990, la réalisation de tests fonctionnels était recommandée (mesure du débit sécrétoire et enzymatique après injection de sécrétine), mais cela a été complètement abandonné. En pratique, on utilise les dosages de l’élastase fécale sur échantillon de selles pour rechercher une insuffisance pancréatique exocrine et le dosage de l’Hba1c et de la glycémie à jeun pour rechercher un diabète, qui sont deux des principales complications de la pancréatite chronique.
Des études sont en cours pour rechercher des marqueurs diagnostiques de pancréatite chronique, mais aucun dosage biologique n’a actuellement fait la preuve de son intérêt.
Diagnostics différentiels
L’imagerie joue un rôle crucial pour distinguer la pancréatite chronique d’autres affections, en particulier l’adénocarcinome pancréatique et les tumeurs intracanalaires papillaires et mucineuses (TIPMP), notamment dans leur forme diffuse (tableau).
Pancréatite chronique versus adénocarcinome pancréatique
Le risque de développer un adénocarcinome pancréatique est augmenté chez les patients atteints de pancréatite chronique.9 Le diagnostic différentiel dans une forme focale pseudotumorale peut être difficile en imagerie.10 Les signes principaux en faveur d’un adénocarcinome pancréatique sont les suivants :
- interruption nette du conduit pancréatique principal, dilaté en amont de la masse, éventuellement associée à une dilatation biliaire en cas de lésion céphalique (« double duct sign ») ;
- infiltration des plans graisseux périvasculaires associée à la déformation ou à une occlusion des vaisseaux péripancréatiques ;
- apparition ou majoration d’une dilatation du conduit pancréatique principal en amont d’une masse ;
- modification de la morphologie et/ou du rehaussement de la glande avec déplacement ou disparition de calcifications préexistantes ;
- apparition et/ou présence d’un hypersignal focal dans les séquences de diffusion avec restriction sur la cartographie ADC (apparent diffusion coefficient).
Les signes principaux en faveur d’une pancréatite chronique (même dans une forme pseudotumorale) sont la présence d’une dilatation irrégulière mais sans obstruction du conduit pancréatique principal et l’absence d’interruption du conduit principal dans la masse (signe du canal pénétrant ou « duct penetrating sign »). Ce signe a montré une sensibilité de 85 % et une spécificité de 96 %.11 En cas de doute, une biopsie guidée par EUS (écho-endoscopie) est utile pour établir un diagnostic définitif.
Pancréatite chronique versus TIPMP
L’aspect de la dilatation du conduit pancréatique principal (régulier et homogène dans la TIPMP vs irrégulier avec des sténoses dans la pancréatite chronique), l’aspect de dilatation des conduits secondaires (kystique en boule dans les TIPMP vs en flammèches dans la pancréatite chronique) ainsi que la présence d’une atrophie parenchymateuse (typique de la pancréatite chronique) sont des éléments clés pour ce diagnostic différentiel. Bien que les calcifications soient typiques de la pancréatite chronique, surtout si elles sont diffuses, elles peuvent également être observées dans les TIPMP (10 % des cas) en rapport avec du mucus calcifié.10
Diagnostic plus complexe dans les formes débutantes que dans les formes évoluées
Le diagnostic de pancréatite chronique, bien que facile dans les formes évoluées, peut s’avérer complexe dans les formes débutantes, notamment en raison de l’absence de preuve histologique et de l’hétérogénéité de la maladie.
Au cours de ces cinquante dernières années, les progrès de la génétique et de l’imagerie ont largement contribué à mieux comprendre et identifier la pancréatite chronique. La TDM et l’IRM sont les examens clés pour le diagnostic.
La principale difficulté diagnostique est de ne pas méconnaître une TIPMP (avec son risque de dégénérescence) et une tumeur obstructive (principalement un petit adénocarcinome pancréatique) responsable d’une pancréatite chronique d’amont.
Une fois le diagnostic posé, la prise en charge du patient comprend la recherche de la cause (alcool, tabac, génétique, auto-immune, radique, ischémique…) et l’évaluation des complications (douleurs, insuffisance pancréatique exocrine, diabète, cholestase, cancer).
Pancréatite chronique : Le savez-vous ?
Peut-on parler de pancréatite chronique si le conduit pancréatique est fin et régulier ?
Dans les formes débutantes, l’imagerie par résonance magnétique (IRM) peut mettre en évidence de petits conduits secondaires en flammèches, permettant d’évoquer le diagnostic. L’écho-endoscopie peut également apporter des arguments en faveur du diagnostic de pancréatite chronique débutante.
La présence de calcifications pancréatiques signe-t-elle le diagnostic de pancréatite chronique ?
Non, il y a d’autres causes possibles.
À quoi penser devant des calcifications de la région pancréatique ?
À des calcifications vasculaires (notamment de l’artère splénique), des tumeurs pancréatiques calcifiées (tumeurs neuro-endocrines, cystadénomes séreux), du mucus calcifié d’une tumeur intracanalaire papillaire et mucineuse (TIPMP), une transformation kystique des acini (entité bénigne avec un ou plusieurs kystes pancréatiques contenant des calcifications). La tomodensitométrie (TDM) – sans puis avec injection de produit de contraste – est l’examen clé.
Quels diagnostics évoquer devant une dilatation du conduit pancréatique principal ?
En dehors de la pancréatite chronique, il faut rechercher une TIPMP du conduit principal (dilatation sans obstacle) ou un obstacle (calcification obstructive, sténose canalaire fibreuse, tumeur bénigne, adénocarcinome pancréatique, tumeur neuroendocrine…) responsable d’une pancréatite chronique d’amont.
La pancréatite chronique peut-elle être localisée exclusivement dans une partie du pancréas ?
Oui, dans le cas de la pancréatite chronique en amont d’un obstacle ou en cas de variante canalaire pancréatique (par exemple, pancréatite chronique du pancréas dorsal en cas de pancréas divisum complet). Le diagnostic de pancréatite auto-immune dans une forme focale pseudotumorale peut également être évoqué.
La présence d’une masse pancréatique en imagerie élimine-t-elle le diagnostic de pancréatite chronique ?
Non, il peut s’agir d’un authentique cancer sur pancréatite chronique (qui en elle-même est un facteur de risque de cancer). Il faut également évoquer une poussée aiguë sur pancréatite chronique (rechercher des signes inflammatoires en TDM) et les formes focales pseudotumorales de pancréatite auto-immune.
Une atrophie parenchymateuse signe-t-elle forcément une pancréatite chronique ?
Il peut s’agir de la sénescence du pancréas chez le sujet âgé. Le pancréas peut également être le siège d’une infiltration graisseuse, focale ou diffuse, sans lésion canalaire associée. Enfin, l’atrophie peut être la séquelle d’une pancréatite aiguë nécrosante quelle que soit sa cause, ou l’évolution d’une pancréatite auto-immune.
Une insuffisance pancréatique exocrine signe-t-elle la présence d’une pancréatite chronique ?
Non, il y a d’autres causes (maladie cœliaque, montage chirurgical, diabète…).
2. Beyer G, Habtezion A, Werner J, et al. Chronic pancreatitis. Lancet 2020;396 (10249):499-512.
3. Thierens ND, Verdonk RC, Löhr JM, et al. Chronic pancreatitis. Lancet 2025;404 (10471):2605-18.
4. Hegyi P, Párniczky A, Lerch MM, et al. International Consensus Guidelines for risk factors in chronic pancreatitis. Recommendations from the working group for the international consensus guidelines for chronic pancreatitis in collaboration with the International Association of Pancreatology, the American Pancreatic Association, the Japan Pancreas Society, and European Pancreatic Club. Pancreatology 2020;20(4):579-85.
5. Sinha A, Singh VK, Cruise M, et al. Abdominal CT predictors of fibrosis in patients with chronic pancreatitis undergoing surgery. Eur Radiol 2015;25(5):1339-46.
6. Tirkes T, Shah ZK, Takahashi N, et al. Reporting standards for chronic pancreatitis by using CT, MRI, and MR cholangiopancreatography: The consortium for the study of chronic pancreatitis, diabetes, and pancreatic cancer. Radiology 2019;290(1):207-15.
7. Sarner M, Cotton PB. Classification of pancreatitis. Gut 1984;25(7):756-9.
8. Catalano MF, Sahai A, Levy M, et al. EUS-based criteria for the diagnosis of chronic pancreatitis: The Rosemont classification. Gastrointest Endosc 2009;69(7):1251-61.
9. Talamini G, Falconi M, Bassi C, et al. Incidence of cancer in the course of chronic pancreatitis. Am J Gastroenterol 1999;94(5):1253-60.
10. Schima W, Böhm G, Rösch CS, et al. Mass-forming pancreatitis versus pancreatic ductal adenocarcinoma: CT and MR imaging for differentiation. Cancer Imaging 2020;20:52.
11. Ichikawa T, Sou H, Araki T, et al. Duct-penetrating sign at MRCP: Usefulness for differentiating inflammatory pancreatic mass from pancreatic carcinomas. Radiology 2001;221(1):107-16.

 Encadrés
Encadrés