La démarche diagnostique de la la maladie stéatosique du foie liée au syndrome métabolique (metabolic dysfunction-associated steatotic liver disease [MASLD]) suppose de reconnaître la stéatose, les facteurs de risque et les cofacteurs, de définir qui et comment la dépister et d’identifier les patients à risque de progression de la maladie hépatique afin de mettre en place un suivi spécialisé.
Conduite à tenir devant une stéatose hépatique
Il est nécessaire d’identifier et de quantifier la stéatose hépatique, puis d’en évaluer les conséquences.
Diagnostic de stéatose hépatique
La stéatose hépatique correspond à la présence de vacuoles lipidiques intrahépatocytaires, plus souvent macrovacuolaires que microvacuolaires ou mixtes. Elle est le plus souvent de découverte fortuite, dans le cadre d’un examen morphologique systématique (douleurs abdominales, par exemple) ou d’anomalies biologiques hépatiques sur un bilan sanguin systématique ou ciblé du fait de facteurs de risque de syndrome métabolique.
Place de l’échographie
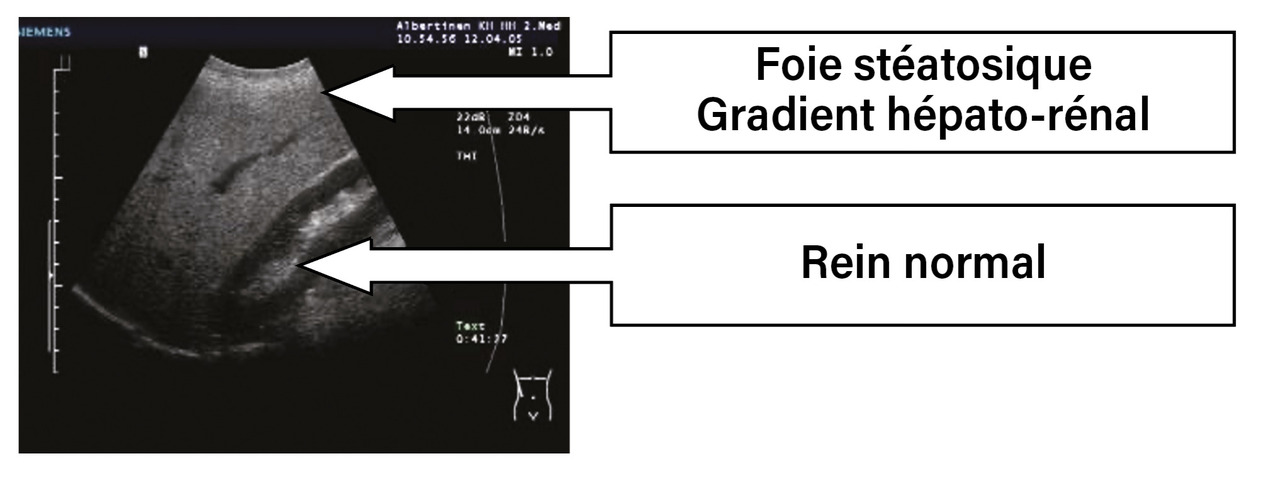
En présence d’une stéatose hépatique, l’échographie met en évidence un gradient hépato-rénal : le foie apparaît brillant par rapport aux autres organes abdominaux (rein, pancréas, rate), qui ont normalement la même échogénicité que celle du foie (fig. 1). Une stéatose hépatique échographique est observée lorsque plus de 25 à 30 % des hépatocytes contiennent de la graisse : il peut donc exister une stéatose histologique sans stéatose échographique. L’échographie est en effet un examen très spécifique mais peu sensible pour la détection de la stéatose hépatique.
Constantes biologiques altérées de façon inconstante
Les anomalies biologiques hépatiques (augmentation des enzymes hépatiques, notamment de la gamma-GT [enzyme membranaire], des transaminases [enzymes intracellulaires cytosoliques et mitochondriales] ou hyperferritinémie) sont inconstantes et témoignent du stress cellulaire induit par la distension par les vacuoles lipidiques de la membrane hépatocytaire dont la perméabilisation favorise l’exocytose des enzymes ou protéines fabriquées par le foie.
La découverte d’une stéatose hépatique justifie l’évaluation de son impact hépatique et de sa cause.
Quantification de la stéatose hépatique
Plusieurs scores biologiques ont été proposés pour la détection de la stéatose hépatique, incluant le SteatoTest, le fatty liver index (FLI), l’hepatic steatosis index (HSI), le lipid accumulation product (LAP), l’index of NASH (ION), et le NAFLD liver fat score (NAFLD-LFS). Ils ont des performances superposables pour ce qui concerne le diagnostic de stéatose,1 mais leur coût et leur non-remboursement peuvent en limiter l’application en pratique clinique.
L’échographie conventionnelle reste l’imagerie la plus fréquemment utilisée pour le diagnostic de stéatose, en raison de sa large disponibilité, de son innocuité et de son faible coût. Le degré de stéatose peut être évalué sur l’échographie subjectivement en faible, modéré ou sévère. Dans une méta-analyse prenant la biopsie hépatique comme référence (34 études, 2 815 patients ayant une hépatopathie suspectée ou connue), la sensibilité et la spécificité de l’échographie pour la détection d’une stéatose modérée à sévère (plus de 33 %), par comparaison à l’absence de stéatose, étaient respectivement de 85 % (80 - 89 %) et 93 % (87 - 97 %).2 En pratique clinique, c’est surtout la détection de la présence ou de l’absence de la stéatose qui compte. Selon les recommandations nationales et européennes, l’échographie reste l’examen d’imagerie de première intention pour le diagnostic de stéatose.3
Plus récemment, le CAP (paramètre d’atténuation contrôlée), mesuré par le FibroScan, a été proposé pour la détection et la quantification de la stéatose. Le CAP mesure le degré d’atténuation échographique de la stéatose, en même temps, sur le même volume et à partir du même signal, que la mesure de l’élasticité hépatique.4 Les résultats sont immédiats, exprimés en décibels par mètre (dB/m) et varient de 100 à 400 dB/m. Le CAP a une bonne reproductibilité inter-observateur, avec une concordance comprise entre 0,822 et 0,84.5 Un résultat supérieur à 250 dB/m est associé à une stéatose significative (plus de 33 %).
L’IRM-PDFF (magnetic resonance imaging proton density fat fraction) est une technique d’imagerie, précise et reproductible, pour quantifier la stéatose hépatique.6 En dépit de ses performances élevées pour la quantification de la stéatose, son coût et sa disponibilité restreinte limitent son utilisation en pratique clinique courante.
Conséquences de la stéatose : stéatose simple ou stéato-hépatite ?
La stéatose doit être distinguée de la stéato-hépatite, où l’inflammation associée à la stéatose favorise les dépôts de fibrose, qu’il convient de rechercher et de quantifier.
Il est crucial d’évaluer précisément le stade de la fibrose car elle conditionne le pronostic, le suivi et le risque de complications hépatiques (décompensation hépatique, carcinome hépatocellulaire) mais aussi extra-hépatiques (risques d’accidents cardiovasculaires ou de cancers augmentés chez les patients ayant des fibroses hépatiques significatives).7
Si la biopsie hépatique reste l’examen de référence, de nombreux tests non invasifs permettent une évaluation sensible de la fibrose hépatique : les tests usuels de la prise en charge des hépatopathies (FibroScan, Fibromètre, Fibrotest, FIB- 4, Hépascore) mais aussi ceux plus spécifiques de la MASLD comme le NAFLD fibrosis score, eLift ou ELF.
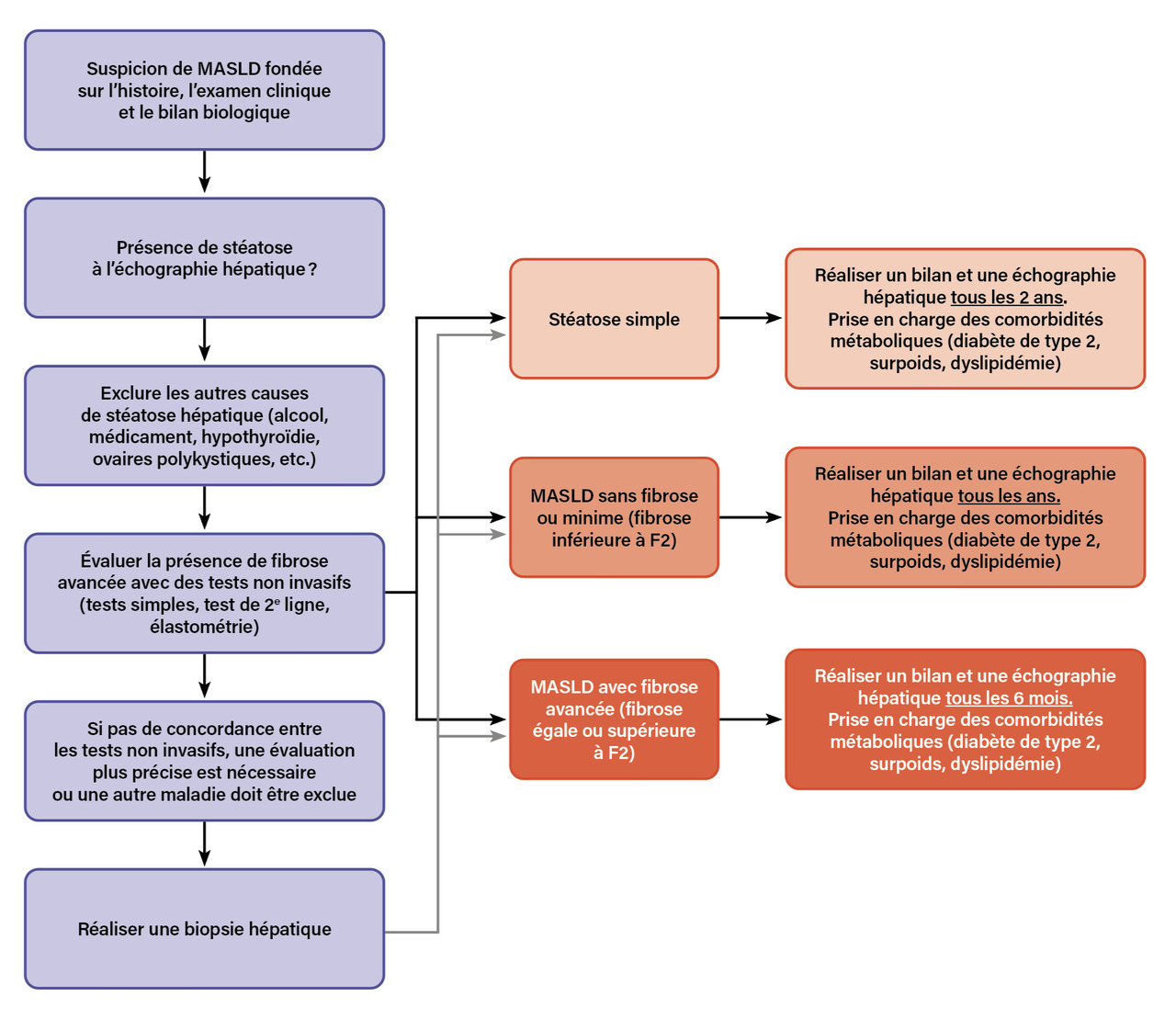
À partir de tests simples (eLift ou FIB- 4), il est possible de développer des algorithmes conduisant à des diagnostics précis de la sévérité de la maladie hépatique, et tout patient ayant une fibrose significative est adressé à l’hépatologue pour un suivi spécialisé (fig. 2).
L’algorithme proposé par les sociétés nationales et internationales d’hépatologie consiste en la réalisation du FIB- 4 (fondé sur les transaminases, l’âge et le taux de plaquettes) en première intention. (lire le Focus « FIB- 4 : un test sanguin simple pour identifier les patients à risque de complications hépatiques », page 398). Lorsque la valeur du FIB- 4 est inférieure à 1,3 (valeur excluant une fibrose significative), il est recommandé d’effectuer une simple surveillance biologique et échographique tous les un à trois ans et de suivre des règles hygiénodiététiques.8 À l’inverse, en cas de FIB- 4 supérieur ou égal à 1,3, il est recommandé d’effectuer un FibroScan. Un FibroScan inférieur à 8 kPa conduit à une surveillance simple ; un FibroScan supérieur ou égal à 8 kPa nécessite une consultation hépatologique spécialisée.8 L’algorithme proposé par la Société européenne d’hépatologie est résumé dans la figure 2.
Chez qui dépister une MASLD ?
Il n’est pas recommandé de réaliser de dépistage systématique de la stéatose dans la population générale malgré la prévalence du surpoids, d’autant moins qu’il n’y a pas de traitement radical spécifique à proposer en dehors des règles hygiénodiététiques. Néanmoins, l’intégration systématique dans les laboratoires d’analyses biologiques du calcul du FIB- 4 pourrait permettre, selon certains, de façon aléatoire de dépister les sujets ayant une potentielle fibrose hépatique.
Le dépistage est recommandé lorsqu’il existe au moins un facteur de risque métabolique (hypertension artérielle, diabète de type 2, dyslipidémie, surpoids, syndrome d’apnées du sommeil…), chez les sujets à haut risque de MASLD fibrosante (homme âgé de plus de 50 ans) pour lesquels une échographie et un bilan hépatique sont justifiés. En présence de stéatose, une évaluation de la fibrose par des marqueurs non invasifs s’impose, selon l’algorithme décrit (fig. 2).8
La biopsie hépatique ne peut pas être utilisée en première ligne pour le dépistage de la stéatose ou la différenciation stéatose/stéato-hépatite du fait de son caractère invasif et de la prévalence élevée de la stéatose en population générale. Cependant, chez les diabétiques avec stéatose, elle a montré son intérêt et la limite des tests non invasifs.
Alors qu’une fibrose avancée était suggérée par le test de Forns chez 8 % des diabétiques de la cohorte Constances (environ 150 000 sujets de la population générale), la cohorte QUID-NASH – qui comporte plus de 500 biopsies de patients diabétiques de type 2 ayant une stéatose échographique mais des anomalies biologiques hépatiques modestes – a montré une prévalence de fibrose F3 -F4 de 38 %. Les tests non invasifs étaient imparfaits par comparaison à la biopsie hépatique pour la prédiction des fibroses significatives, avec environ 27 % de faux négatifs chez les patients ayant un FIB- 4 inférieur à 1,3 et 32 % de faux positifs chez les patients ayant un FIB- 4 supérieur à 1,3 et une élastométrie supérieure ou égale à 8 KPa. C’est pourquoi, dans les situations de diabète avec stéatose, la biopsie hépatique resterait indiquée, avec l’identification dans 38 % des cas d’une fibrose F3 -F4 à risque élevée de cancers.9 Les deux autres indications de la biopsie hépatique sont la discordance de tests non invasifs entre eux ou avec l’imagerie hépatique, et la suspicion d’une comorbidité hépatique.
Stéatopathies métaboliques (MASLD) et alcooliques (ALD)
La définition des stéatopathies a été élargie et la nomenclature modifiée (lire « Épidémiologie et définitions : de la stéatose à la cirrhose », page 388).10
On distingue des MASLD « pures » des ALD (alcoholic liver disease), des stéatopathies cryptogéniques ou spécifiques médicamenteuses, génétiques (déficit en lipase acide lysosomale, maladie de Wilson, hypobêtalipoprotéine…) ou liées au virus de l’hépatite C (VHC), à la malnutrition ou à la maladie cœliaque.
À la frontière des MASLD et des ALD, on parle de MetALD (MASLD avec consommation d’alcool accrue définie par une consommation hebdomadaire de 140 à 350 g chez les femmes et de 210 à 420 g chez les hommes, soit des consommations quotidiennes respectives de 20 à 50 g et 30 à 60 g). En fonction de la consommation quotidienne d’alcool, on parle de MetALD à MASLD prédominante ou de MetALD à ALD prédominante. L’alcool apparaît comme un véritable facteur de majoration de la fibrose, et on considère que la moitié des patients ayant un syndrome métabolique ont une consommation excessive d’alcool, et réciproquement, puisque la coexistence d’une consommation élevée d’alcool et d’un excès de poids est fréquemment rencontrée en pratique clinique quotidienne.11,12
L’alcool et l’obésité sont donc des facteurs de risque indépendants de développer une stéato-hépatite mixte métabolique et alcoolique, mais les interactions entre ces deux causes sont importantes. La consommation d’alcool à risque aggrave la maladie hépatique de façon synergique chez les patients avec MASLD, en particulier chez ceux en surpoids ou en situation d’obésité. Une consommation modérée d’alcool chez ces patients (moins de 30 g/j chez l’homme et de 20 g/j chez la femme) a-t-elle une influence sur la MASLD ? Des données contradictoires existent dans la littérature.
Certaines études supportent la notion qu’une faible consommation d’alcool (inférieure ou égale à 10 g/j) a un effet protecteur sur la MASLD, mais ces études sont rétrospectives et comportent des biais, notamment sur la fiabilité de l’autodéclaration de la consommation d’alcool régulière et/ou des épisodes d’alcoolisation aiguë.13 Une méta-analyse de 2023 a montré que la consommation modérée d’alcool était négativement reliée à l’incidence de la MASLD et de la fibrose.14 Enfin, il est suggéré que même une consommation modérée d’alcool augmente le risque de carcinome hépatocellulaire chez les patients ayant une MASLD15 et il semble logique en pratique de recommander une abstinence d’alcool chez les patients avec MASLD. Ainsi, MASLD et ALD sont intriquées et justifient une prise en charge combinée.
Dépistage des complications de la fibrose significative
En cas de fibrose significative, le dépistage du carcinome hépatocellulaire (et du cholangiocarcinome) est recommandé par la réalisation d’une échographie semestrielle : le risque de survenue d’un carcinome hépatocellulaire sans cirrhose est trois fois plus élevé que ce qui est observé dans les pathologies liées à l’excès d’alcool ou aux hépatites virales. Au cours des stéato-hépatites métaboliques, l’incidence du carcinome hépatocellulaire est de 0,21 pour 1 000 patients/année quel que soit le stade par comparaison à 0,02 pour 1 000 patients/année dans la population contrôle. En cas de cirrhose, l’incidence du carcinome hépatocellulaire est de 10,6 pour 1 000 patients/année.
L’obésité est un facteur de risque connu de cancer, mais il existe seulement chez les patients ayant une MASLD avec un risque relatif d’environ 2 pour les cancers digestifs ou utérins, par exemple.
En cas de fibrose significative, le dépistage des varices œsophagiennes des stéato-hépatites relève des critères de Baveno VII.16 Il est recommandé de ne pas effectuer de fibroscopie œso-gastro-duodénale (FOGD) en cas de FibroScan inférieur à 20 kPa et de plaquettes supérieures à 150 000/mL, permettant d’éviter environ la moitié des FOGD, avec une valeur prédictive négative de 99 %, c’est-à-dire d’exclure une « hypertension portale cliniquement significative », définie par la présence de varices significatives justifiant un traitement pharmacologique (bêtabloquants non cardiosélectifs) ou endoscopique (ligature élastique). En cas de cirrhose sur MASLD, les patients non obèses avec des valeurs de FibroScan comprises entre 20 et 25 kPa et un nombre de plaquettes inférieur à 150 000/mL ou des valeurs entre 15 et 20 kPa et un nombre de plaquettes inférieur à 110 000/mL ont un risque d’« hypertension portale cliniquement significative » d'au moins 60 %.
Nombreuses comorbidités
La MASLD est une maladie avec des comorbidités comme l’obésité, le diabète de type 2, la dyslipidémie, l’hypertension artérielle, le syndrome d’apnées du sommeil, les maladies cardiovasculaires, des endocrinopathies qui doivent être prises en charge lors du diagnostic. Si la mortalité en cas de surpoids reste majoritairement liée aux pathologies vasculaires ou aux cancers (un tiers chacun, respectivement), la MASLD rend compte d’environ 15 % des décès. La morbi-mortalité croissante liée à la MASLD justifie son dépistage, la confirmation du diagnostic, l’évaluation de la sévérité de la maladie hépatique et un suivi en fonction du stade de la maladie.
2. Hernaez R, Lazo M, Bonekamp S, et al. Diagnostic accuracy and reliability of ultrasonography for the detection of fatty liver: A meta-analysis. Hepatology 2011;54(3):1082‑90.
3. European Association for the Study of the Liver (EASL); European Association for the Study of Diabetes (EASD); European Association for the Study of Obesity (EASO). EASL-EASD-EASO Clinical Practice Guidelines on the management of metabolic dysfunction-associated steatotic liver disease (MASLD). J Hepatol 2024;81(3):492-542.
4. Sasso M, Beaugrand M, de Ledinghen V, et al. Controlled attenuation parameter (CAP): A novel VCTE guided ultrasonic attenuation measurement for the evaluation of hepatic steatosis: Preliminary study and validation in a cohort of patients with chronic liver disease from various causes. Ultrasound Med Biol 2010;36(11):1825‑35.
5. Recio E, Cifuentes C, Macias J, et al. Interobserver concordance in controlled attenuation parameter measurement, a novel tool for the assessment of hepatic steatosis on the basis of transient elastography. Eur J Gastroenterol Hepatol 2013;25(8):905‑11.
6. Castera L, Rinella ME, Tsochatzis EA. Noninvasive assessment of liver fibrosis. N Engl J Med 2025;393(17):1715-29.
7. Sanyal AJ, Van Natta ML, Clark J, et al. Prospective study of outcomes in adults with nonalcoholic fatty liver disease. N Engl J Med 2021;385(17):1559‑69.
8. European Association for the Study of the Liver; Clinical Practice Guideline Panel; Chair; et al. EASL Clinical Practice Guidelines on non-invasive tests for evaluation of liver disease severity and prognosis 2021 update. J Hepatol 2021;75(3):659‑89.
9. Castera L, Laouenan C, Vallet‑Pichard A, et al. High prevalence of NASH and advanced fibrosis in type 2 diabetes: A prospective study of 330 outpatients undergoing liver biopsies for elevated ALT, using a low threshold. Diabetes Care 2023;46(7):1354‑62.
10. Rinella ME, Lazarus JV, Ratziu V, et al. A multisociety Delphi consensus statement on new fatty liver disease nomenclature. Hepatology 2023;79(6):1542-56.
11. Boyle M, Masson S, Anstee QM. The bidirectional impacts of alcohol consumption and the metabolic syndrome: Cofactors for progressive fatty liver disease. J Hepatol 2018;68(2):251‑67.
12. Elmustafa F, Tyagi M, Kaur H, et al. Met-ALD and ALD- Does differentiating these impact management and clinical outcomes? Curr Hepatol Rep 2025;24(1):10.1007/s11901-025-00712-8.
13. Gunji T, Matsuhashi N, Sato H, et al. Light and moderate alcohol consumption significantly reduces the prevalence of fatty liver in the Japanese male population. Am J Gastroenterol 2009;104(9):2189‑95.
14. Magherman L, Van Parys R, Pauwels NS, et al. Meta-analysis: The impact of light‑to‑moderate alcohol consumption on progressive non-alcoholic fatty liver disease. Aliment Pharmacol Ther 2023;57(8):820‑36.
15. Ascha MS, Hanouneh IA, Lopez R, et al. The incidence and risk factors of hepatocellular carcinoma in patients with nonalcoholic steatohepatitis. Hepatology 2010;51(6):1972‑8.
16. de Franchis R, Bosch J, Garcia-Tsao G, et al; Baveno VII Faculty. Baveno VII. Renewing consensus in portal hypertension. J Hepatol 2022;76(4):959-74.