En 2018 puis en 2023, le Haut Conseil de la santé publique (HCSP) s’était prononcé contre la mise en œuvre du dépistage des infections à cytomégalovirus (CMV) chez la femme enceinte, faute d’éléments suffisants pour en démontrer le bénéfice. L’émergence de nouvelles données sur l’efficacité du valaciclovir et l’évolution des pratiques (un tiers des femmes enceintes bénéficie déjà de ce dépistage, surtout en Île-de-France) ont conduit à une remise en question de cette position. Ainsi, la HAS a été saisie par la DGS pour donner son avis sur ce dépistage. Focus sur ces recos et les implications pratiques.
Infection congénitale par le CMV : quels risques ?
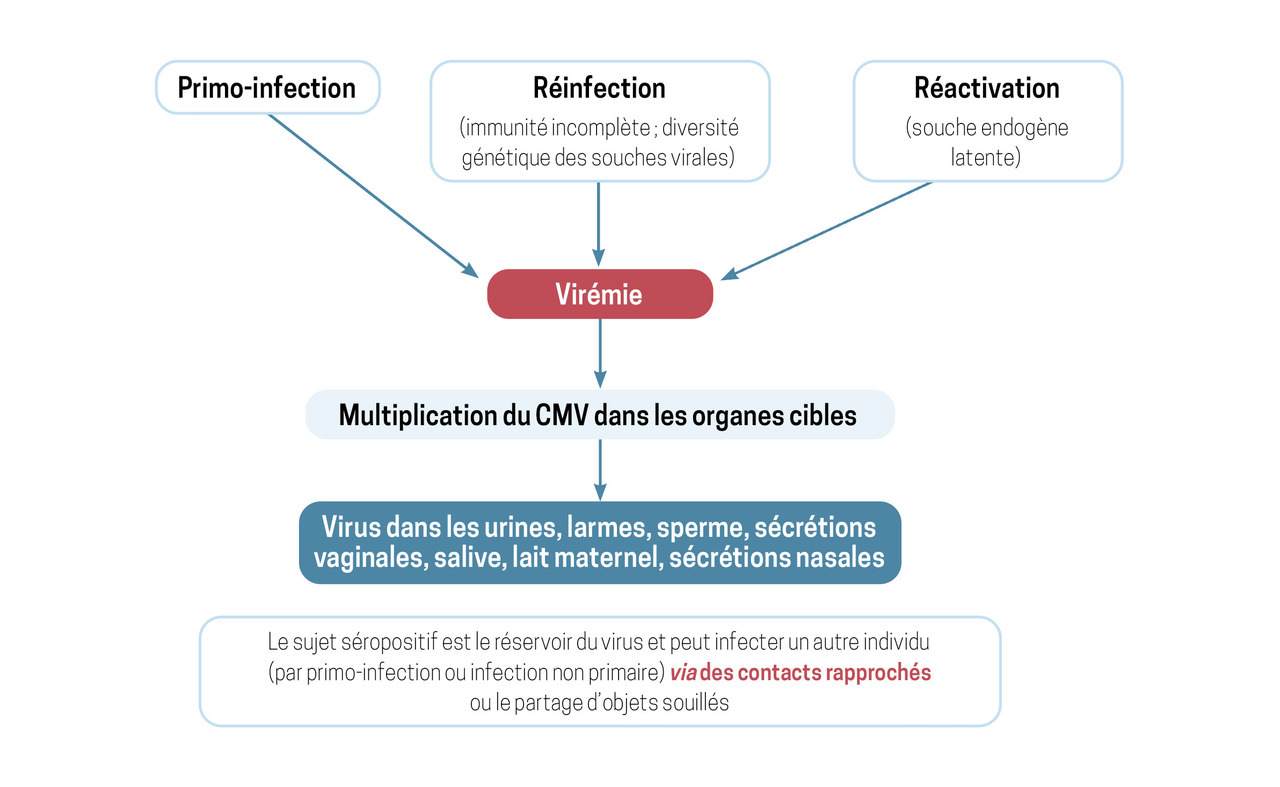
Le CMV se transmet par contact direct (fig. 1) avec les liquides biologiques contaminés (salive, sécrétions respiratoires, urines, larmes, sécrétions cervicovaginales, sperme et lait maternel). En France, environ 46 % des femmes âgées de 15 à 49 ans ont déjà été en contact avec le CMV, mais la séroprévalence varie fortement selon les régions, pouvant atteindre jusqu’à 90 % dans les départements d’outre-mer.1
L’infection touche 1 à 4 % des femmes enceintes ; elle peut être primaire (primo-infection) ou non primaire (réactivation ou réinfection). La primo-infection maternelle a un risque élevé de transmission verticale du CMV au fœtus, surtout au 1er trimestre (36,8 % dans cette période). L’infection est dans 90 % des cas asymptomatique et sans conséquence, mais elle peut dans certains cas induire des complications graves pour le fœtus. En particulier, deux catégories de symptômes sont décrites (fig. 2) :
- les symptômes néonataux liés à la primo-infection fœtale généralisée aiguë, largement dominés par le retard de croissance ;
- les séquelles neurosensorielles pouvant être présentes dès la naissance ou survenir de façon retardée. Ces séquelles auditives ou neurologiques ne surviennent que chez les enfants infectés à la suite d’une infection maternelle du 1er trimestre.2
Qui et comment dépister ?
La HAS recommande de mettre en place un dépistage systématique, à destination de toutes les femmes enceintes dont le statut sérologique est inconnu ou négatif. Il devra être réalisé au 1er trimestre de grossesse.
Pour faire le diagnostic : une séroconversion des immunoglobulines G (IgG) confirme la primo-infection maternelle. Lorsque cette dernière ne peut pas être mise en évidence, les dosages des anticorps IgG et IgM et les tests d’avidité permettent de distinguer une primo-infection récente d’une infection ancienne. Le profil sérologique typique de la primo-infection associe des IgM élevées, des IgG basses et une avidité basse des IgG. Dans ce contexte, la HAS préconise de ne recourir qu’à des tests d’avidité IgG avec des seuils minimaux de performance (sensibilité et spécificité) de 95 %.
L’algorithme à suivre pour la réalisation des tests sérologiques est indiqué dans l’encadré 1 ci-dessous.
Ces tests n’étant pas fiables en cas d’infection non primaire à CMV (réactivation ou réinfection), les experts ne recommandent pas de dépistage sérologique de routine chez les femmes déjà séropositives avant la grossesse.
Stratégies de prévention selon le statut sérologique
Chez les femmes n’ayant jamais été infectées par le CMV (séronégatives), des mesures d’hygiène préventives doivent être mises en place. Elles sont indiquées dans le tableau ci-contre.
Les femmes ayant déjà un enfant en bas âge sont particulièrement à risque.
Pour les femmes dont le statut sérologique révèle une primo-infection récente, un traitement antiviral est proposé pour réduire le risque de transmission au fœtus (valaciclovir à haute dose), ainsi qu’un suivi dans un centre pluridisciplinaire de diagnostic prénatal (suivi de la grossesse par imagerie ; discussion d’une PCR sur liquide amniotique ; en cas d’atteinte grave du fœtus : interruption médicale de grossesse possible). Après la naissance, le nouveau-né est régulièrement suivi, notamment en ce qui concerne son audition et son développement moteur, à la recherche d’éventuelles séquelles.
La HAS précise que, sous valaciclovir, les patientes devront être sensibilisées au maintien d’une hydratation suffisante et à l’administration du traitement en plusieurs doses réparties sur 24 heures afin d’éviter l’apparition de potentiels effets secondaire rénaux ; la prise concomitante de médicaments potentiellement néphrotoxiques doit être évitée.
Autre point important : si les données disponibles sur le valaciclovir ne montrent aucun signal de tératogénicité (anomalie ou déformation fœtale) sur la période 2007 - 2023, il persiste encore des incertitudes quant à l’ampleur de son efficacité sur la réduction du risque de séquelles et de leur gravité (encadré 2) et il est nécessaire de surveiller l’apparition d’effets indésirables non encore identifiés (une surveillance obstétricale adaptée est recommandée).
Une recommandation sous conditions
La HAS précise que cette recommandation devra faire l’objet d’une réévaluation au bout de trois ans et qu’elle devra être accompagnée des mesures suivantes :
- Information des patientes : des supports d’information devront être diffusés auprès des femmes enceintes, afin de garantir leur consentement libre et éclairé. Ces documents rappelleront notamment les mesures d’hygiène préventive destinées à limiter le risque d’infection, en particulier chez les femmes séronégatives.
- Formation des professionnels.
- Évaluation des outils diagnostiques (performance des tests de dépistage).
- Réalisation d’études pour lever les incertitudes énoncées sur l’efficacité et la sécurité du valaciclovir sur le long terme et à plus large échelle.
Tests sérologiques : ordre de réalisation
En France, un algorithme comparable à celui de l’initiative européenne (ECCI) est proposé par le CNR Herpèsvirus :
1. répétition de la sérologie maternelle toutes les 4 semaines jusqu’à 14 - 16 semaines en cas de résultat IgG positif et IgM négatifs ;
2. séquence de tests (IgG, IgM et test d’avidité des IgG) ;
3. test d’avidité en cas de résultats IgG et IgM positifs ;
4. répétition du test d’avidité en cas de résultats intermédiaires.
Efficacité du valaciclovir dans la prévention de la transmission du CMV au fœtus
Deux méta-analyses3,4confirment l’efficacité du traitement par valaciclovir, à la dose de 8 g/j, dans la prévention de l’infection congénitale à CMV après une primo-infection maternelle, en particulier lorsqu’elle survient en période périconceptionnelle ou au 1er trimestre de grossesse.
Chatzakis C, et al.3 rapportent une réduction du risque de transmission verticale de 64 à 70 %, une baisse des infections néonatales et des interruptions médicales de grossesse, avec un taux bas d’effets indésirables sévères (2,1 %). D’Antonio F, et al.4 ont observé également une diminution significative du risque d’infection congénitale (OR ≈ 0,37) et une augmentation des cas asymptomatiques, sans preuve claire d’un impact sur les événements périnataux graves. Toutefois, ces méta-analyses se fondent sur une seule étude randomisée5 et deux études observationnelles6,7 ayant un risque de biais élevé.
HAS. Évaluation de la pertinence d’un dépistage systématique de l’infection à cytomégalovirus (CMV) au cours de la grossesse – recommandation. 5 juin 2025.
Leruez-Ville M, Ville Y. Infection par le cytomégalovirus chez la femme enceinte. Rev Prat Med Gen 2023;37(1073);28-35.
Références :
1. Antona D, Lepoutre A, Fonteneau L, et al. Seroprevalence of cytomegalovirus infection in France in 2010. Epidemiol Infect 2017;145(7);1471-8.
2. Faure-Bardon V, Magny JF, Parodi M, et al. Sequelae of Congenital Cytomegalovirus Following Maternal Primary Infections Are Limited to Those Acquired in the First Trimester of Pregnancy. Clin Infect Dis 2019;69(9);1526-32.
3. Chatzakis C, Shahar-Nissan K, Faure-Bardon V, et al. The effect of valacyclovir on secondary prevention of congenital cytomegalovirus infection, following primary maternal infection acquired periconceptionally or in the first trimester of pregnancy. An individual patient data meta-analysis. Am J Obstet Gynecol 2024;230(2);109-17.
4. D’Antonio F, Marinceu D, Prasad S, et al. Effectiveness and safety of prenatal valacyclovir for congenital cytomegalovirus infection: systematic review and meta-analysis. Untrasoud Obstet Gynecol 9 décembre 2022.
5. Shahar-Nissan K, Pardo J, Peled O, et al. Valaciclovir to prevent vertical transmission of cytomegalovirus after maternal primary infection during pregnancy: a randomised, double-blind, placebo-controlled trial. Lancet 2020;396(10253);779-85.
6. Egloff C, Vauloup-Fellous C, Picone O. La prévention de l’infection congénitale à cytomégalovirus. J Pédiatr Puéric 2024;37(4);233-9.
7. Faure-Bardon V, Fourgeaud J, Stirnemann J, et al. Secondary prevention of congenital cytomegalovirus infection with valacyclovir following maternal primary infection in early pregnancy. Ultrasoud Obtet Gynecol 16 mai 2021.

 Encadrés
Encadrés