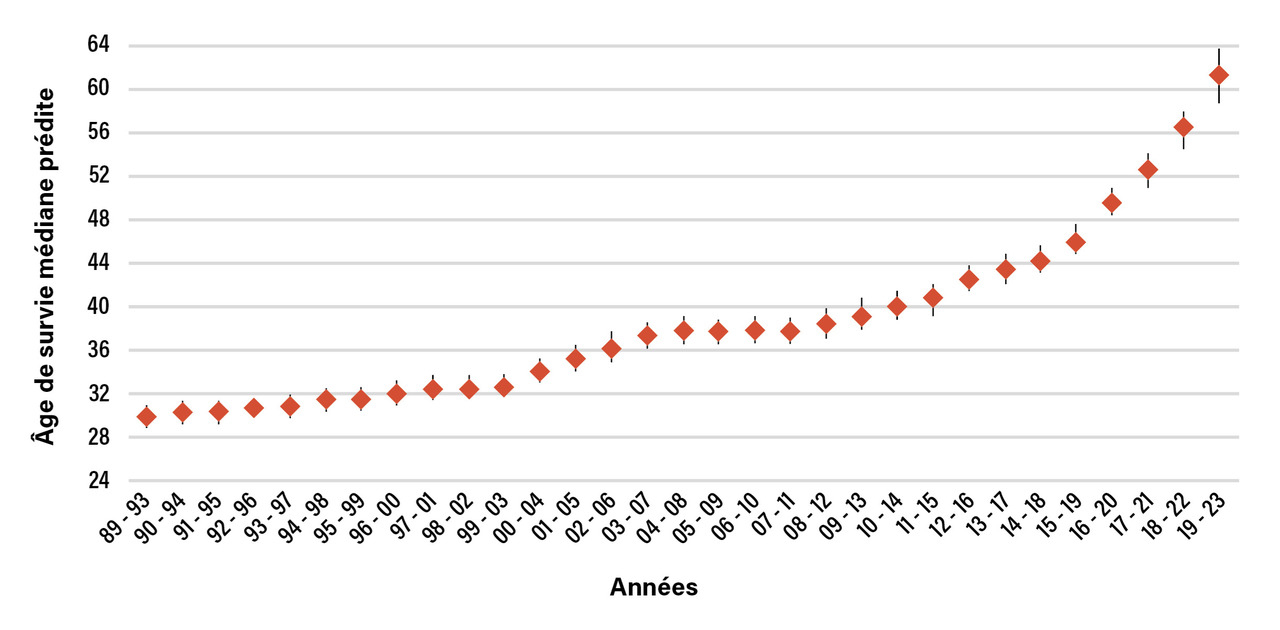
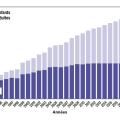
En France comme dans la plupart des pays occidentaux, l’organisation des soins en centres spécialisés, la généralisation du dépistage néonatal, l’amélioration des traitements symptomatiques, en particulier à visée nutritionnelle (prévention et traitement de la dénutrition) et à visée respiratoire (prévention et traitement des exacerbations bronchiques) ont conduit à une amélioration progressive de l’espérance de vie des patients atteints de mucoviscidose quelle que soit la méthode statistique utilisée.1 Dans les données du registre nord-américain, la médiane de survie prédite pour les enfants nés entre 2017 et 2021 est estimée à 53 ans contre 36 pour ceux nés entre 2001 et 2006 et environ 30 ans pour ceux nés entre 1989 et 1993 (fig. 1).2 De nombreux facteurs pronostiques ont été identifiés au cours du temps, comme le sexe, le génotype CFTR ou le niveau socio-économique. D’autres facteurs, comme la nutrition, la fonction respiratoire, la colonisation par Pseudomonas aeruginosa, impactent également le pronostic, et des stratégies thérapeutiques ont été mises en place pour les contrôler.
Par exemple, la croissance staturo-pondérale au cours des premières années de vie3 et les paramètres nutritionnels du jeune enfant sont prédictifs de la fonction respiratoire à l’âge de 6 ans4 et justifient le dépistage néonatal systématique de la maladie. La fonction respiratoire est également un indicateur clé de la survie chez les patients atteints de mucoviscidose (pwCF).5 Les essais cliniques et les études en vie réelle sur les modulateurs de la protéine CFTR ont montré leur efficacité sur la fonction respiratoire et sur l’état nutritionnel des patients.6 Par conséquent, leur utilisation précoce et sur une proportion de plus en plus large de malades est amenée à modifier considérablement l’état de santé des patients traités, ainsi que leur survie.
Évolution démographique
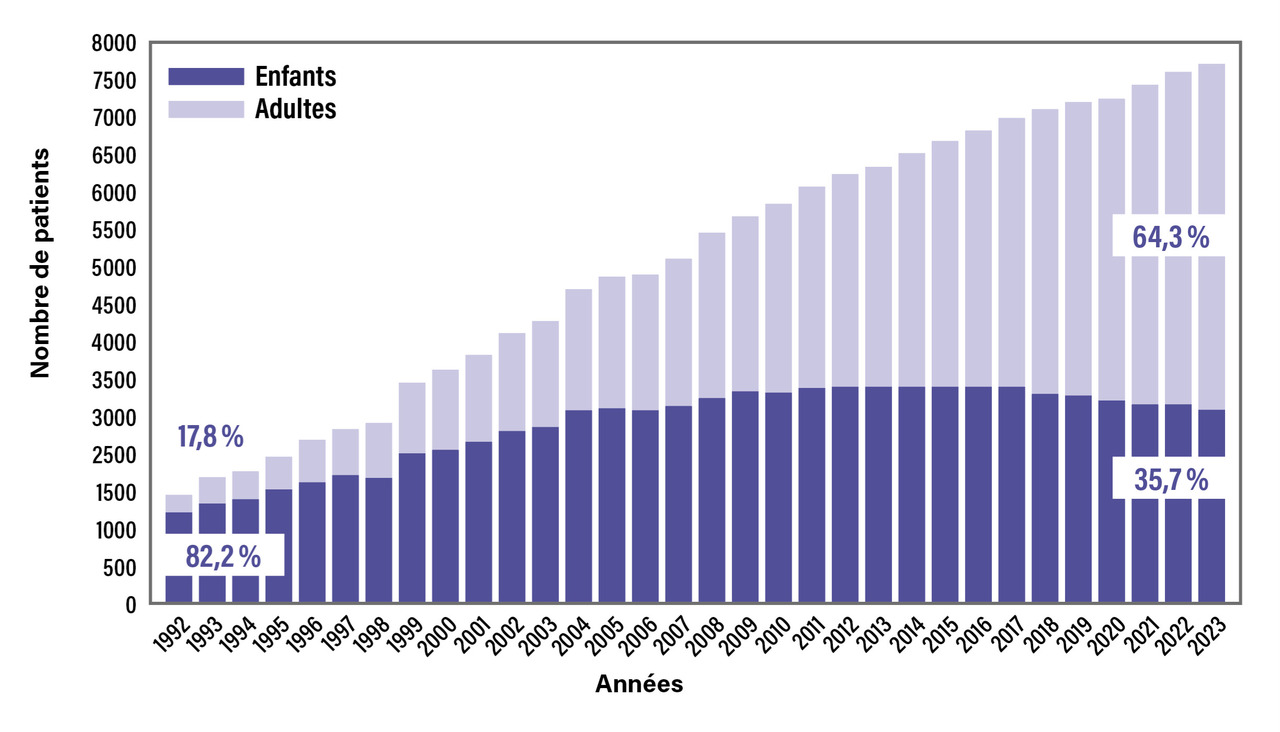
L’évolution démographique mesurée dans les registres est un marqueur indirect de l’amélioration de la survie (fig. 1). Ainsi, le nombre de malades recensés dans le registre français de la mucoviscidose est passé d’environ 4 000 en 2003 à 6 239 en 2013 et 7 801 en 2023. La proportion d’adultes était de respectivement 37 %, 52 % puis 64 % aux mêmes dates (fig. 2).7 Cette évolution démographique avait été modélisée dès 2015 par Burgel et al. à partir des données des registres européens, c’est-à-dire avant même l’utilisation large des modulateurs de CFTR, seul l’ivacaftor étant alors commercialisé.8
Plus récemment, en 2023, Lopez et al. ont publié une étude proposant une estimation de l’évolution de la survie des pwCF homozygotes pour la mutation F505del traités par élexacaftor-tézacaftor-ivacaftor (ETI). Pour cela, ils ont utilisé un modèle de microsimulation construit à partir des éléments connus de progression de la maladie et des études de suivi publiées sur les bénéfices attendus des traitements. La survie médiane projetée des patients pwCF traités par ETI serait de 71 ans en moyenne et elle est estimée à 82 ans lorsque le traitement est introduit dès l’âge de 12 ans.9
Impacts de l’amélioration pronostique
Fonction respiratoire
Chez le grand enfant et l’adulte, la fonction respiratoire mesurée par le volume expiratoire maximal par seconde (VEMS) s’améliore rapidement, en quelques semaines, sous traitement par ETI. Chez l’enfant de moins de 6 ans, ce sont des biomarqueurs de type indice de clairance pulmonaire ou imagerie scanographique qui s’améliorent, et la fonction respiratoire (lorsqu’elle est mesurable à l’âge de 6 ans) reste préservée.
Dans le registre nord-américain,2 la proportion de pwCF âgés de 18 ans ayant une fonction normale ou légèrement altérée (VEMS ≥ 70 % de la valeur prédite) a plus que doublé en vingt ans, passant de 42 % en 1993 à 90,8 % en 2023.
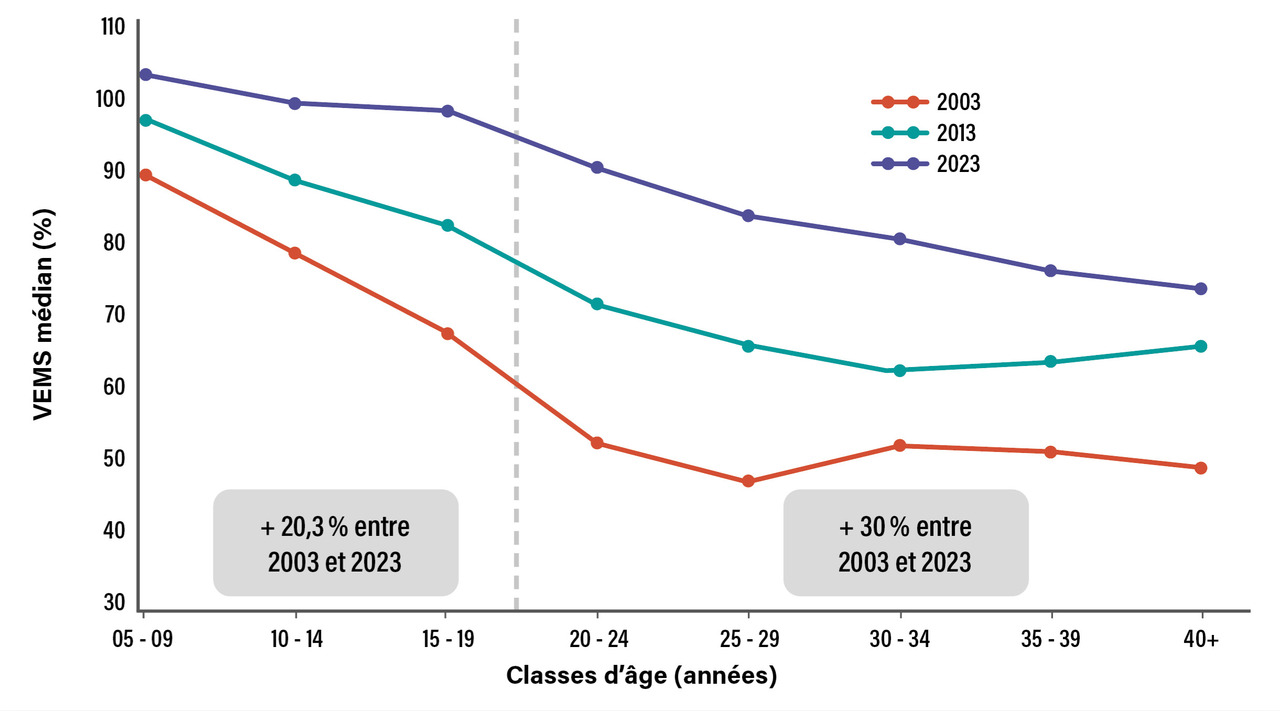
Dans le registre français,7 le gain de VEMS médian est de plus de 20 % dans la même tranche d’âge ; il est proche de 100 % dans la tranche d’âge de 6 à 19 ans (fig. 3).
Recours à la transplantation pulmonaire
L’amélioration de la fonction respiratoire lors de l’introduction du traitement par ETI a également été démontrée chez les pwCF avec une altération sévère de la fonction respiratoire (VEMS < 40 %).10 En France, ces derniers ont bénéficié d’un programme d’accès précoce au traitement fin décembre 2019. L’introduction de l’ETI a été associée à une amélioration rapide de la fonction respiratoire, d’une amplitude similaire à ce qui a été rapporté dans les essais cliniques, conduisant fréquemment à un sevrage de l’oxygénothérapie mais également à la suspension de l’indication de transplantation pulmonaire. Ainsi, en France, le nombre de transplantations pulmonaires a concerné 8 patients en 2023 contre une centaine en 2013 et 88 en 2019, année précédant à la fois la pandémie de Covid- 19 et l’introduction de l’ETI en accès précoce.7
Nombre de grossesses
Contrairement aux hommes, la fertilité des patientes est généralement conservée. Néanmoins, elle peut être altérée tout à la fois par des anomalies épithéliales du tractus génital et des modifications de la glaire cervicale, ou par l’altération de l’état clinique des patientes. L’hypofertilité peut justifier le recours à l’assistance médicale à la procréation. Le pronostic de la grossesse au cours de la mucoviscidose a été bien étudié au cours des dernières décennies : la fonction respiratoire est peu aggravée, mais des taux élevés de naissances prématurées sont décrits.11 Le nombre de grossesses et leur issue est ainsi un bon marqueur de l’état de santé d’une population de patientes atteintes de maladie chronique. Dans les registres, le nombre annuel de grossesses a doublé depuis l’introduction de l’ETI : aux États-Unis, environ 300 grossesses annuelles jusqu’en 2019, plus de 600 depuis 2020 ;2 en France, une cinquantaine de grossesses annuelles jusqu’en 2019, une centaine actuellement.7
Comorbidités émergentes
L’expression phénotypique « classique » de la mucoviscidose, avec l’atteinte respiratoire, l’insuffisance pancréatique et nutritionnelle et le diabète, évolue notablement. On décrit ainsi aujourd’hui des complications émergentes comme le surpoids, voire l’obésité, des complications cardiovasculaires très peu décrites par le passé et la survenue de cancers, en particulier digestifs, sans doute plus fréquents et plus précoces que dans la population générale.
Risque cardiovasculaire
Les essais cliniques et les études de suivi en vie réelle ont rapporté un gain de poids chez les patients traités par ETI. Plusieurs études ont relevé une augmentation de la prévalence du surpoids, voire de l’obésité, l’apparition de dyslipidémies antérieurement inexistantes et un accroissement des valeurs tensionnelles.12
L’impact sur le diabète est plus discuté. Plusieurs études ont toutefois montré une amélioration de l’équilibre glycémique chez les pwCF diabétiques traités par ETI13,14 par des mécanismes restant à préciser : diminution de l’insulinorésistance associée au meilleur contrôle des infections pulmonaires ou effet propre à la restauration de la fonction CFTR sur les cellules pancréatiques α ou β. L’impact de l’ETI prescrit précocement sur l’incidence et l’âge de survenue du diabète associé à la mucoviscidose reste à étudier.
Une étude de cohorte rétrospective multinationale sur une population britannique et nord-américaine de pwCF a mis en évidence un risque plus élevé d’événements cardiovasculaires majeurs, dont l’infarctus du myocarde, l’insuffisance cardiaque gauche et la fibrillation atriale, par rapport à une population sans mucoviscidose appariée. Le risque mesuré était comparable à celui constaté au cours d’autres maladies inflammatoires associées à un risque cardiovasculaire élevé comme le lupus érythémateux systémique et la polyarthrite rhumatoïde. La survenue de ces événements cardiovasculaires était associée au diabète et à l’hypertension artérielle, ainsi qu’à des facteurs de risque spécifiques de la maladie, notamment l’altération de la fonction pulmonaire et la fréquence des exacerbations bronchiques.15 Cette étude, qui a inclus les données des années 2016 - 2020, ne reflète que pour partie l’impact des traitements par modulateur de la protéine CFTR, en particulier l’ETI.
Au total, l’utilisation de l’ETI semble associée à une augmentation de certains facteurs de risque cardiovasculaire en augmentant le risque de surpoids, d’hypertension artérielle et possiblement de dyslipidémie. Toutefois, l’utilisation de l’ETI s’accompagne d’une diminution de la fréquence des infections et de l’état inflammatoire pro-oxydant et probablement d’une amélioration de l’équilibre glycémique chez certains pwCF diabétiques.
Risque de cancers
Le sur-risque de cancer observé chez les pwCF a été montré dès 2013 par Maisonneuve et al.16 et concerne particulièrement les cancers digestifs.17 Ceci a conduit à recommander leur dépistage avancé dès l’âge de 40 ans, par la réalisation d’endoscopies digestives. Le dépistage des cancers gynécologiques est également recommandé.18 Ce sur-risque peut être lié à l’état inflammatoire chronique mais semble également dû à la dysfonction de la protéine CFTR qui a des fonctions régulatrices de certaines protéines pro-oncogènes.
L’allongement de la survie des pwCF devrait conduire à observer une prévalence plus élevée du nombre de cancers. L’impact de la restauration de la fonction CFTR sur ce risque reste inconnu.
L’amélioration de la survie entraîne de nouvelles problématiques
L’évolution de la prise en charge de la mucoviscidose a conduit à une amélioration régulière et constante de la survie des malades au cours des dernières décennies. La révolution thérapeutique apportée par la dernière génération des modulateurs de CFTR (désormais nommés « CFTR variant-specific therapy ») constitue une nouvelle étape qui conduit à redéfinir le modèle de soins pour s’adapter à la demande des malades d’allègement des thérapeutiques et du suivi, aux changements phénotypiques et aux nouvelles complications, à redéfinir la place du médecin traitant dans le parcours de soins, l’organisation des dépistages, le traitement des facteurs de risque cardiovasculaire, etc.
Plusieurs défis demeurent. Le premier d’entre eux concerne le traitement des pwCF ne répondant pas aux molécules actuellement disponibles et qui doivent garder une pression thérapeutique symptomatique lourde. Le deuxième est lié au caractère non curatif des traitements modulateurs, puisque leur arrêt s’accompagne en quelques jours de la réapparition des signes cliniques et justifie, pour l’instant, le maintien du traitement « à vie ». Les interrogations concernant l’efficacité et la tolérance à long terme persistent. Enfin, la soutenabilité du coût du traitement et sa généralisation à l’échelle internationale constituent un autre défi.
2. Cystic Fibrosis Foundation Patient Registry Annual Data Report 2023.
3. Corey M, McLaughlin FJ, Williams M,et al. A comparison of survival, growth, and pulmonary function in patients with cystic fibrosis in Boston and Toronto. J Clin Epidemiol 1988;41(6):583-91.
4. Konstan MW, Butler SM, Wohl MEB, et al. Growth and nutritional indexes in early life predict pulmonary function in cystic fibrosis. J Pediatr 2003;142(6):624-30.
5. Kerem E, Reisman J, Corey M, et al. Prediction of mortality in patients with cystic fibrosis. N Engl J Med 1992;326(18):1187-91.
6. Middleton PG, Mall MA, Dřevínek P, et al. Elexacaftor-tezacaftor-ivacaftor for cystic fibrosis with a single Phe508del allele. N Engl J Med 2019;381(19):1809-19.
7. Registre français de la mucoviscidose. Bilan des données 2023. Vaincre la Mucoviscidose. Paris. Décembre 2024.
8. Burgel PR, Bellis G, Olesen HV, et al. Future trends in cystic fibrosis demography in 34 European countries. Eur Respir J 2015;46(1):133-41.
9. Lopez A, Daly C, Vega-Hernandez G, et al. Elexacaftor/tezacaftor/ivacaftor projected survival and long-term health outcomes in people with cystic fibrosis homozygous for F508del. J Cyst Fibros 2023;22(4):607-14.
10. Burgel PR, Sermet-Gaudelus I, Durieu I, et al. The French compassionate programme of elexacaftor/tezacaftor/ivacaftor in people with cystic fibrosis with advanced lung disease and no F508del CFTR variant. Eur Respir J 2023;61(5):2202437.
11. Reynaud Q, Rousset Jablonski C, Poupon-Bourdy S, et al. Pregnancy outcome in women with cystic fibrosis and poor pulmonary function. J Cyst Fibros 2020;19(1):80-3.
12. Petersen MC, Begnel L, Wallendorf M, et al. Effect of elexacaftor-tezacaftor-ivacaftor on body weight and metabolic parameters in adults with cystic fibrosis. Journal of Cystic Fibrosis 2022;21(2):265-71.
13. Grancini V, Gramegna A, Zazzeron L, et al. Effects of elexacaftor/tezacaftor/ivacaftor triple combination therapy on glycaemic control and body composition in patients with cystic fibrosis-related diabetes. Diabetes Metab 2023;49(5):101466.
14. Burgel PR, Paillasseur JL, Durieu I, et al. Multisystemic effects of elexacaftor-tezacaftor-ivacaftor in adults with cystic fibrosis and advanced lung disease. Ann Am Thorac Soc2024;21(7):1053-64.
15. Frost F, Nazareth D, Fauchier L, et al. Prevalence, risk factors and outcomes of cardiac disease in cystic fibrosis: A multinational retrospective cohort study. Eur Respir J 2023;62(4):2300174.
16. Maisonneuve P, Marshall BC, Knapp EA, et al. Cancer risk in cystic fibrosis: A 20-year nationwide study from the United States. J Natl Cancer Inst 2013;105(2):122-9.
17. Yamada A, Komaki Y, Komaki F, et al. Risk of gastrointestinal cancers in patients with cystic fibrosis: A systematic review and meta-analysis. Lancet Oncol 2018;19(6):758-67.
18. Rousset-Jablonski C, Reynaud Q, Nove-Josserand R, et al. High proportion of abnormal pap smear tests and cervical dysplasia in women with cystic fibrosis. Eur J Obstet Gynecol Reprod Biol 2018;221:40-5.