Quelques rappels sur la tuberculose
Infection bactérienne chronique due à des myco-bactéries du complexe Tuberculosis : M. tuberculosis dans la majorité des cas, plus rarement M. bovis et M. africanum.
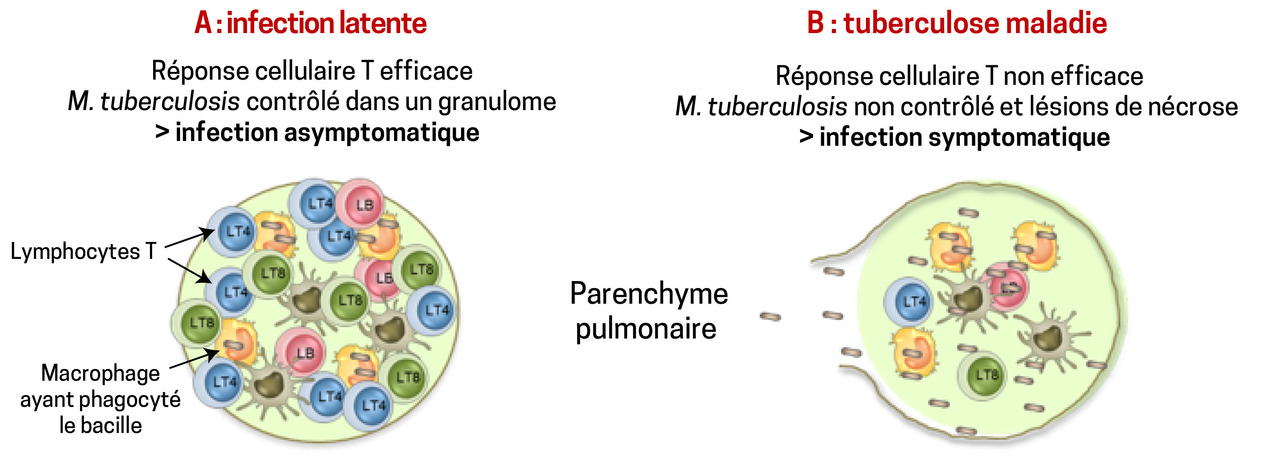
Contamination interhumaine, par voie aérienne directe, qui se traduit par une tuberculose-infection récente (primo-infection), souvent asymptomatique ; dans 90 % des cas, la prolifération de M. tuberculosis est contrôlée par les réponses immunes spécifiques de l’hôte.
Cependant, les bacilles peuvent rester vivants sous forme quiescente dans l’organisme : infection latente. Dans environ 10 % des cas : évolution en tuberculose active ou tuberculose maladie (surtout les 2 premières années ;
Intradermoréaction à la tuberculine (IDR)
Utilisée depuis plus d’un siècle, détecte la réponse immunitaire de l’hôte après l’entrée du pathogène.
Met en évidence l’hypersensibilité retardée induite par l’injection de composants antigéniques de M. tuberculosis (contenus dans la tuberculine) : induration locale à 48-72 h (composée de cellules T et macrophages sécrétant des cytokines) :
– si le diamètre de la zone d’induration < 5 mm → IDR négative ;
– si comprise entre 5 et 10 mm → IDR positive (sujet vacciné ou infecté) ;
– si > 10 mm → en faveur d’une infection récente.
Limites : liées à sa réalisation (lecture, interprétation non standardisées) et au manque de sensibilité (valeur prédictive négative, VPN trop faible) ; risque de faux positifs en cas d’exposition massive aux mycobactéries environnementales et chez les patients vaccinés avec le BCG (VPP faible).
Tests indirects
QuantiFERON-TB Gold et T-SPOT.TB
Sont réalisés sur un prélèvement du sang total (QuantiFERON-TB Gold) ou sur les lymphocytes préalablement séparés (T-SPOT.TB).
Après stimulation par des antigènes de M. tuberculosis, les cellules T mémoires effectrices spécifiques (LT CD4) dirigées contre le bacille sécrètent de l’IFN-γ : on mesure cette cytokine le lendemain (tests indirects ;
Plus reproductibles et surtout plus spécifiques par rapport à l’IDR (les antigènes utilisés sont absents du BCG et la plupart des mycobactéries atypiques ;
Résultats qualitatifs, à interpréter selon les recommandations du fabricant.
QuantiFERON-TB Gold Plus : utilisé depuis peu en pratique, mesure aussi la réponse T CD8, avec une sensibilité au moins équivalente, voire meilleure en cas de contage récent chez l’adulte et chez les patients infectés par le VIH ayant un déficit en LT CD41 (
Conditions de prélèvement, d’analyse et d’interprétation : rigoureuses +++ ;2 résultats proches du seuil de positivité, à interpréter avec prudence et en fonction du contexte clinique et thérapeutique.
Remboursement limité aux situations suivantes (recherche de tuberculose dans le but de la traiter) :
– enfants migrants de moins de 15 ans provenant d’une zone de forte endémie tuberculeuse ;
– patients infectés par le VIH (dépistage systématique dans le bilan initial) ;
– avant la mise en route d’un traitement anti-TNF ;
– tuberculose paucibacillaire de diagnostic difficile chez l’enfant ou extrapulmonaire (discussion clinico-biologique indispensable pour les moins de 5 ans).
Indications médicalement justifiées, mais non prises en charge : personnel professionnellement exposé (à l’embauche), enquête autour d’un cas index.
Trois types de résultats :
– négatif : absence d’infection par M. tuberculosis dans la majorité des cas. Chez un sujet immunocompétent : risque de tuberculose maladie ultérieure quasi-nul. Chez l’immunodéprimé : prudence (la moins bonne immunité peut rendre ces tests moins sensibles) ;
– positif : témoigne la plupart du temps d’une infection par M. tuberculosis, mais ne permet pas de faire la différence entre infection récente/ancienne, forme latente/active, ni d’évaluer le risque d’évolution vers une tuberculose maladie. Dans de très rares cas : infection par des mycobactéries environnementales telles que M. marinum (aquarium), M. kansasii (vétérinaires) et M. szulgai (fleurs). Tout test positif doit être confronté aux données cliniques et aux résultats des examens complémentaires ;
– indéterminé (contrôle négatif ou positif non valides) : si le sujet est immunocompétent, refaire le test (problème technique possible) ; chez l’immunodéprimé, un nouveau test peut être envisagé à distance si l’immunité s’améliore.
1. Telisinghe L, Amofa-Sekyi M, Maluzi K, et al. The sensitivity of the quanti- FERON-TB Gold Plus assay in Zambian adults with active tuberculosis. Int J Tuberc Lung Dis 2017;21:690-6.
2. Pai M, Denkinger CM, Kik SV, et al. Gamma interferon release assays for detection of Mycobacterium tuberculosis infection. Clin Microbiol Rev 2014;27:3-20.
3. Diel R, Loddenkemper R, Nienhaus A. Evidence-based comparison of commercial interferon-gamma release assays for detecting active TB: a metaanalysis. Chest 2010;137:952-63.
4. Diel R, Goletti D, Ferrara G, et al. Interferon-γ release assays for the diagnosis of latent Mycobacterium tuberculosis infection: a systematic review and meta-analysis. Eur Respir J 2011;37:88-99.