La metabolic dysfunction-associated steatotic liver disease (MASLD), anciennement appelée non-alcoholic fatty liver disease (NAFLD), est l’archétype d’une maladie chronique et complexe (de causes multiples : génétiques, épigénétiques et surtout environnementales) liée à un excès de tissu adipeux (surpoids ou obésité) de répartition androïde. La MASLD est généralement associée à des manifestations d’insulinorésistance et d’inflammation métabolique de bas grade (métaflammation), comme un trouble de la régulation glycémique, voire un diabète de type 2, une hypertension artérielle (HTA), une dyslipidémie, une athérosclérose et ses complications cardiovasculaires, une maladie rénale chronique et des cancers extra-hépatiques.1 - 3
Prise en charge selon la sévérité de l’atteinte hépatique
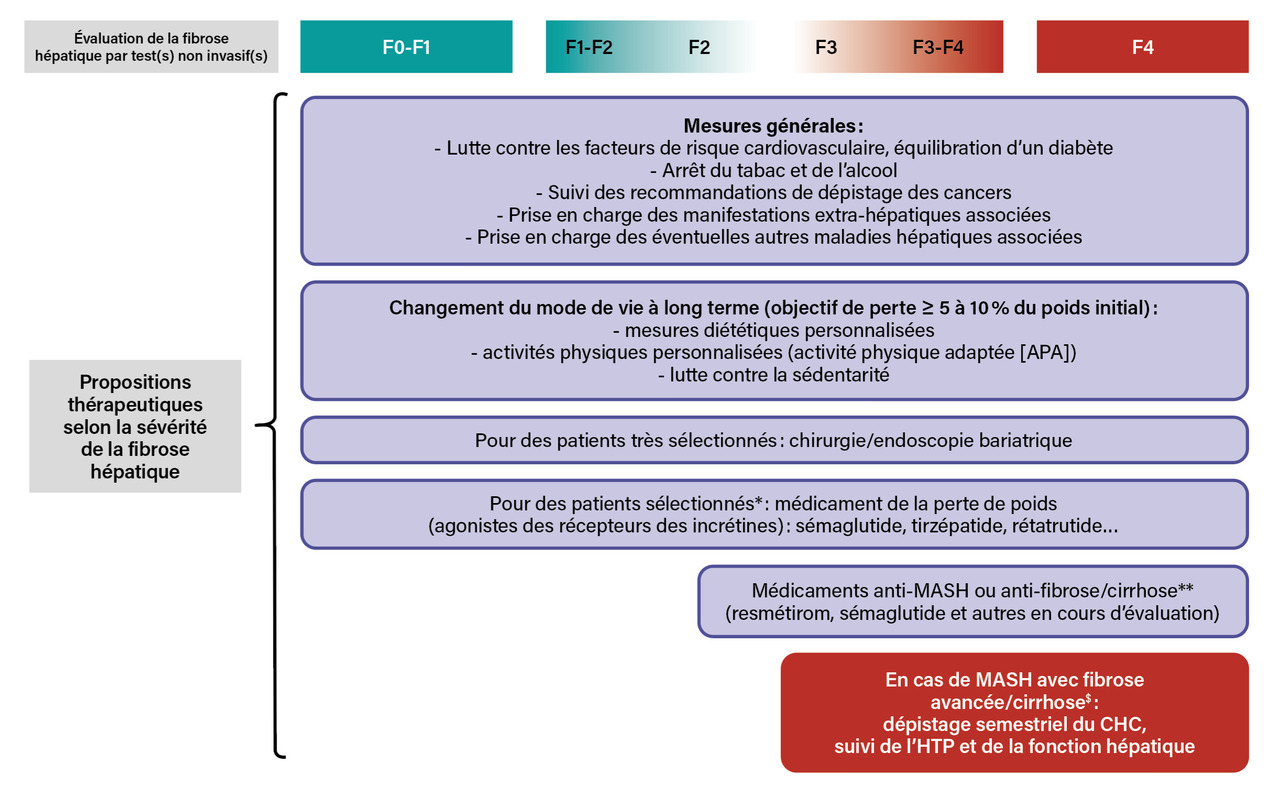
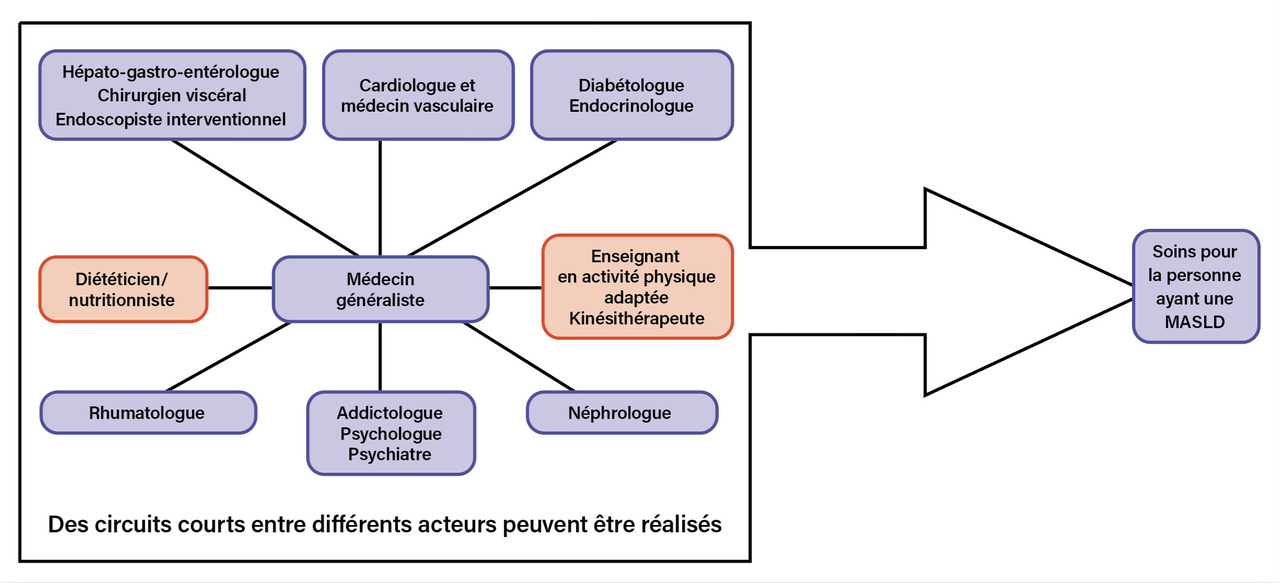
La figure 1 illustre les différentes approches thérapeutiques pour une personne ayant une MASLD selon la sévérité de la fibrose hépatique évaluée à l’aide de tests non invasifs (sériques ou physiques). Compte tenu de la grande fréquence de la MASLD (environ 11 % des femmes et 25,8 % des hommes en France métropolitaine), les médecins généralistes sont en première ligne pour repérer les personnes atteintes et réaliser une prise en charge globale, au long cours. Ils coordonnent les soins réalisés par les différents correspondants médicaux et paramédicaux (fig. 2). Les personnes avec une MASLD sans fibrose avancée (la majorité) doivent bénéficier d’une réévaluation de la fibrose hépatique par un ou deux test(s) non invasif(s) tous les deux à trois ans en l’absence de diabète de type 2, et tous les ans en cas de diabète de type 2. La reconnaissance des personnes avec une cirrhose liée à une metabolic dysfunction-associated steatohepatitis (MASH) ou avec une « fibrose avancée » (F3 -F4) selon les tests non invasifs est fondamentale car elle permet d’initier un suivi par un hépato-gastro-entérologue.4 Celui-ci dépiste le carcinome hépatocellulaire (CHC) par échographie abdominale et dosage sanguin de l’alphafœtoprotéine, et suit l’hypertension portale et la fonction hépatique, tous les six mois. L’apparition d’un CHC doit faire référer le patient dans un centre de recours habitué à prendre en charge cette complication. L’apparition de la première décompensation de la fonction hépatocytaire (score de Child-Pugh B ou C) doit faire adresser les patients de moins de 70 ans en centre de transplantation hépatique.
L’application des différentes approches thérapeutiques (fig. 1) peut nécessiter un rythme de suivi plus ou moins rapproché (trimestriel à annuel) afin d’entretenir la motivation de la personne ayant une MASLD et de suivre l’efficacité et la tolérance des thérapeutiques non médicamenteuses et médicamenteuses entreprises.
Mesures générales
Quatre groupes de mesures générales sont à adopter en premier lieu. Ces mesures générales sont d’autant plus importantes que la plupart des personnes ayant une MASLD sans cirrhose vont principalement décéder d’une pathologie cardiovasculaire ou d’un cancer extra-hépatique.2 Les personnes avec une cirrhose liée à une MASH meurent principalement d’une cause hépatique (insuffisance hépatocellulaire et carcinome hépatocellulaire).6 - 8
Recherche des autres causes d’atteinte hépatique
Tout d’abord, il faut rechercher et prendre en charge les éventuelles autres causes d’atteinte hépatique qui peuvent être associées à une MASLD, en particulier une prise excessive de boissons alcoolisées, mais également une hépatite virale B ou C et potentiellement toute cause d’hépatopathie chronique.
Prise en charge des facteurs de risque cardiovasculaire
Il faut rechercher et prendre en charge les différents facteurs de risque cardiovasculaire. Les facteurs de risque modifiables sont le tabagisme (prise en charge addictologique à organiser), un excès de LDL-cholestérol (la prescription d’une statine ou d’une autre molécule ou association de molécules diminuant le LDL-cholestérol est possible au cours de la MASLD) et la plupart des éléments constitutifs du syndrome métabolique. L’équilibre optimal d’un diabète de type 2 est crucial. Il est souvent obtenu grâce à l’association de metformine et d’un médicament agoniste du récepteur du glucagon-like peptide- 1 (GLP- 1), qui permet une perte de poids significative, comme le sémaglutide, le dulaglutide ou le liraglutide ou d’un inhibiteur du cotransporteur sodium-glucose de type 2 (iSGLT2) comme la dapagliflozine, l’empagliflozine ou la canagliflozine. Le calcul du niveau de risque cardiovasculaire peut être obtenu chez les personnes sans diabète (SCORE : https ://agla.ch/fr/calculateurs-outils/calculateur-esc-score2) ou avec un diabète de type 2 (SCORE2 -Diabetes : https ://agla.ch/fr/calculateurs-outils/calculateur-esc-score2 -diabete).
Dépistage des cancers
Il faut dépister les cancers fréquents, comme recommandé en population générale (cancers colorectal, du sein, de la prostate…). En effet, le faible niveau d’adhésion global au dépistage et le risque accru de cancers extra-hépatiques chez les personnes ayant une MASLD rend cette mesure nécessaire.5
Gestion des manifestations extra-hépatiques
Il est essentiel de rechercher et prendre en charge les manifestations extra-hépatiques fréquemment présentes : syndrome d’apnées-hypopnées obstructives du sommeil, troubles du sommeil, ostéoporose, maladie rénale chronique, syndrome des ovaires polykystiques, hypothyroïdie, lithiase biliaire…
Mesures hygiénodiététiques ou modification thérapeutique du mode de vie
Les mesures hygiénodiététiques (MHD), définies par l’association d’une prise en charge nutritionnelle, d’une augmentation de l’activité physique et d’une lutte contre la sédentarité, le tout inclus dans un changement durable du mode de vie initié et entretenu par une approche motivationnelle, constituent la pierre angulaire de la prise en charge des personnes ayant une MASLD.9 Elles peuvent s’intégrer dans une approche de type éducation thérapeutique du patient (ETP).
Obtenir une perte de poids durable
L’objectif est d’obtenir une perte du poids d’au moins 5 à 10 % du poids initial.10 Une amélioration des lésions histologiques hépatiques est d’autant plus importante que la perte de poids est significative (stéatose dès 5 %, stéato-hépatite dès 7 %, fibrose dès 10 % du poids initial).4 L’efficacité des MHD nécessite une détermination et un savoir-faire appliqués idéalement par une équipe multidisciplinaire comportant une diététicienne et un enseignant en activité physique adaptée (APA). Le manque de disponibilité et de remboursement de ces acteurs de la santé peut être limitant.
Il n’y a pas de « recette » ou de « régime » miracle à appliquer uniformément. Les régimes restrictifs sont déconseillés dans les recommandations de la Haute Autorité de santé (HAS) 2023 pour l’obésité de l’adulte (https ://urls.fr/2B0MhP).
Une évaluation diététique spécifique est réalisée en utilisant une enquête alimentaire et/ou des questionnaires et/ou des applications dédiées, puis des conseils personnalisés écrits sent remis à la personne et un suivi régulier est assuré. Le tableau 1 donne une idée du rythme et de quelques modalités de suivi. La perte de poids n’est pas le seul élément d’évaluation objective de l’efficacité de la prise en charge. Une amélioration des paramètres anthropométriques (tour de taille, répartition entre la masse grasse et la masse maigre), métaboliques (glycémie, insulinémie, bilan lipidique) et hépatiques est également à prendre en compte. Une diminution de la quantité calorique quotidienne totale de 500 à 750 kcal maximum peut être utile pour obtenir une perte de poids.4,5,11
Au cours de l’obésité et/ou de la MASLD, différents « régimes » (appauvris en lipides (« low fat »), appauvris en glucides (« low carb »), le jeûne intermittent et le régime méditerranéen ont été évalués dans la littérature.10,12 - 21 Leur efficacité respective à court terme est relativement similaire. Le plus important est l’adhésion de la personne, meilleure si les modifications nutritionnelles proposées correspondent à ses goûts et à ses contraintes (le régime méditerranéen semble l’un des mieux suivis à long terme). Cela est conforme aux différentes recommandations internationales.4,5,17,22,23 L’éviction des boissons alcoolisées, des sodas, des aliments ultratransformés (tous deux enrichis en fructose industriel), des aliments à haute densité énergétique ainsi que la limitation de la consommation de viande rouge est recommandée.24 La consommation de café, d’huile d’olive et d’aliments végétaux riches en antioxydants est encouragée.4, 25
Prescrire une activité physique adaptée
L’APA est le domaine scientifique et professionnel où l’activité physique (caractérisée par son type, son intensité, sa durée) est un outil thérapeutique à visée préventive et curative considérant l’état clinique de la personne, c’est-à-dire la sévérité de la pathologie, les capacités fonctionnelles et le risque médical du patient. Cette prise en charge a pour objectif d’accompagner la personne vers un état de bien-être bio-psycho-social. L’APA est principalement réalisée par des professionnels issus des filières APA santé formés dans les facultés des sciences et techniques des activités physiques et sportives (STAPS), par les enseignants en APA ou par les kinésithérapeutes. Bien que non clairement mentionnée dans la loi n° 2022 - 296 du 2 mars 2022 visant à démocratiser le sport en France (https ://urls.fr/v6m1Kc), la MASLD, selon la sévérité de la fibrose hépatique, peut probablement être considérée comme un facteur de risque ou une maladie relevant de la prescription d’APA que tout médecin peut désormais faire. Il existe un guide de consultation et prescription médicale d’activité physique à des fins de santé chez l’adulte, mis à jour par la HAS en 2022 (https ://urls.fr/e-mnGZ).
L’ouverture sur le territoire français métropolitain et ultramarin de maisons sport-santé (environ 500 prévues prochainement) permet à tout médecin de trouver près de son lieu d’exercice un centre avec des professionnels compétents dans ce domaine (https ://www.sports.gouv.fr/maisons-sport-sante). Les maisons sport-santé sont appelées à travailler en collaboration avec les réseaux de soins organisés par les communautés professionnelles territoriales de santé (CPTS).
Nouvelles approches thérapeutiques médicamenteuses permettant une perte de poids : la révolution des agonistes des récepteurs des incrétines
L’approche médicamenteuse de la perte de poids est révolutionnée par l’arrivée de nouvelles molécules agonistes du récepteur des incrétines ou du glucagon (tableau 2). Ces médicaments permettent une perte de poids, une action insulino-sensibilisante et une équilibration du diabète de type 2.
Sémaglutide bientôt par voie orale
Le sémaglutide (agoniste du récepteur du GLP- 1) a démontré une réduction des événements cardiovasculaires et rénaux. Il a déjà l’indication pour le traitement du diabète de type 2 et pour la perte de poids. Il peut être prescrit par tout médecin en France depuis juin 2025, mais son remboursement dans l’indication « perte de poids » est toujours en cours de discussion.
La révolution continue avec des molécules doubles agonistes des récepteurs du GLP- 1 et du glucose-dependent insulinotropic polypeptide (GIP) ou du GLP- 1 et du récepteur du glucagon (GCG) ou des molécules triples agonistes (GLP- 1, GIP, GCG). Leur grande efficacité à faire perdre du poids (jusque 25 % du poids initial) devrait changer profondément la prise en charge des personnes en situation d’obésité.26 - 28 Ces molécules s’administrent actuellement surtout par voie sous-cutanée.
Le sémaglutide améliore la MASH sans diminuer la fibrose par rapport au groupe placebo, dans une étude de phase II réalisée chez des personnes ayant une MASH fibrosante sans cirrhose.29 Les résultats intermédiaires de l’étude de phase III (ESSENCE) ont retrouvé une amélioration de la MASH sans aggravation de la fibrose (62,9 % dans le groupe sémaglutide contre 34,3 % dans le groupe placebo) et une amélioration de la fibrose sans aggravation de la MASH (36,8 % dans le groupe sémaglutide contre 22,4 % dans le groupe placebo).30 Cependant, le sémaglutide n’a pas permis de réversion de la MASH ou d’amélioration de la fibrose par rapport au groupe placebo, dans une étude de phase II menée chez des personnes ayant une cirrhose liée à une MASH.31
À la suite de ces résultats, le sémaglutide a obtenu, en août 2025, l’autorisation de mise sur le marché (AMM) dans cette nouvelle indication (MASH sans cirrhose), aux États-Unis.
Une forme orale du sémaglutide a également été développée. Une étude de phase III a évalué le sémaglutide oral à la dose de 50 mg, une fois par jour, chez des patients avec un surpoids ou une obésité, sans diabète de type 2. Le traitement a entraîné une variation moyenne du poids de - 15,1 % à soixante-huit semaines, en comparaison à - 2,4 % dans le groupe placebo.32 À la dose de 25 mg, par voie orale, une fois par jour, la variation moyenne du poids était de - 13,6 % chez les patients avec un surpoids ou une obésité sans diabète de type 2, contre - 2,2 % dans le groupe placebo, après soixante-quatre semaines.33 Les principaux effets indésirables étaient gastro-intestinaux (nausées, vomissements, diarrhées). Le sémaglutide oral a obtenu l’AMM aux États-Unis en décembre 2025 (accord de la Food and Drug Administration [FDA]), pour la perte pondérale. Concernant la transition d’une forme à l’autre, selon le résumé des caractéristiques du produit, les patients traités par 0,5 mg de sémaglutide par voie sous-cutanée peuvent switcher vers la forme orale à 4 ou 9 mg, une fois par jour. Ceux traités par 1 mg de sémaglutide en sous-cutané peuvent prendre du sémaglutide oral à 9 ou 25 mg, et ceux traités avec 2 mg en sous-cutanée peuvent effectuer la transition vers la forme orale à 25 ou 50 mg. Les patients peuvent débuter le traitement avec la forme orale, une semaine après la dernière dose de sémaglutide en sous-cutané.
Survodutide, tirzépatide et rétatrutide encore à l’étude
Le survodutide est un double agoniste des récepteurs du GLP- 1 et du GCG. Dans une étude de phase II, cette molécule, testée à 2,4 ou 4,8 ou 6 mg par semaine (injections sous-cutanées [SC]), a permis une amélioration de la MASH sans aggravation de la fibrose (pour 43 à 62 % des personnes traitées contre 14 % des patients sous placebo). L’amélioration de la fibrose sans aggravation de la MASH sous traitement n’était pas significative dans cette étude.34 Une tendance à l’amélioration des tests non invasifs de la fibrose hépatique a été suggérée pour 18 patients cirrhotiques inclus dans une étude de phase I.35 Deux études de phase III sont en cours, chez des patients avec une MASH fibrosante (NCT06632444) et chez des patients avec une cirrhose MASH (NCT06632457).
Le tirzépatide, lui, est un double agoniste des récepteurs du GLP- 1 et du GIP. Dans une étude de phase II, ce traitement était associé à une amélioration de la MASH sans aggravation de la fibrose (44 à 62 % des patients du groupe tirzépatide contre 10 % des patients du groupe placebo). Une tendance à l’amélioration de la fibrose sans aggravation de la MASH a aussi été observée.36 Le tirzépatide était utilisé à des doses allant de 5 à 15 mg par semaine (injections SC).
Enfin, le rétatrutide, un triple agoniste des récepteurs du GLP- 1, du GIP et du GCG, a permis, chez des patients en situation d’obésité, une perte pondérale allant de 22,8 % (à la dose de 8 mg par semaine [injections SC]) à 24,2 % (à la dose de 12 mg par semaine) contre 2,1 % dans le groupe placebo après 48 semaines de traitement.28 Ce traitement a également réduit la stéatose hépatique de 42,9 à 82,4 % (selon la dose utilisée : de 1 à 12 mg par semaine), contre une augmentation de 0,3 % de la graisse intra-hépatique pour les patients du groupe placebo.37
Une étude de phase III va étudier le rétatrutide et le tirzépatide, contre placebo, en prévention des événements majeurs liés au foie chez les patients avec une MASH fibrosante, évaluée selon des tests non invasifs (NCT07165028).
À terme, ces molécules, pourraient devenir la colonne vertébrale des traitements anti-MASLD et anti-MASH.29,34,36,37 Cependant, beaucoup de personnes diabétiques sont déjà traitées par un agoniste du récepteur du GLP- 1 et, malgré cela, certaines ont une MASH fibrosante ou une cirrhose liée à une MASH. Il est donc important de pouvoir proposer d’autres traitements anti-MASH et anti-fibrose hépatique.
Développement de nouvelles molécules anti-MASH et anti-fibrose liée à la MASH
Après l’échec ou l’insuffisance de nombreuses molécules développées dans le domaine de la MASH (emricasan, élafibranor, acide obéticholique, cénicriviroc, simtuzumab, sélonsertib, cilofexor, firsocostat, aramchol, aldafermine, pegbelfermine…), quelques molécules ouvrent une nouvelle ère thérapeutique (tableau 2).
Resmétirom
Le resmétirom (agoniste sélectif du récepteur hépatique bêta des hormones thyroïdiennes), à la dose per os de 80 ou 100 mg/j, a démontré une amélioration de la MASH et de la fibrose dans un essai de phase III, chez des personnes ayant une MASH fibrosante (F2, F3) sans cirrhose.38 Le resmétirom est la première molécule à avoir obtenu un accord de la FDA et de l’European Medicines Agency (EMA), ainsi qu’une commercialisation aux États-Unis et en Europe dans l’indication MASH hors cirrhose. Un essai de phase III chez des personnes avec une cirrhose MASH est en cours (NCT05500222).
Selon les recommandations américaines et les avis d’experts, le traitement peut être administré en présence d’une élasticité hépatique entre 8 et 15 kPa au FibroScan (et à discuter entre 15,1 et 19,9 kPa), ou entre 3,1 et 4,4 kPa à l’élasto-IRM (et à discuter entre 4,5 et 4,9 kPa) ou en cas de score ELF entre 9,2 et 10,4 (à discuter entre 10,5 et 11,3).39,40 Le traitement s’administre per os à la dose de 80 mg si le poids est de moins de 100 kg et 100 mg pour les patients de 100 kg ou plus. Une évaluation et, si nécessaire, une équilibration de la fonction thyroïdienne sont recommandées avant l’instauration de ce traitement.
Si le resmétirom est utilisé en association avec un inhibiteur du cytochrome P450 2C8 (par exemple le clopidogrel), une réduction de la dose de resmétirom est recommandée (60 mg/j pour les personnes pesant moins de 100 kg et 80 mg/j pour les personnes pesant 100 kg ou plus).
Enfin, l’administration concomitante de ce traitement avec des statines modifie le métabolisme de ces dernières et risque d’augmenter leurs effets indésirables. Par conséquent, lorsqu’elles sont prises en même temps que le resmétirom, la dose maximale recommandée pour la rosuvastatine et la simvastatine est de 20 mg/j et la dose maximale recommandée pour l’atorvastatine et la pravastatine est de 40 mg/j.
En février 2026, la commission de la Transparence de la HAS a autorisé l’accès précoce du resmétirom en France « en association avec un régime alimentaire et de l’exercice physique pour le traitement des adultes atteints de stéato-hépatite associée à un dysfonctionnement métabolique sans cirrhose (MASH) avec fibrose hépatique avancée (fibrose de stade F3) » (https ://urls.fr/72G9nx).
Analogues à longue durée d’action du fibroblast growth factor 21
Les analogues à longue durée d’action du fibroblast growth factor 21 (FGF21) comme le pégozafermine, l’éfruxifermine ou l’éfimosfermine sont aussi prometteurs.41 - 44
Le pégozafermine a permis une amélioration de la MASH sans aggravation de la fibrose dans une étude de phase II pour des patients avec une MASH fibrosante sans cirrhose. Une amélioration de la fibrose sans aggravation de la MASH a également été observée (26 à 27 % des patients traités contre 7 % des patients sous placebo).41 Le pégozafermine était utilisé par voie sous-cutanée, aux posologies de 30 mg et 44 mg toutes les deux semaines. Une étude de phase III est en cours (NCT06318169).
Dans une étude de phase II testant l’éfruxifermine chez des patients avec une MASH fibrosante sans cirrhose, une amélioration de la MASH sans aggravation de la fibrose a été mise en évidence (47 à 76 % des personnes sous éfruxifermine contre 15 % des patients sous placebo). Une amélioration de la fibrose sans aggravation de la MASH a également été observée (39 à 41 % des patients traités contre 20 % des patients sous placebo).42 L’éfruxifermine était administré par voie sous-cutanée, aux doses de 28 mg et 50 mg par semaine. Une étude de phase III est en cours, chez des patients avec une MASH fibrosante sans cirrhose (NCT06215716). Cette molécule a été testée également chez des patients avec une cirrhose MASH compensée, mais n’a pas réduit la fibrose de manière significative à trente-six semaines.45
L’éfimosfermine, administré par voie sous-cutanée, de façon mensuelle ou bimensuelle, a été testé chez des patients avec une MASH fibrosante (Congrès européen d’hépatologie, 2025). Cette molécule a permis une réduction significative d’au moins 50 % de la fraction de graisse hépatique, évaluée par l’IRM-PDFF (magnetic resonance imaging-proton density fat fraction), aux doses de 75 mg et 150 mg toutes les deux semaines, et de 150 mg et 300 mg toutes les quatre semaines, après douze semaines de traitement.43 Administré mensuellement, à la dose de 300 mg, l’éfimosfermine a entraîné une amélioration de la fibrose sans aggravation de la MASH après vingt-quatre semaines (45 % des patients traités contre 21 % des patients sous placebo).44 Une résolution de la MASH sans aggravation de la fibrose a également été observée (68 % des patients traités contre 29 % pour les patients sous placebo).44 Une étude de phase III chez des patients avec une MASH fibrosante prouvée histologiquement est en cours (NCT07221227).
Agonistes des récepteurs PPAR
Les agonistes des récepteurs PPAR (peroxisome proliferator-activated receptors), tels que le lanifibranor sont également à l’étude dans cette indication. Cette molécule, utilisée par voie orale à la dose de 1 200 mg, était associée, dans une étude de phase II, à une amélioration de la MASH sans aggravation de la fibrose (55 % des personnes sous lanifibranor contre 33 % des patients sous placebo). Une amélioration de la fibrose sans aggravation de la MASH a aussi été mise en évidence.46 Une étude de phase III est en cours chez des patients avec une MASH fibrosante sans cirrhose (NCT04849728).
Révolution thérapeutique en cours
Au total, si l’approche thérapeutique médicamenteuse de la MASH connaît une révolution, de nombreuses questions restent non résolues, comme la disponibilité en France (AMM, remboursement) de certaines molécules en cours de développement ou développées, leur efficacité au cours de la cirrhose liée à la MASH, la durée optimale de traitement, l’efficacité et la tolérance des futures associations médicamenteuses.47
2. Anty R, Gual P. Physiopathologie des stéatoses hépatiques métaboliques. La Presse Médicale 2019;48:1468-83.
3. Friedman SL, Neuschwander-Tetri BA, Rinella M, et al. Mechanisms of NAFLD development and therapeutic strategies. Nat Med 2018;24:908-22.
4. Tacke F, Horn P, Wai-Sun Wong V, et al. EASL–EASD–EASO Clinical Practice Guidelines on the management of metabolic dysfunction-associated steatotic liver disease (MASLD). J Hepatol 2024;81:492-542.
5. Rinella ME, Neuschwander-Tetri BA, Siddiqui MS, et al. AASLD practice guidance on the clinical assessment and management of nonalcoholic fatty liver disease. Hepatology 2023;77:1797.
6. Dulai PS, Singh S, Patel J, et al. Increased risk of mortality by fibrosis stage in nonalcoholic fatty liver disease: Systematic review and meta‐analysis. Hepatology 2017;65:1557.
7. Simon TG, Roelstraete B, Khalili H, et al. Mortality in biopsy-confirmed nonalcoholic fatty liver disease: Results from a nationwide cohort. Gut 2021;70:1375-82.
8. Taylor RS, Taylor RJ, Bayliss S, et al. Association between fibrosis stage and outcomes of patients with nonalcoholic fatty liver disease: A systematic review and meta-analysis. Gastroenterology 2020;158:1611-25.e12.
9. Romero-Gómez M, Zelber-Sagi S, Trenell M. Treatment of NAFLD with diet, physical activity and exercise. J Hepatol 2017;67:829-46.
10. Vilar-Gomez E, Martinez-Perez Y, Calzadilla-Bertot L, et al. Weight loss through lifestyle modification significantly reduces features of nonalcoholic steatohepatitis. Gastroenterology 2015;149:367-378.e5.
11. Younossi ZM, Corey KE, Lim JK. AGA clinical practice update on lifestyle modification using diet and exercise to achieve weight loss in the management of nonalcoholic fatty liver disease: Expert review. Gastroenteroly 2021;160:912-8.
12. Saeed N, Nadeau B, Shannon C, et al. Evaluation of dietary approaches for the treatment of non-alcoholic fatty liver disease: A systematic review. Nutrients 2019;11:3064.
13. Meir AY, Rinott E, Tsaban G, et al. Effect of green-Mediterranean diet on intrahepatic fat: The DIRECT PLUS randomised controlled trial. Gut 2021;70:2085-95.
14. Properzi C, O’Sullivan TA, Sherriff JL, et al. Ad libitum Mediterranean and low‐fat diets both significantly reduce hepatic steatosis: A randomized controlled trial. Hepatology 2018;68:1741.
15. Sackner-Bernstein J, Kanter D, Kaul S. Dietary intervention for overweight and obese adults: Comparison of low-carbohydrate and low-fat diets. A meta-analysis. PLOS ONE 2015;10:e0139817.
16. Shai I, Schwarzfuchs D, Henkin Y, et al. Weight loss with a low-carbohydrate, Mediterranean, or low-fat diet. N Engl J Med 2008;359:229-41.
17. Bischoff SC, Bernal W, Dasarathy S, et al. ESPEN practical guideline: Clinical nutrition in liver disease. Clin Nutr 2020;39:3533-62.
18. Katsagoni CN, Papatheodoridis GV, Ioannidou P, et al. Improvements in clinical characteristics of patients with non-alcoholic fatty liver disease, after an intervention based on the Mediterranean lifestyle: A randomised controlled clinical trial. Br J Nutr 2018;120:164-75.
19. Jospe MR, Roy M, Brown RC, et al. Intermittent fasting, Paleolithic, or Mediterranean diets in the real world: Exploratory secondary analyses of a weight-loss trial that included choice of diet and exercise. Am J Clin Nutr 2020;111:503-14.
20. Willmann C, Heni M, Linder K, et al. Potential effects of reduced red meat compared with increased fiber intake on glucose metabolism and liver fat content: A randomized and controlled dietary intervention study. Am J Clin Nutr 2019;109:288-96.
21. Holmer M, Lindqvist C, Petersson S, et al. Treatment of NAFLD with intermittent calorie restriction or low-carb high-fat diet: A randomised controlled trial. JHEP Rep 2021;3:100256.
22. Jensen MD, Ryan DH, Apovian CM, et al. 2013 AHA/ACC/TOS Guideline for the management of overweight and obesity in adults. Circulation 2014;129:S102-38.
23. Semlitsch T, Stigler FL, Jeitler K, et al. Management of overweight and obesity in primary care: A systematic overview of international evidence-based guidelines. Obesity Reviews 2019;20:1218-30.
24. Preston JM, Iversen J, Hufnagel A, et al. Effect of ultra-processed food consumption on male reproductive and metabolic health. Cell Metabol 2025;37(10):1950-60.
25. Hayat U, Siddiqui AA, Okut H, et al. The effect of coffee consumption on the non-alcoholic fatty liver disease and liver fibrosis: A meta-analysis of 11 epidemiological studies. Ann Hepatol 2021;20:100254.
26. Abdelmalek MF, Harrison SA, Sanyal AJ. The role of glucagon-like peptide-1 receptor agonists in metabolic dysfunction-associated steatohepatitis. Diabetes Obes Metabol 2024;26:2001-16.
27. Farrugia MA, Pini E, Tran A, et al. Incretins and MASLD: At the crossroads of endocrine and hepatic disorders. Curr Obes Rep 2025;14:56.
28. Jastreboff AM, Kaplan LM, Frías JP, et al. Triple–hormone-receptor agonist retatrutide for obesity: A phase 2 Trial. N Engl J Med 2023;389:514-26.
29. Newsome PN, Buchholtz K, Cusi K, et al. A placebo-controlled trial of subcutaneous semaglutide in nonalcoholic steatohepatitis. N Engl J Med 2021;384:1113-24.
30. Sanyal AJ, Newsome PN, Kliers I, et al. Phase 3 trial of semaglutide in metabolic dysfunction–associated steatohepatitis. N Engl J Med 2025;392:2089-99.
31. Loomba R, Abdelmalek MF, Armstrong MJ, et al. Semaglutide 2·4 mg once weekly in patients with non-alcoholic steatohepatitis-related cirrhosis: A randomised, placebo-controlled phase 2 trial. Lancet Gastroenterol Hepatol 2023;8:511-22.
32. Knop FK, Aroda VR, Vale RD, et al. Oral semaglutide 50 mg taken once per day in adults with overweight or obesity (OASIS 1): A randomised, double-blind, placebo-controlled, phase 3 trial. The Lancet 2023;402:705-19.
33. Wharton S, Lingvay I, Bogdanski P, et al. Oral semaglutide at a dose of 25 mg in adults with overweight or obesity. N Engl J Med 2025;393:1077-87.
34. Sanyal AJ, Bedossa P, Fraessdorf M, et al. A phase 2 randomized trial of survodutide in MASH and fibrosis. N Engl J Med 2024;391:311-9.
35. Lawitz EJ, Fraessdorf M, Neff GW, et al. Efficacy, tolerability and pharmacokinetics of survodutide, a glucagon/glucagon-like peptide-1 receptor dual agonist, in cirrhosis. J Hepatol 2024;81:837-46.
36. Loomba R, Hartman ML, Lawitz EJ, et al. Tirzepatide for metabolic dysfunction–associated steatohepatitis with liver fibrosis. N Engl J Med 2024;391:299-310.
37. Sanyal AJ, Kaplan LM, Frias JP, et al. Triple hormone receptor agonist retatrutide for metabolic dysfunction-associated steatotic liver disease: A randomized phase 2a trial. Nat Med 2024;30:2037-48.
38. Harrison SA, Bedossa P, Guy CD, et al. A phase 3, randomized, controlled trial of resmetirom in NASH with liver fibrosis. N Engl J Med 2024;390:497-509.
39. Noureddin M, Charlton MR, Harrison SA, et al. Expert panel recommendations: Practical clinical applications for initiating and monitoring resmetirom in patients with MASH/NASH and moderate to noncirrhotic advanced fibrosis. Clin Gastroenterol Hepatol 2024;22:2367-77.
40. Chen VL, Morgan TR, Rotman Y, et al. Resmetirom therapy for metabolic dysfunction-associated steatotic liver disease: October 2024 updates to AASLD practice guidance. Hepatology 2025;81:312.
41. Loomba R, Sanyal AJ, Kowdley KV, et al. Randomized, controlled trial of the FGF21 analogue pegozafermin in NASH. N Engl J Med 2023;389:998-1008.
42. Harrison SA, Frias JP, Neff G, et al. Safety and efficacy of once-weekly efruxifermin versus placebo in non-alcoholic steatohepatitis (HARMONY): A multicentre, randomised, double-blind, placebo-controlled, phase 2b trial. Lancet Gastroenterol Hepatol 2023;8:1080-93.
43. Loomba R, Kowdley KV, Rodriguez J, et al. Efimosfermin alfa (BOS-580), a long-acting FGF21 analogue, in participants with phenotypic metabolic dysfunction-associated steatohepatitis: A multicentre, randomised, double-blind, placebo-controlled, phase 2a trial. Lancet Gastroenterol Hepatol 2025;10:734-45.
44. Loomba R, Kowdley K, Bain G, et al. OS-012 Efimosfermin alfa once monthly treatment improves collagen biomarker profiles and rapidly induces histological fibrosis regression in subjects with MASH stage F2-F3 fibrosis in a 24-week phase 2 trial. J Hepatol 2025;82:S18-9.
45. Noureddin M, Rinella ME, Chalasani NP, et al. Efruxifermin in compensated liver cirrhosis caused by MASH. N Engl J Med 2025;392:2413-24.
46. Francque SM, Bedossa P, Ratziu V, et al. A randomized, controlled trial of the pan-PPAR agonist lanifibranor in NASH. N Engl J Med 2021;385:1547-58.
47. Harrison SA, Frias JP, Lucas KJ, et al. Safety and efficacy of efruxifermin in combination with a GLP-1 receptor agonist in patients with NASH/MASH and type 2 diabetes in a randomized phase 2 study. Clin Gastroenterol Hepatol 2025;23:103-13.
Dans cet article
- Prise en charge selon la sévérité de l’atteinte hépatique
- Mesures générales
- Mesures hygiénodiététiques ou modification thérapeutique du mode de vie
- Nouvelles approches thérapeutiques médicamenteuses permettant une perte de poids : la révolution des agonistes des récepteurs des incrétines
- Développement de nouvelles molécules anti-MASH et anti-fibrose liée à la MASH
- Révolution thérapeutique en cours