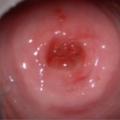
Le cancer du col de l’utérus est le douzième cancer le plus fréquent chez la femme en France. Chaque année, près de 3 000 femmes développent un cancer du col de l’utérus et 1 100 femmes en meurent.
C’est un cancer viro-induit dû à certains types de papillomavirus humain (HPV). Cette infection est très fréquente (environ 8 femmes sur 10 sont exposées à ces virus au cours de leur vie) ; la transmission se fait par contact sexuel et elle peut aussi être indirecte (sous-vêtements, autres).
Une grande majorité des infections à HPV sont éliminées naturellement par le système immunitaire. Dans 10 à 20 % des cas, la persistance du portage viral expose au développement de lésions précancéreuses du col utérin qui, pour un petit nombre d’entre elles, peuvent évoluer vers des lésions malignes.
Papillomavirus humain et cancers
En France et en Europe, les cancers du col de l’utérus sont causés dans près de trois quarts des cas par les HPV 16 et 18. Ces derniers sont aussi les principaux types d’HPV responsables d’autres cancers, plus rares, de la région anogénitale chez la femme (cancer du vagin, de la vulve), chez l’homme (cancer du pénis), du cancer de l’anus et de certains cancers de la sphère oropharyngée.
Dépistage organisé
Depuis 2018, le dépistage des lésions précancéreuses du cancer du col de l’utérus par prélèvement cervico-utérin (PCU) s’inscrit dans le cadre d’un programme national organisé. L’objectif initial était d’atteindre un taux de couverture de 80 %. Ce dernier, qui avoisinait les 59 % sur la période 2018 - 2020, reste insuffisant au niveau national.1
En population générale
Il concerne les femmes asymptomatiques (notamment sans métrorragies provoquées) de 25 à 65 ans inclus, n’ayant pas d’antécédent d’hystérectomie totale ou de traitement conservateur du col de l’utérus pour une lésion précancéreuse ou cancéreuse du col de l’utérus.
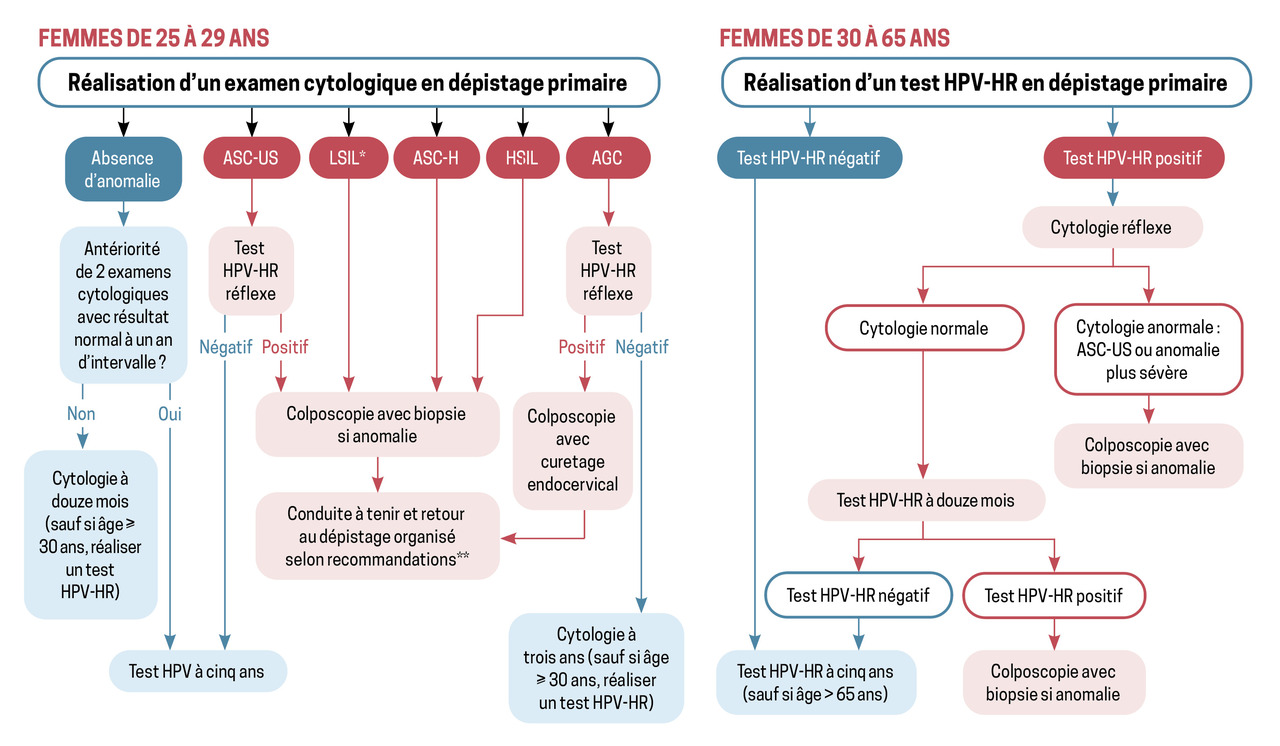
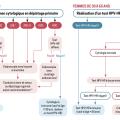
Pour les femmes âgées de 25 à 29 ans, une cytologie tous les trois ans après deux cytologies normales réalisées à un an d’intervalle est recommandée (fig. 1).
Pour les femmes âgées de 30 à 65 ans, la Haute Autorité de santé a fait évoluer les modalités de dépistage en 2019 et recommande la réalisation d’un test HPV en dépistage primaire du cancer du col de l’utérus (fig. 1). Le test HPV est à réaliser trois ans après le dernier examen cytologique dont le résultat était normal :
- si le test HPV est négatif, un nouveau test de dépistage doit être proposé cinq ans plus tard ;
- si le test HPV est positif, un examen cytologique réflexe doit être réalisé : si le résultat de la cytologie est positif (quel que soit son niveau de gravité), une colposcopie est nécessaire ;
- si le résultat de la cytologie est négatif, un test HPV est réalisé un an plus tard ;
- en cas de cytologie avec présence de cellules cylindriques AGC (glandulaires/endocervicales/endométriales), une échographie pelvienne et une biopsie endométriale doivent être effectuées après 45 ans.
Cette stratégie a une meilleure sensibilité que le dépistage par cytologie seule, mais elle augmente le nombre de colposcopies.
En population spécifique
Chez les femmes immunodéprimées (patientes greffées, sous immunosuppresseurs), le suivi gynécologique annuel recommandé repose sur un examen complet de la vulve, du col et du vagin, avec un PCU.
Le suivi doit être poursuivi après 65 ans, y compris lorsqu’il y a eu une hystérectomie.
Chez les femmes porteuses du VIH, le dépistage est le même qu’en population générale si le VIH est contrôlé avant 30 ans et quel que soit le statut immunovirologique après 30 ans. Si le VIH est non contrôlé avant 30 ans, il faut réaliser une cytologie annuelle. 3
Autotests
Les autoprélèvements peuvent constituer une alternative au classique PCU fait par un professionnel de santé. La Haute Autorité de santé préconise ainsi la mise à disposition de kits d’autoprélèvement pour les femmes ayant un défaut de participation aux campagnes de dépistage. Le professionnel de santé peut demander l’envoi d’un kit lorsqu’il est face à des patientes éligibles : femmes refusant le PCU pour des raisons de pudeur, culturelles ou ayant subi des traumatismes (violences sexuelles, mauvaise expérience médicale antérieure…) ou pour lesquelles l’examen gynécologique n’est pas possible.
En cas de test HPV positif, il convient de réaliser un PCU sur lequel est effectuée la cytologie.2
Retentissement de l’annonce d’un test HPV positif
Une revue systématique de la littérature a récemment rappelé le retentissement négatif de l’annonce d’un résultat positif du test HPV, avec apparition de symptômes anxieux, d’une moins bonne qualité de vie et des conséquences négatives sur la vie sexuelle.3
Cette anxiété est souvent liée à une mésinformation et semble être un facteur de mauvaise adhésion au suivi.
Afin d’éviter cet impact sur la patiente, il est conseillé de :
- privilégier la transmission du résultat par téléphone ou en consultation plutôt que par courrier ;
- se procurer des documents d’information et d’éducation (supports papier) pour améliorer la compréhension (par exemple, l’examen colposcopique non expliqué génère de l’anxiété) ;
- expliquer que la présence d’HPV n’est pas une maladie ni le signe d’une « vie de débauche » ;
- préciser que la recherche HPV au sein d’un couple retrouve rarement le même type ;
- rappeler que la mise en évidence du même génotype viral au sein d’un couple ne signifie pas que l’origine de la contamination est le partenaire actuel ; il peut s’agir de la réactivation d’une infection ancienne.
Programmer la colposcopie
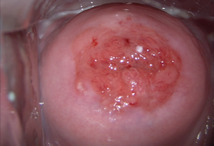
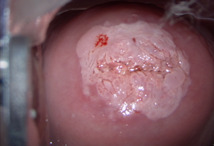
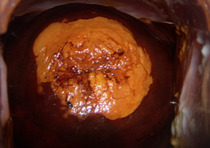
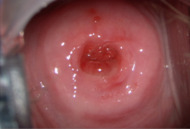
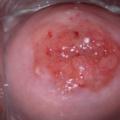
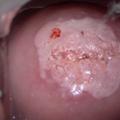
Les patientes nécessitant un examen colposcopique doivent être contactées dans les plus brefs délais par le prescripteur. Celui-ci doit expliquer à la patiente la signification du résultat, puis l’adresser à un professionnel répondant aux critères de la charte de qualité en colposcopie dans un délai de six mois pour les lésions de haut grade, de huit mois pour les lésions de bas grade. Pour les patientes ménopausées, un traitement estrogénique de deux semaines est indispensable avant la colposcopie (fig. 2 à 4).
Conisation et modalités de surveillance
La conisation est le traitement des lésions précancéreuses du col de l’utérus ; le geste est simple, réalisé en chirurgie ambulatoire, sous anesthésie locale et sous contrôle colposcopique peropératoire (fig. 5).
Le meilleur outil de suivi – considéré comme un test de guérison – est la négativité d’un test HPV six mois après la conisation.
Une patiente qui a développé une lésion intraépithéliale de haut grade, même guérie, a plus de risque de refaire une pathologie HPV-induite que la population générale ; c’est pourquoi ces femmes doivent faire l’objet d’un suivi spécifique : test HPV tous les trois ans, à vie.4
Prévention primaire et perspectives
La couverture vaccinale est particulièrement faible en France alors que l’efficacité du vaccin contre le cancer invasif du col a été démontrée : réduction de 88 % lorsque la vaccination est instaurée avant l’âge de 17 ans.5
Le vaccin nonavalent est recommandé à ce jour pour :
- les filles et garçons de 11 à 14 ans ;
- en rattrapage de 15 à 19 ans ;
- chez les hommes ayant des relations sexuelles avec des hommes, jusqu’à 26 ans ;
- à partir de 9 ans chez les candidats à une transplantation d’organe solide.
Le cancer du col de l’utérus est donc un cancer évitable, et les trois niveaux de prévention (primaire : la vaccination ; secondaire : le dépistage ; tertiaire : la conisation) dont nous disposons actuellement devraient rendre ce cancer très rare.
L’objectif de la stratégie 2030 de l’Organisation mondiale de la santé est une quasi-éradication du cancer du col de l’utérus à l’échelle de la planète avant la fin du XXIe siècle.
2. INCa. Référentiel national. Dépistage du cancer du col de l’utérus. Cadre et modalités de recours aux autoprélèvements vaginaux. Mai 2022.
3. ANRS | MIE et CNS | Argumentaire. Dépistage et prise en charge des cancers chez les personnes vivant avec le VIH. Mars 2024.
4. Carcopino X. Suivi post-thérapeutique : nouvelles recommandations. Colposcopie - La lettre. Mars 2020.
5. Lei J, Ploner A, Elfström KM, et al. HPV Vaccination and the Risk of Invasive Cervical Cancer. N Engl J Med 2020;383(14):1340-8.
Voir aussi : Bruna JL, Bergeron C, Averous G, et al. Conduite à tenir devant une femme ayant une cytologie cervico-utérine anormale : actualisation des recommandations INCa après la mise en place du dépistage par le test HPV. Gynécologie Obstétrique Fertilité & Sénologie 2025;53(2):2025, Pages 54-75