Les transformations profondes du mode de vie, au cours du siècle dernier, ont déséquilibré la balance énergétique quotidienne, par l’augmentation des apports caloriques et la diminution des dépenses énergétiques métaboliques du fait de la sédentarisation. En conséquence, en 2022, à l’échelle mondiale, 43 % des adultes étaient en surpoids (soit 2,5 milliards de personnes), dont 890 millions étaient en situation d’obésité (indice de masse corporelle [IMC] supérieur ou égal à 30 kg/m2). Aujourd’hui, la plupart de la population mondiale vit dans des régions où le surpoids et l’obésité font davantage de morts que la malnutrition et l’insuffisance pondérale.1 Cette pandémie d’obésité conduit à la diffusion des complications métaboliques au sein des populations, telles que le diabète ou, à l’échelle hépatique, la stéatopathie métabolique (metabolic dysfunction-associated steatotic liver disease [MASLD]). En quelques décennies, la stéatopathie métabolique est devenue la première cause de perturbation du bilan hépatique à l’échelle mondiale. Le spectre nosologique de la stéatopathie métabolique s’étend à de la stéatose simple (SLD) – qui relève davantage du facteur de risque cardiovasculaire que de la pathologie hépatique – à la stéato-hépatite (MASH) – qui correspond à la forme inflammatoire et progressive de la maladie, évoluant vers la cirrhose et le carcinome hépatocellulaire.
Démarche thérapeutique pour la stéato-hépatite métabolique
Le traitement de première intention de la stéato-hépatite métabolique (metabolic dysfunction-associated steatohepatitis [MASH]) s’appuie sur la correction de l’excès de masse adipeuse corporelle,2 soit le plus souvent sur une diminution du poids. La perte de poids obtenue grâce à l’optimisation des règles hygiénodiététiques (RHD) et à la lutte contre la sédentarité via l’activité physique est une stratégie extrêmement efficace, avec près de 90 % de disparition histologique de la stéato-hépatite lorsque cette perte de poids atteint plus de 10 % de la masse corporelle.3 Malheureusement, cette stratégie, bien que sans risque et efficace, reste très limitée, car seulement 10 % des patients parviennent à atteindre l’objectif de perte pondérale ; par ailleurs, près de la moitié d’entre eux perdent leur bénéfice trois à cinq ans après le début de la prise en charge. Dans ce contexte, des options médicamenteuses offrent un espoir aux patients à haut risque d’évolution vers la cirrhose ou aux patients à haut risque de mortalité hépatique : parmi ces options thérapeutiques, on peut citer, entre autres, la famille des agonistes du récepteur du GLP- 1, les agonistes du récepteur B de la thyroïde ou les agonistes pan-PPAR (lire « Modalités de prise en charge non chirurgicale de la stéato-hépatite non alcoolique et perspectives thérapeutiques », page 400).4,5
Néanmoins, les approches chirurgicales se sont largement développées depuis les années 1990. Les données concernant leur efficacité et leur sécurité sont aujourd’hui bien connues et les recommandations pour la prise en charge de l’obésité de grade III sont définies et validées.6 Les bénéfices des stratégies chirurgicales dépassent largement le cadre de l’obésité avec une amélioration significative des complications, comme les événements cardiovasculaires, le diabète mais aussi l’atteinte métabolique hépatique.
De la chirurgie bariatrique à la chirurgie métabolique
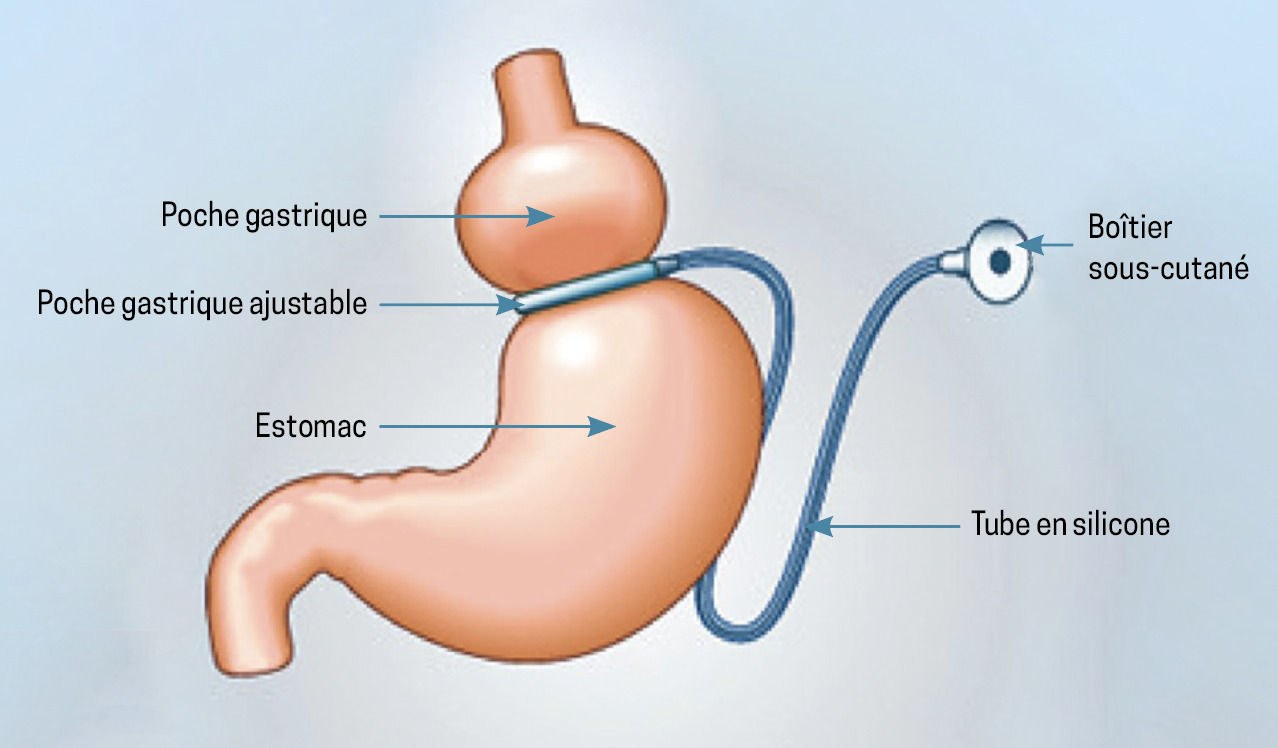
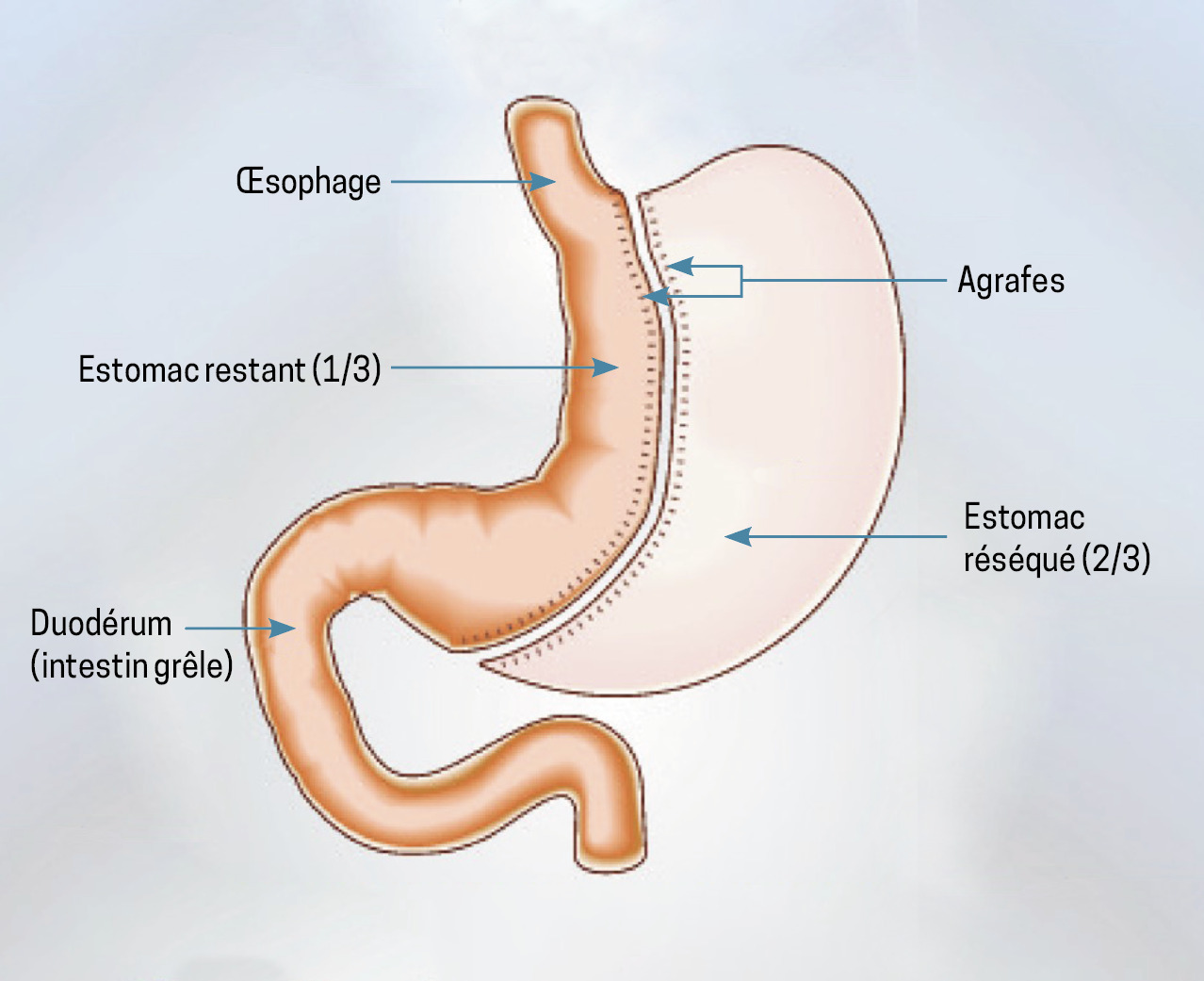
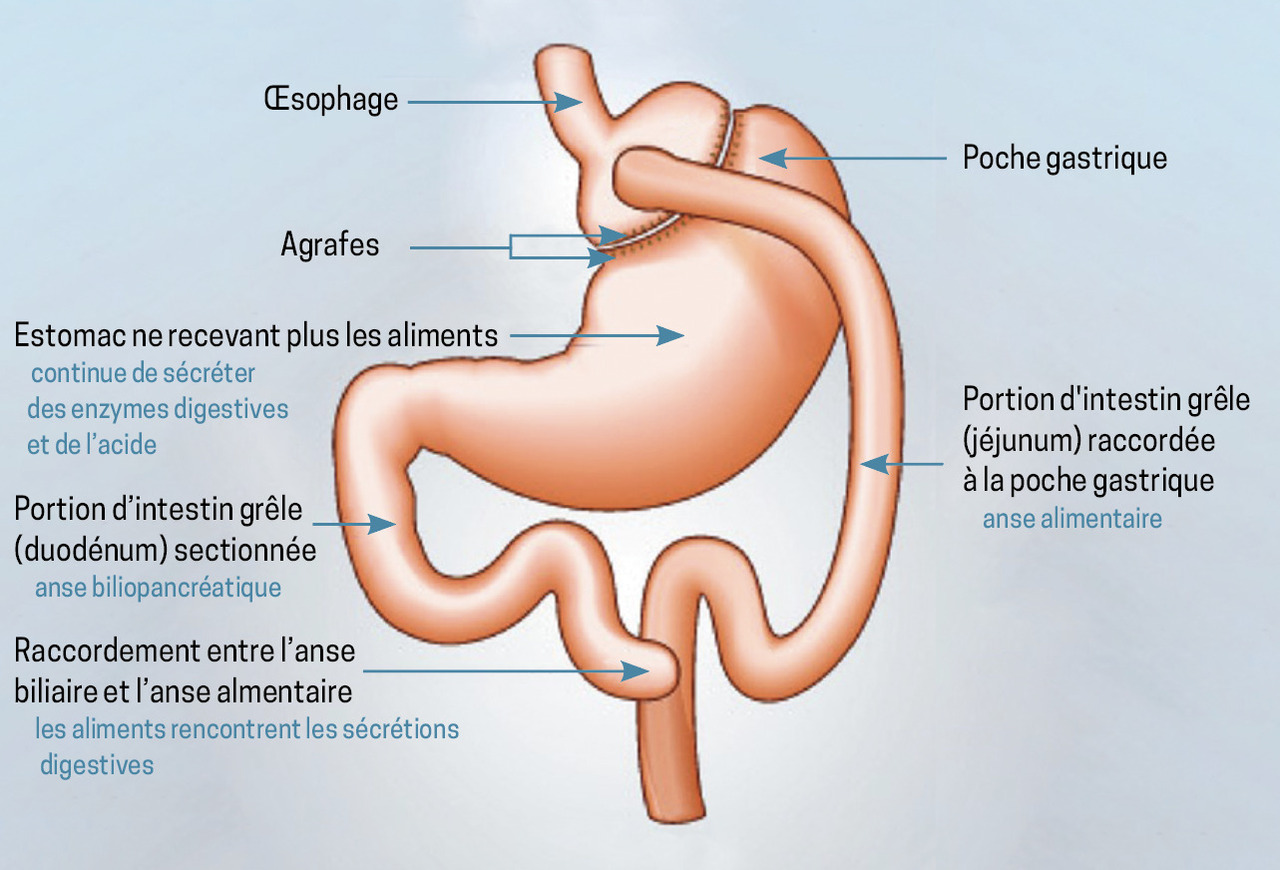
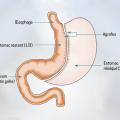
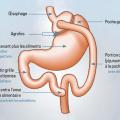
La chirurgie bariatrique comprend trois interventions recommandées par la Haute Autorité de santé (HAS) et couramment pratiquées en France, principalement par cœlioscopie : l’anneau gastrique [fig. 1], la sleeve gastrectomie (SG) [fig. 2] et le bypass gastrique (Roux-en-Y gastric bypass [RYGB]) [fig. 3]. Le bypass dit en « oméga » n’est plus recommandé en France en raison de ses nombreuses complications somatiques, nutritionnelles et carentielles. Il reste néanmoins pratiqué dans de nombreux pays, et certains patients sont susceptibles de bénéficier de ce type d’intervention dans des contextes de nomadisme médical. En dehors de cette situation, les données internationales fournies par les cohortes et les essais randomisés démontrent un bénéfice de survie, une diminution durable et pérenne dans le temps de la perte de poids (15 à 25 % du poids), une diminution des événements cardiovasculaires et oncologiques et une rémission du diabète.7,8
Les indications retenues par la HAS en 2024 ciblent les obésités de grade III (IMC ≥ 40 kg/m2) ou de grade II (IMC ≥ 35 kg/m2) associées à des complications métaboliques : diabète de type 2, hypertension artérielle, MASH ou syndrome d’apnées du sommeil. La stéatose hépatique isolée (SLD) ne constitue pas une indication chirurgicale.
L’efficacité de la chirurgie est totalement acceptée et reconnue dans les recommandations internationales. Les preuves s’accumulent, notamment grâce à l’étude BRAVE (essai randomisé comparant la chirurgie aux RHD),9 qui a démontré la supériorité de la chirurgie pour la rémission de la MASH, observée chez 70 % des patients opérés (50 % en intention de traiter). Les études de cohorte confirment ces résultats, avec près de 80 % de disparition de la MASH à un an - un effet persistant à cinq ans et une amélioration significative de la fibrose hépatique.10 En effet, la résolution du processus inflammatoire intra-hépatique permet une régression progressive de la fibrose, avec une disparition complète pour 45 % des patients initialement atteints. Une étude comparative a, par ailleurs, montré que les patients opérés présentaient une réduction significative du risque de complications cardiovasculaires et hépatiques (cirrhose, carcinome hépatocellulaire) par rapport à ceux suivis médicalement (RHD seules, en l’absence de traitement médicamenteux spécifique à l’époque).11
Plus récemment, un lien a été établi entre la rémission de la stéato-hépatite et l’amélioration de la survie globale à long terme.12 Ces résultats encourageants incitent à proposer ces stratégies aux patients les plus gravement atteints.
Toutefois, en cas de cirrhose, même compensée, la chirurgie est une contre-indication relative et est réservée à des centres experts disposant d’un plateau technique adapté avec une évaluation peropératoire rigoureuse. Malgré les risques, des données récentes suggèrent un bénéfice potentiel chez ces patients atteints de cirrhose métabolique compensée, comparativement au traitement médical (RHD).13 Une étude randomisée est en cours pour évaluer ce bénéfice (programme hospitalier de recherche clinique français NASHSURG). En revanche, les atteintes Child B et C ainsi que l’antécédent de décompensation hépatique constituent des contre-indications formelles.
Les recommandations internationales ont récemment redéfini le spectre nosologique de la stéatopathie métabolique. Les patients dont la consommation d’alcool se situe entre 30 et 60 g/j sont désormais identifiés sous le terme « Met-ALD ».14 Chez ceux présentant une fibrose sévère ou une cirrhose, la prévalence de la consommation d’alcool à risque ou excessive est plus élevée, en raison de la toxicité hépatique accrue de l’alcool. Orienter ces patients vers un projet bariatrique reste délicat. En effet, les bénéfices d’une approche chirurgicale ne sont pas établis pour ce profil « mixte » de maladie hépatique, et un surrisque de mésusage d’alcool post-chirurgie bariatrique a été identifié. Une évaluation addictologique approfondie en préopératoire est donc indispensable.
Le caractère invasif de la chirurgie bariatrique est souvent un frein pour les patients. Dans ce contexte, l’endoscopie bariatrique apparaît comme une alternative intéressante.
Endoscopie bariatrique, alternative à la chirurgie
Alors que la chirurgie bariatrique est indiquée pour les obésités sévères, la prise en charge des patients en situation d’obésité modérée ou non éligibles à la chirurgie a connu des avancées majeures grâce à l’endoscopie bariatrique. Trois techniques se distinguent actuellement : le ballon intragastrique (moins efficace mais non contre-indiqué), l’EndoBarrier et la sleeve gastroplastie endoscopique ou endosleeve. Ces stratégies permettent une perte de poids supérieure à 10 % chez 40 % des patients à un an, et une amélioration d’une ou plusieurs comorbidités chez 80 % d’entre eux (versus 40 % pour le régime seul).15 Leurs intérêts résident dans leur réversibilité et leur faible taux de complications. Toutefois, leur efficacité plus limitée que la chirurgie les rend plus vulnérables à la concurrence des nouvelles stratégies médicamenteuses du traitement de l’obésité. Aucune de ces interventions endoscopiques n’est actuellement remboursée en France.
Ballon intragastrique, solution temporaire
La stratégie endoscopique la plus ancienne est le ballon intragastrique, solution temporaire et peu invasive dont l’objectif consiste à placer un ballon en silicone dans l’estomac puis à le gonfler pour réduire la capacité gastrique et favoriser une satiété précoce. Les effets sont modestes, avec une perte de poids moyenne de 10 à 15 kg par rapport au poids initial, permettant une amélioration des paramètres métaboliques comme la glycémie ou la pression artérielle. Le ballon ne peut pas être laissé en place (maximum six mois) et les résultats sont transitoires. Les effets indésirables les plus fréquents incluent des nausées et des douleurs abdominales en début de traitement, ainsi que des occlusions intestinales hautes. Compte tenu de sa tolérance limitée et de ses complications, cette procédure est de moins en moins proposée.
EndoBarrier, prothèse duodénale
L’EndoBarrier est une prothèse duodénale qui agit en limitant l’absorption des nutriments et en améliorant le contrôle glycémique. Cette approche est toujours en phase d’évaluation en France et son utilisation reste restreinte à des centres experts. Elle n’est pas remboursée en dehors de protocoles de recherche. Les complications potentielles comme les migrations ou les hémorragies imposent une surveillance rigoureuse. Les contre-indications incluent les pathologies biliaires non traitées ou les antécédents de pancréatite.
Endosleeve, sans résection gastrique
La sleeve gastroplastie endoscopique, ou endosleeve, est une technique plus durable qui reproduit les effets d’une sleeve chirurgicale sans résection gastrique. Elle consiste à réduire le volume de l’estomac par des sutures internes réalisées sous endoscopie. Les résultats montrent une perte de poids de 10 à 15 % en douze à vingt-quatre mois.16 En France, cette technique commence à être prise en charge dans certains centres agréés par la HAS et la Société française d’endoscopie digestive, sous réserve d’une inclusion dans un registre national et d’une prise en charge pluridisciplinaire. Toutefois, le succès de cette procédure repose aussi sur l’évaluation pré-interventionnelle et sur le suivi nutritionnel post-endoscopique. Par conséquent, une évaluation psychologique préalable est indispensable pour écarter les troubles du comportement alimentaire, et un suivi nutritionnel strict est nécessaire pour éviter les carences et les rechutes.
Chirurgie bariatrique efficace
La prise en charge chirurgicale de la stéato-hépatite est efficace et bien étudiée chez les patients en situation d’obésité de grade III. Les stratégies endoscopiques, bien que moins invasives, n’ont pas démontré de bénéfices probants à long terme sur la maladie hépatique, et leur avenir est incertain du fait de l’avènement de stratégies médicamenteuses prometteuses. Le positionnement de ces techniques dans l’algorithme de prise en charge ou du projet thérapeutique du patient doit encore être précisé, avec l’arrivée des nouveaux traitements médicamenteux.
2. European Association for the Study of the Liver (EASL); European Association for the Study of Diabetes (EASD); European Association for the Study of Obesity (EASO). EASL-EASD-EASO Clinical Practice Guidelines on the management of metabolic dysfunction-associated steatotic liver disease (MASLD). J Hepatol 2024;81(3):492-542.
3. Vilar-Gomez E, Martinez-Perez Y, Calzadilla-Bertot L, et al. Weight loss through lifestyle modification significantly reduces features of nonalcoholic steatohepatitis. Gastroenterology 2015;149(2):367-e15.
4. Harrison SA, Bedossa P, Guy CD, et al; MAESTRO-NASH Investigators. A phase 3, randomized, controlled trial of resmetirom in NASH with liver fibrosis. N Engl J Med 2024;390(6):497-509.
5. Sanyal AJ, Newsome PN, Kliers et al; ESSENCE Study Group. Phase 3 trial of semaglutide in metabolic dysfunction-associated steatohepatitis. N Engl J Med 2025;392(21):2089-99.
6. Haute Autorité de santé. Obésité de l’adulte : prise en charge de 2e et 3e niveaux. Partie II : pré- et post-chirurgie bariatrique. Recommandations 2024.
7. Sjöström L, Peltonen M, Jacobson P, et al. Bariatric surgery and long-term cardiovascular events. JAMA 2012;307(1):56-65.
8. Schauer PR, Bhatt DL, Kirwan JP, et al. Bariatric surgery versus intensive medical therapy for diabetes - 5-Year outcomes. N Engl J Med 2017;376(7):641-51.
9. Verrastro O, Panunzi S, Castagneto-Gissey L, et al. Bariatric-metabolic surgery versus lifestyle intervention plus best medical care in non-alcoholic steatohepatitis (BRAVES): A multicentre, open-label, randomised trial. Lancet 2023;401(10390):1786-97.
10. Lassailly G, Caiazzo R, Ntandja-Wandji LC, et al. Bariatric surgery provides long-term resolution of nonalcoholic steatohepatitis and regression of fibrosis. Gastroenterology 2020;159(4):1290-1301.e5.
11. Aminian A, Al-Kurd A, Wilson R, et al. Association of bariatric surgery with major adverse liver and cardiovascular outcomes in patients with biopsy-proven nonalcoholic steatohepatitis. JAMA 2021;326(20):2031-42.
12. Lassailly G, Caiazzo R, Goemans A, et al. Resolution of metabolic dysfunction-associated steatohepatitis with no worsening of fibrosis after bariatric surgery improves 15-year survival: A prospective cohort study. Clin Gastroenterol Hepatol 2025;23(9):1567-76.e9.
13. Aminian A, Aljabri A, Wang S, et al. Long-term liver outcomes after metabolic surgery in compensated cirrhosis due to metabolic dysfunction-associated steatohepatitis. Nat Med 2025;31(3):988-95.
14. Rinella ME, Lazarus JV, Ratziu V, et al. A multisociety Delphi consensus statement on new fatty liver disease nomenclature. J Hepatol 2023;78(6):1542-56.
15. Haute Autorité de santé. Nouvelles techniques de chirurgie bariatrique : identification, état d’avancement et opportunité d’évaluer. HAS synthèse, 10 septembre 2020. https://urls.fr/G8hpFI
16. Abu Dayyeh BK, Bazerbachi F, Vargas EJ, et al. Endoscopic sleeve gastroplasty for treatment of class 1 and 2 obesity (MERIT): A prospective, multicentre, randomised trial. Lancet 2022;400(10350):441-51.