La prise en charge hospitalière d’un nouveau-né prématuré dépend avant tout du degré de prématurité et du poids de naissance. Ainsi, les grands ou très grands prématurés sont pris en charge dans un service de soins critiques (réanimation, soins intensifs) au sein duquel ils reçoivent les soins nécessaires et adaptés aux risques qu’ils encourent et bénéficient d’une surveillance renforcée.1 Les principes de prise en charge doivent prendre en compte l’immaturité de chaque organe en lien avec cette prématurité. Lorsque leur état s’améliore et une fois stabilisés, ils sont orientés vers un service de néonatologie. La présence des parents dans ces secteurs de soins très techniques et multidisciplinaires est indispensable et encouragée sans restriction.
Il convient de prendre en compte les spécificités de la prise en charge des prématurés (respiratoire, hémodynamique, digestive, métabolique, hématologique, infectieuse, neurologique et sensorielle) au cours de l’hospitalisation pour adapter au mieux leur suivi après le retour à domicile.
Spécificités cardiovasculaires en cas de prématurité
Persistance du canal artériel
Le canal artériel est une connexion normale entre l’artère pulmonaire et l’aorte ; il est nécessaire à la circulation sanguine fœtale. À la naissance, il doit se fermer.
Chez le prématuré, la fermeture peut être retardée de plusieurs jours ou semaines, en particulier en cas de détresse respiratoire associée. L’incidence de la persistance du canal artériel (PCA) augmente avec la diminution de l’âge gestationnel.
Les conséquences dépendent de la taille canalaire. Sur le plan hémodynamique, la PCA entraîne un shunt droit-gauche, une aggravation de la pathologie respiratoire et un risque d’hémorragie pulmonaire. Sur le plan systémique, la PCA crée un vol diastolique de l’aorte vers l’artère pulmonaire, qui entraîne une hypoperfusion cérébrale, rénale et mésentérique.
Les signes cliniques apparaissent après la baisse physiologique des pressions pulmonaires mais restent aspécifiques et inconstants (polypnée, tachycardie, souffle, hyperpulsatilité artérielle, baisse de la pression diastolique).
L’échocardiographie est l’examen diagnostique de référence.
La prise en charge est médicale et chirurgicale. Deux molécules sont utilisées. L’ibuprofène (seule molécule ayant une autorisation de mise sur le marché [AMM] dans cette indication) est un inhibiteur de la cyclo-oxygénase exerçant un effet vasoconstricteur sur les fibres ductales, dont l’efficacité atteint 60 à 70 %, mais avec un risque d’effets indésirables potentiellement graves (insuffisance rénale, perforation digestive). L’efficacité du paracétamol est maintenant démontrée avant J14, et ses effets indésirables semblent moins importants. La ligature chirurgicale par thoracotomie a longtemps été l’option retenue en cas de contre-indication au traitement médical, avec un risque d’effets indésirables (paralysie laryngée ou phrénique, chylothorax, infection). La fermeture percutanée du canal artériel au moyen d’un cathéter introduit par voie fémorale permettant l’implantation d’un dispositif obstructif dans le canal s’est développée depuis plusieurs années ; elle est réalisable chez des enfants de poids de plus en plus petit.
Il n’existe actuellement aucun consensus sur le choix de la stratégie thérapeutique, le moment de son instauration et ses modalités optimales.
Bradycardies
Le rythme cardiaque normal du nouveau-né oscille entre 75 battements par minute (batt/min) pendant le sommeil et 170 batt/min à l’éveil. Une bradycardie est définie par un rythme inférieur à 70 batt/min ; elle est dite extrême si la fréquence cardiaque est inférieure à 60 batt/min. Les causes en sont nombreuses :
- apnées et désaturations (lire « Diagnostic et prise en charge des pathologies respiratoires de la prématurité », page 277) ;
- causes générales (infections, troubles hémodynamiques, vaccins) ;
- hyper-réactivité vagale, qui correspond à un déséquilibre transitoire de régulation de la balance sympathovagale au profit de l’activité parasympathique pouvant être dépistée par holter électrocardiogramme (ECG). Plus fréquente chez l’ancien prématuré, seule la maturation physiologique du nerf vague permet une disparition des bradycardies, aucun traitement médicamenteux n’ayant fait la preuve de son efficacité.
En revanche, il n’y a aucune preuve de lien direct entre bradycardies et reflux gastro-œsophagien (RGO) dans la littérature.
Tous les nouveau-nés prématurés nécessitent une surveillance par scope pendant l’hospitalisation. Les protocoles varient, mais prolonger l’hospitalisation reste la recommandation tant que la fréquence des bradycardies est significative : en moyenne, la sortie est envisageable après trois à cinq jours sans bradycardie.
Particularités digestives, nutritionnelles et hépatiques
L’intestin du prématuré est immature, avec une motricité plus pauvre et un déséquilibre du microbiote.
Plus la prématurité est grande, plus la nutrition parentérale (sur voie veineuse périphérique ou fréquemment sur cathéter central) est nécessaire.
Les objectifs sont une croissance analogue à la croissance intra-utérine.
La surveillance repose sur les courbes de croissance post-natales (poids, taille, périmètre crânien) et des dosages sanguins réguliers (électrolytes, vitamines).
Nutrition entérale dès que possible
Les grands principes de la nutrition entérale sont fondés sur les recommandations du comité de nutrition de la Société européenne de gastroentérologie, hépatologie et nutrition pédiatrique (ESPGHAN).2
Elle est commencée le plus tôt possible pour limiter le risque d’atrophie muqueuse avec perturbation de l’absorption, le déficit immunitaire local et l’exacerbation des réponses inflammatoires locales. Les principales contre-indications sont l’instabilité hémodynamique ou un trouble digestif majeur (perforation, entérocolite…). Elle est débutée par de faibles volumes (alimentation dite « trophique ») d’environ 20 à 30 mL/kg/j, avec une augmentation progressive des apports guidée par la tolérance, jusqu’à des apports totaux variant de 150 à 200 mL/kg/j en fonction du type de lait, de la courbe de croissance et des comorbidités. L’administration du colostrum est par ailleurs encouragée les premiers jours de vie. La nutrition entérale est administrée par une sonde nasogastrique jusqu’à autonomisation alimentaire.
Différents types de lait
Le lait est évidemment l’aliment essentiel à la croissance du nouveau-né prématuré. Le lait maternel est toujours préféré, mais il doit être enrichi. L’allaitement maternel n’étant pas toujours possible, des laits spécifiques existent.
Lait maternel
Il est impératif d’encourager et de soutenir l’allaitement maternel. Il s’agit du meilleur lait pour les enfants prématurés, au moins jusqu’à 36 semaines d’aménorrhée. Néanmoins, l’allaitement maternel en néonatologie étant difficile (fatigue, stress, contraintes du tire-lait…) et les dons étant insuffisants, les lactariums réservent les stocks aux enfants les plus à risque d’intolérance digestive, soit ceux dont le poids est inférieur à 1 500 à 1 800 g ou ceux ayant une condition clinique spécifique.
L’enrichissement du lait maternel est nécessaire pour couvrir les besoins nutritionnels spécifiques des prématurés, notamment protéiques, énergétiques et en minéraux.
Préparations infantiles pour faible poids de naissance
Il existe plusieurs catégories de préparation infantile pour faible poids de naissance adaptées au poids, en fonction de l’importance du contenu en protéines et en énergie. Elles sont recommandées jusqu’à un poids du nourrisson de 3 kg et sont à base de lait de vache.
Hydrolysats de protéines de lait de vache
Les indications des hydrolysats de protéines de lait de vache sont très limitées ; ils sont réservés aux cas d’allergie avérée aux protéines de lait de vache ou de pathologie digestive spécifique et sont à discuter au cas par cas avec les gastroentérologues pédiatres.
Développement de l’oralité
Chez le prématuré, la succion non nutritive est mature entre 27 et 29 SA ; elle est associée à l’apaisement et à la stimulation de la zone buccale. La succion nutritive apparaît vers 30 SA et mature progressivement jusqu’à 40 SA (coordination succion-déglutition-respiration).
Pour stimuler l’oralité, des protocoles spécifiques sont mis en place tout au long de l’hospitalisation afin de permettre un meilleur investissement de la sphère orale associé à une autonomisation alimentaire et un retour à domicile plus précoces, à la diminution des troubles de la prise alimentaire, voire des troubles du langage.
Gestion du reflux gastro-œsophagien
Le reflux gastro-œsophagien (RGO) est fréquent chez les nouveau-nés prématurés, avec une incidence d’environ 11 % ; il est le plus souvent bénin. L’immaturité du sphincter inférieur de l’œsophage constitue son mécanisme physiopathologique principal.
Un RGO est défini comme pathologique si les régurgitations sont fréquentes, y compris pendant le sommeil, associées à des pleurs excessifs pendant l’alimentation ou à des refus de s’alimenter.
Le diagnostic positif de RGO repose sur la réalisation d’une pH-métrie des vingt-quatre heures, rarement réalisée en pratique durant le séjour en néonatologie en raison des difficultés techniques.
La prise en charge du RGO chez les nourrissons repose sur les recommandations de la Haute Autorité de santé publiées en février 2024 :3
- les régurgitations simples touchent jusqu’à 70 % des nourrissons de quatre mois et se caractérisent par une survenue en post-prandial, pluriquotidienne, de courte durée et spontanée. Elles peuvent entraîner des pleurs, qui témoignent surtout de la gêne de l’enfant mais ne traduisent pas l’existence de douleurs. L’évolution naturelle est une résolution spontanée vers l’âge d’un an. Elles ne nécessitent aucun test pour être documentées ;
- la distinction entre régurgitations simples et RGO pathologique est parfois délicate. Ce dernier est peu fréquent chez l’enfant de moins d’ un an. Les symptômes devant alerter sont une hématémèse, une perte de poids, un refus de s’alimenter ou un ralentissement de la croissance associés à un changement de comportement. La principale complication digestive est l’œsophagite, qui reste très rare ;
- une irritabilité ou des pleurs excessifs isolés ne doivent pas conduire à un diagnostic de RGO pathologique, d’autant que le développement est par ailleurs normal ;
- une allergie aux protéines du lait de vache est à évoquer devant des régurgitations persistantes ou excessives chez un nourrisson qui présente également un eczéma et/ou un terrain familial atopique au premier degré associé ou non à des rectorragies ou à une diarrhée chronique ;
- les mesures de positionnement en décubitus ventral et décubitus latéral gauche ne sont possibles que sous surveillance scopée lors de l’hospitalisation. La position en proclive n’a pas fait la preuve de son efficacité ;
- les mesures diététiques comportent le fractionnement des repas, une ration alimentaire adaptée au poids de l’enfant et l’épaississement du lait.
À ce jour, il n’y a pas de recommandations pour un traitement médicamenteux du RGO du prématuré :
- les inhibiteurs de la pompe à protons (IPP) n’ont pas d’AMM chez le nouveau-né. Ils peuvent néanmoins être prescrits en cas de RGO compliqué d’œsophagite (prouvée) avec une réévaluation après un mois. Une augmentation du risque d’infection secondaire et d’entérocolite est décrite ;
- les alginates sur une courte durée peuvent être proposés chez les nouveau-nés allaités en alternative aux épaississants ou en cas d’échec des mesures diététiques ;
- les prokinétiques ne sont pas indiqués dans le traitement du RGO ; la plupart sont même contre-indiqués dans cette population.
Métabolisme phosphocalcique
Il existe, chez le prématuré, un risque de maladie osseuse métabolique. Complication spécifique des extrêmes prématurés, surtout si le poids de naissance est inférieur à 1 000 g, elle correspond à une diminution du contenu minéral osseux secondaire à une carence phosphocalcique (80 % du stock se constitue au troisième trimestre de la grossesse), aggravée en post-natal par une inadéquation entre les apports et les besoins très élevés du fait d’une cinétique de croissance très rapide.
Les signes cliniques sont très tardifs : principalement des fractures spontanées (surtout costales). Les signes radiologiques, tardifs également, ne sont pas spécifiques : hypominéralisation osseuse, fractures.
La prise en charge repose sur un dépistage systématique des prématurés à risque et sur l’optimisation des apports phosphocalciques et vitaminiques.
Ictères
Deux mécanismes physiopathologiques d’ictère sont possibles : hyperbilirubinémie ou cholestase.
Hyperbilirubinémie
L’hyperbilirubinémie est plus fréquente chez le prématuré en raison d’une destruction accélérée de l’hémoglobine fœtale, de la présence d’hématomes, d’infections et d’inflammation, du jeûne, du stress oxydant et de l’hypoxie, de l’immaturité enzymatique hépatique, d’une hypoalbuminémie relative.
Le traitement curatif repose sur la photothérapie à lumière bleue dépourvue d’ultraviolets.
Cholestase
La cholestase est due à un dysfonctionnement hépatobiliaire avec diminution de la sécrétion biliaire.
La première cause à éliminer est l’atrésie des voies biliaires, rare (1/10 000) mais nécessitant une prise en charge chirurgicale urgente.
La cause la plus fréquente en réanimation néonatale est la cholestase liée à la nutrition parentérale, habituellement transitoire et de bon pronostic, les autres causes étant plus rares (fœtopathies, maladies métaboliques). Elle est plus fréquente en cas de retard de croissance intra-utérin.
Spécificités des risques infectieux
Chez le prématuré, il existe une immaturité médullaire et hépatique entraînant l’équivalent d’un déficit immunitaire, et les taux d’anticorps sont plus faibles, les anticorps maternels traversant le placenta à partir du troisième trimestre.
L’utilisation de dispositifs médicaux invasifs, tels que des cathéters et des sondes d’intubation, augmente par ailleurs le risque d’infection.
Cette fragilité immunitaire expose donc à une augmentation des infections bactériennes mais aussi virales et fongiques. La surveillance du risque infectieux doit donc être très rapprochée et le schéma vaccinal adapté (lire « Sortie et suivi d’un prématuré » page 286).4,5
Infections néonatales bactériennes précoces
Les infections néonatales sont considérées comme précoces si les symptômes surviennent dans les trois premiers jours de vie.6 La transmission peut se faire par voie hématogène, amniotique ou lors du passage de la filière génitale. Le risque d’infections néonatales bactériennes précoces (INBP) est plus élevé chez les prématurés du fait de leur vulnérabilité immunitaire très importante. Les conséquences des INBP sont potentiellement graves ; c’est une cause évitable de mortalité. La mortalité varie en fonction de l’âge gestationnel du nouveau-né : plus de 20 % chez le prématuré versus 2 à 3 % chez le nouveau-né à terme.
Le germe le plus fréquemment retrouvé chez les nouveau-nés prématurés est Escherichia coli, alors que le streptocoque du groupe B est à l’origine de la majorité des INBP chez le nouveau-né à terme. La listéria est très rare actuellement, identifiée dans moins de 1 % des INBP.
Les symptômes d’infection néonatale sont aspécifiques, ce qui rend leur repérage difficile. La confirmation du diagnostic repose sur la réalisation d’une hémoculture avec un volume minimum de 1 mL quel que soient le poids et le terme de l’enfant, avant l’instauration d’une antibiothérapie. La ponction lombaire est indiquée en cas de signes neurologiques évocateurs (hypotonie, convulsions) ou en cas d’hémoculture positive à un germe pathogène. L’examen cytobactériologique des urines, l’analyse bactériologique du liquide gastrique et des prélèvements périphériques (oreilles, anus, aisselles) ne sont plus recommandés chez le nouveau-né.
La Haute Autorité de santé a publié des recommandations en 2017 sur l’antibiothérapie initiale devant une suspicion d’INBP chez les nouveau-nés nés après 34 SA, mais pas chez ceux nés avant.4 Cette antibiothérapie doit être choisie en tenant compte des bactéries les plus fréquentes, des résistances bactériennes aux antibiotiques et des bactéries éventuellement identifiées chez la mère. Une antibiothérapie probabiliste (bithérapie par amoxicilline ou céfotaxime et gentamicine ou amikacine) est souvent débutée chez les très grands prématurés dans un contexte de prématurité spontanée inexpliquée. La poursuite ou non de l’antibiothérapie doit être discutée quarante-huit heures après son instauration. Si l’antibiothérapie est poursuivie, sa durée dépend du type d’infection et de la bactérie identifiée.
Infections nosocomiales
Les infections nosocomiales acquises après plus de soixante-douze heures d’hospitalisation peuvent se présenter comme une septicémie (souvent associée à la présence d’un cathéter), une infection urinaire, une pneumopathie (acquise au cours d’une ventilation mécanique) ou une méningite.
Les bactéries les plus fréquemment identifiées sont les staphylocoques à coagulase négative de façon majoritaire, d’autres Cocci à Gram positif (Staphylococcus aureus, streptocoques, entérocoques…) et des entérobactéries.
Les facteurs de risque principaux d’infection nosocomiale sont la prématurité, le faible poids de naissance, la présence d’un cathéter veineux central ou d’autres prothèses, le retard de mise en place d’une alimentation entérale et une administration préalable d’antibiotiques.
Les signes cliniques de sepsis chez le nouveau-né prématuré ne sont pas spécifiques. Le diagnostic repose sur l’isolement d’un agent pathogène dans un prélèvement (hémoculture, ponction lombaire, aspiration trachéale). Les marqueurs biologiques pour aider au diagnostic d’infection sont la protéine C réactive (CRP) et la procalcitonine.
L’antibiothérapie repose le plus souvent sur l’association de la vancomycine avec un aminoside pour couvrir le staphylocoque à coagulase négative. En cas de point d’appel digestif, un traitement couvrant les bacilles à Gram négatif est ajouté. Le choix de l’antibiothérapie est par ailleurs adapté à l’épidémiologie spécifique du service et au patient (colonisation connue).
Infections fongiques
Les infections fongiques invasives (IFI) sont l’une des principales causes de morbidité et de mortalité chez les nouveau-nés très grands prématurés ou de faible poids de naissance (inférieur à 1 000 g). En effet, ces nouveau-nés immunodéprimés et exposés à des antibiotiques à large spectre ont des barrières épithéliales immatures et subissent souvent des procédures invasives, les exposant à un risque accru d’infection fongique opportuniste.
La majorité des IFI sont dues à Candida sp. ; C. albicans reste prédominant pour les infections néonatales précoces et C. parapsilosis est plus fréquent pour les infections nosocomiales.
Le diagnostic des IFI est difficile à établir et repose sur l’isolement du Candida dans les hémocultures et/ou le liquide céphalorachidien.
Si l’amphotéricine B reste la molécule de référence pour le traitement des candidoses systémiques, en particulier méningées, le fluconazole et les échinocandines – micafungine –, plus récents, moins toxiques et d’utilisation plus simple, sont préférentiellement utilisés.
Chez le très grand prématuré, l’utilisation prophylactique du fluconazole pour réduire le risque d’infections nosocomiales invasives est proposée par certaines équipes et dépend de la fréquence des infections fongiques dans le service.
Particularités neurologiques et sensorielles
Le développement cérébral est très intense au cours du troisième trimestre de grossesse, et l’environnement peut avoir des effets délétères sur la maturation cérébrale des prématurés exposés à des stimuli inexistants pendant la vie fœtale (lire « Soins de confort et développement du prématuré », page 280).
Deux types de lésion cérébrale
On distingue deux types de lésion cérébrale :
- celles de la substance blanche périventriculaire, focale ou diffuse, aussi appelées leucomalacie ; elles sont multifactorielles, combinant des facteurs pré-, péri- et post-nataux, notamment l’âge gestationnel et le poids de naissance bas, l’hypoxie-ischémie et l’inflammation ;
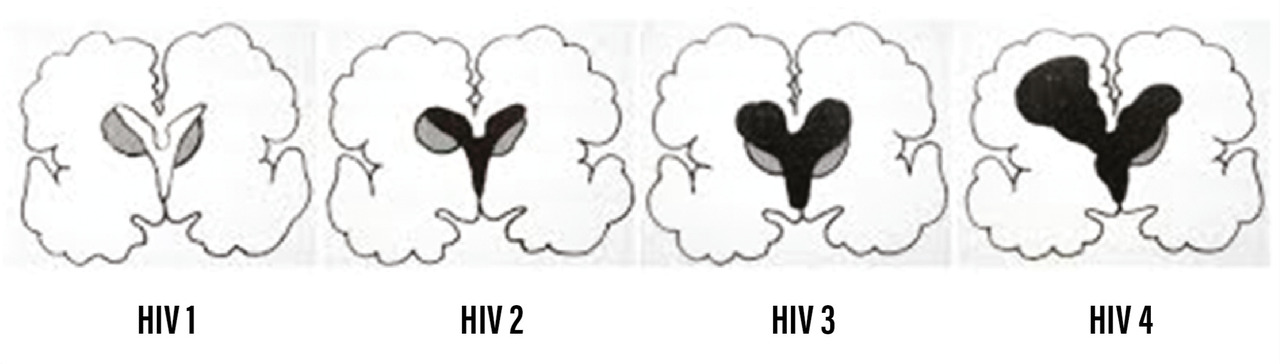
- les hémorragies intraventriculaires classées en quatre stades (figure), qui apparaissent presque toujours dans la première semaine de vie ; leur physiopathologie implique une fragilité vasculaire de la matrice germinative et une absence d’autorégulation vasculaire cérébrale (variation du flux sanguin cérébral), voire des troubles de la coagulation (type coagulation intravasculaire disséminée).
Les hémorragies intracrâniennes sévères de grades 3 et 4 sont une cause importante de décès néonataux (spontanément ou par limitation des thérapeutiques actives). Le risque de handicap à type de paralysie cérébrale, difficultés cognitives et troubles du comportement (troubles du spectre autistique, trouble du déficit attentionnel/hyperactivité) augmente d’autant plus que les lésions sont étendues.
La surveillance neurologique en milieu hospitalier repose sur les examens suivants :
- échographie transfontanellaire, examen de référence pour l’exploration anatomique et vasculaire intracrânienne, pouvant se faire au lit du patient, non invasive et ayant une bonne sensibilité. Les examens sont répétés dans le temps pour suivre l’évolution ;
- électroencéphalogrammes, qui permettent d’apprécier la maturation cérébrale et de suspecter d’éventuelles lésions cérébrales, notamment de la substance blanche (pointes positives rolandiques et temporales) ; ils sont également répétés au cours de l’hospitalisation ;
- imagerie par résonance magnétique (IRM) qui est plus performante pour le diagnostic des lésions parenchymateuses et l’analyse de la fosse postérieure mais nécessite de déplacer l’enfant ; elle est donc privilégiée pour le bilan des lésions à terme, chez les extrêmes prématurés ou si une lésion a été détectée sur les échographies transfontanellaires.
Suivi neurosensoriel
Le dépistage auditif et visuel est un élément clé du suivi hospitalier initial.
Dépistage auditif
Le risque de surdité augmente chez les prématurés (hypoxie-ischémie, médicaments ototoxiques…). Les recommandations imposent la réalisation des potentiels évoqués auditifs, possible à partir de 35 SA. En cas d’échec, une orientation rapide vers un ORL doit être envisagée.7
Rétinopathie du prématuré
La rétinopathie du prématuré est responsable de la majorité des séquelles visuelles du prématuré (entre 10 et 37 % des cécités infantiles selon les pays).
Elle se développe en deux phases : ischémique caractérisée par une dégénérescence vasculaire rétinienne, puis proliférative associée à la prolifération anarchique de néovaisseaux pouvant conduire à des hémorragies intraoculaires et des décollements de rétine.
Elle est multifactorielle, favorisée par le faible de poids de naissance, le faible âge gestationnel, l’oxygénothérapie mal contrôlée, les comorbidités néonatales, etc.
Son dépistage impose une surveillance régulière dès 31 SA par fond d’œil pour tous les prématurés nés avant 32 SA et/ou avec un poids de naissance inférieur à 1 250 g. Cinq stades sont décrits.
L’injection intravitréenne d’anti-VEGF (nouvelles molécules arrivées sur le marché) ou une photocoagulation laser, voire une vitrectomie, sont les différentes possibilités thérapeutiques en fonction des lésions et de l’évolution.
Dermatologie
Cliniquement, la peau des grands prématurés est fine, collante, fragile au contact, rouge, luisante, brillante voire translucide. Les manipulations peuvent être douloureuses. Toutes les fonctions de barrière cutanée sont immatures, avec de nombreuses conséquences :
- métaboliques (perte hydrique, déperdition de chaleur), en partie compensées par l’utilisation d’incubateurs humides et chauffés. En salle de travail, les prématurés sont placés sur des tables radiantes, sous des couvertures en plastique ;
- infectieuses, liées à la perméabilité cutanée anormale et aux multiples effractions et lésions iatrogènes (adhésifs, brûlures par les électrodes ou les excipients, accidents de perfusion...). La plupart des lésions guérissent rapidement, mais des cicatrices plus durables sont possibles. Les petites cicatrices punctiformes du dos de la main ou du talon sont fréquentes ;
- toxiques, par immaturité épidermique associée à un volume de distribution réduit (importance du rapport poids-surface). Une grande prudence s’impose avant application de tout produit sur la peau (crèmes, désinfectants...).
Prolonger le suivi de l’enfant et de sa famille au-delà de l’hospitalisation
La prise en charge hospitalière des nouveau-nés prématurés repose sur une surveillance et des soins adaptés à leur immaturité organique et aux complications spécifiques rencontrées.
Une fois stabilisés, ces enfants sont plus vulnérables et nécessitent un suivi médical pluridisciplinaire régulier pour prévenir, dépister et traiter précocement les complications, notamment neurodéveloppementales et sensorielles.
Cette surveillance vise à mettre en place le plus tôt possible des interventions adaptées (kinésithérapie, orthophonie, ergothérapie), maximisant ainsi les chances d’un développement optimal. Ce suivi doit également inclure un accompagnement familial renforcé pour assurer une transition vers le domicile et favoriser le développement global de l’enfant.
Prise en charge du nouveau-né prématuré en salle de naissance
La naissance d’un enfant prématuré requiert une organisation rigoureuse et une stabilisation néonatale conforme aux recommandations internationales (ILCOR : International Liaison Committee on Resuscitation) ainsi qu’aux principes de la Golden Hour, première heure déterminante pour la prévention des complications liées à l’immaturité.
La prise en charge du prématuré en salle de naissance repose sur des actions coordonnées visant à assurer la prévention des pertes thermiques, la stabilisation rapide respiratoire et circulatoire, la réduction des stress physiologiques et l’organisation rigoureuse du transfert en néonatologie. La communication avec les parents doit rester continue, et le peau à peau doit être proposé dès que l’état du nouveau‑né le permet, même avant le départ vers l’unité de néonatologie.
Thermorégulation
La thermorégulation constitue la priorité immédiate. Les mesures incluent le préchauffage de la salle (de 23 à 25 °C), la préparation de la table de réanimation, l’enveloppement systématique dans un film plastique ou un sac en polyéthylène pour les nouveau-nés de moins de 32 semaines d’aménorrhée, l’utilisation d’un bonnet et l’installation sous une source de chaleur radiante ou en incubateur. L’objectif est de maintenir une température corporelle comprise entre 36,5 et 37,5 °C afin de limiter les risques d’acidose, d’hypoglycémie et d’instabilité respiratoire.
Évaluation clinique
L’évaluation clinique initiale repose sur l’analyse rapide de la respiration, de la fréquence cardiaque et du tonus, complétée par le score d’Apgar aux 1re, 5e et 10e minutes. L’aspiration des voies aériennes n’est indiquée qu’en cas d’obstruction manifeste, afin d’éviter les effets délétères d’une aspiration systématique (bradycardie, désaturation).
Stabilisation respiratoire
La stabilisation respiratoire repose sur l’application précoce d’un CPAP (continuous positive airway pressure ou PPC : pression positive continue) dès la naissance chez les prématurés respirant spontanément, afin de limiter le recours à l’intubation. En cas d’apnées, de bradycardie ou de ventilation inefficace, une ventilation en pression positive est instaurée, avec surveillance continue de la saturation préductale. L’administration d’oxygène est titrée selon les cibles saturatoires recommandées, afin d’éviter tant l’hypoxie que l’hyperoxie. L’intubation trachéale est réservée aux situations d’échec de la ventilation ou aux indications de surfactant précoce (INSURE, LISA selon les pratiques locales).
Prise en charge hémodynamique et métabolique
La prise en charge hémodynamique et métabolique vise à prévenir l’hypoglycémie et l’hypoperfusion. La pose d’une voie veineuse ombilicale ou périphérique est effectuée précocement pour permettre l’administration de glucose. En présence d’une fréquence cardiaque inférieure à 60 battements par minute malgré une ventilation adéquate, un massage cardiaque externe (ratio 3 :1) est initié, suivi, si nécessaire, d’une administration d’adrénaline par voie veineuse ombilicale. Un remplissage vasculaire peut être envisagé en cas de suspicion d’hypovolémie.
Les principes de la Golden Hour encouragent la limitation des stimulations inutiles (gestes regroupés, maintien de la chaleur, environnement calme), l’optimisation de la stabilité thermique et hémodynamique, la réduction du stress et la continuité du monitoring (saturation en oxygène, fréquence cardiaque, température). La prévention de l’hypoxie, de l’hyperoxie et de l’hypothermie constitue la priorité. L’administration de vitamine K est systématique.
Transfert en néonatologie
Le transfert en néonatologie ne doit être entrepris qu’après obtention d’une stabilisation respiratoire, circulatoire et thermique satisfaisante. Le transport s’effectue en incubateur chauffé, monitoré, en maintenant le dispositif respiratoire utilisé en salle de naissance (CPAP ou ventilation en PPC).

 Encadrés
Encadrés