Le terme NASH (stéato-hépatite non alcoolique) a été évoqué pour la première fois en 1980 par Ludwig, suivi en 1986 par Schaffner, qui a proposé le terme NAFLD (maladie du foie gras non alcoolique), pour désigner l’ensemble des pathologies stéato-hépatiques, en particulier celles liées à l’obésité ou au syndrome métabolique. Cependant, les termes « fatty » et « alcohol » étaient stigmatisants, et la définition de la maladie nécessitait l’exclusion d’autres causes de maladies chroniques du foie et ne reconnaissait pas l’association avec le syndrome métabolique.
Évolution de la terminologie
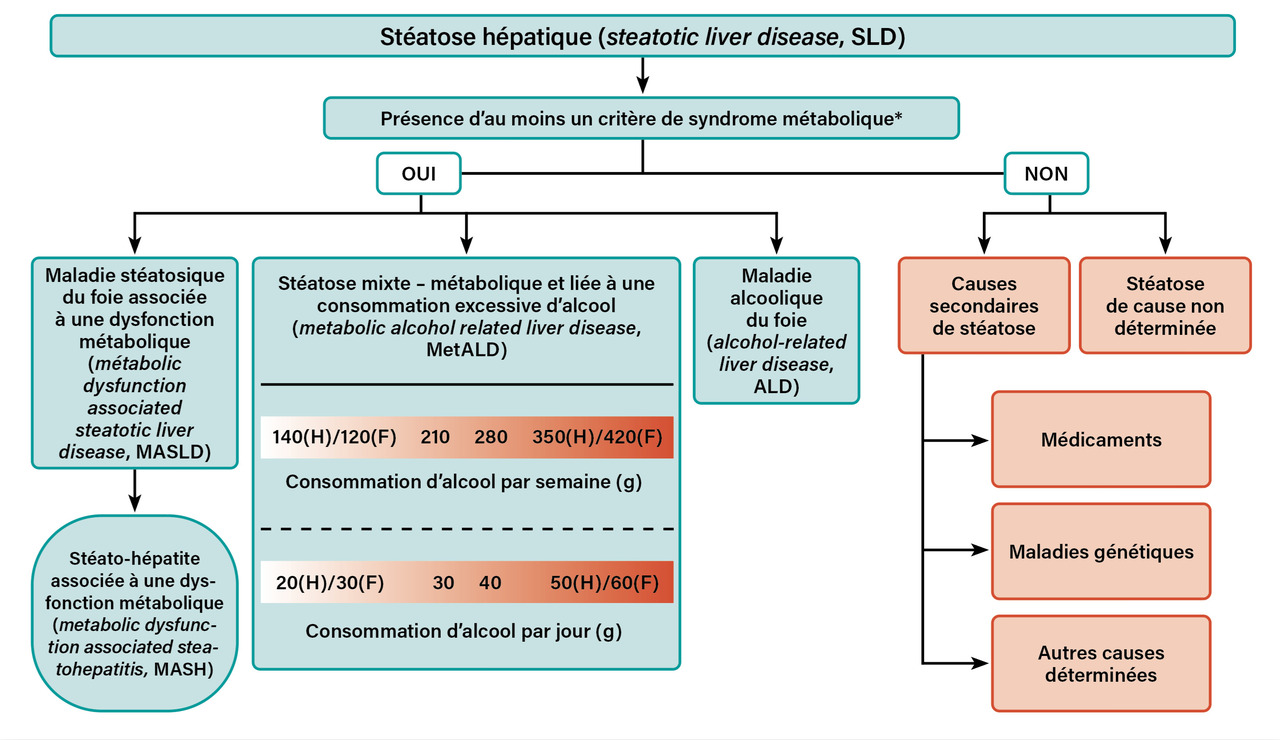
Ces limites ont conduit à une évolution et à un changement de nomenclature pour mieux refléter la pratique clinique. Les sociétés savantes – l’Association américaine pour l’étude des maladies du foie (AASLD) et l’Association européenne pour l’étude du foie (EASL) – ont proposé le terme plus global de « maladie hépatique stéatosique » ou « stéatose hépatique » (SLD), et elles identifient désormais cinq catégories de stéatose en fonction de l’étiologie (figure).1
Parmi les différentes causes de stéatose (SLD), la stéatose métabolique du foie (metabolic dysfunction-associated steatotic liver disease, MASLD) est définie par la présence d’au moins un facteur de risque métabolique parmi les suivants : obésité tronculaire, surpoids, insulinorésistance, prédiabète, diabète, hypertension artérielle, dyslipidémie avec une élévation des triglycérides et une baisse du HDL-cholestérol. Le terme de metabolic dysfunction-associated steatohepatitis (MASH) remplace le terme de nonalcoholic steatohepatitis (NASH).
La nouvelle catégorie MetALD (stéatose mixte métabolique et liée à une consommation excessive d’alcool) inclut les patients avec une consommation d’alcool supérieure ou égale à 20 ou 30 g/j mais inférieure à 50 ou 60 g/j chez les femmes et chez les hommes, respectivement. Dans le cadre du MetALD, il existe un continuum dans lequel, de manière conceptuelle, l’entité peut être considérée comme MASLD ou ALD prédominante. Cela peut varier au fil du temps chez un individu donné.1
Ce changement de terminologie vise à éliminer la stigmatisation et à établir un diagnostic positif fondé sur la présence de facteurs de risque cardiométabolique. Il permet aussi de classifier plus précisément et de manière non discriminatoire les différentes origines de la stéatose hépatique. Cette définition permet d’inclure dans la catégorie MASLD des cas anciennement nommés « NASH maigre » ou non obèse. Enfin, cette classification permet d’identifier une nouvelle catégorie (MetALD) et d’analyser de manière plus fine l’interaction entre alcool et facteurs de risque métabolique sur la progression des lésions hépatiques et le pronostic de ces patients.
Prévalence en augmentation
Plusieurs études récentes ont rapporté une prévalence globale de la MASLD dans le monde de 30 à 33 %.2 En 2019, l’Europe de l’Est affichait le taux de prévalence le plus élevé en Europe, atteignant 20,72 %, avec une légère augmentation annuelle de 0,54 % (de 1990 à 2009) puis de 0,83 % (de 2010 à 2019). L’Europe centrale se classait au deuxième rang, avec un taux de 20,26 % et une augmentation annuelle similaire. La prévalence en Europe de l’Ouest était de 16,88 % en 2019.2
Dans les pays socio-économiquement plus développés, la prévalence de la MASLD était significativement plus élevée chez ceux se trouvant dans le tertile supérieur d’insécurité alimentaire par rapport à ceux du tertile inférieur (moyenne de 26,73 % contre 18,87 %). En revanche, dans les pays socio-économiquement moins développés, c’était l’inverse (19,45 % contre 24,96 %).3
En France, la prévalence de la MASLD est estimée à 18,2 % dans la population générale (selon la cohorte CONSTANCES, de 2012 à 2018), soit 8,491 millions de personnes adultes en extrapolant ces données à la population générale de France métropolitaine. Cette étude montre que la prévalence de la MASLD est nettement plus élevée chez les hommes que chez les femmes (25,8 % vs 11,4 %) et augmente avec l’âge pour les deux sexes : de 4 % chez les femmes de 18 à 27 ans à 44,2 % chez les hommes de 68 à 78 ans. La prévalence de la MASLD atteint 79 % des sujets en situation d’obésité, 62 % des personnes atteintes de diabète de type 2 et 51 % de celles ayant des taux élevés d’alanine aminotransférase (ALT). En considérant la combinaison de l’obésité, du diabète et/ou des niveaux élevés d’ALT, le taux de MASLD augmente, de 5 % chez les patients ne présentant aucun de ces facteurs à 97 % chez ceux ayant les trois.4
La proportion des cas de cirrhose dues à la MASLD a également augmenté. Il est estimé en France que le nombre des cas de cirrhose compensée liée à la MASLD devrait, d’ici 2030, augmenter de 156 %, celui de cirrhose décompensée de 164 % et les cas de carcinome hépatocellulaire (CHC) de 125 %.5 Enfin, la MASLD est actuellement la deuxième cause de transplantation hépatique en Europe et aux États-Unis.6
Risque de mortalité accru
Une étude récente de cohorte en Suède, incluant tous les adultes ayant une MASLD confirmée par biopsie, a évalué les risques de mortalité globale et spécifique selon la sévérité des lésions histologiques sur une période de trente ans. La MASLD était associée à une augmentation du risque relatif de mortalité globale de 93 % et à un excès du risque absolu de 15,3 % sur vingt ans. Un risque accru de mortalité globale était observé à tous les stades de la MASLD, avec une augmentation proportionnelle à la sévérité histologique. Plus précisément, l’excès du risque absolu de mortalité sur vingt ans était supérieur de 10,7 % avec une simple stéatose, de 18,5 % avec une MASH sans fibrose, de 25,6 % avec une fibrose non cirrhotique et de 49,4 % avec cirrhose, par rapport à la population générale. Ce risque excessif était principalement dû à une mortalité spécifique associée aux cancers non liés au foie et à la cirrhose, tandis que la mortalité due aux maladies cardiovasculaires et au carcinome hépatocellulaire (CHC) était relativement modeste.7
Évolution de la MASLD
Progression de la fibrose
Dans les études rétrospectives provenant de centres spécialisés, on constate une fibrose hépatique significative (c’est-à-dire une fibrose en pont disséquant le lobule hépatique) dans 25 à 33 % des cas de stéato-hépatite au moment du diagnostic, dont 10 à 15 % présentent des cirrhoses déjà établies. En comparaison avec d’autres maladies chroniques du foie, comme l’hépatite C, la progression de la fibrose est généralement plus lente chez les patients atteints de MASLD. La vitesse de progression de la fibrose est en moyenne d’un stade tous les quatorze ans chez les patients avec stéatose, tandis qu’elle est d’un stade tous les sept ans chez ceux atteints de MASH. Cependant, certains patients présentent une progression plus rapide : la fibrose en pont et la cirrhose se développent dans un intervalle moyen de six ans chez environ un quart des patients atteints de MASLD.
Les facteurs de risque métabolique, particulièrement l’obésité, le diabète et la résistance à l’insuline, sont des éléments clés déterminant l’évolution (progression ou régression) des lésions histologiques.8 - 10 L’accumulation de facteurs de risque et leur impact variable (par exemple, risque de progression plus élevé associé au diabète et à l’obésité par rapport à l’hypertension artérielle ou à la dyslipidémie) ainsi que la durée d’exposition et l’évolution dans le temps de la sévérité de ces facteurs expliquent pourquoi certains patients progressent plus vite et développent des formes plus sévères de la maladie.
Des facteurs génétiques et des polymorphismes de gènes tels que PNPLA3, TM6SF2, MBOAT7 ainsi que des facteurs épigénétiques sont aussi associés à la sévérité de l’atteinte hépatique dans la MASLD et contribuent à l’hétérogénéité de la maladie.11 - 13
Cirrhose plus fréquente
Une cirrhose se développe chez 15 à 30 % des patients atteints de MASLD, généralement à un âge plus avancé que dans d’autres maladies chroniques du foie, en raison d’une progression plus lente de la fibrose et d’un retard dans le diagnostic de la maladie. Au stade de cirrhose compensée (Child A), les patients atteints de MASLD ont un meilleur pronostic en matière de survie et de risque de décompensation par rapport à ceux infectés par le virus de l’hépatite C. En revanche, dans les stades Child B et C, les risques de décompensation et de décès sont similaires à ceux des patients atteints d’hépatite C.14 Une étude rétrospective aux États-Unis montre que les adultes avec cirrhose MASH compensée ont un risque annuel de 10 % de décompensation ou de décès. Ce risque triple après un premier événement de décompensation. Les principaux facteurs de risque de décompensation sont la présence du diabète de type 2 et de varices œsophagiennes non hémorragiques. Après un premier épisode de décompensation, près de la moitié des individus en développent un deuxième ou ont besoin d’une transplantation hépatique dans les deux ans. Par conséquent, la première décompensation doit entraîner une vigilance accrue et une surveillance étroite pour prévenir la morbidité élevée et le fardeau sanitaire associés aux hospitalisations et aux visites d’urgence.
La même étude a montré que vingt ans après le diagnostic de MASLD, le taux de mortalité est d’environ 22 %, dont 20 % sans cirrhose. Les principales causes de décès sont un cancer non lié au foie (26 %) et les maladies cardiovasculaires (20 %), tandis que les décès liés au foie représentent 6 %.15
Carcinome hépatocellulaire
La prévalence et l’incidence du carcinome hépatocellulaire (CHC) associé à la MASH a fortement augmenté au cours des dix dernières années. Le CHC associé à la MASH présente plusieurs particularités par rapport aux autres causes de maladies chroniques du foie :
les patients sont souvent plus âgés et ont plus de comorbidités ;
les tumeurs apparaissent fréquemment sur un foie non cirrhotique (environ la moitié des cas) et sont généralement de plus grande taille et mieux différenciées ;
peu de cas sont diagnostiqués précocement grâce à la surveillance échographique, notamment en raison de l’absence d’identification des facteurs de risque sur un foie non cirrhotique et des recommandations de dépistage qui en découlent.
En raison de l’âge avancé, des comorbidités multiples et d’un diagnostic tardif, moins de patients ont accès à un traitement curatif. Cependant, pour un même stade tumoral, le pronostic à long terme est similaire à celui des autres causes de maladies chroniques du foie.16,17
Augmentation des transplantations hépatiques
La prévalence de la MASH comme indication de transplantation hépatique a fortement augmenté en Europe et aux États-Unis. Selon une analyse du registre UNOS/OPTN, la MASLD est désormais la deuxième cause de maladies hépatiques chroniques chez les patients en attente de transplantation aux États-Unis et en Europe, avec une augmentation de 170 % au cours des dix dernières années. Les résultats à long terme des patients greffés pour cirrhose due à la MASH sont comparables à ceux des patients greffés pour d’autres causes. Toutefois, les patients atteints de MASH présentent des caractéristiques spécifiques, telles qu’un âge plus avancé, une obésité et d’autres comorbidités métaboliques, qui peuvent affecter la durée d’attente et les résultats à court terme.18,19
Fréquentes complications extra-hépatiques
Risque cardiovasculaire augmenté
La MASLD est étroitement associée à la maladie cardiovasculaire en raison de facteurs de risque et de mécanismes pathogéniques communs, tels que l’inflammation chronique et la dyslipidémie athérogène. De nombreuses études montrent une prévalence élevée d’athérosclérose précoce et de dysfonction endothéliale chez ces patients, avec des lésions athéroscléreuses apparaissant cinq à dix ans plus tôt que dans la population générale.20
Une méta-analyse récente a montré que la MASLD est associée à un risque accru d’événements cardiovasculaires fatals ou non fatals à long terme. Le risque cardiovasculaire augmente avec la progression de la maladie hépatique, en particulier aux stades de fibrose plus avancés. Ces résultats suggèrent que la MASLD pourrait être un facteur de risque indépendant pour la morbidité et la mortalité cardiovasculaires.21 De ce fait, les sociétés savantes européennes en hépatologie, diabète et obésité recommandent d’évaluer le risque cardiovasculaire chez les patients atteints de MASLD. Inversement, il n’y a pas suffisamment de données pour recommander le dépistage systématique de la stéatose chez les patients atteints de coronaropathie qui consultent en cardiologie.
Néoplasies extra-hépatiques
Au-delà du risque de carcinome hépatocellulaire, les patients avec MASLD sont à risque de développer des cancers extra-hépatiques, en lien probable avec l’obésité et la résistance à l’insuline. De nombreuses études montrent que l’obésité, en particulier l’obésité abdominale, augmente le risque de cancer. Cela s’explique par des mécanismes tels que la résistance à l’insuline, l’augmentation de l’IGF- 1 et l’inflammation, qui provoquent la production de cytokines pro-inflammatoires. Une étude américaine révèle que la MASLD, qu’elle soit associée ou non à l’obésité, double ou triple le risque de cancers, en particulier ceux du système digestif (foie, côlon, pancréas, estomac). En revanche, l’obésité seule, sans MASLD ni facteurs de risque métabolique, n’augmente pas ce risque. Toutefois, le lien entre MASLD et augmentation du risque de cancer reste à expliquer.22
Changement de dénomination pour éviter la stigmatisation
Le changement de terminologie, remplaçant le terme NAFLD (maladie du foie gras non alcoolique) par MASLD (maladie du foie liée à une dysfonction métabolique), vise à réduire la stigmatisation et à établir un diagnostic positif fondé sur la présence de facteurs de risque cardiométabolique. Cette nouvelle terminologie permet également de classifier plus précisément et sans discrimination les diverses causes de stéatose hépatique. L’histoire naturelle de la MASLD présente une grande hétérogénéité, avec d’importantes variations interindividuelles selon le profil clinique de chaque patient. Située au cœur du syndrome métabolique et de la résistance à l’insuline, la progression de la maladie affecte le foie (avec évolution de la fibrose, apparition de cirrhose et de ses complications) mais comporte également un risque significatif de complications extra-hépatiques, notamment cardiovasculaires, métaboliques et néoplasiques.
2. Younossi ZM, Wong G, Anstee QM, et al. The global burden of liver disease. Clin Gastroenterol Hepatol 2023;21(8):1978-91.
3. Younossi ZM, Zelber-Sagi S, Kuglemas C, et al. Association of food insecurity with MASLD prevalence and liver-related mortality. J Hepatol 2025;82(2):203-10.
4. Nabi O, Lacombe K, Boursier J, et al. Prevalence and risk factors of nonalcoholic fatty liver disease and advanced fibrosis in general population: The French nationwide NASH-CO study. Gastroenterology 2020;159(2):791-3.e792.
5. Estes C, Anstee QM, Arias-Loste MT, et al. Modeling NAFLD disease burden in China, France, Germany, Italy, Japan, Spain, United Kingdom, and United States for the period 2016-2030. J Hepatol 2018;69(4):896-904.
6. Haldar D, Kern B, Hodson J, et al. Outcomes of liver transplantation for non-alcoholic steatohepatitis: A European liver transplant registry study. J Hepatol 2019;71(2):313-22.
7. Simon TG, Roelstraete B, Khalili H, et al. Mortality in biopsy-confirmed nonalcoholic fatty liver disease: Results from a nationwide cohort. Gut 2021;70(7):1375-82.
8. Pais R, Charlotte F, Fedchuk L, et al. A systematic review of follow-up biopsies reveals disease progression in patients with non-alcoholic fatty liver. J Hepatol 2013;59(3):550-6.
9. McPherson S, Hardy T, Henderson E, et al. Evidence of NAFLD progression from steatosis to fibrosing-steatohepatitis using paired biopsies: Implications for prognosis and clinical management. J Hepatol 2015;62(5):1148-55.
10. Singh S, Allen AM, Wang Z, et al. Fibrosis progression in nonalcoholic fatty liver vs nonalcoholic steatohepatitis: A systematic review and meta-analysis of paired-biopsy studies. Clin Gastroenterol Hepatol 2015;13(4):643-54.e649.
11. Eslam M, Valenti L, Romeo S. Genetics and epigenetics of NAFLD and NASH: Clinical impact. J Hepatol 2018;68(2):268-79.
12. Sookoian S, Castaño GO, Scian R, et al. Genetic variation in transmembrane 6 superfamily member 2 and the risk of nonalcoholic fatty liver disease and histological disease severity. Hepatology 2015;61(2):515-25.
13. Sookoian S, Pirola CJ. Meta-analysis of the influence of I148M variant of patatin-like phospholipase domain containing 3 gene (PNPLA3) on the susceptibility and histological severity of nonalcoholic fatty liver disease. Hepatology 2011;53(6):1883-94.
14. Sanyal AJ, Banas C, Sargeant C, et al. Similarities and differences in outcomes of cirrhosis due to nonalcoholic steatohepatitis and hepatitis C. Hepatology 2006;43(4):682-9.
15. Allen AM, Therneau TM, Ahmed OT, et al. Clinical course of non-alcoholic fatty liver disease and the implications for clinical trial design. J Hepatol 2022;77(5):1237-45.
16. Choi DT, Davila JA, Sansgiry S, et al. Factors associated with delay of diagnosis of hepatocellular carcinoma in patients with cirrhosis. Clin Gastroenterol Hepatol 2021;19(8):1679-87.
17. Piscaglia F, Svegliati-Baroni G, Barchetti A, et al. Clinical patterns of hepatocellular carcinoma in nonalcoholic fatty liver disease: A multicenter prospective study. Hepatology 2016;63(3):827-38.
18. Pais R, Barritt 4th AS, Calmus Y, et al. NAFLD and liver transplantation: Current burden and expected challenges. J Hepatol 2016;65(6):1245-57.
19. Burra P, Becchetti C, Germani G. NAFLD and liver transplantation: Disease burden, current management and future challenges. JHEP Rep 2020;2(6):100192.
20. Targher G, Byrne CD, Tilg H. NAFLD and increased risk of cardiovascular disease: Clinical associations, pathophysiological mechanisms and pharmacological implications. Gut 2020;69(9):1691-705.
21. Mantovani A, Csermely A, Petracca G, et al. Non-alcoholic fatty liver disease and risk of fatal and non-fatal cardiovascular events: An updated systematic review and meta-analysis. Lancet Gastroenterol Hepatol 2021;6(11):903-13.
22. Allen AM, Hicks SB, Mara KC, et al. The risk of incident extrahepatic cancers is higher in non-alcoholic fatty liver disease than obesity - A longitudinal cohort study. J Hepatol 2019;71(6):1229-36.