La stéatose hépatique associée à un dysfonctionnement métabolique (metabolic dysfunction-associated steatotic liver disease [MASLD]) et sa forme inflammatoire, la stéato-hépatite (metabolic dysfunction-associated steatohepatitis [MASH]),1 sont fréquemment rencontrées en chirurgie hépatique. Cette situation s’explique par l’augmentation de la prévalence du syndrome métabolique dans la population générale, par l’effet stéatogène de certaines chimiothérapies utilisées dans le traitement des métastases hépatiques des cancers colorectaux2,3 et par le fait que la MASH constitue un facteur de risque de cirrhose, de carcinome hépatocellulaire (CHC)4 et de cholangio-carcinome,5 trois situations susceptibles de relever d’un traitement par résection ou transplantation.
Un foie stéatosique régénère moins bien après une hépatectomie, et cette altération est majorée dès l’apparition des premières lésions de fibrose. Après une résection tumorale, cette moindre capacité de régénération expose à un risque accru d’insuffisance hépatique postopératoire et de complications générales. La surcharge graisseuse devient ainsi un élément déterminant de l’évaluation préopératoire et de la stratégie chirurgicale.
Lorsque la MASH évolue vers une cirrhose avancée ou se complique d’un CHC, elle constitue une indication de transplantation hépatique. Toutefois, après la greffe, la stéatose peut récidiver ou apparaître de novo sur le greffon, exposant à nouveau au risque de cirrhose ou de CHC.
Enfin, le vieillissement des donneurs et la progression du syndrome métabolique dans la population générale conduisent à greffer, sous la pression de la pénurie d’organes, des greffons porteurs de MASLD ou de MASH. Ces greffons tolèrent moins bien l’ischémie et peuvent présenter une dysfonction initiale, augmentant le risque de complications précoces après transplantation.
Résection hépatique sur foie de MASLD ou de MASH
Le pronostic immédiat d’une résection du parenchyme hépatique dépend de la capacité du foie résiduel à reprendre un volume et une fonction normaux. Peu d’études ont étudié l’impact de la MASLD et de la MASH sur la régénération hépatique et les complications postopératoires après résection. Pourtant, la situation est fréquente, qu’il s’agisse de résections d’un adénome sur un foie de MASLD chez la jeune femme en situation d’obésité,6 de la résection d’un CHC ou d’un cholangiocarcinome développés sur un foie de MASH7 ou encore de la résection de métastases hépatiques des cancers colorectaux qui ne se conçoit plus sans qu’elle ait été précédée d’une chimiothérapie comportant du 5 -fluoro-uracile et souvent de l’irinotécan, associée à une incidence de MASLD et de MASH pouvant aller jusqu’à respectivement 50 %8 et 20 %.9
En 1998, dans une étude rétrospective, Behrns et al.10 ont, les premiers, montré qu’après résection hépatique majeure, une stéatose modérée à sévère était associée à un taux de complications postopératoires plus de quatre fois plus élevé que si le foie n’était pas stéatosique (3 % versus 14 %). Truant et al.11 ont ensuite montré que dans une population d’obèses bénéficiant d’une résection hépatique, la régénération du foie restant était significativement plus lente et moins importante.D’Assignies et al.12 ont montré qu’une stéatose hépatique objectivée par l’imagerie par résonance magnétique et supérieure ou égale à 5 % suffisait à augmenter significativement le risque de complications postopératoires.
La surcharge graisseuse des hépatocytes augmenterait l’importance du stress oxydatif lors des manœuvres chirurgicales et désorganiserait les signaux de prolifération cellulaire, si bien qu’après une résection le foie régénérerait plus lentement et de façon moins efficace.13
Ces données font de la MASLD et de la MASH des facteurs de risque incontestables de complications après résection. Il est prématuré, cependant, de conclure que cette morbidité accrue est le seul fait d’une réduction de la capacité du foie à se régénérer.
MASH et transplantation hépatique
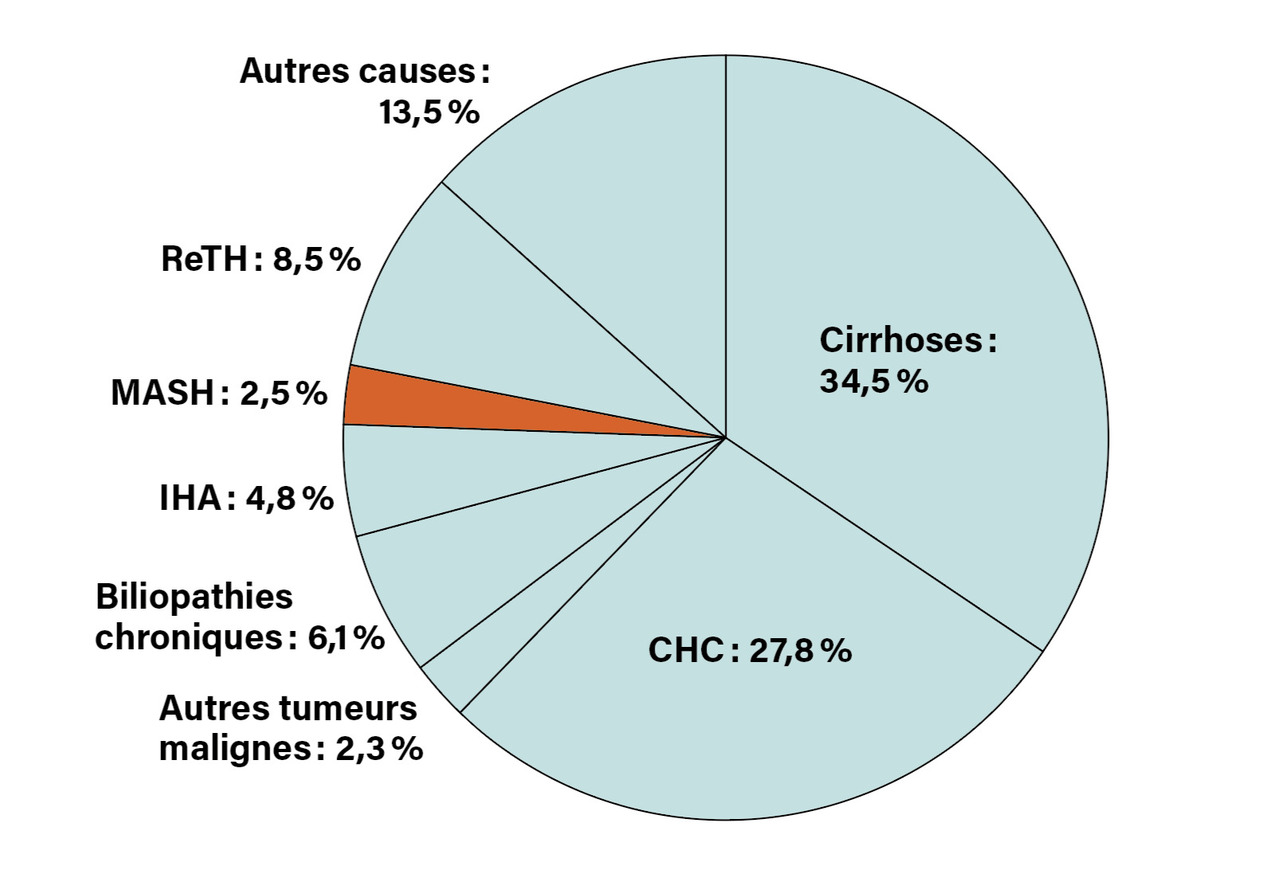
La MASLD n’est une indication de greffe que lorsqu’elle est associée à une maladie chronique du foie. La MASH, en revanche, devient une indication fréquente lorsqu’elle est compliquée d’un CHC, parfois d’un cholangiocarcinome et/ou d’une cirrhose grave. Le dernier rapport médical et scientifique de l’Agence de la biomédecine (ABM) rapporte que 1 439 malades ont été greffés d’un foie en 2024 (rapport médical et scientifique de l’ABM, 2024. https ://rams.agence-biomedecine.fr/greffe-hepatique- 0). La majorité l’était pour une cirrhose compliquée ou non d’un CHC [fig. 1]. En 2024 toujours, seuls 2,5 % des malades étaient greffés pour une MASH alors qu’aux États-Unis elle était déjà, en 2022, à l’origine de 31 % des indications de greffe, constituant ainsi la première indication de transplantation hépatique.14 Cette différence surprenante entre taux américains et français, alors que les deux populations semblent soumises au même mode de vie, tient au fait que l’item « MASH » (ou NASH à l’époque) ne figurait pas dans le registre des indications de transplantation hépatique de l’ABM avant 2018 et, plus vraisemblablement, qu’une proportion inconnue de malades classés dans la rubrique CHC avaient une MASH sans cirrhose constituée ou une cirrhose d’origine dysmétabolique, et qu’enfin, dans le groupe des transplantés hépatiques pour cirrhose figuraient des cirrhoses post-MASH mal classées. En France, au cours de la période 2002 - 2016, le taux de candidats à la greffe avec un indice de masse corporelle (IMC) supérieur ou égal à 35 kg/m2 représentait déjà 5,5 % des malades inscrits en liste. Il est donc vraisemblable qu’en France comme en Europe, la MASH devienne rapidement l’une des plus fréquentes indications de transplantation hépatique et impose de modifier les modes de prise en charge des candidats à la greffe ou après la greffe.
Le profil des patients transplantés hépatiques évolue
La MASH est présente chez près de 80 % des personnes en situation d’obésité, et l’obésité fait courir un risque vital aux candidats à la transplantation hépatique. L’analyse des données de la base CRISTAL* de l’ABM a montré que l’accès à la greffe des malades inscrits en liste d’attente avec un IMC supérieur ou égal à 35 kg/m2 était diminué par rapport à celui des autres malades en raison d’un taux supérieur d’incompatibilité morphologique entre greffon et receveur, et d’un taux supérieur d’aggravation de la maladie ou de décès en liste d’attente. Après la greffe, l'obésité était un facteur de risque indépendant de dysfonction du greffon, de complications dans les trois premiers mois et de mortalité à long terme, en particulier lorsque l’obésité était associée à un diabète.15
Ainsi, en France comme en Europe, la population des malades candidats à la greffe s’est transformée. À la population des malades en insuffisance hépatique terminale, cachectiques, à la paroi abdominale distendue par une ascite abondante et souvent ictériques s’est substituée une population de malades d’un âge moyen proche de 60 ans, proposés à la greffe pour un CHC développé sur une MASH ou une cirrhose grave, dans un contexte dysmétabolique où l’hypertension artérielle (HTA), le diabète, la dyslipidémie et, in fine, la maladie athéromateuse, contribuent à une morbidité et une mortalité importantes avant, pendant ou rapidement après la greffe. La prise en charge des malades inscrits sur la liste d’attente de transplantation hépatique, autrefois articulée autour de la gestion de l’insuffisance hépatique, est maintenant dominée par la prise en charge diététique, l’équilibre du diabète, la prévention et le traitement des complications thromboemboliques et cardiovasculaires.
Association transplantation hépatique et chirurgie bariatrique
Chez les candidats à la transplantation hépatique en situation d’obésité se pose la question de la place et du moment de la chirurgie bariatrique pour faire baisser l’IMC. Avec l’indispensable accompagnement des malades par une équipe spécialisée en éducation nutritionnelle, un geste de chirurgie bariatrique avant la greffe est envisageable au stade de MASH. Toutes les équipes s’accordent à dire qu’il faut préférer la sleeve gastrectomy au bypass qui, s’il est plus efficace, est associé à un risque plus élevé de complications anastomotiques, parfois très graves.16 Il est cependant montré que la chirurgie bariatrique améliore la stéato-hépatite et les anomalies métaboliques qui l’accompagnent, et certains candidats à la greffe peuvent même quitter la liste d’attente à la suite de l’amélioration de leur condition.17 Au stade de cirrhose, la chirurgie bariatrique est associée au risque de décompensation et favorise le développement d’adhérences péritonéales, sources potentielles d’hémorragie au moment de la transplantation hépatique, mais ce risque serait faible lorsque la cirrhose est compensée.18 Le principal avantage d’une chirurgie bariatrique pendant la transplantation hépatique (après que le greffon a été implanté) est qu’elle ne nécessite qu’une seule intervention, avec un risque moindre de complications périopératoires associées à l’hypertension portale. Les expériences sont à ce jour peu nombreuses mais démontrent la faisabilité du geste combiné.19 Dans une étude cas-contrôle récente, Tsamalaidze et al.20 ont observé qu’à l’exception d’une hospitalisation plus longue, les malades opérés après transplantation hépatique avaient des résultats superposables à ceux des malades opérés hors d’un contexte de transplantation hépatique. La chirurgie bariatrique dans le contexte d’une transplantation hépatique peut donc être envisagée avant, pendant ou après la greffe, et ses résultats, apparemment bons, restent à consolider.
Récidive quasi inévitable
Toutes les données convergent pour faire de la récidive de la MASLD et de la MASH sur le greffon une évolution inéluctable. Cette notion a été évoquée pour la première fois en 2009 par le groupe de Pittsburg21, qui rapportait que, sur une série de 79 greffés pour MASH, 70 % avaient une récidive de MASLD et 24 % une récidive de MASH après un délai moyen de 3,4 ans post-greffe. Plus récemment, en 2023, dans une étude rétrospective engageant 19 centres français et un centre suisse de transplantation hépatique, Villeret et al.22 ont montré sur une série de 150 malades transplantés pour MASH, qu’après un délai de cinq ans post-transplantation hépatique, les taux cumulés de récidive sur le greffon de la MASLD et de la MASH étaient respectivement de 80 % et 60,3 %. Dans la population de l’étude, les incidences cumulées du syndrome métabolique un, cinq et dix ans après la greffe étaient respectivement de 73,5 %, 86,2 % et 92,5 %. Plus préoccupant encore, 73,1 % des greffés avaient au moment de l’analyse un IMC supérieur à 25 kg/m2 et 60 % étaient en situation d’obésité (IMC ≥ 30 kg/m2).
Autant dire qu’après une greffe pour MASH, la récidive de l’infiltration graisseuse du greffon est quasi constante. Pour expliquer ce phénomène, deux raisons, non exclusives l’une de l’autre, sont avancées : la persistance après la greffe des facteurs génétiques et comportementaux qui sont à l’origine du syndrome métabolique et des anomalies hépatiques qui l’accompagnent, et les traitements immunosuppresseurs (anticalcineurines, tacrolimus et ciclosporine) connus pour induire diabète, HTA, hyperlipémie et insuffisance rénale, qui font le lit du syndrome métabolique. Le maintien des taux plasmatiques des anticalcineurines le plus bas possible est une priorité dès les premiers jours post-greffe.23
La récidive de l’infiltration graisseuse du greffon a bouleversé le contenu de la consultation de suivi post-transplantation hépatique. Il y a peu de temps très centré sur la gestion de l’immunosuppression (prévention et traitement des rejets, gestion des doses et des taux sanguins d’immunosuppresseurs à un niveau efficace), le suivi d’un greffé du foie est aujourd’hui dominé par la gestion du syndrome métabolique post-greffe et le maintien des doses et des taux sanguins d’immunosuppresseurs à un niveau le moins délétère possible. La consultation de suivi du greffé s’organise aussi autour du conseil diététique, de la surveillance et du traitement du diabète, de l’HTA, de l’insuffisance rénale et de la dyslipidémie. Cette prise en charge fait appel à des compétences multidisciplinaires, et le médecin généraliste référent y tient une place centrale.
MASLD et MASH chez le donneur
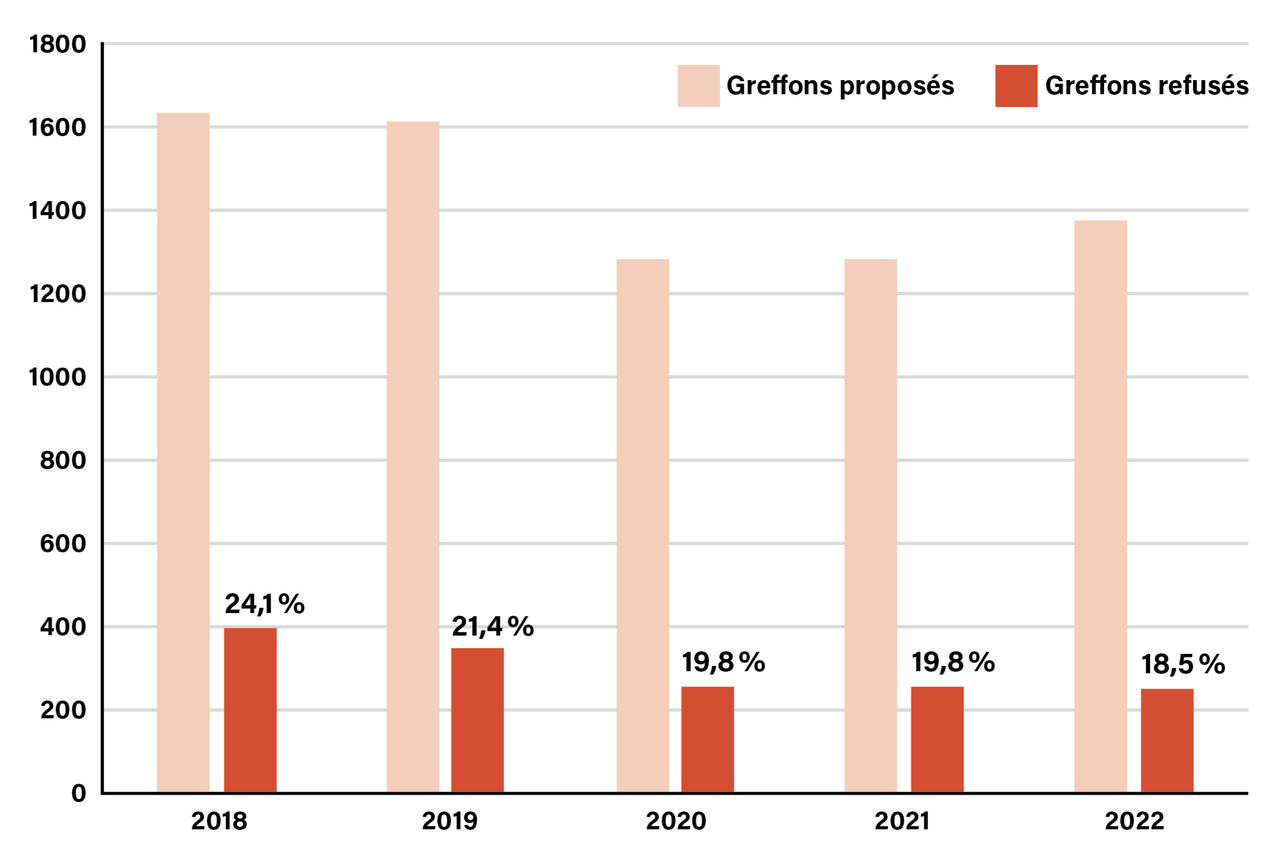
En France, 85 % des greffons hépatiques sont prélevés sur des donneurs en état de mort encéphalique, et près de la moitié de ces donneurs ont 65 ans et plus. Le diabète, l’HTA, la MASLD et finalement la MASH sont fréquents dans cette tranche d’âge et constituent un facteur de risque de dysfonction du greffon après sa revascularisation. Le risque que fait courir au receveur la greffe d’un foie de stéatose ou de stéato-hépatite amène les équipes de greffe à refuser ces greffons ou à ne les accepter que pour être implantés chez des malades qui ne peuvent plus attendre du fait de la gravité de leur situation. En effet, ces foies résistent mal à l’ischémie-reperfusion que leur font subir le prélèvement chez le donneur, la conservation en ischémie et au froid, puis la revascularisation chez le receveur. Ces greffons, lorsqu’ils sont implantés, sont à l’origine d’un tableau d’insuffisance hépatique modérée, subaiguë (early allograft dysfunction [EAD]) et traînante (delayed graft function [DGF]) qui, si elle ne conduit pas au décès en quelques semaines, se manifeste à plus long terme par une incidence croissante de rejets aigus cellulaires ou chroniques, et aboutit à la perte prématurée du greffon et au décès du receveur s’il n’est pas retransplanté. Une analyse réalisée par l’ABM sur la période 2018 - 2022 (données non publiées) montre que 254 greffons hépatiques avaient été refusés par les équipes françaises de transplantationen raison d’un risque estimé trop important de dysfonction postopératoire. L’évolution du taux de greffons refusés pendant cette période est représenté dans la figure 2.
Ne pas prendre le risque de greffer ces foies dits « marginaux » évite celui des complications post-greffe mais aggrave la pénurie d’organes et augmente le risque de décès des malades en attente de greffe. Beaucoup d’équipes de transplantation ont donc orienté leurs travaux de recherche vers la mise au point de procédés de conservation capables de préserver au mieux, voire d’améliorer la qualité de ces foies stéatosiques entre l’instant du prélèvement chez le donneur et celui de la revascularisation chez le receveur. La conservation des foies par perfusion continue du greffon avec une solution synthétique froide (4 °C) et saturée d’oxygène serait ainsi plus performante que la conservation hypothermique statique.24 L’idéal serait de conserver ces foies avec une machine de perfusion au sang et à 37 °C pour se mettre dans des conditions proches de la physiologie et donner la capacité et le temps aux hépatocytes de se vider de leurs vacuoles de graisse (defatting des Anglo-Saxons) à travers la bêta-oxydation des acides gras. Pour cela, il faut du temps, et l’équipe de greffe de Zurich a rapporté l’exploit d’avoir conservé dans une machine de perfusion normothermique un foie humain pendant trois jours pour faire disparaître la stéatose avant de le greffer avec succès.25
Évolution de la prise en charge des candidats à la résection et à la greffe hépatique
MASLD et MASH constituent désormais un paramètre central de l’évolution de la chirurgie hépatique. L’augmentation de leur prévalence transforme progressivement le profil des patients candidats à une résection. L’évaluation préopératoire des candidats à la chirurgie doit désormais intégrer plus finement la quantification de la stéatose, l’évaluation de la fibrose, l’analyse du risque métabolique global pour inciter à mettre en place des stratégies de « réhabilitation » visant à optimiser le parenchyme avant toute exérèse majeure.
En transplantation, la MASH s’impose comme l’une des premières indications de greffe dans de nombreux pays occidentaux. Nul doute qu’elle le sera en France aussi. Cette évolution modifie la sélection des candidats, complexifie la gestion anesthésique et chirurgicale per- et postopératoire, et impose une prise en charge au long cours centrée sur le contrôle du syndrome métabolique, la prévention de la récidive de la MASLD et la gestion des complications cardiovasculaires. La survie du greffon ne peut plus être dissociée de la maîtrise du syndrome métabolique avant la greffe.
Au-delà de la technique, c’est donc un changement de paradigme qui s’esquisse. La chirurgie hépatique et la transplantation devront s’inscrire dans une approche intégrée, associant hépatologues, chirurgiens, cardiologues, nutritionnistes et spécialistes du métabolisme. Se préoccuper du foie dans la prise en charge ne suffira plus. Il faudra surtout s’occuper du terrain, et le médecin référent y aura un rôle essentiel.
2. Meunier L, Larrey D. Chemotherapy-associated steatohepatitis. Ann Hepatol 2020;19(6):597-601.
3. Veteläinen R, van Vliet A, Gouma DJ, et al. Steatosis as a risk factor in liver surgery. Ann Surg 2007;245(1):20-30.
4. Powell EE, Wong VW, Rinella M. Non-alcoholic fatty liver disease. Lancet 2021;397(10290):2212-24.
5. Michelotti GA, Machado M, Diehl AM. NAFLD, NASH and liver cancer. Nat Rev Gastroenterol Hepatol 2023;10(11):656-65.
6. Bunchorntavakul C, Bahirwani R, Drazek D, et al. Clinical features and natural history of hepatocellular adenomas: The impact of obesity. Aliment Pharmacol Ther 2021;34(6):664-74.
7. Geh D, Manas DM, Reeves HL. Hepatocellular carcinoma in non-alcoholic fatty liver disease: A review of an emerging challenge facing clinicians. Hepatobiliary Surg Nutr 2021;10(1):59-75.
8. Chun YS, Laurent A, Maru D, et al. Management of chemotherapy-associated hepatotoxicity in colorectal liver metastases. Lancet Oncol 2009;10(3):278-86.
9. Robinson SM, Wilson CH, Burt AD, et al. Chemotherapy-associated liver injury in patients with colorectal liver metastases: A systematic review and meta-analysis. Ann Surg Oncol 2012;19(13):4287-99.
10. Behrns KE, Tsiotos GG, DeSouza NF, et al. Hepatic steatosis as a potential risk factor for major hepatic resection. J Gastrointest Surg 1998;2(3):292-8.
11. Truant S, Bouras AF, Petrovai G, et al. Volumetric gain of the liver after major hepatectomy in obese patients: A case-matched study in 84 patients. Ann Surg 2013;258:696-702.
12. d’Assignies G, Fayard C, Leitao H, et al. Liver steatosis assessed by preoperative MRI: An independent risk factor for severe complications after major hepatic resection. Surgery 2016;159(4):1050-7.
13. Wu D, van de Graaf SFJ. Maladaptive regeneration and metabolic dysfunction associated steatotic liver disease: Common mechanisms and potential therapeutic targets. Biochem Pharmacol 2024;227:116437.
14. Younossi ZM, Stepanova M, Al Shabeeb R, et al. The changing epidemiology of adult liver transplantation in the United States in 2013-2022: The dominance of metabolic dysfunction-associated steatotic liver disease and alcohol-associated liver disease. Hepatol Commun 2023;8(1):e0352.
15. Delacote C, Favre M, El Amrani M, et al. Morbid obesity increases death and dropout from the liver transplantation waiting list: A prospective cohort study. United European Gastroenterol J 2022;10(4):396-408.
16. Ahmed Z, Ali Khan M, Vazquez-Montesino LM, et al. Bariatric surgery, obesity and liver transplantation. Transl Gastroenterol Hepatol 2022;7:25-35.
17. Lassailly G, Caiazzo R, Buob D, et al. Bariatric surgery reduces features of nonalcoholic steatohepatitis in morbidly obese patients. Gastroenterology 2015;149(2):379-88.
18. Lin MY, Tavakol MM, Sarin A, et al. Laparoscopic sleeve gastrectomy is safe and efficacious for pretransplant candidates. Surg Obes Relat Dis 2013;9(5):653-8.
19. Heimbach JK, Watt KD, Poterucha JJ, et al. Combined liver transplantation and gastric sleeve resection for patients with medically complicated obesity and end-stage liver disease. Am J Transplant 2013;13(2):363-8.
20. Tsamalaidze L, Stauffer JA, Arasi LC, et al. Laparoscopic sleeve gastrectomy for morbid obesity in patients after orthotopic liver transplant: A matched case-control study. Obes Surg 2018;28(2):444-50.
21. Malik SM, deVera ME, Fontes P, et al. Outcome after liver transplantation for NASH cirrhosis. Am J Transplant 2009;9(4):82-93.
22. Villeret F, Dharancy S, Erard D, et al. Inevitability of disease recurrence after liver transplantation for NAFLD cirrhosis. JHEP Rep 2023;5(3):100668.
23. Boudjema K, Camus C, Saliba F, et al. Reduced-dose tacrolimus with mycophenolate mofetil vs. standard-dose tacrolimus in liver transplantation: A randomized study. Am J Transplant 2011;11(5):965-76.
24. Lesurtel M, Mohkam K, Allard MA, et al. A French multicenter randomized controlled trial of hypothermic oxygenated perfusion in extended criteria donor liver transplantation. Am J Transplant 2025;S1600-6135(25)03053-9.
25. Clavien PA, Dutkowski P, Mueller M, et al. Transplantation of a human liver following 3 days of ex situ normothermic preservation. Nat Biotechnol 2022;40(11):1610-16.