Si la carence en B12 est classiquement associée à l’anémie de Biermer, ses causes sont pourtant essentiellement liées à des malabsorptions, pouvant survenir à toutes les étapes de son métabolisme. Les symptômes cliniques peuvent être polymorphes et concernent le système hématologique, neuropsychiatrique et digestif.
Un métabolisme complexe
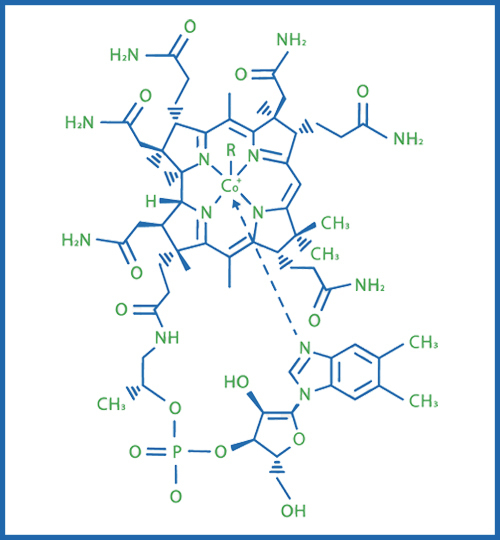
La vitamine B12 ou cobalamine est indispensable à la synthèse de la méthionine et de l’ADN, au développement de la myélinisation et à la fonction du système nerveux.
Cette vitamine est apportée exclusivement par l’alimentation animale (lait, viande…). L’absorption se réalise par deux voies distinctes. La première, par diffusion passive, ne concerne que 1 à 5 % de l’apport alimentaire en B12. La deuxième nécessite la liaison à des transporteurs successifs. La B12 est initialement liée aux protéines alimentaires, puis s’en dissocie sous l’influence de l’acidité gastrique ; elle se lie à des protéines de transport (haptocorrines) qui seront digérées dans le duodénum puis au facteur intrinsèque, ce qui permet son endocytose au niveau de l’iléon terminal. De nouveau libre, la B12 forme ensuite, avec la transcobalamine II, un complexe appelé holotranscobalamine. L’ensemble passe alors dans la circulation sanguine pour assurer le transport de la B12 aux cellules.
Les réserves hépatiques de 1,5 mg et l’existence d’un cycle entérohépatique expliquent le délai de 5 à 10 ans entre l’installation d’un déficit en B12 et l’apparition de manifestations cliniques.
Quand rechercher un déficit ?
Le risque de déficit en B12 est augmenté en cas de régime végétalien strict, de gastrite auto-immune, d’antécédents familiaux de déficit en B12, de pathologies intestinales, d’infections ou chirurgies digestives, en cas de grossesse ou en période néonatale, mais aussi en cas de prise médicamenteuses chronique et de consommation excessive de N2O (protoxyde d'azote, dit aussi « gaz hilarant »). L’âge supérieur à 65 ans est également un facteur de risque.
Les manifestations cliniques sont essentiellement hématologiques, neurologiques et digestives, et ne sont pas spécifiques (tableau 1).
Les troubles hématologiques sont le plus souvent de découverte fortuite devant des anomalies quantitatives de la NFS, comme une macrocytose +/- une anémie. La macrocytose n’est pas toujours présente, notamment en cas de carence en fer associée.
Les troubles neurologiques se manifestent par des paresthésies, une ataxie, une polynévrite, des troubles sensitifs, mais aussi des troubles cognitifs. La supplémentation en folate (vitamine B9) peut augmenter les signes neurologiques d’une carence en B12 car ces deux vitamines sont des co-facteurs de réactions chimiques communes et l’apport de B9 entraîne une diminution des réserves en B12.
Les troubles neurologiques par intoxication au gaz hilarant N2O peuvent entraîner une sclérose combinée de la moelle, de résolution très lente. Les troubles digestifs sont à type de diarrhées, dénutrition, malabsorption.
Devant une personne à risque d’avoir une carence en B12 ou ayant des signes cliniques ou biologiques évocateurs d’une carence, il peut être judicieux de rechercher un déficit fonctionnel de la B12 afin d’instaurer rapidement une supplémentation. Néanmoins, la carence en B12 est parfois difficile à objectiver par des tests de biologie.
Statut vitaminique en B12 : quels marqueurs ?
Il n’existe pas de tests de référence. Si le diagnostic ne pose pas de problème particulier devant une valeur fortement diminuée de B12, on peut toutefois observer d’authentiques carences malgré des dosages normaux, voire avec des valeurs augmentées de B12.
Le dosage de la cobalamine / cyanocobalamine est un reflet du taux total de la vitamine B12 circulant dans le sang, liée aux protéines de transport. Seule la fraction liée à la transcobalamine II (environ 6 à 20 %) est biodisponible et donc biologiquement active. Ce test n’est ni sensible ni spécifique. D’authentiques carences fonctionnelles peuvent être masquées par un taux normal de B12 dans les cas de déficit en transcobalamine ou dans les anomalies constitutionnelles ou acquises du métabolisme cellulaire de cobalamines. Les taux de B12 peuvent être faussement élevés en cas de taux d’haptocorrine diminué (grossesse) ou faussement abaissés en cas d’haptocorrine augmentée (néoplasie myéloproliférative, hépatome).
Le dosage de l’holotranscobalamine (complexe transcobalamine II-B12) quantifie directement la forme « active » biodisponible. Les sensibilités et spécificités sont meilleures que le dosage de la cobalamine. Le taux augmente en cas d’insuffisance rénale. Cependant, ce test est peu utilisé en pratique.
Le taux d’homocystéine (HC) augmente en cas de carence en B12. C’est un marqueur sensible et précoce mais de faible spécificité. En effet, il est augmenté en cas de carence en vitamine B6, B9, d’insuffisance rénale, d’hypothyroïdie, de polymorphisme MTHFR677C > T, de tabagisme actif, de consommation alcoolique ou de café.
Enfin, le taux d’acide méthylmalonique (AMM) augmente quand la disponibilité de la B12 est insuffisante. Il s’agit d’un marqueur très sensible, spécifique dans les valeurs élevées, mais cher et peu diffusé. Le taux diminue dès les premiers jours de supplémentation. À la différence de l’homocystéine, il n’est pas augmenté en cas de déficit carentiel ou fonctionnel en B9. Cependant, il augmente avec l’âge, en cas d’insuffisance rénale même modérée, dans certaines infections bactériennes intestinales et dans certaines maladies héréditaires du métabolisme.
Que faire en pratique pour évaluer le statut en B12 ?
En 1re intention, dosage de la cobalamine :
- 300 pg/mL : pas de carence ;
- < 200 pg/mL : carence très probable.
Ou dosage de l’holotranscobalamine :
- 70 pmol/L : pas de carence ;
- < 25 pmol/L : carence très probable.
Si les valeurs des cobalamines sont comprises entre 200 et 300 pg/mL ou celles de l’holotranscobalamine comprises entre 25 et 70 pmol/L, l’interprétation est plus délicate. L’évaluation du statut de la B12 peut alors être facilitée par la prescription des effecteurs métaboliques que sont l’acide méthylmalonique et l’homocystéine :
- AMM et HC normaux : pas de carence en B12 ;
- AMM et HC augmentés : carence confirmée (reflet du déficit cellulaire). L’AMM est plus spécifique que l’HC, qui peut être élevé pour d’autres raisons, notamment le déficit en folates (sensibilité 94 % et spécificité 99 %).
Principales causes de carence en cobalamines
En pratique, les carences d’apport sont rares tandis que les malabsorptions sont fréquentes et parfois liées à des prises médicamenteuses au long cours. L’usage de gaz hilarant provoque des neuropathies ou une sclérose combinée de la moelle par effet délétère du N2O sur le métabolisme de la B12 (tableau 2).
Les carences d’apport sont liées à un régime végétalien ou très pauvre en produits laitiers et viande. La carence d’apport est à rechercher également chez les nourrissons allaités (mère carencée, allaitement > 4 mois) afin de prévenir les conséquences sur la croissance, les complications neurologiques et le risque de déficit intellectuel.
Les défauts d’absorption sont plus fréquents (gastrectomies, résections iléales, chirurgie bariatrique, bypass gastrique).
La classique anémie de Biermer doit être recherchée et les anticorps anti-facteur intrinsèque (présents dans 70 % des cas, bonne spécificité) et anticorps anti-cellules pariétales (présents dans 80 % des cas, mais mauvaise spécificité) doivent être prescrits.
Hypervitaminémie B12
Les hypervitaminémies B12 sont fréquentes, souvent de découverte fortuite lors d’un bilan vitaminique. Il peut s’agir d’un excès d’apport essentiellement par voie parentérale ou d’une augmentation des concentrations sériques d’haptocorrine ou de transcobalamine, soit par excès de production ou de libération tissulaire de ces transporteurs – hémopathies (leucémie myéloïde chronique, maladie de Vaquez, myélofibrose primitive, syndrome hyperéosinophilique primitif, leucémie aiguë), néoplasies, hépatopathies, maladies auto-immunes ou inflammatoires –, soit par défaut de clairance (insuffisance rénale). Paradoxalement, une carence cellulaire en B12 peut exister même en présence de concentrations sériques élevées.
En raison des pathologies graves auxquelles elle peut être associée, une hypervitaminémie B12 peut motiver une recherche étiologique en fonction du contexte général du patient.
Andrès E, Vogel T, Kaltenbach G, et al. Malabsorption des cobalamines alimentaires et carence en vitamine B12 chez l’adulte et chez le sujet âgé : quel est le problème ? Rev Med Intern 2016;37(8):511-3.
Wolffenbuttel BH, Owen PJ, Ward M, et al. Vitamin B12. BMJ 2023:383:e071725.
Harrington DJ, Stevenson E, Sobczyńska-Malefora A. The application and interpretation of laboratory biomarkers for the evaluation of vitamin B12 status. Ann Clin Biochem 2025;62(1):22-33.
Nexo E, Parkner T. Vitamin B12-Related Biomarkers. Food Nutr Bull 2024;45(1_suppl):S28-33.