L’hypertension artérielle (HTA) est la maladie chronique la plus fréquente en France avec 17 millions de personnes touchées, dont plus de 6 millions qui l’ignorent. Un patient sur deux est traité par un ou des médicaments antihypertenseurs appartenant majoritairement à 5 grandes classes pharmacologiques : inhibiteurs de l’enzyme de conversion (IEC), antagonistes des récepteurs de l’angiotensine II (ARA2, ou sartans), bêtabloquants, inhibiteurs des canaux calciques (ICC), diurétiques.
Pourtant, environ 5 à 30 % des patients hypertendusont une HTA qui, en apparence, est résistante à un traitement conventionnel. Si plusieurs facteurs peuvent causer une HTA pseudo-résistante (inertie médicale, HTA « blouse blanche », inobservance thérapeutique), la physiopathologie complexe et multifactorielle de l’HTA ne permet pas aux classes médicamenteuses classiques (même combinées) de traiter tous les cas de figure, notamment en présence de diabète ou de MRC.
Face aux angles morts des médicaments actuels, de nouvelles approches thérapeutiques ont vu le jour et ont bien progressé dans leur développement clinique ces 10 dernières années.
Une équipe internationale de six experts de l’HTA (5 cardiologues et 1 néphrologue) a réalisé une revue de la littérature brossant un panorama de ces potentielles nouvelles options dans l’HTA (résumées dans le tableau ci-contre, avec leurs baisses de pression artérielle approximatives dans les essais randomisés vs placebo). Elle est parue le 7 mars 2026 dans le Lancet.
Revisiter l’inhibition du système rénine-angiotensine-aldostérone
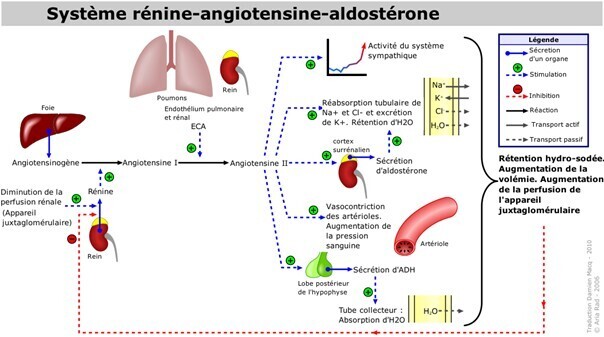
Tout comme les IEC et les sartans, certains candidats médicaments visent le système rénine-angiotensine-aldostérone (SRAA), un système de régulation hormonal qui maintient l’homéostasie hydrosodée en déterminant la volémie (ou hydratation extracellulaire) au niveau rénal via la modulation de la réabsorption de sodium, entraînant une vasoconstriction des vaisseaux sanguins, notamment par la sécrétion d’angiotensine 2. Dans la cascade enzymatique du SRAA (figure), les IEC inhibent l’enzyme de conversion, catalysant la réaction synthétisant l’angiotensine 2 à partir de l’angiotensine 1, tandis que les sartans sont des antagonistes des récepteurs de l’angiotensine 2.
Deux grandes options à l’étude ciblent le SRAA de manière novatrice :
- les thérapies à base d’ARN, représentées aujourd’hui par le zilébésiran, un petit ARN interférent (siRNA) en cours d’évaluation en phase 3 dans l’HTA non contrôlée avec haut risque CV (étude Zenith). Injecté par voie sous-cutanée, il est séquestré dans les endosomes tardifs hépatiques d’où il se relâche lentement dans le cytoplasme. Une administration est efficace au moins 6 mois, ce qui en fait une option très attendue pour améliorer l’observance, problème majeur dans le traitement de l’HTA. Dans le cytoplasme, le zilébésiran s’apparie à l’ARNm de l’angiotensinogène et entraîne sa dégradation, supprimant ainsi la production de cette protéine, seul substrat du SRAA ;
- les thérapies ciblant le système des peptides natriurétiques (peptide atrial natriurétique [ANP] et peptide natriurétique de type B [BNP]). Ces peptides, via la signalisation guanosine monophosphate cyclique (GMPc), baissent la volémie et inhibent la sécrétion de rénine, diminuant l’activité du SRAA. Ils ont une courte demi-vie physiologique (quelques minutes dans la circulation sanguine), étant rapidement éliminés par des enzymes comme la néprilysine. Cette stratégie thérapeutique regroupe :
- des inhibiteurs de la néprilysine (sacubritil, en combinaison avec le valsartan ; commercialisé en France dans l’insuffisance cardiaque ; revues systématiques dans l’HTA résistante ou dans l’HTA vs olmésartan) ;
- des activateurs directs du système des peptides natriurétiques (analogues de l’ANP, en phase précoce de développement clinique [deuxétudes de preuve de concept dans l’HTA chez l’homme]).
Bloquer la synthèse ou l’action de l’aldostérone
L’aldostérone est une hormone corticosurrénale qui peut provenir de différentes voies de synthèse (dont une activée par l’angiotensine 2). Elle agit sur la pression artérielle par sa liaison au récepteur des minéralocorticoïdes, qui lui permet de réguler la balance hydrosodée d’une manière similaire au SRAA, en modulant la réabsorption de sodium.
L’aldostérone contribue ainsi à la vasoconstriction, et son inhibition fait déjà l’objet en France d’une quatrième ligne de traitement de l’HTA résistante sous trithérapie initiale, par la spironolactone. Cette dernière est un antagoniste du récepteur des minéralocorticoïdes (ARM) stéroïdien ; les ARM, stéroïdiens ou non stéroïdiens, sont des diurétiques épargneurs de potassium.
Cependant, la spironolactone a des effets indésirables dose-dépendants – gynécomastie, mastodynies, troubles des règles chez la femme et dysfonction érectile chez l’homme –, et son utilisation nécessite une surveillance de la kaliémie et de la créatininémie. Par ailleurs, les patients doivent avoir un DFG ≥ 45 mL/min/1,73 m² et une kaliémie ≤ 4,5 mmol/L.
Face à ces limites, et alors que les scientifiques considèrent de plus en plus que de nombreux patients hypertendus présentent une dérégulation de l’aldostérone (surproduction d’aldostérone indépendante de la rénine), les spécialistes soulignent le besoin de mieux cibler les récepteurs des minéralocorticoïdes tout en améliorant la tolérance à ces médicaments.
Dans ce contexte, deux classes médicamenteuses prometteuses émergent pour l’HTA, utilisables en combinaison avec les gliflozines en cas de (risque de) MRC ou d’insuffisance cardiaque :
- les inhibiteurs de l’aldostérone synthase (IAS) de 2e génération : ils pourraient limiter l’échappement de l’aldostérone, c’est-à-dire son augmentation après mise sous IEC ou sartans, témoignant d’une sécrétion par d’autres voies que le SRAA. Déjà étudiés en phase 3, baxdrostat (étude BaxHTN) et lorundrostat (étude Launch-HTN) sont les plus proches de la clinique : le 1er est en cours d’évaluation dans l’HTA depuis peu par l’EMA et la FDA, tandis que le 2nd est évalué par la FDA. Une nouvelle étude de phase 3 positive sur le baxdrostat dans l’HTA résistante, Bax24, vient de paraître dans le même numéro de Lancet que la revue actuelle ;
- les ARM non stéroïdiens, qui ont une structure chimiques différente des ARM stéroïdiens et sont plus sélectifs et antagonistes des récepteurs des minéralocorticoïdes. Parmi eux, la finérénone bénéficie d’études de phase 3 et est approuvée par l’EMA, mais dans la MRC avec diabète de type 2 (non commercialisée en France). Seule, elle diminue modérément l’HTA (2 - 5 mmHg pour 10 - 20 mg/jour), moins que la spironolactone par exemple. Elle est en cours d’étude avec des gliflozines, une combinaison qui diminue davantage la pression artérielle que chaque médicament isolé.
Cibler l’endothéline- 1
Enfin, les derniers médicaments à l’étude sont les antagonistes des récepteurs de l’endothéline- 1, un des plus puissants vasoconstricteurs produits par l’endothélium vasculaire. Ce neuropeptide exerce ses effets vasoconstricteurs par le biais de deux récepteurs couplés aux protéines G, ET-A et ET-B. Antagoniste des 2 types de récepteurs, l’aprocitentan a été étudié en phase 3 et est approuvé par la FDA et l’EMA dans l’HTA résistante, mais reste non commercialisé en France.
Azizi M, Brown JM, Dwyer JP, et al. Effect of baxdrostat on ambulatory blood pressure in patients with resistant hypertension (Bax24): A phase 3, randomised, double-blind, placebo-controlled trial. Lancet 2026;407(10532):988-99.
Pour aller plus loin :
Nobile C. HTA : recos européennes 2024. Rev Prat (en ligne) 19 septembre 2024.
Mion B, Malka N, Kantor B, et al. Hypertension artérielle : quels seuils et cibles tensionnels ? Rev Prat Med Gen 2024;38(1083);37-40.
Pariente B, Lorthioir A. Hypertension artérielle résistante. Rev Prat Med Gen 2023;37(1075):117-22.
De Fréminville JB, Lorthioir A, Cornu E, et al. Item 330. Prescription et surveillance des classes de médicaments les plus courantes chez l’adulte et chez l’enfant, hors anti-infectieux (voir item 177). Connaître le bon usage des principales classes thérapeutiques – Partie 2 : Antihypertenseurs. Rev Prat 2021;71(3):e75-81.
Mallordy F. HTA : une méta-analyse compare les traitements et propose un simulateur. Rev Prat (en ligne) 4 septembre 2025.
HAS. Recommandation de bonne pratique. Prise en charge de l’hypertension artérielle de l’adulte. 27 octobre 2016.
Fron JB. Hypertension artérielle (HTA). Recomedicales.fr 28 juin 2024.