Un patient âgé de 60 ans, suivi pour une hémophilie de type A, est adressé en service de rhumatologie pour une douleur mécanique chronique des genoux et des chevilles évoluant depuis l’enfance, traitée par anti-inflammatoires non stéroïdiens, notamment des inhibiteurs sélectifs de la COX-2. À l’interrogatoire, le patient rapporte des épisodes de gonflement articulaire des deux genoux et des deux chevilles depuis l’enfance. Il n’a jamais reçu de facteur de coagulation déficitaire, faute de moyens.
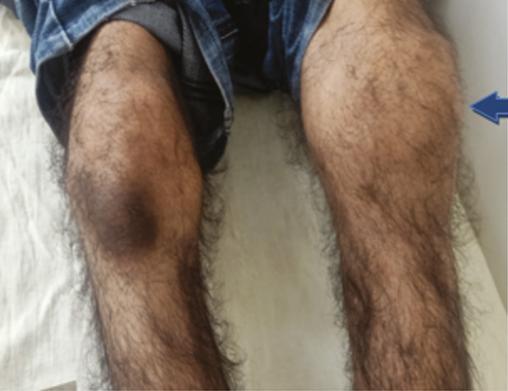
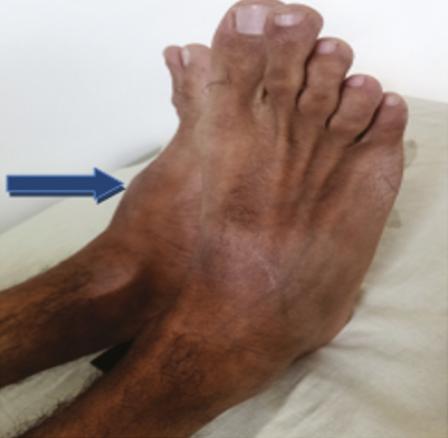
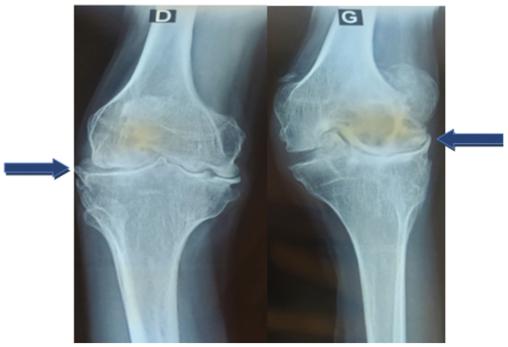
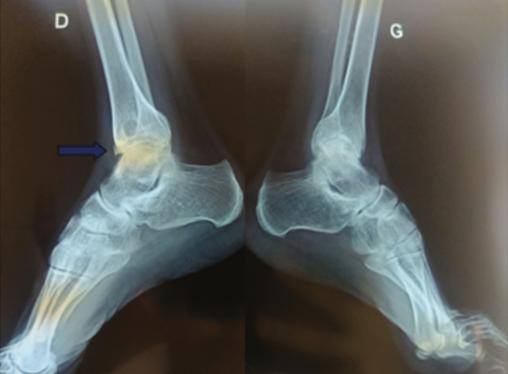
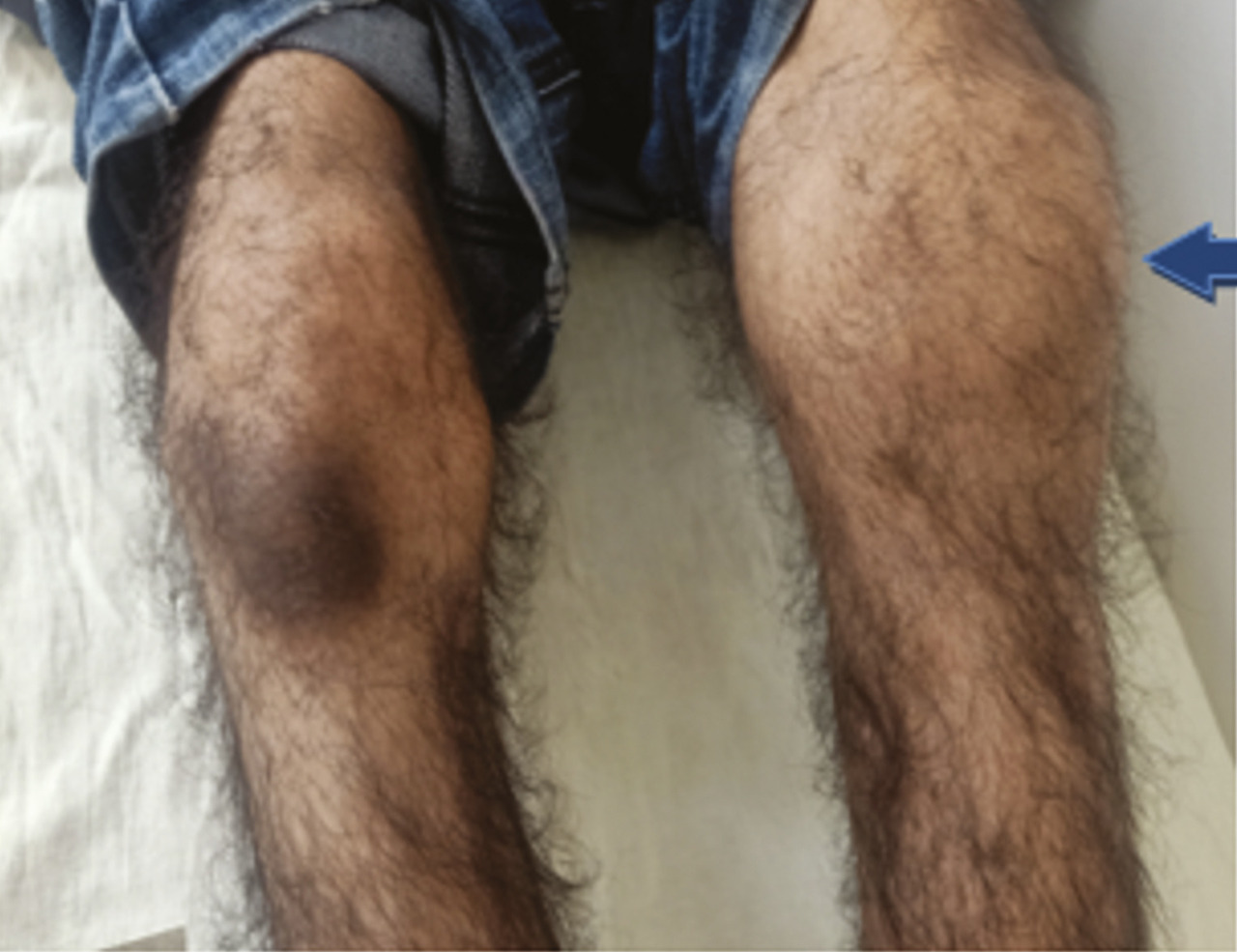
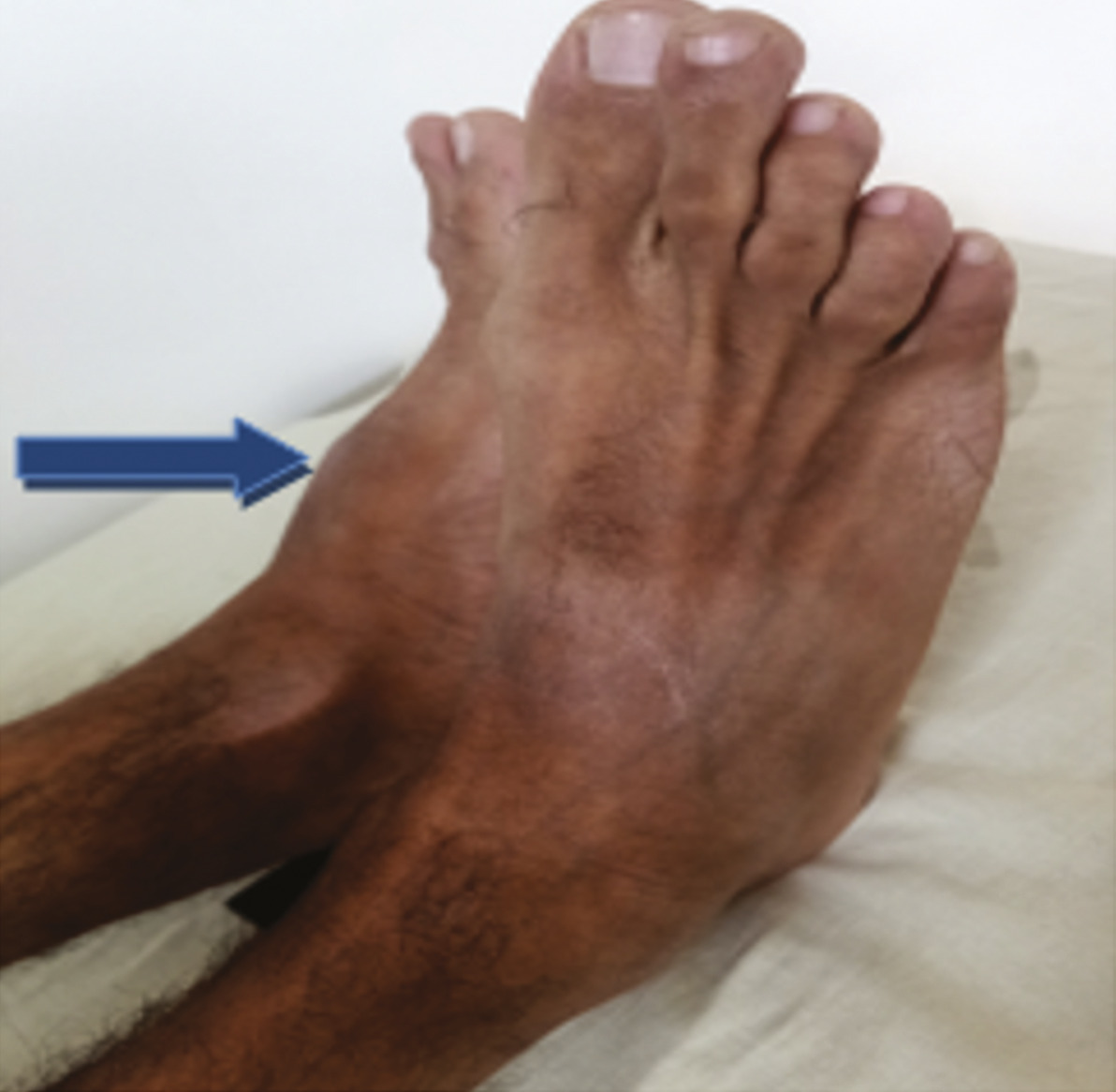
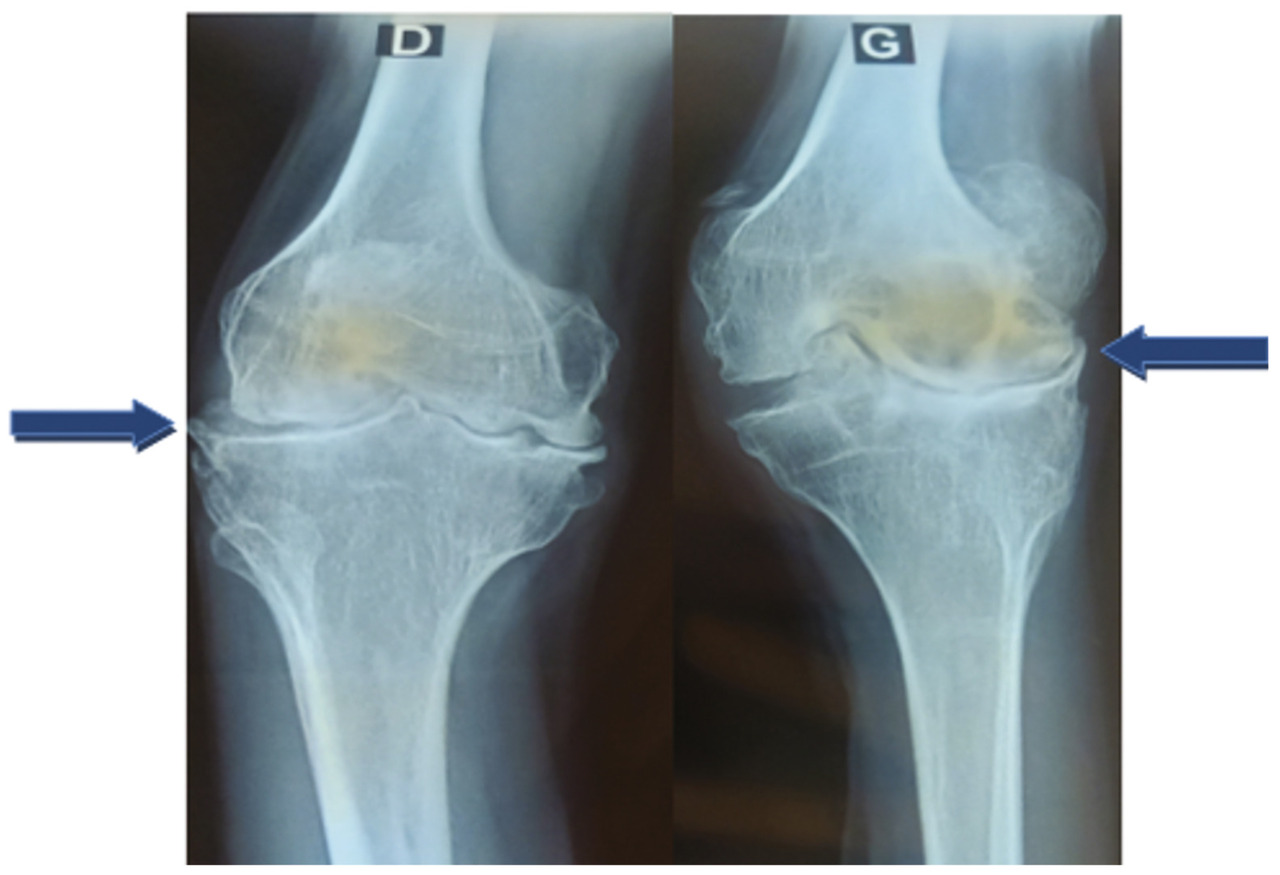
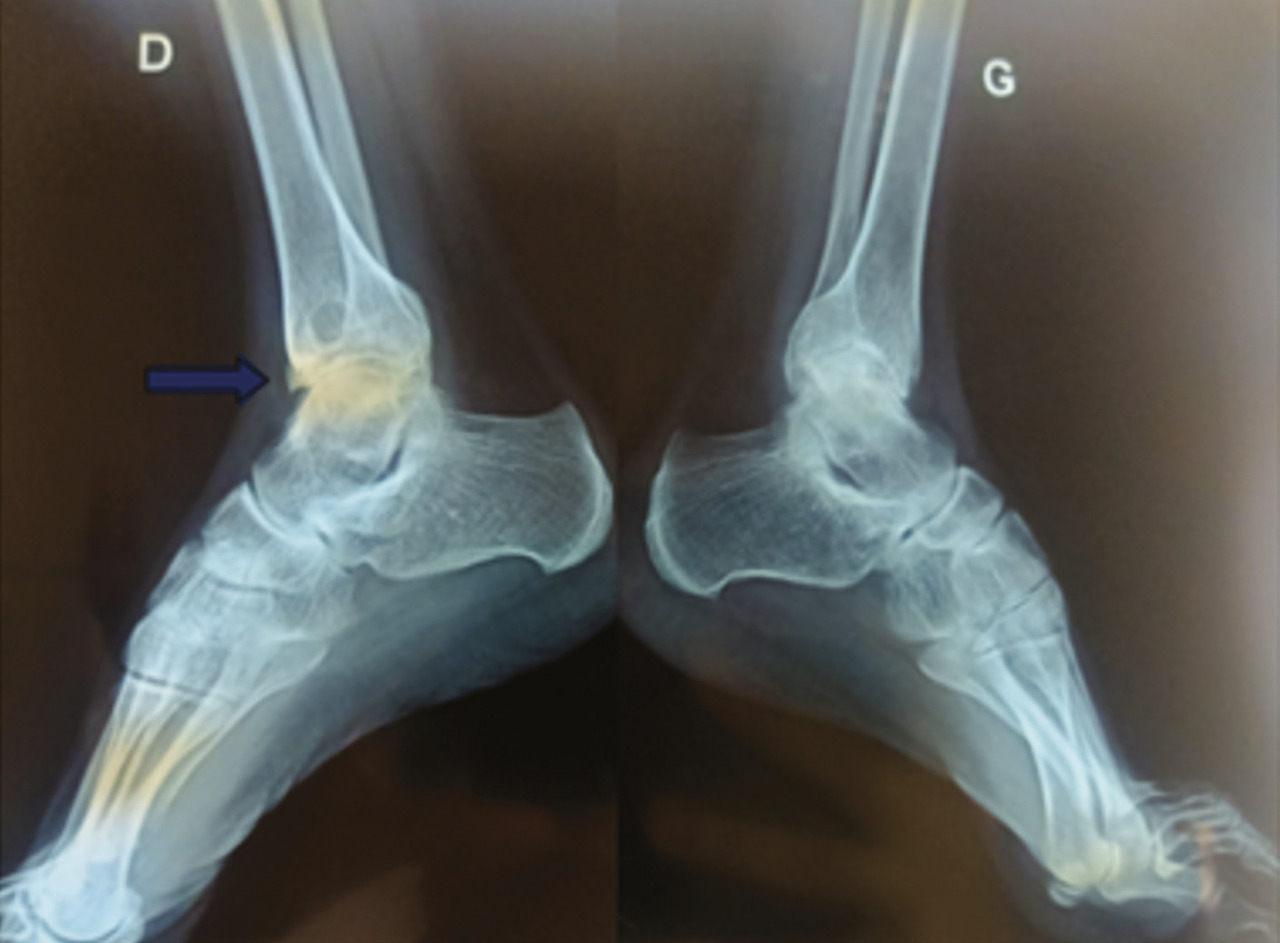
L’examen physique retrouve une hypertrophie articulaire du genou gauche avec un flessum irréductible des deux genoux, plus marqué à gauche, une atrophie du quadriceps et des muscles du mollet, une déformation avec perte de la dorsiflexion et de la flexion plantaire des chevilles (fig. 1 et 2 ). La protéine C-réactive est normale. Les radiographies des deux genoux et des deux chevilles révèlent respectivement une destruction articulaire et un ostéophyte de la partie antérieure de l’articulation talocrurale (fig. 3 et 4 ).
Le diagnostic d’arthropathie hémophilique est retenu sur un faisceau d’arguments associant les signes cliniques, les anomalies à l’imagerie et l’antécédent d’hémophilie A. Le patient a reçu un traitement antalgique associé à une rééducation fonctionnelle et la mise en place d’une prothèse totale des deux genoux a été programmée. Le traitement substitutif par des concentrés de facteur de coagulation déficitaire a été prescrit.
L’examen physique retrouve une hypertrophie articulaire du genou gauche avec un flessum irréductible des deux genoux, plus marqué à gauche, une atrophie du quadriceps et des muscles du mollet, une déformation avec perte de la dorsiflexion et de la flexion plantaire des chevilles (
Le diagnostic d’arthropathie hémophilique est retenu sur un faisceau d’arguments associant les signes cliniques, les anomalies à l’imagerie et l’antécédent d’hémophilie A. Le patient a reçu un traitement antalgique associé à une rééducation fonctionnelle et la mise en place d’une prothèse totale des deux genoux a été programmée. Le traitement substitutif par des concentrés de facteur de coagulation déficitaire a été prescrit.
L’arthropathie hémophilique (AH) est la complication la plus fréquente de l’hémophilie. Elle résulte de la répétition d’un certain nombre d’hémarthroses touchant une articulation dite « cible », responsables d’une impotence fonctionnelle hyperalgique aiguë et de ses complications arthropathiques, allant de l’atteinte inflammatoire isolée de la synoviale, synovite subaiguë ou chronique éventuellement réversible, à la détérioration progressive irréversible du cartilage et de l’os périarticulaire.1 Elle est caractérisée par une hypertrophie des épiphyses, une diminution de l’amplitude articulaire, des rétractions musculo-tendineuses, une amyotrophie et la raréfaction des hémarthroses. Il s’agit d’une conséquence des épisodes d’hémarthroses à répétition au niveau des articulations concernant principalement les genoux, les chevilles et les coudes mais également d’autres articulations comme les épaules, les hanches ou les mains.2
Il existe des similitudes au niveau physiopathologique entre l’AH, l’arthrose et la polyarthrite rhumatoïde.
L’hémophilie est une maladie génétique récessive liée au chromosome X causée par un déficit en facteur VIII (hémophilie A) ou IX (hémophilie B).3 L’AH est l’une des manifestations les plus courantes et les plus typiques au cours des épisodes hémorragiques récurrents chez les patients hémophiles ; elle est la première cause de morbidité chez les patients hémophiles sévères.4
L’AH se traduit cliniquement par une perte de l’amplitude des mouvements, une déformation de l’angle de l’articulation, une amyotrophie et l’apparition de contractures des tissus entourant l’articulation, une gêne dans les activités physiques et sociales et une douleur qui peut devenir extrême lors des mouvements.5
La radiographie standard reste l’examen de base pour rechercher des signes témoignant d’une hémarthrose et/ou d’une arthropathie hémophilique (tuméfaction synoviale, raréfaction osseuse périarticulaire, hypertrophie épiphysaire, pincement articulaire diffus, érosions marginales bien limitées, érosions et géodes centrales, stries d’arrêt de croissance, troubles de la croissance des os et déformations).6
L’intérêt principal de l’échographie est de différencier l’épanchement liquidien, l’hypertrophie et l’hyperhémie synoviale – ce qui peut orienter la prise en charge thérapeutique – et objectiver des anomalies cartilagineuses, des érosions osseuses marginales et des ostéophytes.7
L’imagerie par résonance magnétique (IRM) articulaire est l’examen de choix dans l’exploration de l’AH.6 Elle visualise précocement l’hypertrophie synoviale, les dépôts d’hémosidérine, les atteintes du cartilage, les hémarthroses et les épanchements.8 Elle permet également d’orienter l’orthopédiste en cas de traitement chirurgical de l’arthropathie.
La prise en charge de l’AH a pour objectif de diminuer le nombre d’épisodes de saignements articulaires et de traiter les lésions constituées.
Une hémarthrose aiguë est traitée de manière symptomatique selon le protocole RICE (rest, ice, compression, elevation) classique (immobilisation de courte durée, antalgiques, compression, glaçage, élévation) et surtout étiologique, par l’administration de facteurs de coagulation déficitaires le plus rapidement possible pour arrêter le saignement. Si la douleur n’est pas contrôlée, une ponction évacuatrice peut être proposée.9
Le traitement prophylactique consiste à injecter de façon régulière le facteur antihémophilique en l’absence même d’incident hémorragique. L’administration systématique de facteurs de coagulation au long cours avant l’âge de 2 ans, après le premier saignement, diminue le risque de destruction articulaire et réduit le nombre d’hémarthroses et d’hémorragies.10 Le traitement de la douleur de l’AH repose sur les antalgiques classiques de palier 1 à 3, permettant de soulager les douleurs mécaniques de l’arthropathie. La corticothérapie et les bisphophonates pourraient être intéressants dans certains cas.2
La rééducation par kinésithérapie a toute sa place dans la prise en charge de ces patients, elle permet d’accélérer la récupération fonctionnelle tout en prévenant les complications, améliorant ainsi la qualité de vie. Parfois, l’atteinte articulaire peut nécessiter la pose d’appareil orthopédique et d’orthèse pour soutenir l’articulation douloureuse.
La chirurgie peut être indiquée soit au stade de début (synoviorthèse, synovectomie), soit au stade d’arthropathie évoluée (ostéotomie de réaxation du membre inférieur, prothèse totale surtout de la hanche ou du genou, arthrodèse essentiellement de la cheville).11
Le suivi des patients est multidisciplinaire, nécessitant une collaboration étroite avec les hôpitaux de proximité et les médecins traitants. L’évaluation de l’état articulaire, son évolution, l’impact sur la qualité de vie font partie intégrante de la consultation d’hémophilie.
Il existe des similitudes au niveau physiopathologique entre l’AH, l’arthrose et la polyarthrite rhumatoïde.
L’hémophilie est une maladie génétique récessive liée au chromosome X causée par un déficit en facteur VIII (hémophilie A) ou IX (hémophilie B).3 L’AH est l’une des manifestations les plus courantes et les plus typiques au cours des épisodes hémorragiques récurrents chez les patients hémophiles ; elle est la première cause de morbidité chez les patients hémophiles sévères.4
L’AH se traduit cliniquement par une perte de l’amplitude des mouvements, une déformation de l’angle de l’articulation, une amyotrophie et l’apparition de contractures des tissus entourant l’articulation, une gêne dans les activités physiques et sociales et une douleur qui peut devenir extrême lors des mouvements.5
La radiographie standard reste l’examen de base pour rechercher des signes témoignant d’une hémarthrose et/ou d’une arthropathie hémophilique (tuméfaction synoviale, raréfaction osseuse périarticulaire, hypertrophie épiphysaire, pincement articulaire diffus, érosions marginales bien limitées, érosions et géodes centrales, stries d’arrêt de croissance, troubles de la croissance des os et déformations).6
L’intérêt principal de l’échographie est de différencier l’épanchement liquidien, l’hypertrophie et l’hyperhémie synoviale – ce qui peut orienter la prise en charge thérapeutique – et objectiver des anomalies cartilagineuses, des érosions osseuses marginales et des ostéophytes.7
L’imagerie par résonance magnétique (IRM) articulaire est l’examen de choix dans l’exploration de l’AH.6 Elle visualise précocement l’hypertrophie synoviale, les dépôts d’hémosidérine, les atteintes du cartilage, les hémarthroses et les épanchements.8 Elle permet également d’orienter l’orthopédiste en cas de traitement chirurgical de l’arthropathie.
La prise en charge de l’AH a pour objectif de diminuer le nombre d’épisodes de saignements articulaires et de traiter les lésions constituées.
Une hémarthrose aiguë est traitée de manière symptomatique selon le protocole RICE (rest, ice, compression, elevation) classique (immobilisation de courte durée, antalgiques, compression, glaçage, élévation) et surtout étiologique, par l’administration de facteurs de coagulation déficitaires le plus rapidement possible pour arrêter le saignement. Si la douleur n’est pas contrôlée, une ponction évacuatrice peut être proposée.9
Le traitement prophylactique consiste à injecter de façon régulière le facteur antihémophilique en l’absence même d’incident hémorragique. L’administration systématique de facteurs de coagulation au long cours avant l’âge de 2 ans, après le premier saignement, diminue le risque de destruction articulaire et réduit le nombre d’hémarthroses et d’hémorragies.10 Le traitement de la douleur de l’AH repose sur les antalgiques classiques de palier 1 à 3, permettant de soulager les douleurs mécaniques de l’arthropathie. La corticothérapie et les bisphophonates pourraient être intéressants dans certains cas.2
La rééducation par kinésithérapie a toute sa place dans la prise en charge de ces patients, elle permet d’accélérer la récupération fonctionnelle tout en prévenant les complications, améliorant ainsi la qualité de vie. Parfois, l’atteinte articulaire peut nécessiter la pose d’appareil orthopédique et d’orthèse pour soutenir l’articulation douloureuse.
La chirurgie peut être indiquée soit au stade de début (synoviorthèse, synovectomie), soit au stade d’arthropathie évoluée (ostéotomie de réaxation du membre inférieur, prothèse totale surtout de la hanche ou du genou, arthrodèse essentiellement de la cheville).11
Le suivi des patients est multidisciplinaire, nécessitant une collaboration étroite avec les hôpitaux de proximité et les médecins traitants. L’évaluation de l’état articulaire, son évolution, l’impact sur la qualité de vie font partie intégrante de la consultation d’hémophilie.
Références
1. Leroy M, Albert JD, Guillet B. Atteintes ostéoarticulaires dans l’hémophilie. EMC Appareil locomoteur, 14 août 2017.
2. Frenzel L. L’arthropathie hémophilique en 2015 : doit-on être résigné ou optimiste ? Horizons Hemato 2015;5(2):115-6.
3. Acharya SS. Exploration of the pathogenesis of haemophilic joint arthropathy: Understanding implications for optimal clinical management. Br J Haematol 2012;156:13-23.
4. Bossard D. Management of haemophilic arthropathy. Haemophilia 2008;14(suppl4):11-9.
5. Srivastava A, Santagostino E, Dougall A, Kitchen S, Sutherland M, Pipe SW, et al. WFH Guidelines for the management of hemophilia, 3rd edition. Haemophilia 2020;26(Suppl 6):1-158.
6. Cockenpot E, Pansini V, Cepparo JM, Lefebvre G, Balbi V, Cotton A, et al. Lésions musculosquelettiques dans l’hémophilie. EMC Radiologie, 16 janvier 2012.
7. Yu W. Comparison of radiography. CT and MR imaging in detection of arthropathies in patients with haemophilia. Haemophilia 2009;15:1090-6.
8. Cockenpot E, Boutry N, Cotton A. EMC Hémophilie, 9 juillet 2013.
9. Robertson JD. Acute haemarthrosis of the hip joint: Rapid convalescence following ultrasound-guided needle aspiration. Haemophilia 2009;15:390-3.
10. Manco-Johnson MJ. Prophylaxis versus episodic treatment to prevent joint disease in boys with severe hemophilia. N Engl J Med 2007;357:535-44.
11. Alcalay M, Durand G. Manifestations musculaires, articulaires et osseuses de l’hémophilie. EMC Appareil locomoteur 2008;3(1):1‑15.
2. Frenzel L. L’arthropathie hémophilique en 2015 : doit-on être résigné ou optimiste ? Horizons Hemato 2015;5(2):115-6.
3. Acharya SS. Exploration of the pathogenesis of haemophilic joint arthropathy: Understanding implications for optimal clinical management. Br J Haematol 2012;156:13-23.
4. Bossard D. Management of haemophilic arthropathy. Haemophilia 2008;14(suppl4):11-9.
5. Srivastava A, Santagostino E, Dougall A, Kitchen S, Sutherland M, Pipe SW, et al. WFH Guidelines for the management of hemophilia, 3rd edition. Haemophilia 2020;26(Suppl 6):1-158.
6. Cockenpot E, Pansini V, Cepparo JM, Lefebvre G, Balbi V, Cotton A, et al. Lésions musculosquelettiques dans l’hémophilie. EMC Radiologie, 16 janvier 2012.
7. Yu W. Comparison of radiography. CT and MR imaging in detection of arthropathies in patients with haemophilia. Haemophilia 2009;15:1090-6.
8. Cockenpot E, Boutry N, Cotton A. EMC Hémophilie, 9 juillet 2013.
9. Robertson JD. Acute haemarthrosis of the hip joint: Rapid convalescence following ultrasound-guided needle aspiration. Haemophilia 2009;15:390-3.
10. Manco-Johnson MJ. Prophylaxis versus episodic treatment to prevent joint disease in boys with severe hemophilia. N Engl J Med 2007;357:535-44.
11. Alcalay M, Durand G. Manifestations musculaires, articulaires et osseuses de l’hémophilie. EMC Appareil locomoteur 2008;3(1):1‑15.
Une question, un commentaire ?