Les pancréatites dites génétiques sont une cause rare de pancréatite chronique (1 %). La notion de pancréatite « héréditaire » date de 1952, quand, pour la première fois, Comfort et Steinberg rapportaient des cas de pancréatites familiales sans autre facteur de risque trouvé.1 En 1996, le rôle du gène de prédisposition PRSS1 (et de ses mutations) codant pour le trypsinogène cationique était mis en évidence.2 Parmi les pancréatites génétiques, on distingue la pancréatite héréditaire dont le diagnostic repose sur un critère génétique, la mise en évidence d’une mutation du gène PRSS1 ou sur un critère généalogique, avec la présence d’une pancréatite chronique chez au moins deux apparentés au premier degré ou au moins trois apparentés au deuxième degré, en l’absence d’autres facteurs de prédisposition identifiés. Aujourd’hui, le concept de susceptibilité génétique est supposé chez certains patients qui développent une pancréatite chronique à la suite de l’exposition à des facteurs tels que l’alcool ou le tabac. En effet, moins de 5 % des personnes alcooliques chroniques développent une pancréatopathie chronique au cours de leur vie.
Principales atteintes génétiques et caractéristiques
Gène PRSS1 : gène du trypsinogène cationique
Premier gène identifié, le gène PRSS1 localisé sur le chromosome 7q35 code pour le trypsinogène cationique. Sa mutation entraîne une activation inappropriée de la trypsine au niveau pancréatique (gain de fonction) plutôt que duodénal. Celle-ci est responsable d’une activation de la cascade enzymatique au niveau acinaire et d’une inflammation secondaire. Aujourd’hui, plus de 100 variants de PRSS1 sont identifiés. Parmi eux, 26 sont considérés comme « pathogènes », 51 comme « bénins », les autres sont de répercussion indéterminée.3 La transmission est autosomique dominante. La pénétrance estimée du gène PRSS1 est estimée à plus de 80 %. La prévalence des mutations de la pancréatite héréditaire liée à PRSS1 est de 1/300 000 ; elle reste donc une maladie très rare.
Gène SPINK1 : gène de l’inhibiteur du trypsinogène cationique
Le gène SPINK1, situé sur le chromosome 5q33, code pour une protéine de 56 acides aminés qui inhibe l’action du trypsinogène au niveau acinaire en bloquant son site actif en intracellulaire. La prévalence d’une mutation hétérozygote de SPINK1 est de 1 à 2 % dans la population générale. Moins de 1 % des sujets ayant une mutation hétérozygote développent une pancréatite chronique.4 En effet, l’altération de SPINK1 n’est pas responsable à elle seule de la pancréatite, mais est un facteur favorisant en présence de cofacteurs environnementaux (alcool, tabac, cannabis...) et/ou génétiques (notamment CFTR, CTRC, PRSS1, TRPV6...).
Gène CFTR : gène codant pour les canaux chlore des cellules canalaires
Les mutations du gène CFTR, situé sur le chromosome 7, sont impliquées dans la survenue de la mucoviscidose (porteurs de deux mutations sévères), mais également dans des formes atténuées (porteurs d’une ou deux mutations peu sévères). Ce gène code pour un canal chlore du pôle apical des cellules canalaires ; les mutations provoquent une dysfonction (partielle ou totale) et donc un défaut de sécrétion ductulaire en eau et en ions bicarbonates aboutissant à une précipitation protéique et à une obstruction canalaire, à l’origine de pancréatite. Près de 1 900 mutations du gène CFTR sont connues. La prévalence dans la population générale est de 4 %, c’est-à-dire que 1 personne sur 25 en population générale est porteuse hétérozygote. Seules les mutations les plus sévères exposent à un surrisque de pancréatite en présence de cofacteurs environnementaux.
Autres systèmes géniques impliqués
D’autres systèmes géniques complexes font partie du panel testé actuellement pour explorer une pancréatopathie chronique dite de cause indéterminée. Il s’agit des mutations des gènes CTRC, CaSR, CPA1, TRPV6, PNLIP et CEL-HYB.5
Indications des tests génétiques
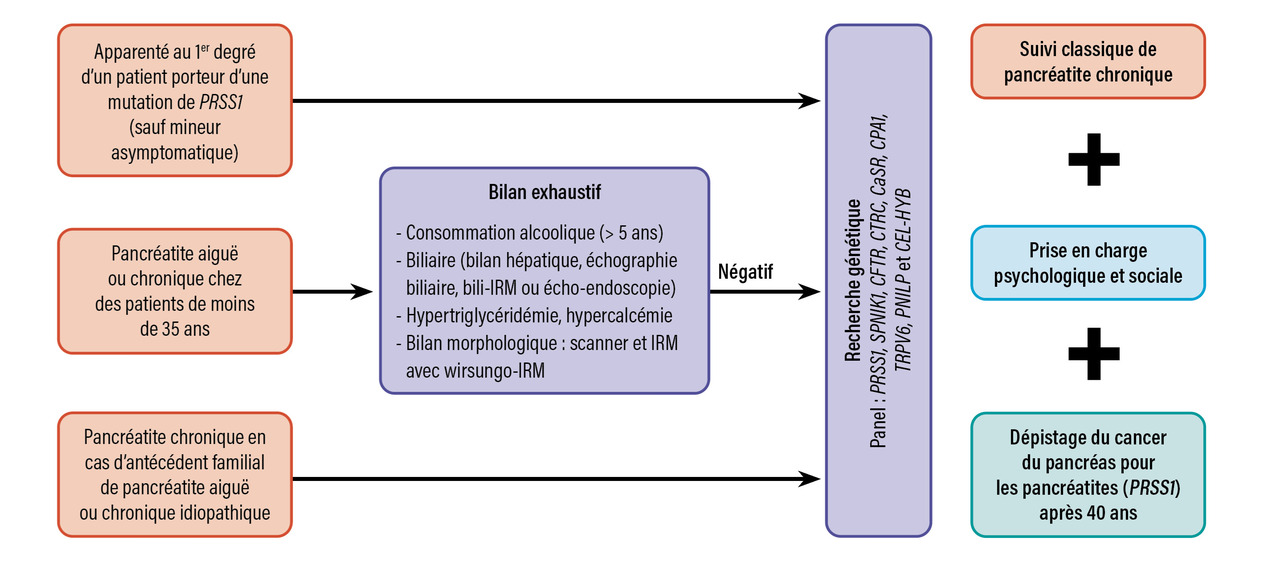
Une origine génétique de la pancréatite doit être évoquée dans les cas suivants (figure) :6
- pancréatite sans cause trouvée malgré un bilan complet exhaustif chez des patients jeunes (moins de 35 ans) ;
- découverte d’une pancréatite chronique quel que soit l’âge en cas d’antécédent familial de pancréatite aiguë ou chronique idiopathique ;
- facteurs de risque identifiés de pancréatite dont l’imputabilité reste discutable, pour expliquer à eux seuls la pancréatite : consommation d’alcool importante mais récente (depuis moins de 5 ans), variation anatomique (ansa pancreatica, pancreas divisum), consommation tabagique modérée, consommation de cannabis, consommation d’alcool chronique modérée ;
- conseil génétique à la suite de l’identification chez un apparenté au premier degré d’une mutation de PRSS1 chez les patients symptomatiques et asymptomatiques en raison du surrisque de cancer. Un dépistage chez les apparentés asymptomatiques mineurs n’est pas recommandé ; l’apparenté décide de faire le test à sa majorité s’il le souhaite. Pour les autres mutations, il n’est pas recommandé de dépistage familial si le patient est asymptomatique du fait de l’absence de risque majoré de cancer.
Après une information claire et l’obtention d’un consentement libre écrit (obligation légale), la recherche d’une cause génétique peut être entreprise. L’analyse est réalisée sur prélèvement sanguin, analyse moléculaire et séquençage de nouvelle génération (NGS), ce qui permet d’analyser rapidement plusieurs gènes en simultané. Plusieurs centres, répertoriés sur le site Orphanet, pratiquent ces tests génétiques en France. Le résultat doit être communiqué au cours d’une consultation dédiée par un praticien formé au conseil génétique ou un conseiller génétique.
Dans les formes pédiatriques de pancréatite aiguë, des causes plus spécifiques sont à évoquer (malformations, traumatismes, virus). Les pancréatites virales (oreillons, paramyxovirus) ne sont, en effet, pas rares chez les enfants, elles sont souvent modérées et ne récidivent généralement pas. Ainsi, il peut être recommandé de faire des tests génétiques après avoir éliminé une malformation et un épisode viral imputable.
Dépistage anténatal
En France, un diagnostic préimplantatoire peut être envisagé en cas de pancréatite héréditaire en lien avec une mutation identifiée de PRSS1. L’indication est validée après concertation au sein d’un centre pluridisciplinaire de diagnostic prénatal. L’ensemble des informations sur le parcours de soins est disponible sur le Protocole national de diagnostic et de soins (PNDS) rédigé par le Centre de référence des maladies rares du pancréas PaRaDis.7
En cas de dépistage de mutation sévère du gène CFTR, un dépistage du partenaire avant conception est recommandé afin de s’assurer de l’absence de mutation sévère chez le conjoint qui ferait courir le risque de mucoviscidose dans la descendance (risque de 25 %).
Prise en charge
La prise en charge des poussées aiguës est similaire à celle des autres formes de pancréatite aiguë. L’hospitalisation est indiquée uniquement en cas de douleurs non contrôlées ou de forme sévère. Il faut savoir limiter les scanners pour réduire l’irradiation tout en s’appliquant à rechercher une cause additionnelle (alcool, biliaire). Une échographie de la vésicule est recommandée en cas de doute quant à une cause biliaire.
De même, le suivi des pancréatites génétiques ne diffère pas de celui des autres formes de pancréatites chroniques, mais les complications apparaissent plus tôt (figure). Ces complications peuvent être des douleurs chroniques, une insuffisance pancréatique exocrine, un diabète et parfois un adénocarcinome pancréatique.
Il est primordial d’insister sur le sevrage en alcool et surtout en tabac, deux facteurs qui favorisent l’aggravation des symptômes liés à la pancréatite génétique.
Les spécificités de la prise en charge d’une pancréatite génétique sont doubles.
Accompagnement psychologique et social
Les répercussions psychologiques du caractère transmissible de la maladie à sa descendance, du surrisque de cancer du pancréas, des douleurs chroniques, de l’errance diagnostique ne doivent pas être sous-estimées. Une prise en charge psychologique doit être systématiquement proposée. De même, un accompagnement social est essentiel du fait d’un absentéisme scolaire et professionnel.
Dépistage de l’adénocarcinome pancréatique
Le risque d’adénocarcinome pancréatique au cours de la pancréatite héréditaire est largement supérieur à celui des pancréatites chroniques d’autres causes, en raison de phénomènes inflammatoires précoces depuis l’enfance.8 - 10
Dans la cohorte nationale française de patients porteurs d’une mutation de PRSS1, les risques cumulés de cancer du pancréas à 50, 60 et 75 ans étaient respectivement de 10 % (intervalle de confiance à 95 % [IC 95 %] : 1 - 18 %), 18,7 % (IC 95 % : 3 - 32 %) et 53,5 % (IC 95 % : 7 - 76 %).11 Dans le cadre spécifique de la pancréatite liée à PRSS1, un dépistage annuel à partir de l’âge de 40 ans est recommandé par la réalisation d’une imagerie par résonance magnétique (IRM) pancréatique avec wirsungo-IRM.
Il n’y a pas de recommandations de dépistage du cancer du pancréas pour les autres mutations, car le risque de cancer n’est pas autant majoré.
2. Whitcomb DC, Gorry MC, Preston RA, et al. Hereditary pancreatitis is caused by a mutation in the cationic trypsinogen gene. Nat Genet 1996;14(2):141-5.
3. Masson E, Zou WB, Pu N, et al. Classification of PRSS1 variants responsible for chronic pancreatitis: An expert perspective from the Franco-Chinese GREPAN study group. Pancreatology 2023;23(5):49-506.
4. Ferec C, Raguenes O, Salomon R, et al. Mutations in the cationic trypsinogen gene and evidence for genetic heterogeneity in hereditary pancreatitis. J Med Genet 1999;36(3):228-32.
5. Laurent L, Rebours V. Génétique de la pancréatite. Hepato-Gastro Oncol Dig 2021;28:853-63.
6. Vedie AL, Laurent L, Rebours V. Pancréatite d’origine génétique. EMC-Hépatologie. 2023.
7. Centre de référence pour les maladies rares du pancréas. Protocole national de diagnostic et de soins : pancréatite héréditaire. Décembre 2020. https://urls.fr/eTaOnw
8. Howes N, Lerch MM, Greenhalf W, et al. Clinical and genetic characteristics of hereditary pancreatitis in Europe. Clin Gastroenterol Hepatol 2004;2(3):252-61.
9. Lowenfels AB, Maisonneuve P, DiMagno EP, et al. Hereditary pancreatitis and the risk of pancreatic cancer. International Hereditary Pancreatitis Study Group. J Natl Cancer Inst 1997;89(6):442-6.
10. Shelton CA, Umapathy C, Stello K, et al. Hereditary pancreatitis in the United States: Survival and rates of pancreatic cancer. Am J Gastroenterol 2018;113(9):1376.
11. Rebours V, Boutron-Ruault MC, Schnee M, et al. The natural history of hereditary pancreatitis: A national series. Gut 2009;58(1):97-103.