L’hémoglobine glyquée est un marqueur incontournable pour le diagnostic, le suivi et l’évaluation des risques de complication du diabète, mais elle peut être mise en défaut chez les patients ayant une hémoglobinose. Devant des résultats incohérents d’HbA1c, il faut donc savoir suspecter une pathologie de l’hémoglobine, pour mettre en place un suivi du patient « comme son propre témoin ».
Le diabète est une des priorités de santé publique mondiale, affectant 442 millions d’adultes, soit 1 personne sur 11 (Organisation mondiale de la santé 2021) ; les hémoglobinoses sont des pathologies fréquentes en population générale, avec une prévalence estimée à 0,6 ‰ chez les patients diabétiques.1 Il est donc important de sensibiliser les praticiens ayant des patients atteints d’hémoglobinoses (ou variants de l’hémoglobine). La fraction glyquée A1c stable de l’hémoglobine A (HbA1c) est un marqueur incontournable pour le diagnostic, le suivi et l’évaluation des risques de complication du diabète. Cependant, dans certaines pathologies de l’hémoglobine comme les hémoglobinoses, son dosage peut être mis en défaut.2 Il existe un risque d’interprétation erronée en cas de variant de l’hémoglobine non connu et non détecté par la méthode de dosage, avec comme conséquences désastreuses un diabète non diagnostiqué et/ou des seuils d’HbA1c inadaptés pour le suivi de l’équilibre glycémique. Dans ce but, nous vous proposons une conduite à tenir face à des résultats incohérents d’HbA1c pouvant être liés à un variant de l’hémoglobine ainsi que des solutions pragmatiques pour un suivi pertinent chez ces patients.
Rappel physiologique HbA1c/variant de l’hémoglobine
L’hémoglobine adulte (HbA) est constituée d’un tétramère de chaî-nes de globines : deux α et deux β. L’HbA1c correspond à la fraction de l’hémoglobine exposée à la glycation irréversible non enzymatique de la valine N-terminale de la chaîne β de l’HbA. L’HbA1c s’exprime en pourcentage de l’hémoglobine totale chez des sujets homozygotes pour l’HbA. Elle reflète la glycémie moyenne des 120 derniers jours (durée de vie moyenne des hématies), le dernier mois comptant pour 50 % de sa valeur. Toute modification de la durée de vie des hématies ou de l’érythropoïèse a un impact sur le taux d’HbA1c.2
Plus de 1 300 variants de l’hémoglobine ont été décrits (HbVar database). Les variants HbS, HbC (population afro-antillaise), HbD (population indienne) et HbE (population asiatique) sont les plus fréquents (hémoglobinoses par mutation ponctuelle sur la chaîne β). Ces mutations sont responsables d’une réduction de la durée de vie des hématies et d’un processus de glycation altéré.2 Le dosage des fructosamines ou protéines glyquées plasmatiques (dont 80 % d’albumine) représente une alternative pour le suivi de l’équilibre glycémique de ces patients. Leurs variations sont totalement indépendantes d’une anomalie de l’hémoglobine. Comme l’HbA1c, elles constituent un marqueur rétrospectif et cumulatif mais limité aux 21 derniers jours.3 Elles peuvent tout de même souffrir d’interférences dans les situations de diminution du taux des protéines (hépatopathies, glomérulopathies, dysthyroïdie, inflammation…) ; un dosage concomitant d’albumine est donc conseillé.3
Plus de 1 300 variants de l’hémoglobine ont été décrits (HbVar database). Les variants HbS, HbC (population afro-antillaise), HbD (population indienne) et HbE (population asiatique) sont les plus fréquents (hémoglobinoses par mutation ponctuelle sur la chaîne β). Ces mutations sont responsables d’une réduction de la durée de vie des hématies et d’un processus de glycation altéré.2 Le dosage des fructosamines ou protéines glyquées plasmatiques (dont 80 % d’albumine) représente une alternative pour le suivi de l’équilibre glycémique de ces patients. Leurs variations sont totalement indépendantes d’une anomalie de l’hémoglobine. Comme l’HbA1c, elles constituent un marqueur rétrospectif et cumulatif mais limité aux 21 derniers jours.3 Elles peuvent tout de même souffrir d’interférences dans les situations de diminution du taux des protéines (hépatopathies, glomérulopathies, dysthyroïdie, inflammation…) ; un dosage concomitant d’albumine est donc conseillé.3
Lire aussi | Surrisque de cancer gastrique en cas de diabète
Intérêt crucial des méthodes séparatives
En cas d’hémoglobinoses, les méthodes de dosage de l’HbA1c ne sont pas toutes équivalentes et peuvent conduire à une interprétation erronée lorsqu’elles ne permettent pas de détecter la présence d’un variant.2, 4 On distingue les méthodes immunologiques, enzymatiques et séparatives.
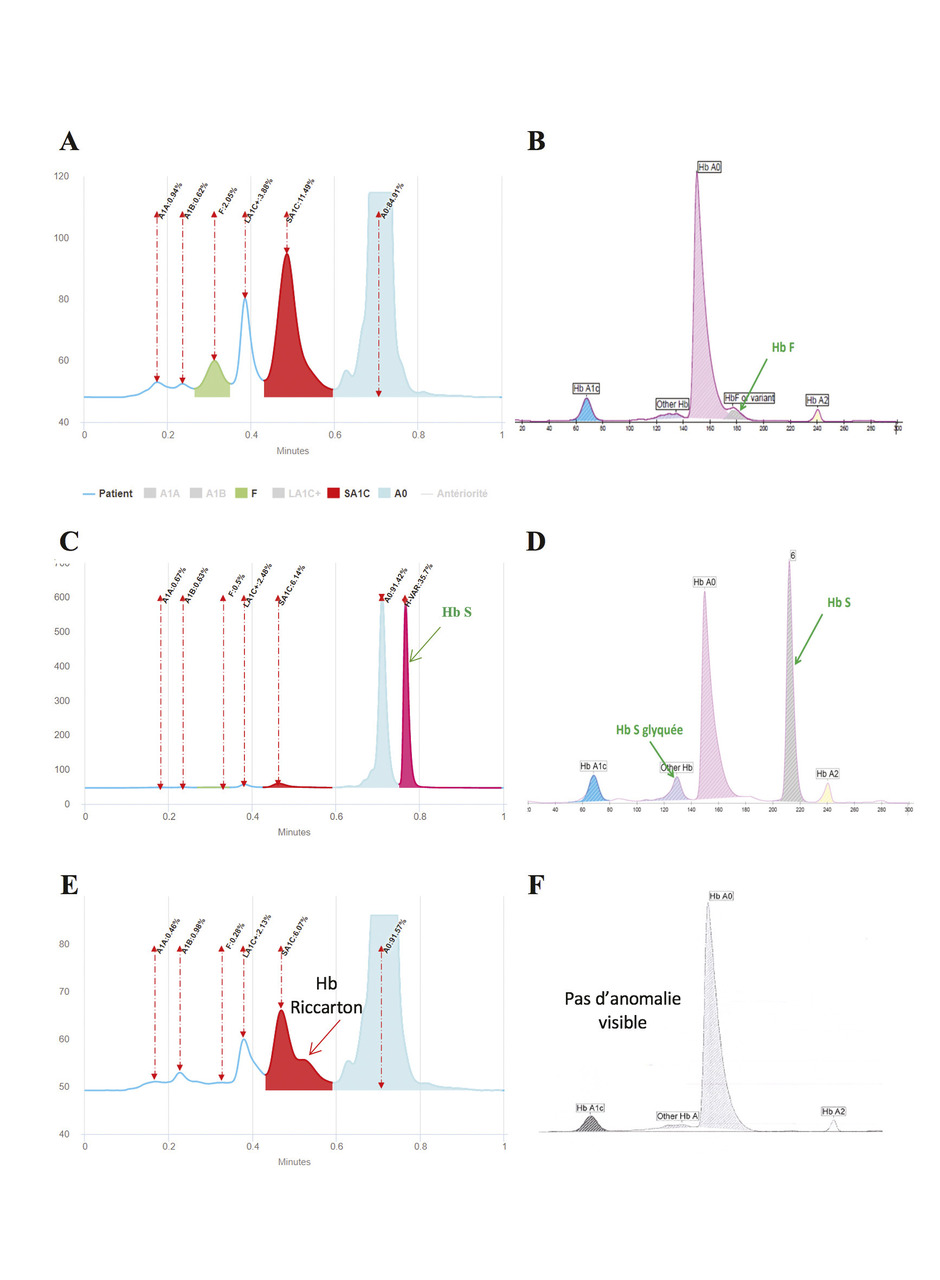
Les méthodes séparatives (adoptées par 75 % des laboratoires en France en 2021) exploitent les modifications physicochimiques de l’hémoglobine à la suite de la fixation du glucose, permettant une séparation de l’HbA1c des autres formes de l’hémoglobine. Par conséquent, outre le dosage de l’HbA1c, elles rendent possible la détection d’une éventuelle hémoglobinose. Sur lafigure 1 sont présentés des exemples de profils en méthodes séparatives, soit par chromatographie HPLC avec échange d’ions (fig. 1A, 1C et 1E ), soit par électrophorèse capillaire (fig. 1B, 1D et 1F ). Les profils A et B correspondent à des patients « normaux » (homozygotes HbA/A). Lorsqu’un variant est présent, différentes anomalies de profil peuvent être visualisées : pic supplémentaire (par exemple une hétérozygotie A/S sur les profils C, D) ou déformation d’une des fractions, ici HbA1c (par exemple variant Riccarton visible sur le profil 1E et pas sur 1F ). Les techniques immunologiques utilisent des anticorps spécifiques détectant la glycation de la valine N-terminale de la β-globine non mutée. Si une mutation altère cette β-globine, la méthode est prise en défaut pour la quantification de l’HbA1c (sous-estimation car les anticorps sont incapables de reconnaître leur cible). Le patient risque alors d’être considéré à tort dans la cible thérapeutique d’HbA1c et son hémoglobinose ne sera pas mise en évidence (défaut partagé par les techniques enzymatiques). Il est recommandé de ne pas rendre des taux faibles d’HbA1c inférieurs à 4,5 % par cette technique et de réorienter vers une méthode séparative.
Les méthodes séparatives (adoptées par 75 % des laboratoires en France en 2021) exploitent les modifications physicochimiques de l’hémoglobine à la suite de la fixation du glucose, permettant une séparation de l’HbA1c des autres formes de l’hémoglobine. Par conséquent, outre le dosage de l’HbA1c, elles rendent possible la détection d’une éventuelle hémoglobinose. Sur la
Quand suspecter une hémoglobinose ?
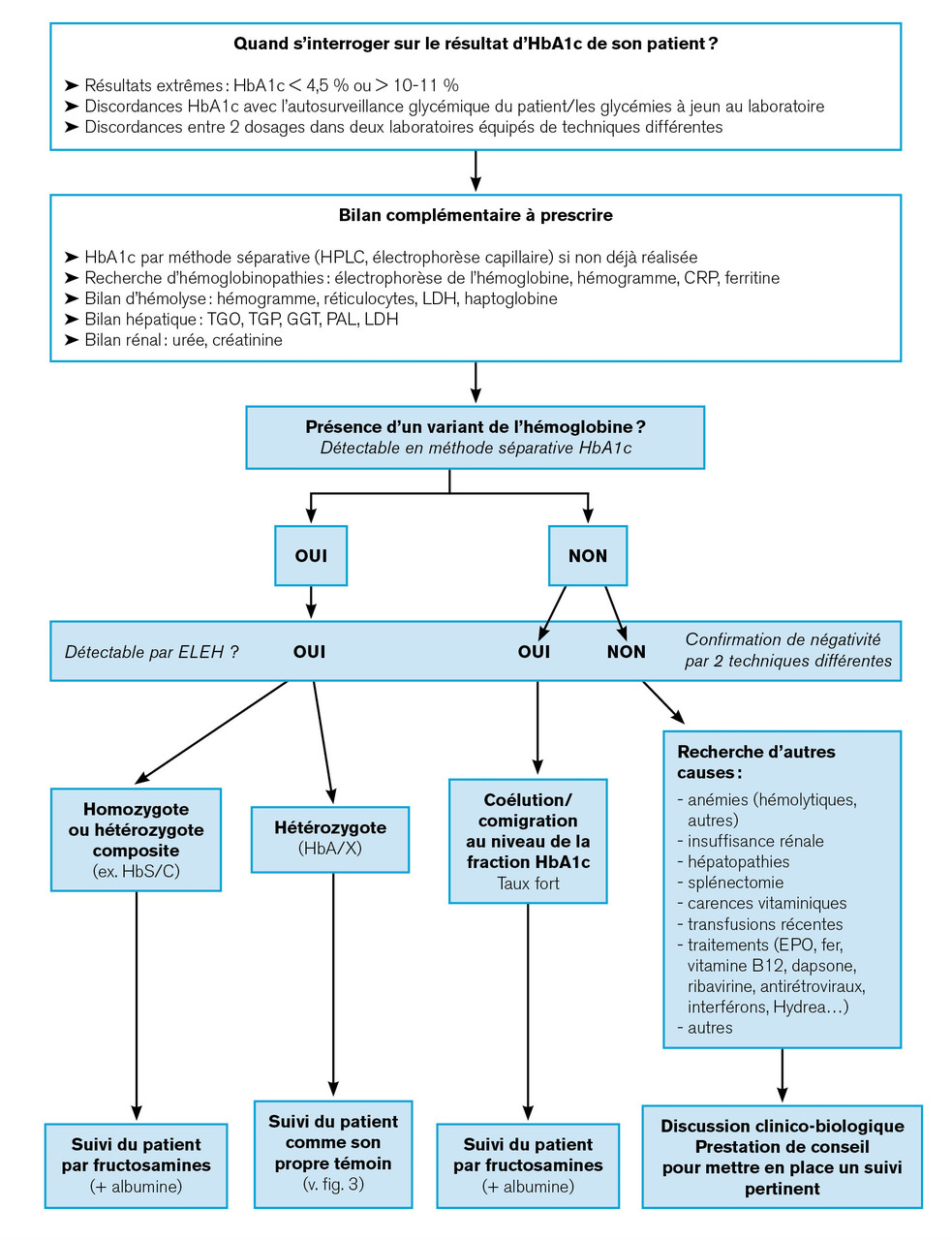
Une hémoglobinose peut être suspectée à partir du résultat d’HbA1c dans trois situations (fig. 2 ) : dosage d’HbA1c très faible, inférieur à 4,5 %, ou élevé, supérieur à 10-11 %, discordance avec la glycémie moyenne (autosurveillance du patient et/ou dosages à jeun au laboratoire) ou, enfin, en cas de discordance entre deux résultats obtenus par deux techniques différentes.4 Aucune technique n’est exempte d’interférences.2 En cas de résultats « douteux », il est important de s’assurer qu’une méthode séparative de l’HbA1c a été utilisée et, sinon, de la prescrire. Dans ce cadre, afin de pouvoir interpréter correctement l’HbA1c, un bilan complémentaire est nécessaire.4 Il comprend la recherche de la pathologie de l’hémoglobine par une électrophorèse. Pour éliminer les autres sources d’interférences, un bilan d’hémolyse complet et un bilan rénal et hépatique sont à envisager ainsi qu’un interrogatoire complet du patient pour connaître tous ses traitements et ses antécédents transfusionnels récents.5
Si un variant est détecté par l’électrophorèse de l’hémoglobine, on distingue deux cas : le patient homozygote ou hétérozygote composite (par exemple HbS/C) avec absence d’HbA, donc d’HbA1c ; le patient hétérozygote avec présence d’HbA. Dans le premier cas, le patient devra être suivi définitivement par les fructosamines. Dans le second, il pourra être suivi « comme son propre témoin » (fig. 3 ).2 Si le variant n’est détectable qu’à l’électrophorèse de l’hémoglobine, le patient sera également suivi définitivement par les fructosamines. Cette situation est à évoquer en particulier pour de forts taux d’HbA1C, supérieurs à 10 %. Le biologiste doit s’assurer qu’une fraction d’un variant ne soit pas « cachée » (coélution/comigration) et qu’il y ait bien une absence de pic supplémentaire ou d’anomalie du profil. Si aucun variant n’est détecté par la technique d’électrophorèse de l’hémoglobine utilisée, le résultat doit être confirmé par une deuxième technique, avant de conclure. D’autres causes de discordance peuvent alors être envisagées en fonction des résultats de l’exploration complémentaire (fig. 2 ). Par exemple, une anémie aiguë entraîne une sous-estimation de la valeur d’HbA1c et, à l’inverse, une insuffisance rénale provoque une surestimation.4, 5
La connaissance du contexte médico-thérapeutique du patient est donc essentielle pour assurer une prise en charge maîtrisée via l’HbA1c.5 En cas de résultat d’interprétation difficile, l’interlocuteur privilégié est le biologiste médical, capable d’expliquer la technique utilisée dans son laboratoire et ses limites, ainsi que les solutions à apporter pour le suivi de tous les patients diabétiques avec ou sans hémoglobinose.4 Enfin, pour un suivi cohérent, il est important de réaliser le dosage d’HbA1c par la même technique et dans le même laboratoire.2
Si un variant est détecté par l’électrophorèse de l’hémoglobine, on distingue deux cas : le patient homozygote ou hétérozygote composite (par exemple HbS/C) avec absence d’HbA, donc d’HbA1c ; le patient hétérozygote avec présence d’HbA. Dans le premier cas, le patient devra être suivi définitivement par les fructosamines. Dans le second, il pourra être suivi « comme son propre témoin » (
La connaissance du contexte médico-thérapeutique du patient est donc essentielle pour assurer une prise en charge maîtrisée via l’HbA1c.5 En cas de résultat d’interprétation difficile, l’interlocuteur privilégié est le biologiste médical, capable d’expliquer la technique utilisée dans son laboratoire et ses limites, ainsi que les solutions à apporter pour le suivi de tous les patients diabétiques avec ou sans hémoglobinose.4 Enfin, pour un suivi cohérent, il est important de réaliser le dosage d’HbA1c par la même technique et dans le même laboratoire.2
Comment suivre les patients diabétiques hétérozygotes (HbA/X) ?
Suivi du patient comme « son propre témoin » avec détermination d’une cible d’HbA1c personnalisée
L’impact des hémoglobinoses diffère selon le type de variant2, 4, 5 et la technique utilisée.2 La majorité des variants sous-estime le dosage d’HbA1c (HbS, C, D, E). Cependant, le dosage peut être surestimé si les fractions variantes sont confondues avec l’HbA1c. La sous-estimation peut occulter le diagnostic de diabète, et lors du suivi, le patient peut être « faussement qualifié d’équilibré » selon les valeurs cibles des recommandations de la Haute Autorité de santé (par exemple HbA1c < 7 %)6 dont la validité en présence de variants n'est pas démontrée. Chez ces patients, un certain nombre de paramètres influencent le taux d’HbA1c. Le processus de glycation des variants est méconnu de même que l’impact des variants sur la durée de vie des hématies (lié à l’anémie, à l’hémolyse).2, 4 Un suivi personnalisé de l’HbA1c peut alors être mis en place (fig. 3 ),2 sans exclure bien sûr l’autosurveillance et/ou les holters glycémiques. Tout l’enjeu est alors de déterminer une cible d’HbA1c propre à ce patient via une collaboration étroite entre biologiste médical et médecin. La littérature scientifique est pauvre sur ce sujet et nécessiterait des études cliniques supplémentaires.
En pratique
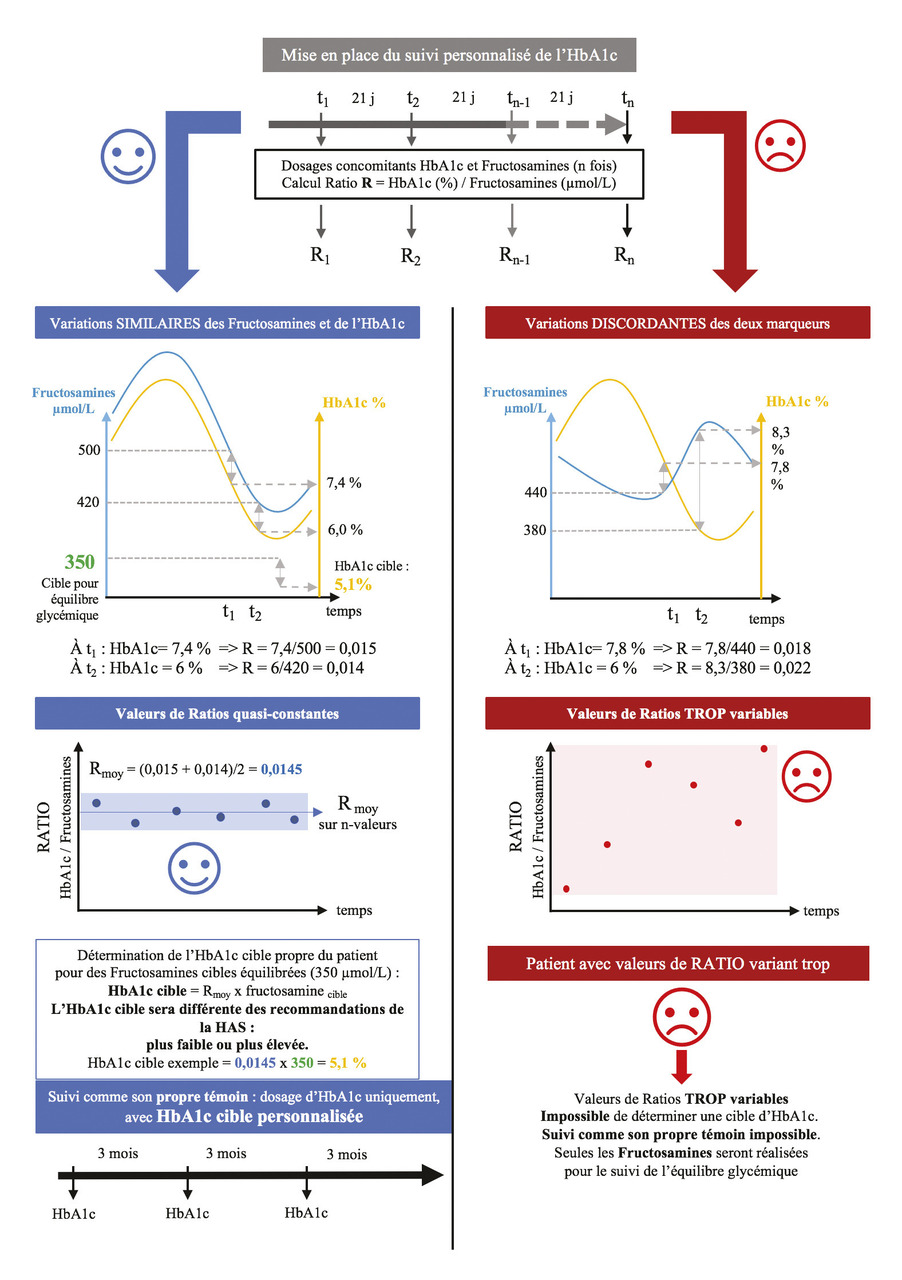
Dans une approche pragmatique, une première phase (fig. 3A ) consiste à réaliser une série de dosages concomitants des fructosamines et de l’HbA1c (au minimum 4) toutes les 3 semaines (indexé sur le temps de renouvellement des fructosamines). Si sur cette période les deux marqueurs évoluent de manière discordante (augmentation-diminution ou diminution-augmentation), seul un dosage des fructosamines sera indiqué pour le suivi, avec l’inconvénient de nécessiter des dosages plus rapprochés (fig. 3 colonne de droite en rouge ).
À l’inverse, si l’on obtient sur cette période une évolution similaire des deux marqueurs (augmentation-augmentation, diminution-diminution, stabilité-stabilité), une cible d’HbA1c personnalisée va pouvoir être déterminée (fig. 3 colonne de gauche en bleu ). Le patient peut dès lors être suivi « comme son propre témoin » avec l’HbA1c seule, dosée dans le même laboratoire tous les trois mois. Le biologiste doit s’assurer de son côté que le profil rendu par sa technique séparative est bien reproductible.
On émet également l’hypothèse que l’hémolyse chronique est constante, d’où l’intérêt d’un bilan d’hémolyse systématiquement associé (fig. 2 ). La valeur cible d’HbA1c personnalisée pour ce patient peut être déterminée à partir de plusieurs paires de dosage et de calculs de ratio (HbA1c/fructosamines), permettant de définir un ratio moyen (Rmoy). Il suffit de multiplier le Rmoy par 350 µmol/L (cible des fructosamines que nous retenons dans cet exemple) pour obtenir la cible d’HbA1c en dessous de laquelle le diabète pourra être considéré comme équilibré. La valeur cible d’équilibre glycémique des fructosamines n’a pas fait pas l’objet d’études cliniques validées ni d’un consensus fort. Des valeurs normales sont bien décrites entre 200-265 ou 205-285 µmol/L selon les techniques, mais pour des populations non diabétiques.3 Il existe des tables de conversion proposées entre fructosamines et HbA1c ou des équations (v. encadré ).7 Une valeur d’équilibre inférieure à 350 µmol/L est communément admise par les endocrinologues.3
À l’inverse, si l’on obtient sur cette période une évolution similaire des deux marqueurs (augmentation-augmentation, diminution-diminution, stabilité-stabilité), une cible d’HbA1c personnalisée va pouvoir être déterminée (
On émet également l’hypothèse que l’hémolyse chronique est constante, d’où l’intérêt d’un bilan d’hémolyse systématiquement associé (
Un suivi différent
Les hémoglobinoses affectent directement l’HbA1c par leur physiopathologie et par le biais analytique qu’elles entraînent. Il nous a paru crucial de sensibiliser les médecins à cette situation, même si sa fréquence varie en fonction des zones géographiques. Ainsi, ils disposent d’un logigramme pour raisonner sur des résultats incohérents permettant de diagnostiquer d’éventuelles hémoglobinoses, de les explorer ou de les infirmer au profit d’autres causes. Les méthodes séparatives, majoritaires en France, permettent de dépister les variants de l’hémoglobine. Le suivi des patients est différent en l’absence ou en présence d'un variant mais aussi selon le type de variant : homozygote (fructosamines strictement) ou hétérozygote (couple fructosamines/HbA1c). En cas d’hétérozygotie, une solution empirique pragmatique est envisageable si l’HbA1c et les fructosamines évoluent dans le même sens. À partir des différents couples de dosage, un ratio HbA1c/fructosamines moyen peut être déterminé. En multipliant ce ratio moyen par une valeur de fructosamines reflétant l’équilibre glycémique, une HbA1c cible propre au patient peut être déterminée, lui offrant un suivi simplifié.
Encadre
Équation de conversion
Fructosamines (µmol/L) = (HbA1c [%] – 1,61) x 58,52 https://www.sentinelles971.com/equivalence-hba1c-fructosamine
Références
1. Reynolds TM, Twomey PJ, Harvey TC, Green BN. The number of unexpected HbA1c variants may be a greater problem in routine practice than in generally realized. Diabet Med 2004;21:1041-4.
2. Gillery P, Hue G, Bordas-Fonfrède M, Chapelle JP, Hue G, Périer C. Dosage de l’hémoglobine A1c et hémoglobinopathies : problèmes posés et conduite à tenir. Ann Biol Clin 2000;58:425-30.
3. Desch G. Aspects biochimiques et analytiques du diagnostic et de la surveillance du diabète. Med Nucl Imag Fonct Metab 2001;25:61-72.
4. Fonfrède M. Un résultat d’HbA1c est-il toujours interprétable ? Spectra Biologie 2006;152:48-53.
5. Wojtusciszyn A. Les pièges de l’HbA1c. Real Cardiol 2012:1-5.
6. Haute Autorité de santé. Stratégie médicamenteuse du contrôle glycémique du diabète de type 2. Recommandations de bonnes pratiques, HAS, 2013.
7. Guillausseau PJ, Charles MA, Godard V, Timsit J, Chanson P, et al. Comparison of fructosamine with glycated hemoglobin as an index of glycemic control in diabetic patients. Diab Res 1990;13:127-31.
2. Gillery P, Hue G, Bordas-Fonfrède M, Chapelle JP, Hue G, Périer C. Dosage de l’hémoglobine A1c et hémoglobinopathies : problèmes posés et conduite à tenir. Ann Biol Clin 2000;58:425-30.
3. Desch G. Aspects biochimiques et analytiques du diagnostic et de la surveillance du diabète. Med Nucl Imag Fonct Metab 2001;25:61-72.
4. Fonfrède M. Un résultat d’HbA1c est-il toujours interprétable ? Spectra Biologie 2006;152:48-53.
5. Wojtusciszyn A. Les pièges de l’HbA1c. Real Cardiol 2012:1-5.
6. Haute Autorité de santé. Stratégie médicamenteuse du contrôle glycémique du diabète de type 2. Recommandations de bonnes pratiques, HAS, 2013.
7. Guillausseau PJ, Charles MA, Godard V, Timsit J, Chanson P, et al. Comparison of fructosamine with glycated hemoglobin as an index of glycemic control in diabetic patients. Diab Res 1990;13:127-31.

 Encadrés
Encadrés