L’embolie pulmonaire (EP) est, avec la thrombose veineuse profonde (TVP), une des deux principales présentations cliniques de la maladie thromboembolique veineuse (MTEV). L’EP est dans 70 % des cas secondaire à une TVP, par migration du thrombus dans les artères pulmonaires. Près de 50 000 personnes ont été hospitalisées pour EP en France en 2022 ; la maladie serait responsable d’environ 10 000 décès/an.
Urgence thérapeutique avant tout prise en charge à l’hôpital, l’EP peut faire l’objet d’un traitement ambulatoire dans certains cas. Que disent les recos sur la démarche à suivre face à une suspicion d’EP en MG, et sur une éventuelle prise en charge ambulatoire ?
Quand suspecter une EP au cabinet ?
Les symptômes de l’EP ne sont pas spécifiques ; certaines EP sont même asymptomatiques. Les symptômes qui font suspecter une EP sont les suivants :
- dyspnée isolée (souvent d’apparition brutale, inexpliquée mais parfois d’installation progressive sur plusieurs semaines, avec auscultation pulmonaire souvent normale) ;
- douleur thoracique (douleur typiquement pleurale, à type de point de côté brutal, parfois augmentée par la percussion ou la pression de la paroi thoracique) ;
- syncope/malaise ou pré-syncope (symptôme rare, mais qui témoigne d’une importante réduction du flux sanguin systémique) ;
- état de choc/instabilité hémodynamique (peu fréquent en MG, signe d’une EP centrale ou étendue) ;
- hémoptysie, en particulier si associée à la douleur thoracique (signe de la constitution d’un infarctus pulmonaire).
Investiguer une suspicion
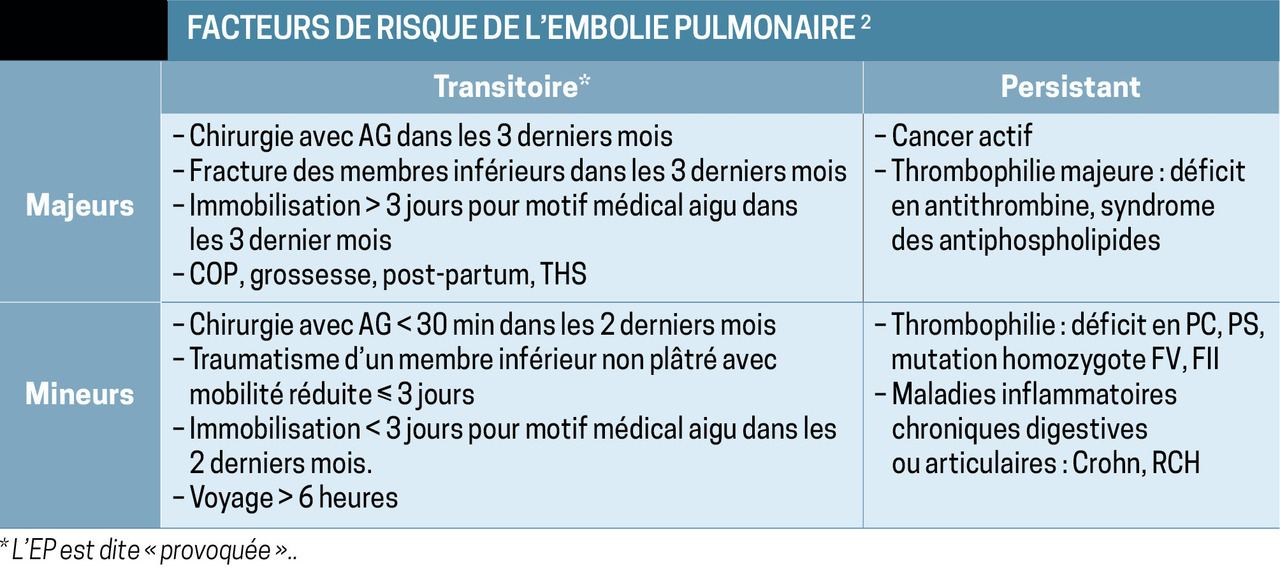
Face à la présence d’un ou plusieurs de ces symptômes, il est important de rechercher les principaux facteurs de risque d’EP (voir figure 1), tout en gardant à l’esprit que 20 à 30 % des EP sont spontanées ou idiopathiques.
L’examen clinique recherche une tachycardie et des signes de retentissement hémodynamique (hypotension artérielle, signes d’insuffisance cardiaque droite). La recherche de signes cliniques en faveur d’une thrombose veineuse associée est importante, bien que souvent négative.
La règle PERC
Si le clinicien considère qu’il y a une probabilité faible d’EP, la règle PERC (pour Pulmonary embolism rule-out criteria, détaillée en 1re colonne du tableau 1 ci-contre), permet de rejeter une EP rapidement,lorsque les 8 critères suivants sont tous négatifs : âge ≥ 50 ans ; fréquence cardiaque ≥ 100 bpm ; Saturation en oxygène (oxymétrie de pouls) < 95 % ; hémoptysie ; œdème unilatéral d’un membre inférieur (asymétrie à l’évaluation visuelle) ; prise d’un traitement oestrogénique ; antécédent personnel de TVP ou d’EP ; hospitalisation pour traumatisme ou chirurgie sous anesthésie générale dans les 4 semaines précédentes.
##Probabilité pré-test
En l’absence d’instabilité hémodynamique, il est recommandé d’évaluer la probabilité clinique pré-test (c’est-à-dire avant examens complémentaires) à partir soit du jugement clinique, soit d’un score validé, comme le score de Wells ou celui de Genève révisé (respectivement, tests en colonnes 2 et 3 du tableau 1). Selon les recos américaines de 2026, la probabilité clinique pré-test d’EP est classée en trois catégories : faible (< 15 %), intermédiaire (15 - 50 %) ou élevée (> 50 %).
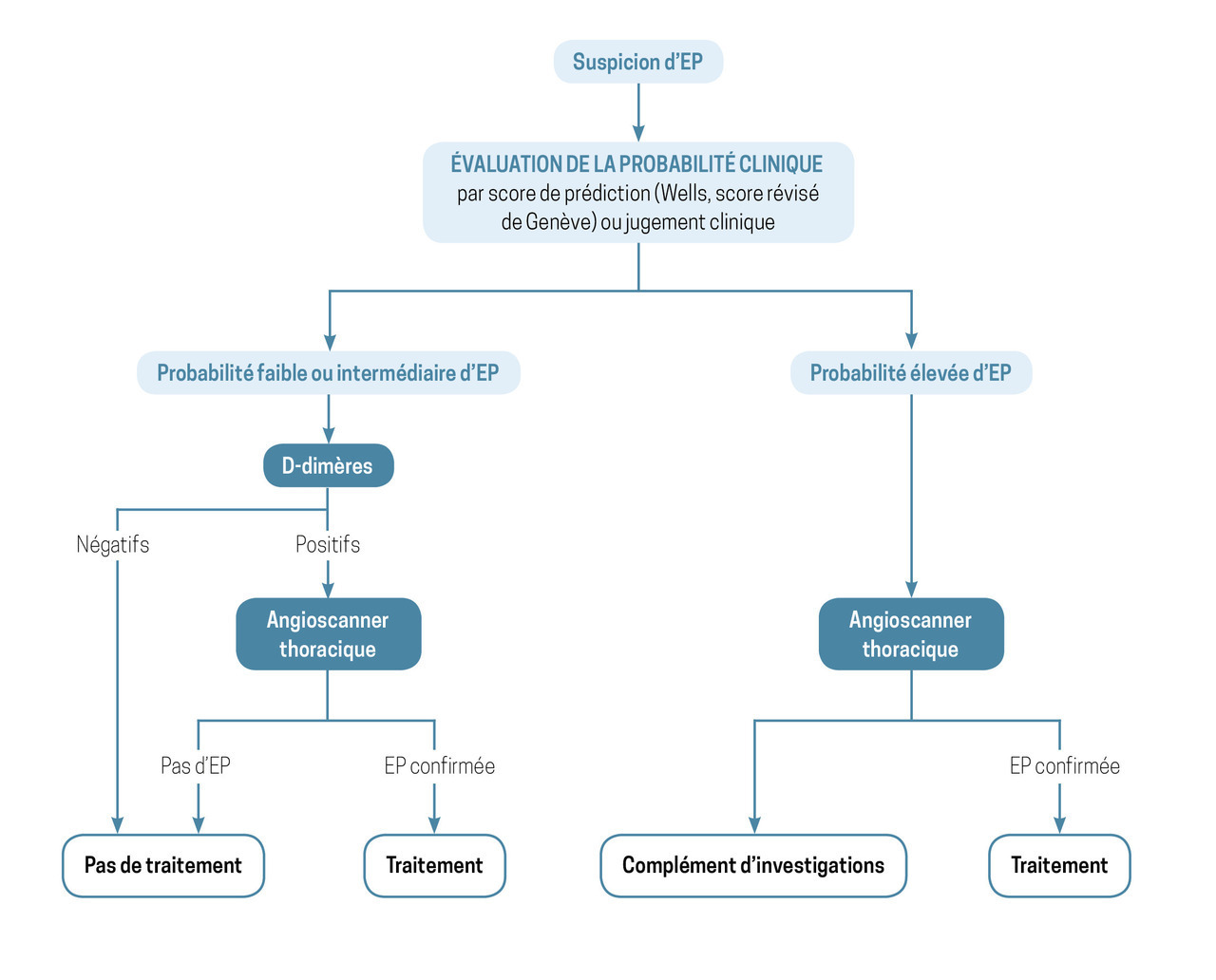
La suite des investigations, réalisée si possible dans les 4 heures (sans délai en présence de troubles hémodynamiques) s’appuie, en fonction du niveau de probabilité, sur un dosage des D-dimères, un angioscanner thoracique, voire une scintigraphie thoracique (voir plus bas). Un algorithme diagnostique en indiqué en figure 2.
D-dimères : situations et seuils à connaître
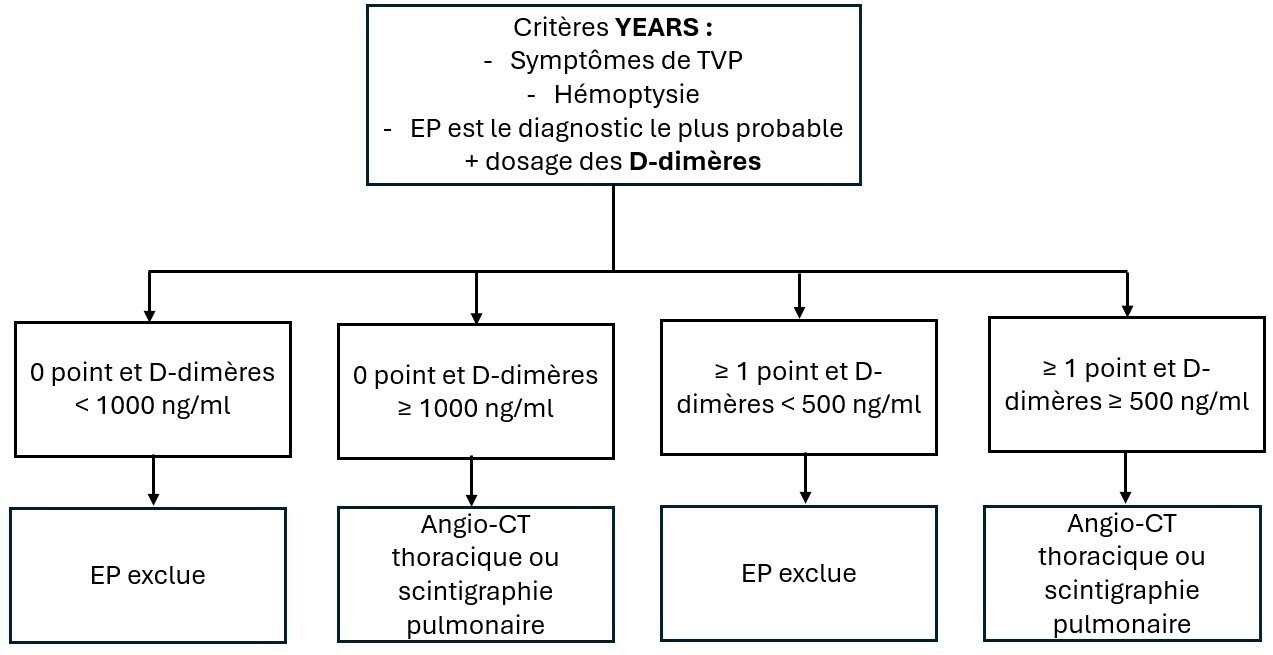
Lorsque la probabilité clinique pré-test est faible ou intermédiaire, il faut réaliser un dosage des D-dimères. Un taux inférieur à un certain seuil autorise l’exclusion d’une EP sans recourir à l’imagerie. Ce seuil varie selon les recos : seuil unique à 500 ng/mL ou adapté à l’âge (âge × 10 ng/mL après 50 ans, 500 ng/mL avant) dans les guidelines françaises et européennes ; le récent algorithme YEARS (voir figure 3), qui combine signes cliniques et dosage des D-dimères, est aussi recommandé par les sociétés savantes européennes et américaines.
Attention toutefois, les D-dimères ont des limites : ce test peut être faussement négatif en cas de thrombus petit ou distal, de prélèvement trop précoce ou tardif après le début des signes cliniques d’EP, et il n’est pas pertinent chez un patient déjà sous anticoagulant à dose thérapeutique. Enfin, il n’est absolument pas spécifique d’une thrombose, d’autres étiologies pouvant expliquer une valeur élevée.
En cas de probabilité pré-test haute, le dosage des D-dimères n’est pas nécessaire et il est recommandé de réaliser directement une imagerie diagnostique (en priorité angioscanner thoracique à la recherche d’emboles, autrement scintigraphie pulmonaire, ou recherche de thrombus proximal à l’échographie veineuse de compression).
Évaluation du pronostic
Une fois l’EP confirmée à l’imagerie, l’évaluation de son pronostic guide la prise en charge.
La présence d’un état de choc ou d’une hypotension artérielle – définie par une PAS < 90 mmHg ou par une baisse de la PAS > 40 mmHg pendant au moins 15 minutes – identifie les patients à haut risque de mortalité précoce (> 25 % à 30 jours ; 5 % des cas environ).
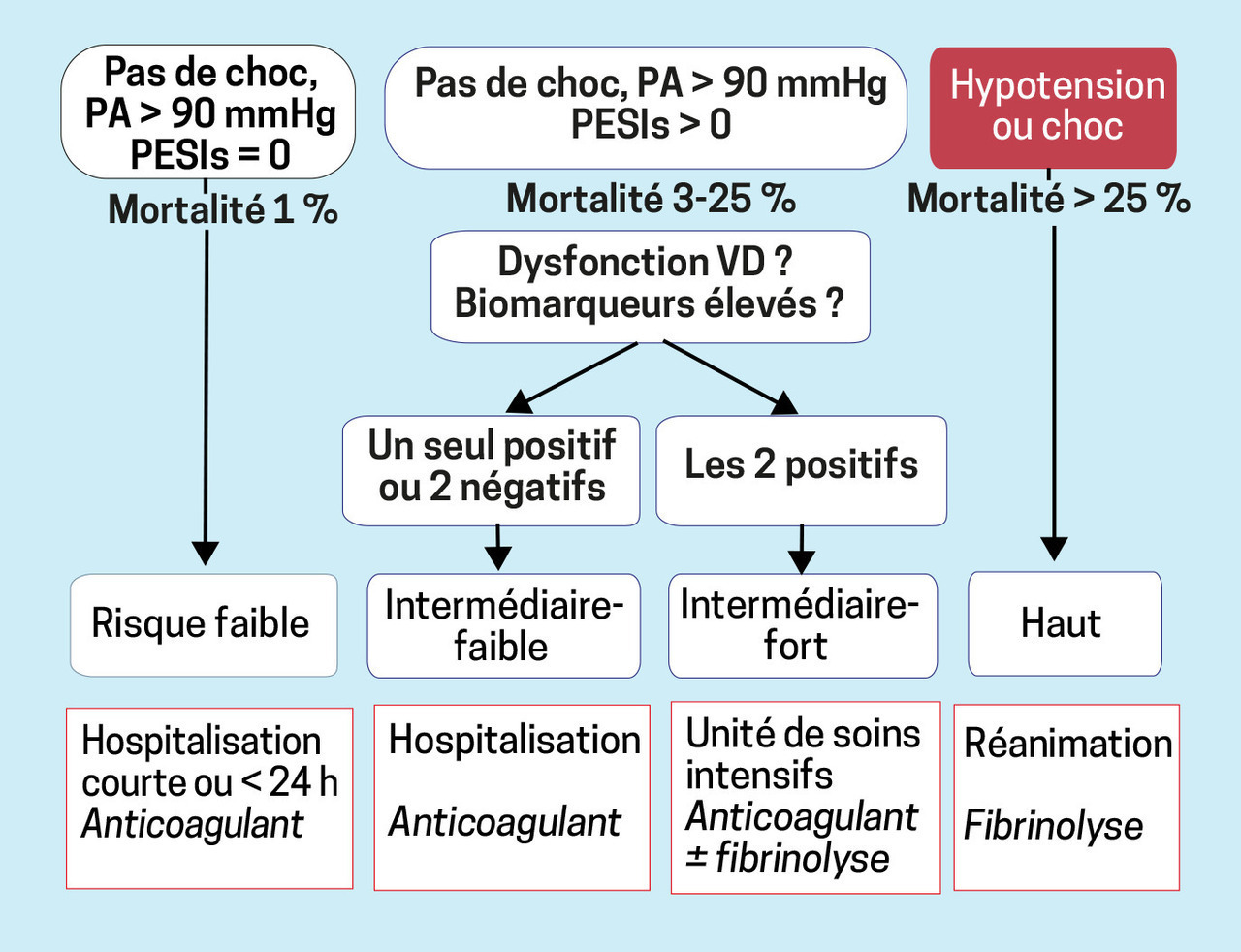
Chez les patients stables sur le plan hémodynamique, il est recommandé d’utiliser un score clinique pronostique (PESI, sPESI, critères HESTIA) (tableau 2) pour identifier les patients à faible risque de mortalité précoce (1 %) des patients à risque intermédiaire-faible ou intermédiaire-fort (3 - 25 %). L’algorithme de catégorisation du risque de l’EP, et la prise en charge associée, sont indiqués en figure 4.
Les patients ayant un score PESI ≤ 85 points ou un sPESI = 0 ou des critères HESTIA tous négatifs – soit les patients à risque faible, ou intermédiaire-faible avec HESTIA négatif – sont éligibles à un traitement ambulatoire, sous réserve qu’ils n’aient pas une des CI suivantes :
- signes d’ischémie justifiant une désobstruction en urgence (principalement par radiologie interventionnelle) ;
- insuffisance rénale sévère justifiant le recours à un traitement par héparine normo-fractionnée ;
- hémorragie active ou situation à haut risque hémorragique justifiant une surveillance étroite ;
- comorbidité décompensée ou problème social justifiant une hospitalisation.
Prise en charge : 3 phases
Dans la phase aigüe – premiers jours ou semaines –, l’objectif est de stopper l’extension du thrombus et d’éviter des récidives emboliques précoces. La phase d’entretien correspond aux 3 à 6 mois suivant l’épisode aigu. Durant cette période, la thrombolyse naturelle permet de déliter les thrombus et les emboles. Enfin, la dernière phase correspond à la prévention secondaire d’une récidive.
Ici, l’enquête systématique à la recherche de facteurs de risque de récidive, persistants ou transitoires, est fondamentale (figure 1). Elle peut comporter un bilan de thrombophilie et/ou la recherche d’une néoplasie sous-jacente. Ainsi, un bilan étiologique est à organiser dans les 3 mois post-EP. Pour ce faire, on conseille d’adresser le patient en service spécialisé, en particulier si une recherche de thrombophilie est envisagée. Le médecin traitant reste cependant le coordonnateur de la chaîne de soins et un élément majeur de l’éducation thérapeutique.
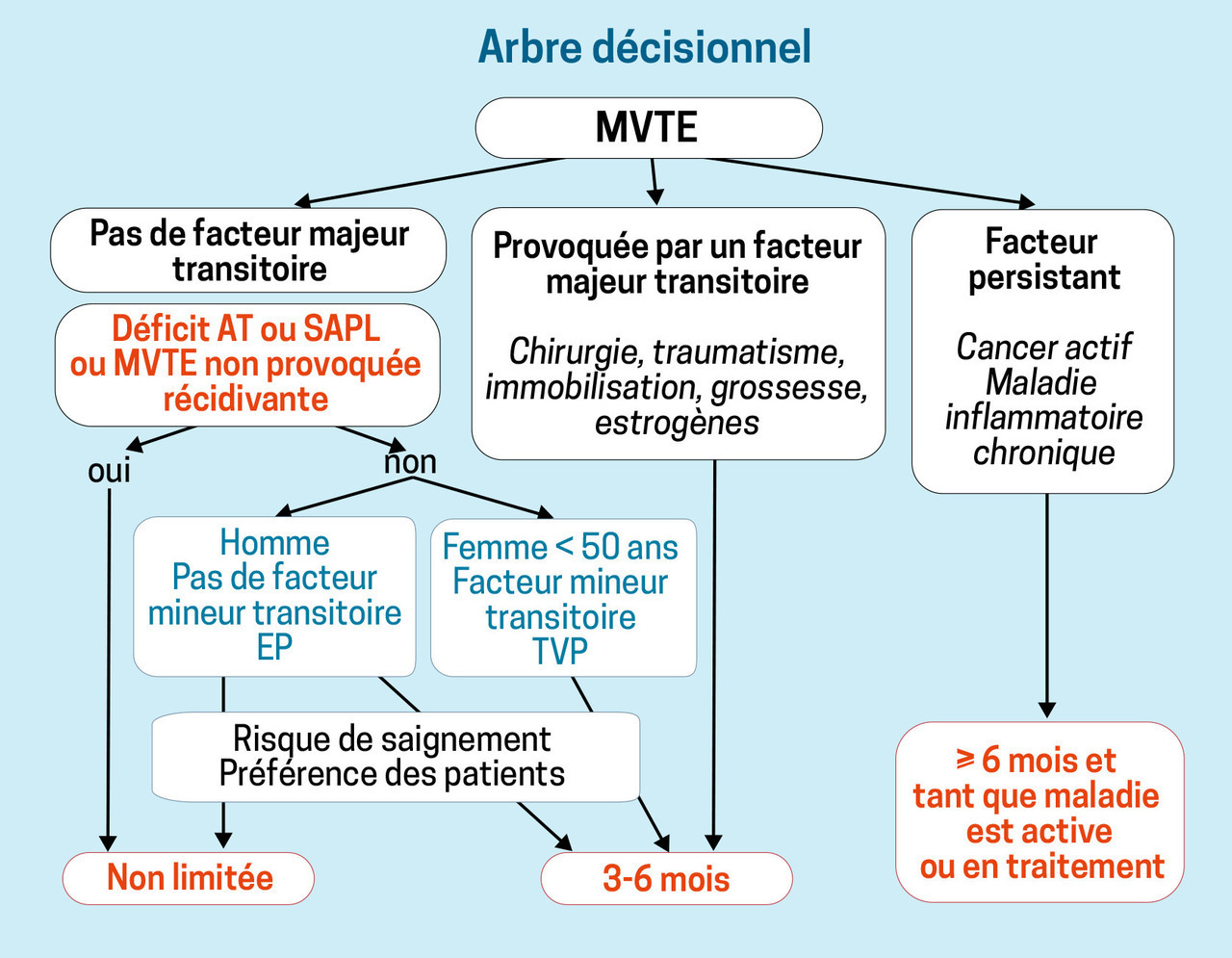
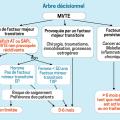
Les facteurs de risque éventuellement découverts lors de ce bilan déterminent la durée de traitement de l’épisode aigu : anticoagulation initiale pour 3 - 6 mois en cas de facteur majeur transitoire, traitement long terme/à vie en cas de facteur majeur persistant, durée moins claire en cas de facteur mineur. Des éléments additionnels peuvent aider à faire pencher la balance entre arrêt à 3 - 6 mois et prolongation des anticoagulants en l’absence de facteur majeur de récidive, à l’image du score HERDOO2 chez les femmes (tableau 3). Un arbre décisionnel sur la durée du traitement anticoagulant initial est proposé en figure 5.
Le traitement se fait aujourd’hui avant tout à base d’anticoagulants oraux directs (AOD), avec ou sans héparinothérapie préalable. En héparinothérapie, les HBPM et le fondaparinux sont aujourd’hui préférées à l’HNF. Les AVK (en relais précoce après héparinothérapie) ne concernent plus que quelques cas très spécifiques (notamment insuffisance rénale terminale non dialysée).
Le suivi ultérieur est essentiellement clinique, et les investigations (écho-doppler, test d’effort, etc.) seront réalisées si des symptômes surviennent.
Tromeur C, Le Mao R, de Moreuil C, et al. Embolie pulmonaire : traitement hospitalier ou ambulatoire ? Rev Prat Med Gen 2019;33(1022):416-8.
Coito S. D-dimères : quand les prescrire, comment les interpréter ? Rev Prat (en ligne) 17 avril 2025.
Mallordy F, Nobile C. Bilan de thrombophilie : qui tester et comment l’interpréter ? Rev Prat (en ligne) 19 novembre 2024.
Creager MA, Barnes GD, Giri J, et al. 2026 AHA/ACC/ACCP/ACEP/CHEST/SCAI/SHM/SIR/SVM/SVN guideline for the evaluation and management of acute pulmonary embolism in adults: A report of the American college of cardiology/American heart association Joint Committee on clinical practice guidelines. Circulation 19 février 2026.
Sanchez O, Benhamou Y, Bertoletti L, et al. Recommandations de bonne pratique pour la prise en charge de la maladie veineuse thromboembolique chez l’adulte. Version courte. Rev Mal Respir 2019;36(2):249-83.
Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European respiratory society (ERS): The task force for the diagnosis and management of acute pulmonary embolism of the European society of cardiology (ESC). Eur Heart J 2020;41(4):543-603.
Vidal Recos. Embolie pulmonaire. Prise en charge. 15 février 2022.
Recomedicales.fr. Embolie pulmonaire (EP). 29 décembre 2025.
Pour aller plus loin :
Gendron N, Khider L. La place du dosage des D-dimères en médecine. Novembre 2021.
Société française de cardiologie. Chapitre 19 – item 226 : thrombose veineuse profonde et embolie pulmonaire. 7 novembre 2024.
Collège des enseignants de pneumologie. Item 226. Embolie pulmonaire et thrombose veineuse profonde. 2023.
Douillet D, Guineberteau C. Anticoagulants oraux directs dans le traitement de la MTEV. Rev Prat Med Gen 2019;33(1025):548-50.