Pathologies veineuses et sinusoïdales du foie : les 10 messages clés
- En savoir plus sur Pathologies veineuses et sinusoïdales du foie : les 10 messages clés
- Se connecter ou s'inscrire pour poster un commentaire
Dépistage de la maladie rénale chronique de l’enfant
- En savoir plus sur Dépistage de la maladie rénale chronique de l’enfant
- Se connecter ou s'inscrire pour poster un commentaire
Histoire de la vaccination contre la typhoïde
- En savoir plus sur Histoire de la vaccination contre la typhoïde
- Se connecter ou s'inscrire pour poster un commentaire
Maladies cardiorespiratoires et séjour en altitude : quelles recommandations ?
- En savoir plus sur Maladies cardiorespiratoires et séjour en altitude : quelles recommandations ?
- Se connecter ou s'inscrire pour poster un commentaire
Trouble de la personnalité borderline
- En savoir plus sur Trouble de la personnalité borderline
- Se connecter ou s'inscrire pour poster un commentaire
Vivre avec une migraine
- En savoir plus sur Vivre avec une migraine
- Se connecter ou s'inscrire pour poster un commentaire
Transposition des gros vaisseaux congénitalement corrigée
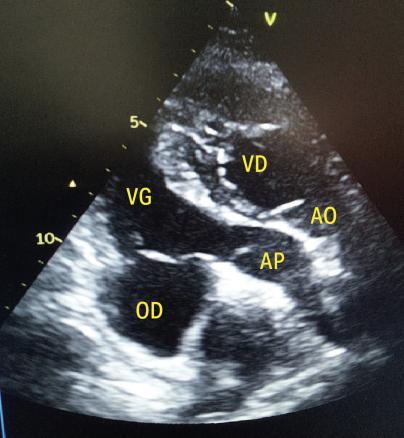
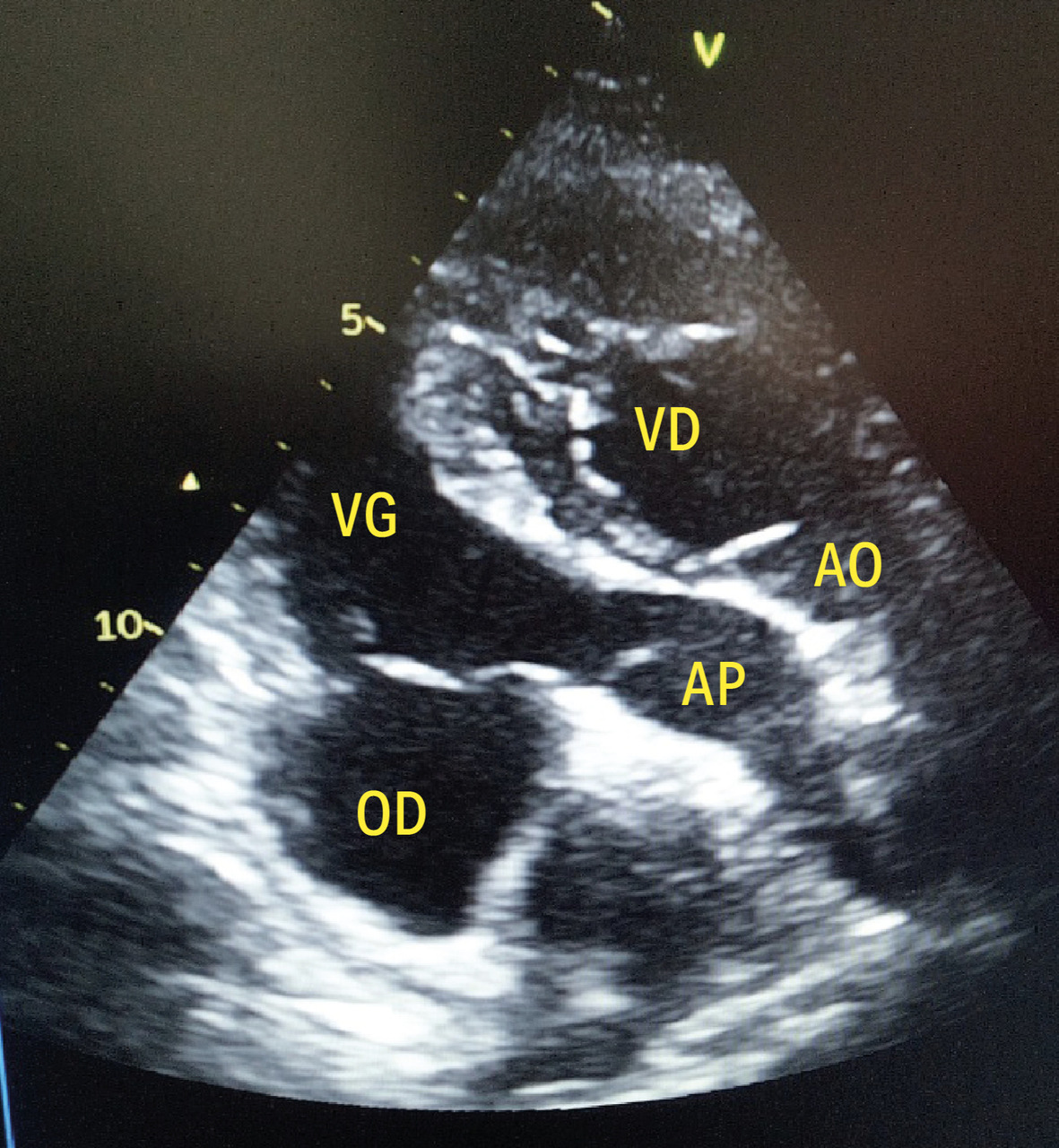
Un homme de 39 ans consulte pour une dyspnée d’effort apparue progressivement et des palpitations intermittentes. L’examen clinique est normal. L’électrocardiogramme montre un PR allongé. L’échocardiographie transthoracique révèle une discordance atrioventriculaire et ventriculo‑artérielle, compatible avec une transposition des gros vaisseaux congénitalement corrigée : l’aorte naît du ventricule droit morphologique, tandis que l’artère pulmonaire émerge du ventricule gauche morphologique, suivant un trajet parallèle (figure). Du fait de l’absence d’anomalies valvulaires associées, un traitement médical symptomatique est instauré, avec une bonne évolution.
Références
1. Baumgartner H, De Backer J, Babu-Narayan SV, et al. 2020 ESC Guidelines for the management of adult congenital heart disease. Eur Heart J 2021;42:563‑645.
2. Wallis GA, Debich-Spicer D, Anderson RH. Congenitally corrected transposition. Orphanet J Rare Dis 2011:6:22.
2. Wallis GA, Debich-Spicer D, Anderson RH. Congenitally corrected transposition. Orphanet J Rare Dis 2011:6:22.
0
Syndrome de Sweet révélant une sarcoïdose pulmonaire
Une patiente âgée de 42 ans – ayant comme antécédents des angines à répétition à raison de six épisodes par an – est admise au sein du service de dermatologie pour des plaques érythémateuses non prurigineuses apparues vingt-cinq jours auparavant, rapidement évolutives, avec une toux et des expectorations blanchâtres, ainsi qu’une fièvre à 39 °C.
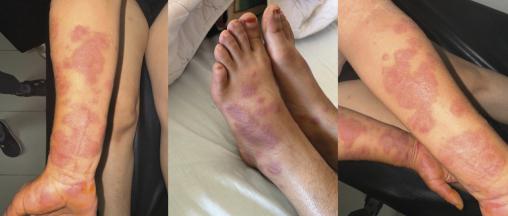
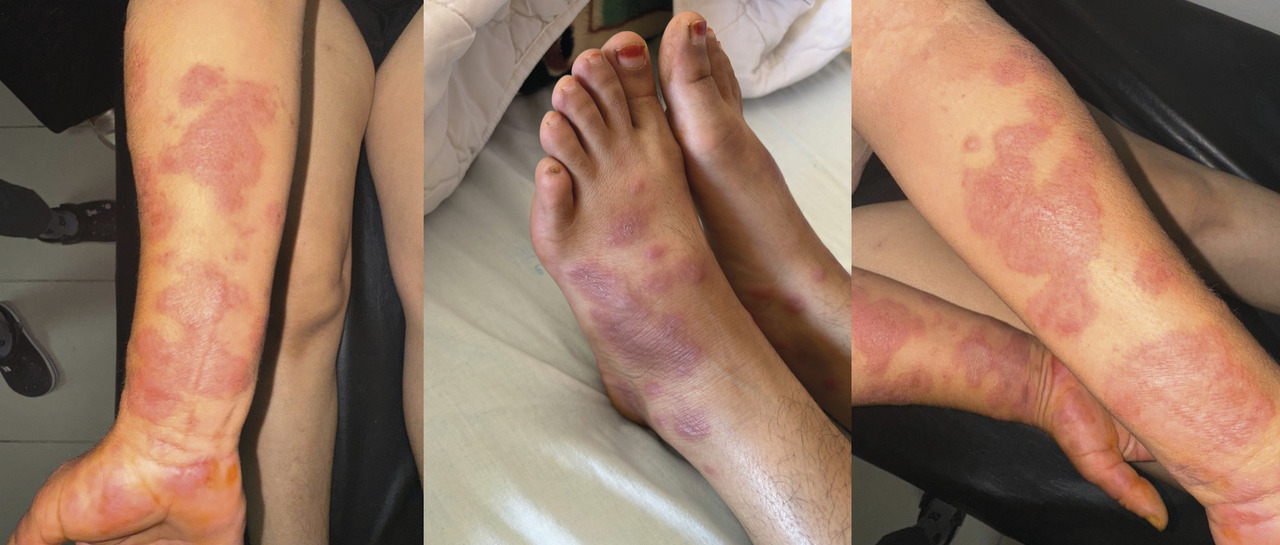
L’examen clinique cutanéo-muqueux met en évidence : de multiples plaques érythémateuses grossièrement ovalaires bien limitées, infiltrées, mesurant de 0,5 à 4 cm de diamètre, siégeant au niveau des avant-bras, des mains et des pieds avec, à la dermoscopie, la présence de plages érythémateuses (fig. 1) ; de multiples lésions papulo-pustuleuses inflammatoires monomorphes, grossièrement dispersées au niveau du dos faisant évoquer une acné cortico-induite ; une lésion papuleuse brunâtre bien limitée grossièrement ovalaire de 1 cm de diamètre siégeant au niveau du sein droit avec, à la dermoscopie, présence d’un réseau d’hyperpigmentation homogène correspondant à une kératose séborrhéique ; une lésion papuleuse brunâtre arrondie bien limitée de 1 cm de diamètre, localisée au niveau de la région lombaire gauche avec, à la dermoscopie, présence d’une pigmentation hétérogène (résultat de biopsie : nævus dermique) ; de multiples macules brunâtres en demi-cercle de taille variable allant de 1 à 2 cm de diamètre, dispersées au niveau de l’abdomen, correspondant à des cicatrices de points de feu ; présence d’une kératodermie plantaire fissuraire en bilatéral.
Les résultats du bilan biologique de retentissement montrent une hyperleucocytose à 16 570/mm3 avec des polynucléaires neutrophiles (PNN) à 13 810/mm3 et une protéine C réactive (CRP) élevée à 102 mg/L. Le bilan biologique étiologique trouve un test QuantiFERON-TB positif (5,02 UI/mL) et une enzyme de conversion de l’angiotensine positive (80 UI/L). Le reste du bilan, y compris les sérologies hépatites B, C, VIH et syphilis, est négatif.
Les cultures mycobactériennes restent stériles. Les marqueurs tumoraux sont négatifs.La biopsie des lésions cutanées conclut à un « aspect morphologique entrant dans le cadre d’une dermatose neutrophilique probable de type syndrome de Sweet : lésion quelque peu évoluée avec légères lésions de vascularite focale ».
Le diagnostic de syndrome de Sweet est donc retenu devant ces critères majeurs (lésions dermatologiques et résultat de la biopsie cutanée) et mineurs (fièvre, toux avec dyspnée et expectorations blanchâtres, CRP, globules blancs et PNN élevés).
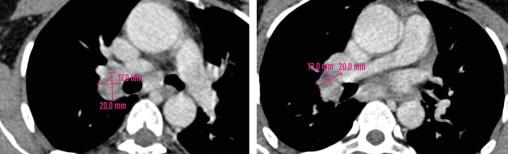
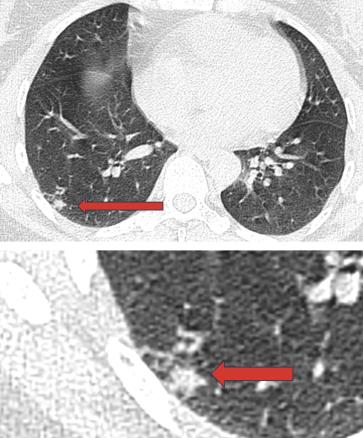
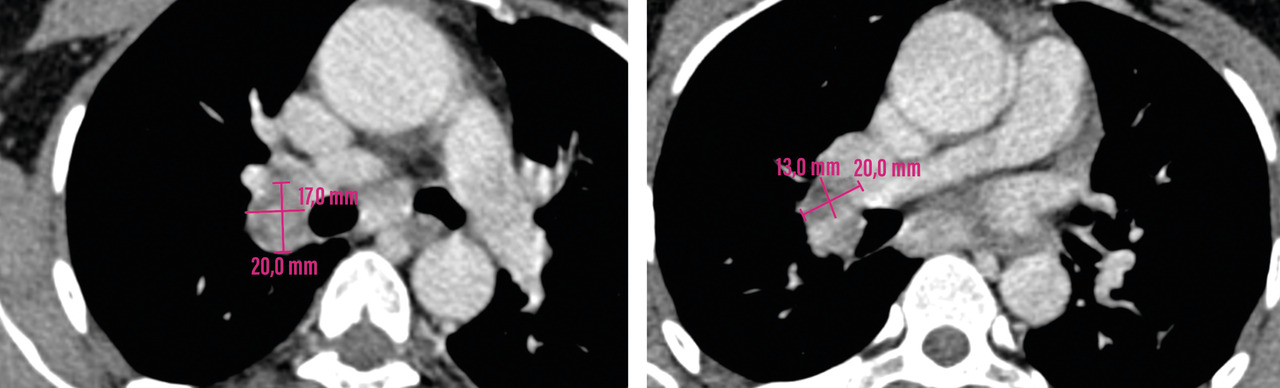
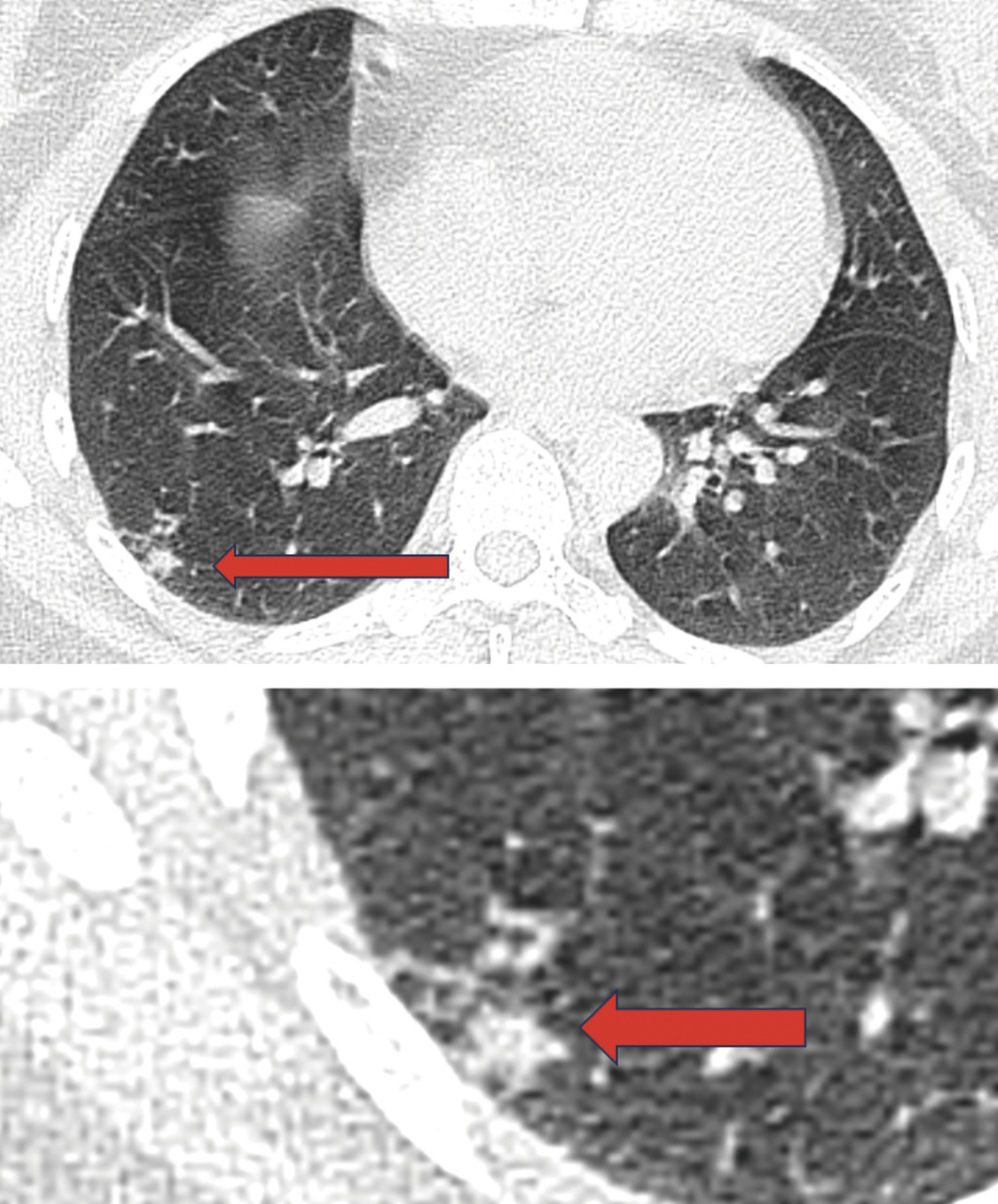
Un scanner cervico-thoraco-abdomino-pelvien est réalisé, à la recherche de signes radiologiques d’une pathologie associée. Il montre des adénopathies médiastino-hilaires droites, nécrotiques (fig. 2) et un foyer de micronodules parenchymateux pulmonaires lobaires inférieurs droits, confluents, avec un nodule central, réalisant le signe de la galaxie, visible sur une tomodensitométrie axiale du thorax (fig. 3). Ces signes sont-ils ceux d’une sarcoïdose pulmonaire active ou d’une atteinte granulomateuse de type tuberculose ou d’une autre cause ?
Une bronchoscopie avec biopsie bronchique est en faveur d’un tissu bronchique siège de lésions granulomateuses épithélioïdes et gigantocellulaires sans nécrose caséeuse. Elle note l’absence de malignité.
L’examen des expectorations ne mettait pas en évidence de bacilles acido-alcoolorésistants (BAAR).Le diagnostic de sarcoïdose pulmonaire active associée au syndrome Sweet a été retenu.
L’examen clinique cutanéo-muqueux met en évidence : de multiples plaques érythémateuses grossièrement ovalaires bien limitées, infiltrées, mesurant de 0,5 à 4 cm de diamètre, siégeant au niveau des avant-bras, des mains et des pieds avec, à la dermoscopie, la présence de plages érythémateuses (fig. 1) ; de multiples lésions papulo-pustuleuses inflammatoires monomorphes, grossièrement dispersées au niveau du dos faisant évoquer une acné cortico-induite ; une lésion papuleuse brunâtre bien limitée grossièrement ovalaire de 1 cm de diamètre siégeant au niveau du sein droit avec, à la dermoscopie, présence d’un réseau d’hyperpigmentation homogène correspondant à une kératose séborrhéique ; une lésion papuleuse brunâtre arrondie bien limitée de 1 cm de diamètre, localisée au niveau de la région lombaire gauche avec, à la dermoscopie, présence d’une pigmentation hétérogène (résultat de biopsie : nævus dermique) ; de multiples macules brunâtres en demi-cercle de taille variable allant de 1 à 2 cm de diamètre, dispersées au niveau de l’abdomen, correspondant à des cicatrices de points de feu ; présence d’une kératodermie plantaire fissuraire en bilatéral.
Les résultats du bilan biologique de retentissement montrent une hyperleucocytose à 16 570/mm3 avec des polynucléaires neutrophiles (PNN) à 13 810/mm3 et une protéine C réactive (CRP) élevée à 102 mg/L. Le bilan biologique étiologique trouve un test QuantiFERON-TB positif (5,02 UI/mL) et une enzyme de conversion de l’angiotensine positive (80 UI/L). Le reste du bilan, y compris les sérologies hépatites B, C, VIH et syphilis, est négatif.
Les cultures mycobactériennes restent stériles. Les marqueurs tumoraux sont négatifs.La biopsie des lésions cutanées conclut à un « aspect morphologique entrant dans le cadre d’une dermatose neutrophilique probable de type syndrome de Sweet : lésion quelque peu évoluée avec légères lésions de vascularite focale ».
Le diagnostic de syndrome de Sweet est donc retenu devant ces critères majeurs (lésions dermatologiques et résultat de la biopsie cutanée) et mineurs (fièvre, toux avec dyspnée et expectorations blanchâtres, CRP, globules blancs et PNN élevés).
Un scanner cervico-thoraco-abdomino-pelvien est réalisé, à la recherche de signes radiologiques d’une pathologie associée. Il montre des adénopathies médiastino-hilaires droites, nécrotiques (fig. 2) et un foyer de micronodules parenchymateux pulmonaires lobaires inférieurs droits, confluents, avec un nodule central, réalisant le signe de la galaxie, visible sur une tomodensitométrie axiale du thorax (fig. 3). Ces signes sont-ils ceux d’une sarcoïdose pulmonaire active ou d’une atteinte granulomateuse de type tuberculose ou d’une autre cause ?
Une bronchoscopie avec biopsie bronchique est en faveur d’un tissu bronchique siège de lésions granulomateuses épithélioïdes et gigantocellulaires sans nécrose caséeuse. Elle note l’absence de malignité.
L’examen des expectorations ne mettait pas en évidence de bacilles acido-alcoolorésistants (BAAR).Le diagnostic de sarcoïdose pulmonaire active associée au syndrome Sweet a été retenu.
Références
1. Sweet RD. An acute febrile neutrophilic dermatosis. Br J Dermatol 1964;76:349-56.
2. Denhove Van A, Freymond N, Isaac S, et al. Syndrome de Sweet révélant un carcinome bronchique épidermoïde. Rev Mal Respir 2007;24(1):77-80.
3. Stuveling EM, Fedder G, Bruns HM, et al. The association of Sweet's syndrome with sarcoidosis. Neth J Med 2001;59(1):31-4.
4. Saliba WR, Habib GS, Elias M. Sweet's syndrome and sarcoidosis. Eur J Intern Med 2005;16(8):545-50.
2. Denhove Van A, Freymond N, Isaac S, et al. Syndrome de Sweet révélant un carcinome bronchique épidermoïde. Rev Mal Respir 2007;24(1):77-80.
3. Stuveling EM, Fedder G, Bruns HM, et al. The association of Sweet's syndrome with sarcoidosis. Neth J Med 2001;59(1):31-4.
4. Saliba WR, Habib GS, Elias M. Sweet's syndrome and sarcoidosis. Eur J Intern Med 2005;16(8):545-50.
0
Dermatite de contact allergique à l’huile d’argan
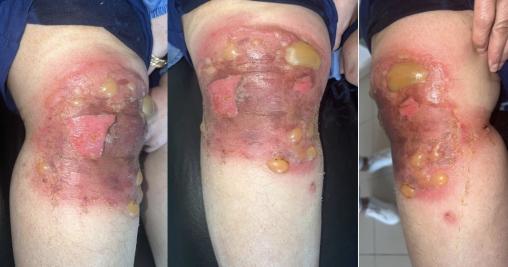
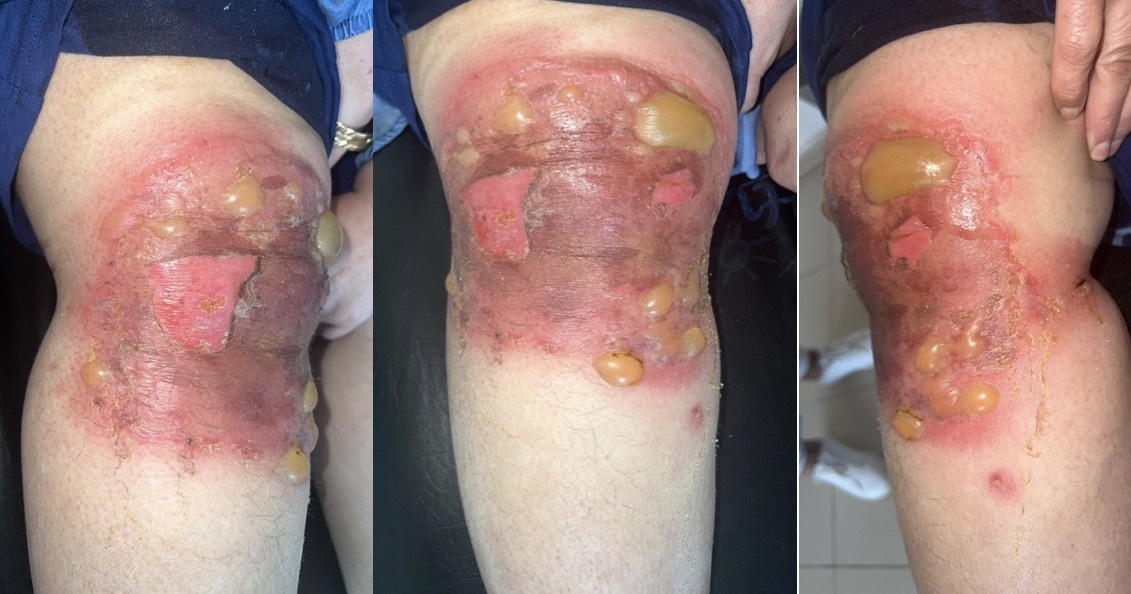
Une femme de 56 ans consulte pour un placard œdémateux, érythémateux et prurigineux localisé au niveau du genou droit, surmonté de lésions vésiculeuses et bulleuses à contenu clair (figure) et accompagné d’une sensation de cuisson. Cette éruption fait suite à l’application locale d’huile d’argan pure, huit heures auparavant, à visée anti-inflammatoire. La patiente n’a pas d’antécédent pathologique notable, notamment aucune atopie personnelle ou familiale ; en revanche, elle est suivie pour une arthrose du genou droit et sous traitement symptomatique (antalgiques et anti-inflammatoires par voie orale à la demande) depuis trois ans.
L’examen clinique révèle une éruption, bien délimitée et localisée à la zone d’application, située sur la face antérieure du genou.
Devant l’aspect clinique typique et le contexte, le diagnostic de dermatite de contact allergique à l’huile d’argan est retenu. Les tests allergologiques, faute de moyens, n’ont pas été réalisés.
La prise en charge a consisté en des soins locaux et dermocorticoïdes pendant dix jours, permettant une régression complète des lésions. Une éducation thérapeutique a été effectuée en parallèle, avec éviction définitive de l’huile d’argan et mise en garde contre toute nouvelle application cutanée.
L’examen clinique révèle une éruption, bien délimitée et localisée à la zone d’application, située sur la face antérieure du genou.
Devant l’aspect clinique typique et le contexte, le diagnostic de dermatite de contact allergique à l’huile d’argan est retenu. Les tests allergologiques, faute de moyens, n’ont pas été réalisés.
La prise en charge a consisté en des soins locaux et dermocorticoïdes pendant dix jours, permettant une régression complète des lésions. Une éducation thérapeutique a été effectuée en parallèle, avec éviction définitive de l’huile d’argan et mise en garde contre toute nouvelle application cutanée.
Références
1. Boukhatem MN, Ferhat MA, Kameli A, et al. Essential oils and their potential as natural preservatives. Journal of Essential Oil Research 2015;27(1):15-22.
2. Diepgen TL, Ofenloch RF, Bruze M, et al. Prevalence of contact allergy in the general population in Europe: A systematic review and meta-analysis. Journal of Investigative Dermatology 2016;136(1):4-14.
3. Goossens A. Contact-allergy to cosmetics. Journal of the European Academy of Dermatology and Venereology 2017;31(4):660-6.
2. Diepgen TL, Ofenloch RF, Bruze M, et al. Prevalence of contact allergy in the general population in Europe: A systematic review and meta-analysis. Journal of Investigative Dermatology 2016;136(1):4-14.
3. Goossens A. Contact-allergy to cosmetics. Journal of the European Academy of Dermatology and Venereology 2017;31(4):660-6.
0