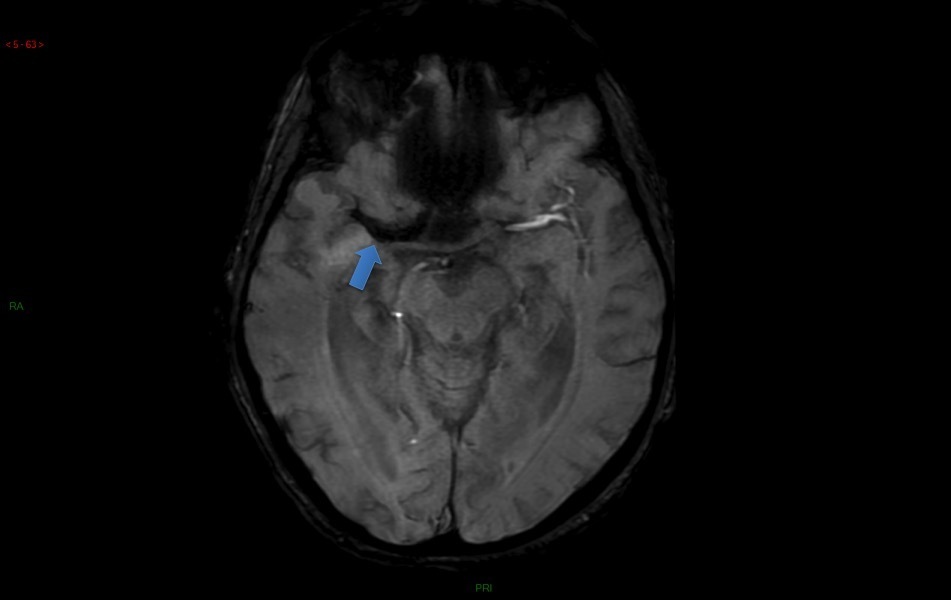
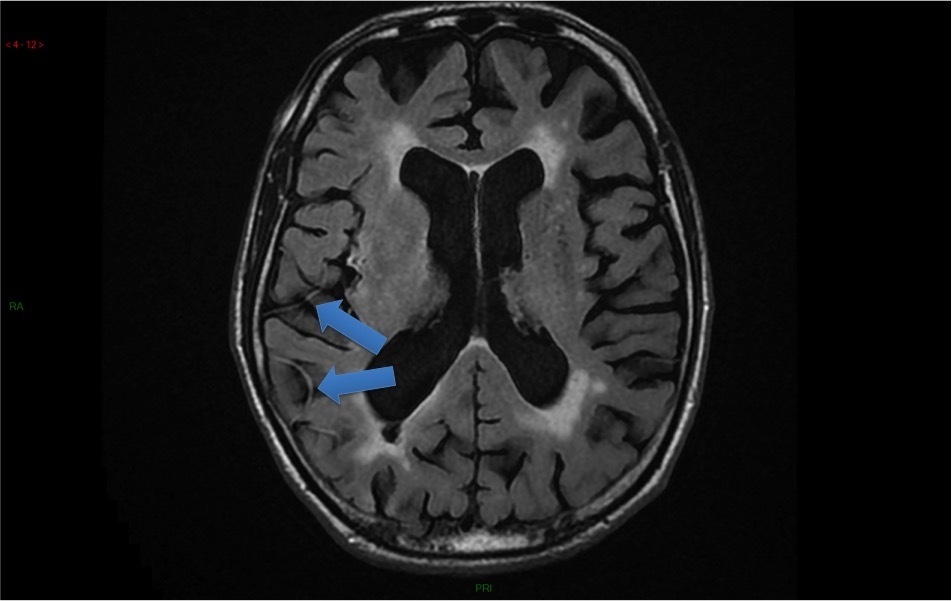
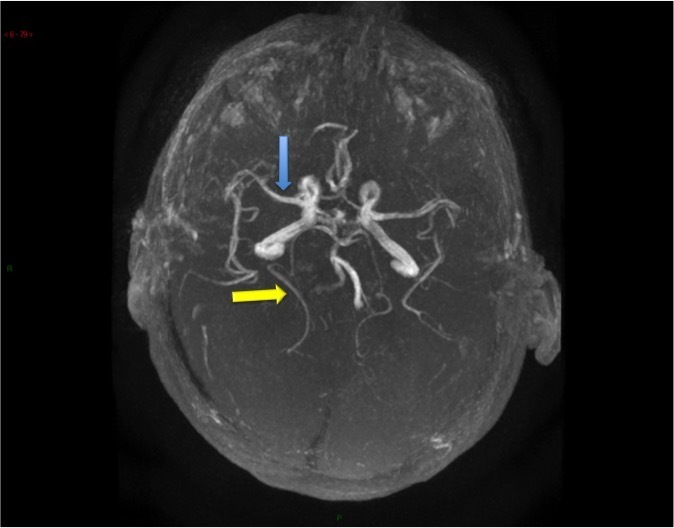
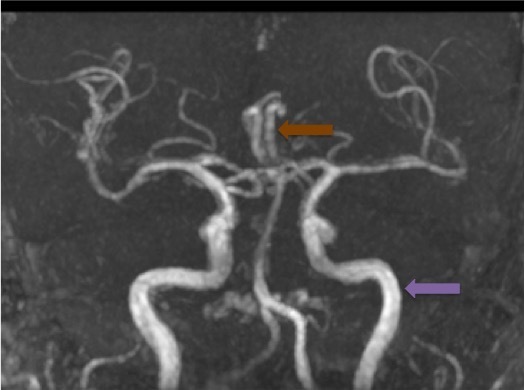
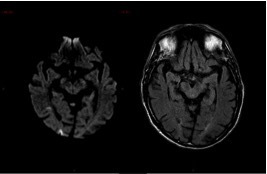
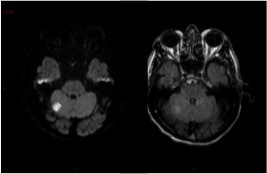
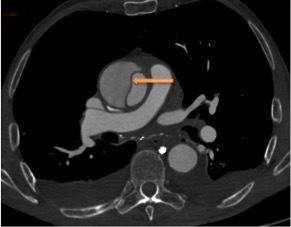
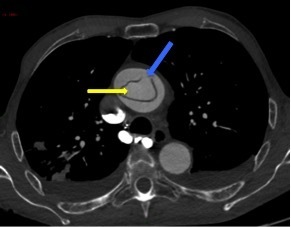
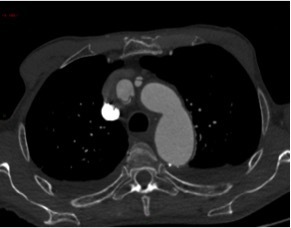
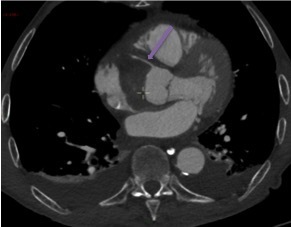
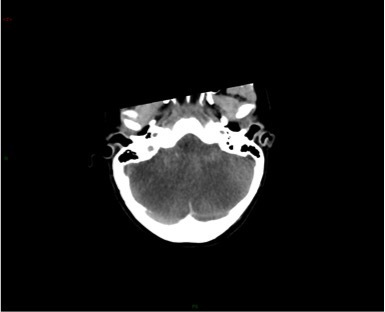
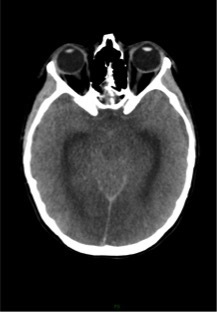
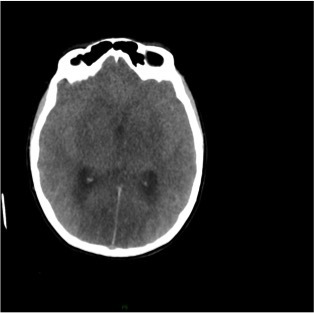
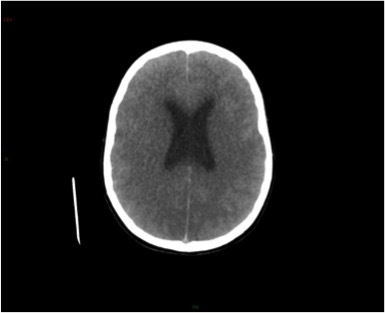
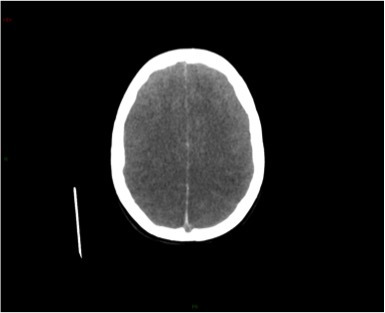
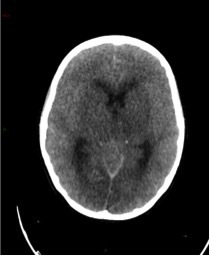
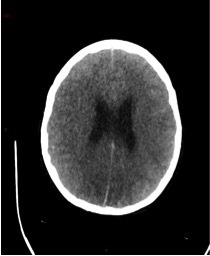
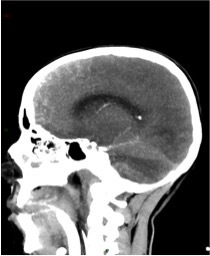
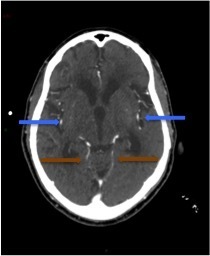
Le SAMU vous contacte pour un homme de 45 ans, sans antécédent connu, qui présente un déficit neurologique focal brutal à type de déficit brachio-facial gauche apparu il y a 3 h 30.
Question 1 : Vos premières hypothèses diagnostiques sont :
Pas de notion de signes méningés (céphalées, raideur de nuque et vomissement). L’apparition brutale de la symptomatologie n’est pas non plus en faveur. Par ailleurs, en l’absence d’encéphalite associée, la présence de déficit neurologique n’est pas expliquée par une méningite.
La persistance des symptômes pendant plus d’une heure exclut ce diagnostic
L’absence de céphalées explosive rend ce diagnostic moins probable. La présence de déficit neurologique est possible, en particulier en cas d’hémorragie méningée associée à un hématome intra-parenchymateux
Tout déficit neurologique focal brutal doit faire évoquer le diagnostic d’AVC, et ce d’autant plus que les délais de thrombolyse ne sont pas dépassés.
L’apparition brutale des symptômes n’est pas en faveur. L’AVC est le premier diagnostic à évoquer.
Les AVC regroupent les ischémies cérébrales artérielles +/- constituées, les hémorragies cérébrales, les thromboses veineuses cérébrales. À ce stade, en dehors de la persistance des symptômes permettant d’exclure un accident ischémique transitoire, il n’est pas possible de trancher entre ces différentes pathologies. Le terrain (cardiopathie emboligène pour l’ischémie, coagulopathie pour la thrombose veineuse), la clinique (déficit neurologique correspondant à un territoire artériel pour l’ischémie, signe d’hypertension intracrânienne pour l’hémorragie) peuvent néanmoins orienter la suspicion.