Vous recevez à votre cabinet de cardiologie Mme N., 78 ans, qui vous est adressée par son médecin traitant dans le cadre d’un suivi général.
Elle a comme antécédent une hystérectomie, un diabète de type 2 traité par metformine, un ulcère gastrique il y a cinq ans, ainsi qu’un asthme.
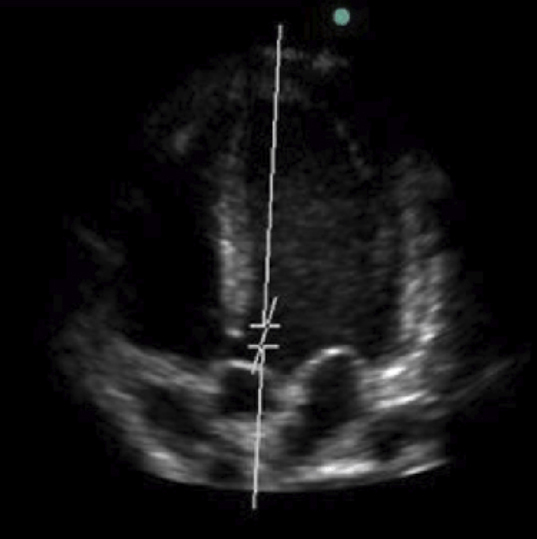
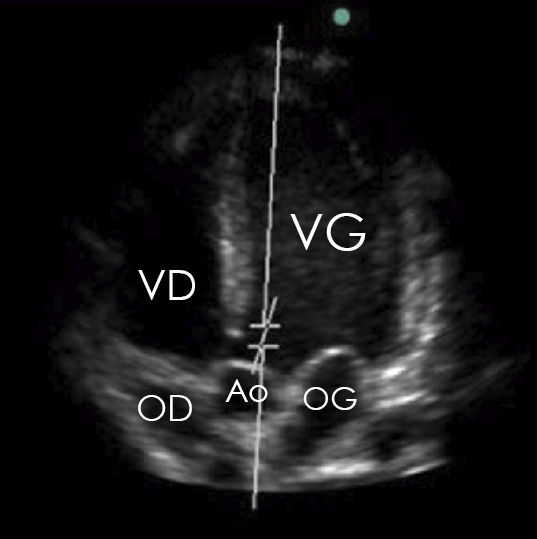
Vous réalisez une auscultation cardiaque qui retrouve un souffle systolique.
Elle a comme antécédent une hystérectomie, un diabète de type 2 traité par metformine, un ulcère gastrique il y a cinq ans, ainsi qu’un asthme.
Vous réalisez une auscultation cardiaque qui retrouve un souffle systolique.
Question 1 - Quelle(s) proposition(s) vous semblent exactes ?
Une résistance à l’éjection ventriculaire correspond à un rétrécissement aortique (RA), dont le souffle est systolique.
Une abolition du B2 indique un RA serré.
Il s’agit d’un souffle d’insuffisance mitrale (IM).
Au-dessus de 70 ans, la cause la plus probable est dégénérative (maladie de Mönckeberg).
Un éclat du B2 peut se rencontrer dans les IM évoluées.
Un souffle systolique doit faire évoquer un RA ou une IM. Les détails sémiologiques de ces souffles sont à maîtriser.