23 mars 2020, 22 h 30 : vous avez été réquisitionné en réanimation pour faire face à la pandémie de SARS-CoV-2. Vous êtes appelé aux urgences pour une désaturation chez Mme K, une femme de 27 ans.
À votre arrivée, la patiente est assise au bord du lit, s’agite et répète « je vais mourir ».
La saturation est à 89 % sous 6 L aux lunettes, la tension à 120/42 mmHg, la fréquence respiratoire à 42 cycles/min, la fréquence cardiaque à 125 battements/min, et la température à 38,1 °C.
Vous passez immédiatement au masque à haute concentration 15 L/min, la saturation remonte à 94 %.
Vous interrogez rapidement la patiente (qui a du mal à répondre aux questions) et son mari : aucun antécédent personnel ou familial, aucun traitement en dehors d’une contraception orale par Leeloo (lévonorgestrel/éthinylestradiol). Elle exerce comme auxiliaire puéricultrice, et vit en couple sans enfants. Elle fume quelques cigarettes par jour et ne prend pas d’autre toxique. Dernier voyage en Thaïlande il y a 2 ans. Elle se sent gênée pour respirer depuis le matin au réveil, avec une aggravation continue. Elle a brièvement perdu connaissance vers 16 h, épisode motivant l’appel des pompiers par le compagnon.
Cliniquement, la patiente est polypnéique sans signes de lutte. Absence de marbrures, extrémités chaudes. L’auscultation cardiopulmonaire est sans particularité en dehors d’une tachycardie régulière. Vous notez une turgescence jugulaire. Absence d’œdèmes des membres inférieurs. Le reste de l’examen est sans particularité.
Pour l’instant, aucun examen complémentaire n’a été effectué en dehors d’une radiographie de poumon qui est strictement normale. Les patients sévèrement atteints de Covid arrivant de partout, il y a presque 2 heures d’attente au scanner.
À votre arrivée, la patiente est assise au bord du lit, s’agite et répète « je vais mourir ».
La saturation est à 89 % sous 6 L aux lunettes, la tension à 120/42 mmHg, la fréquence respiratoire à 42 cycles/min, la fréquence cardiaque à 125 battements/min, et la température à 38,1 °C.
Vous passez immédiatement au masque à haute concentration 15 L/min, la saturation remonte à 94 %.
Vous interrogez rapidement la patiente (qui a du mal à répondre aux questions) et son mari : aucun antécédent personnel ou familial, aucun traitement en dehors d’une contraception orale par Leeloo (lévonorgestrel/éthinylestradiol). Elle exerce comme auxiliaire puéricultrice, et vit en couple sans enfants. Elle fume quelques cigarettes par jour et ne prend pas d’autre toxique. Dernier voyage en Thaïlande il y a 2 ans. Elle se sent gênée pour respirer depuis le matin au réveil, avec une aggravation continue. Elle a brièvement perdu connaissance vers 16 h, épisode motivant l’appel des pompiers par le compagnon.
Cliniquement, la patiente est polypnéique sans signes de lutte. Absence de marbrures, extrémités chaudes. L’auscultation cardiopulmonaire est sans particularité en dehors d’une tachycardie régulière. Vous notez une turgescence jugulaire. Absence d’œdèmes des membres inférieurs. Le reste de l’examen est sans particularité.
Pour l’instant, aucun examen complémentaire n’a été effectué en dehors d’une radiographie de poumon qui est strictement normale. Les patients sévèrement atteints de Covid arrivant de partout, il y a presque 2 heures d’attente au scanner.
Question 1 - Quels sont les examens complémentaires que vous allez demander en priorité ?
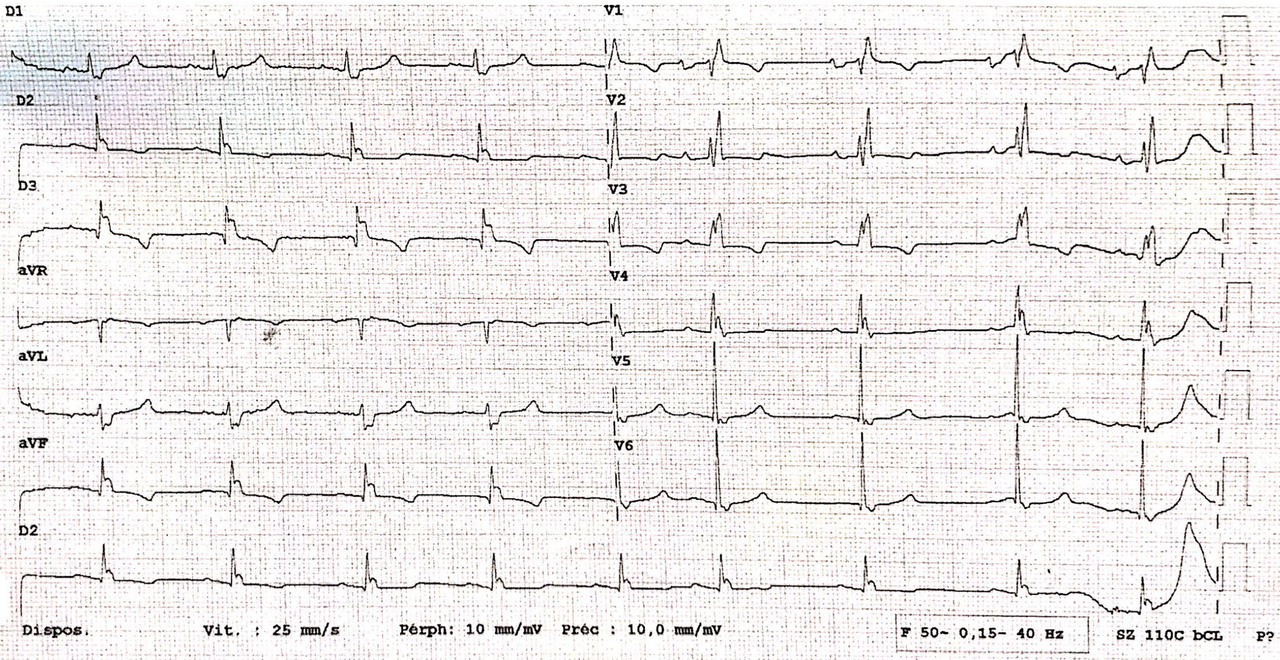
L’ECG pourra vous renseigner s’il a des anomalies en faveur d’une augmentation de la postcharge ventriculaire droite : aspect de bloc de branche droit, S1Q3 (= négativité de la première déflexion en D3 et positivité de la première déflexion en D1), parfois sus-décalage en V2, et/ou ondes T plates dans les dérivations droites.
Le gaz du sang est utile pour l’orientation diagnostique. En cas d’embolie pulmonaire, il montrera typiquement une hypoxémie associée à une hyperventilation alvéolaire (donc une hypocapnie), avec parfois une alcalose respiratoire, conséquence de l’hyperventilation. Il peut y avoir un effet shunt défini par pO2 + pCO2 120 mmHg (ou 110 mmHg selon les définitions).
L’hémostase est utile avant l’initiation d’un traitement anticoagulant ou d’une thrombolyse, et peut renseigner sur une thrombophilie sous-jacente (par exemple l’allongement du TCA en cas d’anticoagulant circulant lupique dans le syndrome des anticorps antiphospholipides [SAPL]).
La scintigraphie de ventilation/perfusion est un examen fastidieux et peu disponible, indiqué en 2e intention en cas de suspicion d’embolie pulmonaire avec angioscanner non contributif, ou en cas d’allergie aux produits de contraste. Elle ne se pratique pas chez les patients instables.
Le dosage des D-dimères est indiqué en cas de probabilité faible d’embolie pulmonaire : leur intérêt réside dans leur valeur prédictive négative. Leur valeur prédictive positive est très mauvaise car leur élévation est peu spécifique (élevée en cas d’inflammation systémique, de cancer, de sepsis...). On les utilise en pratique courante quand la suspicion clinique d’embolie pulmonaire est faible : en cas de négativité des D-dimères, on peut se permettre d’interrompre les explorations.
Dans le cas de notre patiente qui a un tableau typique d’embolie pulmonaire sévère et une fébricule à 38 °C, on se doute bien que les D-dimères seront positifs. De plus, quel que soit leur résultat, on s’acharnera à rechercher et traiter l’embolie pulmonaire. Ils n’apportent donc rien à la démarche actuelle, si ce n’est une perte de temps.
Dans le cas de notre patiente qui a un tableau typique d’embolie pulmonaire sévère et une fébricule à 38 °C, on se doute bien que les D-dimères seront positifs. De plus, quel que soit leur résultat, on s’acharnera à rechercher et traiter l’embolie pulmonaire. Ils n’apportent donc rien à la démarche actuelle, si ce n’est une perte de temps.


Étiologies à évoquer devant une détresse respiratoire avec des signes droits
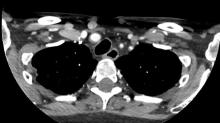
-> Embolie pulmonaire avec cœur pulmonaire aigu
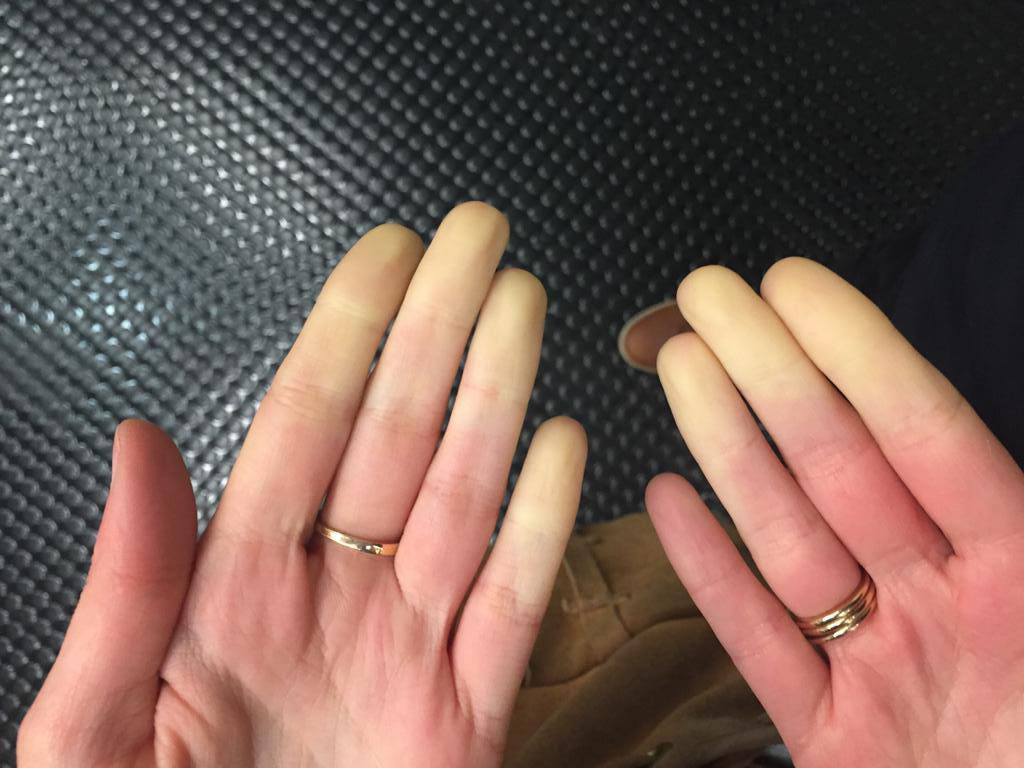
Signes associés : douleur thoracique, syncope, contexte péri-opératoire/oncologique/thrombophilie, douleur unilatérale d’un mollet, hémoptysie si infarctus pulmonaire.
-> Tamponnade péricardique
Signes associés : pouls paradoxal (= diminution de la pression artérielle à l’inspiration, liée à l’augmentation du retour veineux et à la compression du ventricule gauche [VG] par le ventricule droit [VD]).
-> Pneumothorax compressif
Signes associés : silence auscultatoire unilatéral, distension thoracique unilatérale.
-> Asthme aigu grave ou rarement exacerbation sévère de broncho-pneumopathie chronique obstructive (BPCO).
Signes associés : sibilants à l’auscultation.
-> Décompensation cardiaque globale.
Signes associés : insuffisance cardiaque gauche, orthopnée, crépitants bilatéraux.