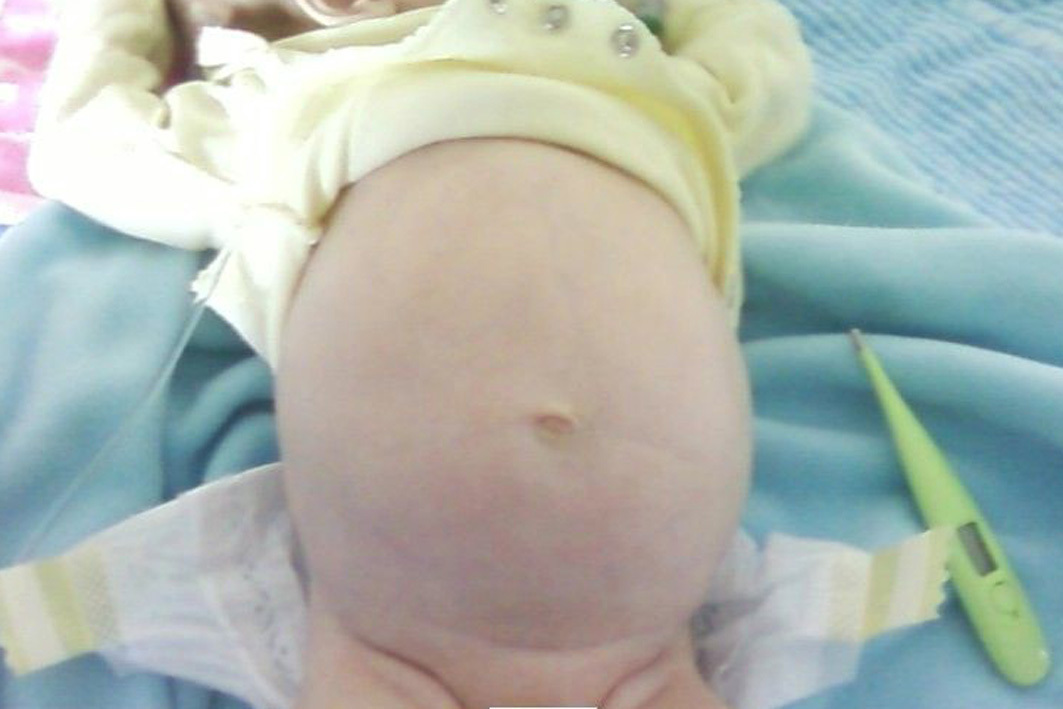
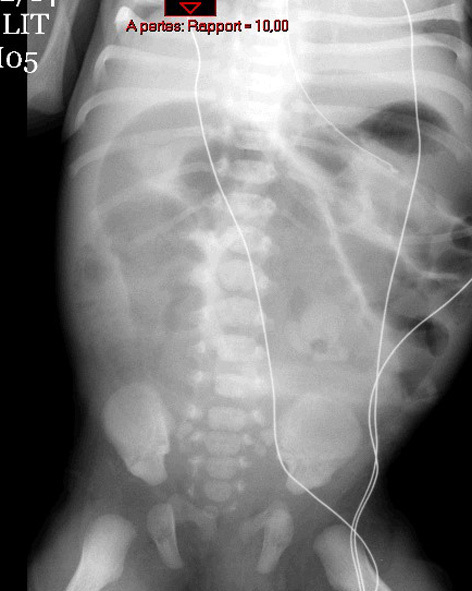
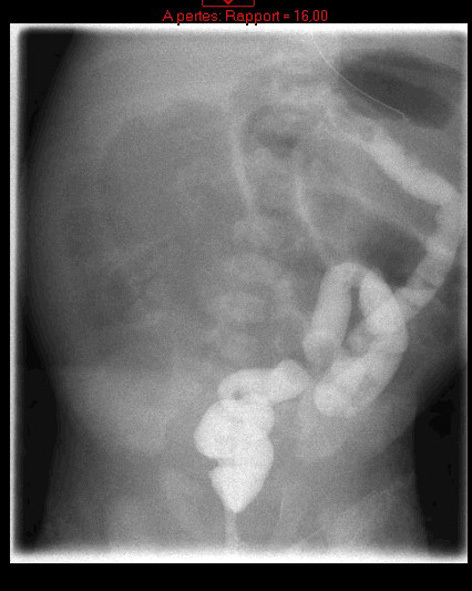
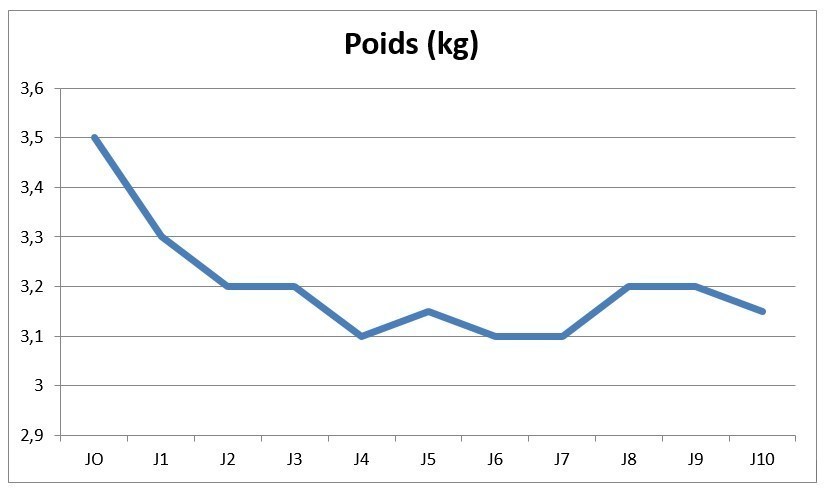
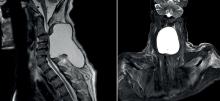
Vous êtes pédiatre en maternité. L’infirmière vous demande d’examiner Léo, né la veille au terme de 38 semaines d’aménorrhée, pour des vomissements verdâtres survenus il y a quelques minutes.
À l’examen du dossier obstétrical de Mme S., la mère de Léo, vous notez les renseignements suivants :
Âge de la mère : 28 ans
Âge du père : 29 ans.
G1P1
Pas d’antécédent personnel ni familial notable.
Echographies anténatales :
12 semaines d’aménorrhée : clarté nucale 1 mm ;
22 semaines d’aménorrhée : morphologie normale. Estimation du poids fœtal au 30ème percentile. Liquide amniotique de quantité normale ;
32 semaines d’aménorrhée : échographie normale.
Pas de dépistage du diabète gestationnel.
Prélèvement vaginal en fin de grossesse positif à streptocoque B.
Mise en travail spontanée à 37 + 6 semaines d’aménorrhée. Rupture de la poche des eaux 30 minutes avant le début des contractions utérines. Durée d’ouverture de la poche des eaux : 14 heures. Liquide amniotique clair. Température maternelle 38,1 °C en fin de travail.
Antibiothérapie par amoxicilline per partum.
Rythme cardiaque fœtal normal. Accouchement par voie basse.
Bonne adaptation à la vie extra-utérine, score d’Apgar 10/10. Examen clinique normal à 1 heure de vie.
Pas d’allaitement maternel souhaité.
À l’examen du dossier obstétrical de Mme S., la mère de Léo, vous notez les renseignements suivants :
Âge de la mère : 28 ans
Âge du père : 29 ans.
G1P1
Pas d’antécédent personnel ni familial notable.
Echographies anténatales :
12 semaines d’aménorrhée : clarté nucale 1 mm ;
22 semaines d’aménorrhée : morphologie normale. Estimation du poids fœtal au 30ème percentile. Liquide amniotique de quantité normale ;
32 semaines d’aménorrhée : échographie normale.
Pas de dépistage du diabète gestationnel.
Prélèvement vaginal en fin de grossesse positif à streptocoque B.
Mise en travail spontanée à 37 + 6 semaines d’aménorrhée. Rupture de la poche des eaux 30 minutes avant le début des contractions utérines. Durée d’ouverture de la poche des eaux : 14 heures. Liquide amniotique clair. Température maternelle 38,1 °C en fin de travail.
Antibiothérapie par amoxicilline per partum.
Rythme cardiaque fœtal normal. Accouchement par voie basse.
Bonne adaptation à la vie extra-utérine, score d’Apgar 10/10. Examen clinique normal à 1 heure de vie.
Pas d’allaitement maternel souhaité.
Question 1: Quel(s) facteur(s) de risque d’infection néonatale bactérienne précoce identifiez-vous chez Léo ?
La prématurité spontanée ( 37 SA) est un facteur de risque d’infection.
Le portage vaginal du streptocoque B est un facteur de risque majeur d’infection. L’antibioprophylaxie per partum permet de diminuer ce risque mais ne l’annule pas.
Dès 12 heures d’ouverture de la poche des eaux, le risque d’infection est multiplié par 3. Après 18 heures d’ouverture, le risque est majeur.
Relation linéaire entre la température de la mère et le risque d’infection, dès 38 °C.
La rupture prématurée des membranes avant 37 SA peut être considérée comme un facteur de risque d’infection, mais pas la rupture avant la mise en travail
RAPPEL :Les facteurs de risque d’infection néonatale bactérienne précoce (anciennement infection materno-fœtale) identifiés dans la littérature sont les suivants :
prématurité spontanée ;
température maternelle > 38 °C, chorioamniotite ;
prélèvement vaginal positif à streptocoque B ;
ouverture de la poche des eaux > 12 heures.
RAPPEL :Les facteurs de risque d’infection néonatale bactérienne précoce (anciennement infection materno-fœtale) identifiés dans la littérature sont les suivants :
prématurité spontanée ;
température maternelle > 38 °C, chorioamniotite ;
prélèvement vaginal positif à streptocoque B ;
ouverture de la poche des eaux > 12 heures.